Дэвид М. Лемаль
Дэвид Маркхэм Лемал (род. 1934) — почетный профессор химии Альберта В. Смита и профессор-исследователь химии в Дартмутском колледже . [1] [2] [3] Он получил степень AB (summa) в Амхерстском колледже в 1955 году и докторскую степень. степень бакалавра химии в Гарвардском университете в 1959 году. [4] В Гарварде он работал с Р.Б. Вудвордом над дезоксисахарами и синтезом алкалоида йохимбина. [5]
и преподавание Исследования
Свою независимую академическую карьеру Лемаль начал в Висконсинском университете в Мэдисоне сначала в качестве преподавателя (1958–60), а затем в качестве доцента (1960–65). В 1965 году он поступил на химический факультет Дартмутского колледжа и в 1969 году стал профессором. Он возглавлял кафедру с 1976 по 1979 год. В 1981 году он был назначен профессором химии Альберта В. Смита. В Висконсине Лемал на протяжении всей своей карьеры интересовался высоконапряженными молекулами, короткоживущими видами и согласованными реакциями. В конце 1960-х годов он увлекся химией фторорганических соединений, которая остается основным направлением его исследований. Лемаль был активным участником Гордонских исследовательских конференций . В 1970 г. он возглавлял конференцию GRC по химии углеводородов, в 1971 г. — GRC по гетероциклическим соединениям; он был членом попечительского совета (1973–79; председатель, 1977–78). Он был сопредседателем международных зимних конференций по фтору в 1987 и 1989 годах, а затем в 1990 году возглавил отделение фтора Американского химического общества. С 1996 по 2004 год он работал в комитете Общества по науке. В 2005 году Лемаль ушел с преподавательской деятельности и стал профессором-исследователем химии, продолжая работать в области синтеза фторорганических соединений до 2016 года. За свою карьеру Лемаль был наставником в исследованиях более сотни студентов, аспирантов и докторантов, а также преподавал курсы химии для 50 лет. [1]
Почести и награды [ править ]
Лемаль был удостоен почестей стипендиата Национального научного фонда (1955–58) и научного сотрудника Фонда Альфреда П. Слоана (1968–70). В 1987 году он получил премию Catalyst Ассоциации производителей химической продукции. В 1989 году Совет по развитию и поддержке образования назвал его профессором года Нью-Гэмпшира. Он был награжден Премией президента Дартмута за выдающееся лидерство и достижения (1991 г.) и Мемориальной премией Роберта А. Фиша за выдающийся вклад в преподавание студентов (1996 г.). В 2002 году он выиграл премию Американского химического общества за творческую работу в области химии фтора. В 2011 году Лемаль стал членом Американского химического общества. [1]
Избранное исследование [ править ]
углеводородов и контрасты Некоторые фторуглеродов
Источник: [6]
Синтезировав и изучив в 1966 году гексаметилпризман, [7] Группу Лемаля интересовало, как будет отличаться по природе и реакционной способности призман, замененный электроноакцепторными вместо донорных групп. Это привело к фотолизу в паровой фазе перфторгексаметилбензола ( 1 ), в результате которого образовался не только призман ( 2 бензол Дьюара ( 3 ) и бензвален ( 4 ). ), но также [8] Английская группа независимо сделала то же открытие. [9] Эти напряженные молекулы были удивительно прочными и термически стабильными по сравнению со своими довольно хрупкими углеводородными аналогами, и этот интригующий контраст привел к дальнейшему исследованию химии фторуглеродов.

Позже они синтезировали перфторгексаметилбициклопропенил ( 5 ), чтобы конкретизировать первый полный набор валентных изомеров бензола. [10] Это соединение термически перегруппировывается до 1 с периодом полураспада ≥ 2 часов при 360 ° C по сравнению с исходным углеводородом, который полимеризуется при -10 ° C. [11] Лемаль ввел термин «перфторалкильный эффект», чтобы обозначить совокупность стабилизирующих влияний, термодинамических и кинетических, которые перфторалкильные группы оказывают на высоконапряженные углеродные каркасы. [12] Эффект оказался общим, но если фторсодержащие группы вместо перфторалкильных групп украшают углеродный скелет, поведение может быть совсем другим, как показывает следующий пример.
Другой случай химического контраста возник, когда группа Лемала подготовила перфторквадрициклан ( 6 ) фотореакцией при -30°C и позволила ему нагреться выше 0°C. [13] Произошла перегруппировка в трициклический изомер 7 , а дальнейшее нагревание до комнатной температуры привело к образованию перфтортропилидена ( 8 ). Вместо этого исходный квадрициклан ( 9 ) перегруппировывается в норборнадиен ( 10 ) в гораздо более энергичных условиях. [14]

Замещение фтора существенно влияет на кето-енольное равновесие. В отличие от кетонов, полученных из углеводородов, енольные таутомеры которых обычно присутствуют в равновесии лишь в следовых количествах, фторированные кетоны иногда гораздо менее стабильны, чем их енолы. [15] [16] [17] [18] кето-енольные равновесия для циклопентанона ( 11 ) и гептафторциклопентанона ( 12 ). Показательным примером являются [17]
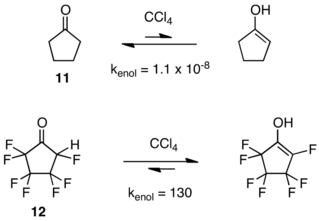
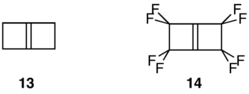
Сильно напряженные и высокореакционноспособные алкены бицикло[2.2.0]гекс-1(4)-ен ( 13 ) и его перфторированный аналог 14 обеспечивают еще один замечательный контраст в стабильности. В то время как 13 димеризуется и полимеризуется при температуре ниже 0 °C, [19] 14 выдерживает нагревание при 140 °C и не образует димера ни при каких условиях. [20]
Циклические согласованные преобразования [ править ]
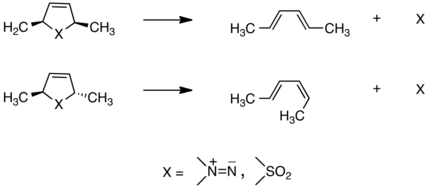
В 1966 году Лемаль и его коллеги изучили класс реакций, которые впоследствии стали называть хелетропными, циклическими согласованными процессами, в которых две связи образуются или разрываются на одном и том же атоме. Обнаружив, что они происходят стереоспецифично, результаты были основаны на идеях Вудворда и Хоффмана о независимой разработке теории этого класса преобразований, которая объяснила экспериментальные результаты группы, показанные здесь: [21] [22]
Десять лет спустя, когда было общепризнано, что все циклические, согласованные процессы (называемые перициклическими) подчиняются правилам орбитальной симметрии Вудворда-Гоффмана (подмножеством которых являются правила для хелетропных реакций), Лемаль и его коллеги обнаружили чрезвычайно легкую вырожденную перегруппировку. это заставило их бросить вызов этому убеждению. [23] Группа S=O в молекуле, представленной ниже, ступенчато движется вокруг 4-членной группы с экстраполированной константой скорости 70 миллионов с. −1 при 25°С! [24]

Учитывая молекулярную геометрию, исследователи предположили, что это может произойти только в том случае, если неподеленная пара серы образует новую SC-связь, когда электронная пара разрываемой SC-связи становится новой неподеленной парой. Позже выяснилось, что это неверно, [25] [26] тем не менее эта идея привела к ключевому пониманию. Лемаль и его коллеги признали, что существует множество циклических согласованных процессов, в которых несвязывающие и связывающие электроны могут меняться ролями, и это процессы, которые не подчиняются правилам орбитальной симметрии. Это привело к появлению термина псевдоперициклический . [23] Эту идею хорошо иллюстрирует пиролиз эфиров, который, как было показано, протекает через плоское переходное состояние:

У карбонильного кислорода неподеленная пара образует связь с водородом, а пи-связь становится новой неподеленной парой. Поскольку эти орбитали лежат в перпендикулярных плоскостях и, таким образом, ортогональны, фактически существует «разрыв» в массиве циклических орбиталей, который освобождает реакцию от ограничений орбитальной симметрии.
Вера в правила была такова, что идея псевдоперициклических реакций игнорировалась почти 20 лет, но затем Дэвид Бирни из Техасского технологического института. за дело взялся [26] В ходе длительного и продолжающегося исследования, в ходе которого эксперименты и вычисления с большим успехом объединились, его группа, а затем и другие, установили, что псевдоперициклические примеры можно найти во всех классах циклических согласованных процессов.
Равновесие Ванцлика » «
В 1960 году Ванцлик сообщил, что тетрааминоэтилен 1 легко диссоциирует на половинки диаминокарбена, [27] и последовала длинная серия статей его группы, описывающих интересные реакции 1 , интерпретируемые как происходящие из карбена. На основе эксперимента по кроссоверу Лемаль и его коллеги показали в 1964 году, что 1 не диссоциирует даже в самых энергичных условиях, которые использовал Ванзлик. [28] Химия реакции была объяснена с точки зрения электрофильной атаки тетрааминоэтилена с последующим разрывом центральной связи.

Много лет спустя, в 1991 году, Ардуенго сделал поразительное открытие: диаминокарбены структуры 2 стабильны и не димеризуются. [29] Это побудило Денка в 1999 году повторить эксперимент Лемала по кроссоверу, найти кроссовер и, таким образом, прийти к выводу, что Ванцлик все-таки был прав насчет диссоциации. [30] Группа Лемала в ответ повторила работу самостоятельно и показала, что устранение электрофильного катализа исключает возникновение кроссовера, тем самым подтвердив результат, полученный Лемалем 36 годами ранее. [31]

Выбрав структуру диаминокарбена, промежуточную по характеру между карбенами Ванцлика и Ардуэнго, группа Лемала нашла и изучила пару карбен-димер, которая действительно существует в равновесии. [32] Здесь димер ( 3 ) находится примерно на 5 ккал/моль ниже своих «половинок» ( 4 ) по свободной энергии при 25 °C.

из лаборатории Лемала соединения Другие
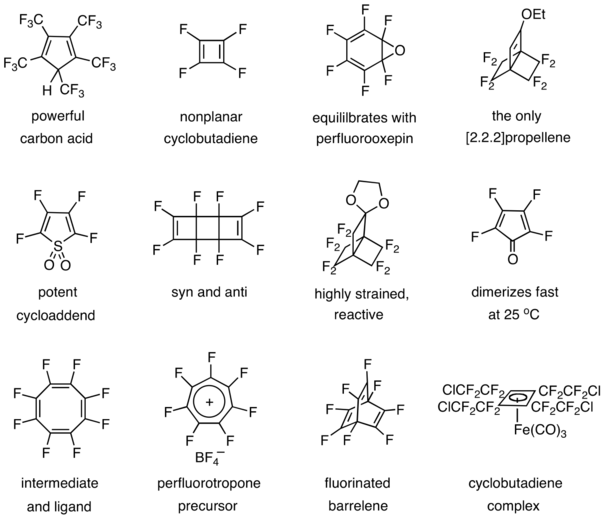
Другие вклады включают получение и исследование мощной угольной кислоты, [33] тетрафторциклобутадиен, [34] [35] оксид гексафторбензола, [36] [37] a [2.2.2]гребные винты, [38] диоксид тетрафтортиофена, [39] октафтортрициклооктадиен, [40] высокореактивный порох, [41] тетрафторциклопентадиенон, [42] октафторциклооктатетраен, [43] соль гептафтортропилия, октафторбаррелен, [44] и циклобутадиеновый комплекс. [45]
Ссылки [ править ]
- ↑ Перейти обратно: Перейти обратно: а б с «Дэвид М. Лемаль» . Дартмут.edu. 2 марта 2016 г. Проверено 17 декабря 2016 г.
- ^ «Лемал, Дэвид М.» WorldCat.org . Проверено 17 декабря 2016 г.
- ^ «Дэвид Лемаль» . Дартмут.edu. Архивировано из оригинала 20 декабря 2016 года . Проверено 17 декабря 2016 г.
- ^ Лемал, Дэвид Маркхэм (1959). Определение путем синтеза конфигурации микарозы и кладинозы . Гарвардский университет. OCLC 1035321051 . Проверено 17 декабря 2016 г. - через WorldCat.org.
- ^ Химия фтора в эпоху тысячелетия: очарована фтором. Глава 20: Порка фторуглеродов . Эльзевир. 2000.
- ^ Лемаль, Дэвид М. (1 января 2004 г.). «Перспектива химии фторуглеродов». Журнал органической химии . 69 (1): 1–11. дои : 10.1021/jo0302556 . ISSN 0022-3263 . ПМИД 14703372 .
- ^ Лемаль, Дэвид М.; Локенсгард, Джеррольд П. (1 декабря 1966 г.). «Гексаметилпризман». Журнал Американского химического общества . 88 (24): 5934–5935. дои : 10.1021/ja00976a046 . ISSN 0002-7863 .
- ^ Лемаль, Дэвид М.; Старос, Джеймс В.; Остел, Волхард (1 июня 1969 г.). «Валентные изомеры (CCF3)6 [гексакис(трифторметил)бензола]». Журнал Американского химического общества . 91 (12): 3373–3374. дои : 10.1021/ja01040a047 . ISSN 0002-7863 .
- ^ Барлоу, Миннесота; Хазелдин, Р.Н.; Хаббард, Р. (1 января 1969 г.). «Изомеры валентной связи гексакис(трифторметил)- и гексакис(пентафторэтил)бензолов». Журнал Химического общества D: Химические коммуникации (5): 202–203. дои : 10.1039/C29690000202 . ISSN 0577-6171 .
- ^ Грейстон, Майкл В.; Лемаль, Дэвид М. (1 марта 1976 г.). «Перфторгексаметилбициклопропенил». Журнал Американского химического общества . 98 (5): 1278–1280. дои : 10.1021/ja00421a048 . ISSN 0002-7863 .
- ^ Биллапс, МЫ; М. Хейли, Майкл; Бозе, Роланд; Блязер, Дитер (1 января 1994 г.). «Синтез бициклопропенилов». Тетраэдр . Международный журнал быстрой публикации критических статей. 50 (36): 10693–10700. дои : 10.1016/S0040-4020(01)89261-9 .
- ^ Лемаль, Д.М.; Данлэп, Л.Г. (1 сентября 1972 г.). «Кинетика и термодинамика взаимопревращений валентных изомеров (CCF3)6». Журнал Американского химического общества . 94 (18): 6562–6564. дои : 10.1021/ja00773a061 . ISSN 0002-7863 .
- ^ Дейли, Уильям П.; Лемаль, Дэвид М. (1 февраля 1984 г.). «Валентные изомеры перфтортропилидена и ион перфтортропилия». Журнал Американского химического общества . 106 (4): 1169–1170. дои : 10.1021/ja00316a087 . ISSN 0002-7863 .
- ^ Добен, Уильям Г.; Каргилл, Роберт Л. (1 января 1961 г.). «Фотохимические превращения — VIII». Тетраэдр . 15 (1): 197–201. дои : 10.1016/0040-4020(61)80026-4 .
- ^ Корреа, Рикардо А.; Линднер, Патрик Э.; Лемаль, Дэвид М. (1 ноября 1994 г.). «Новые кето-еноловые системы». Журнал Американского химического общества . 116 (23): 10795–10796. дои : 10.1021/ja00102a059 . ISSN 0002-7863 .
- ^ Линднер, Патрик Э.; Корреа, Рикардо А.; Джино, Джеймс; Лемаль, Дэвид М. (1 января 1996 г.). «Новые кето-еноловые системы: производные циклобутана». Журнал Американского химического общества . 118 (11): 2556–2563. дои : 10.1021/ja952998h . ISSN 0002-7863 .
- ↑ Перейти обратно: Перейти обратно: а б Линднер, Патрик Э.; Лемаль, Дэвид М. (1 января 1996 г.). «Высокофторированные циклопентаноны и их енолы». Журнал органической химии . 61 (15): 5109–5115. дои : 10.1021/jo9602940 . ISSN 0022-3263 .
- ^ Линднер, Патрик Э.; Лемаль, Дэвид М. (1 апреля 1997 г.). «Перфторированные циклические и ациклические кето-еноловые системы: замечательный контраст». Журнал Американского химического общества . 119 (14): 3259–3266. дои : 10.1021/ja963788n . ISSN 0002-7863 .
- ^ Виберг, Кеннет Б.; Маттурро, Майкл Г.; Окарма, Пол Дж.; Джейсон, Марк Э.; Дейли, Уильям П.; Бургмайер, Джордж Дж.; Бейли, Уильям Ф.; Уорнер, Филип (1 января 1986 г.). «Бицикло[2.2.0]гекс-1(4)-ен» . Тетраэдр . 42 (6): 1895–1902. дои : 10.1016/S0040-4020(01)87609-2 .
- ^ Джанк, Кристофер П.; Он, Йиганг; Чжан, Инь; Смит, Джошуа Р.; Глейтер, Рольф; Касс, Стивен Р.; Ясински, Джерри П.; Лемаль, Дэвид М. (6 февраля 2015 г.). «Синтез и свойства напряженного алкена перфторбицикло[2.2.0]гекс-1(4)-ена». Журнал органической химии . 80 (3): 1523–1532. дои : 10.1021/jo502456h . ISSN 0022-3263 . ПМИД 25574561 .
- ^ Лемаль, Дэвид М.; МакГрегор, Стэнли Д. (1 марта 1966 г.). «Диены из 3-пирролинов. Стереоспецифическое дезаминирование». Журнал Американского химического общества . 88 (6): 1335–1336. дои : 10.1021/ja00958a056 . ISSN 0002-7863 .
- ^ МакГрегор, Стэнли Д.; Лемаль, Дэвид М. (1 июня 1966 г.). «Фрагментации. Термическая реакция 5 → 4 + 11». Журнал Американского химического общества . 88 (12): 2858–2859. дои : 10.1021/ja00964a048 . ISSN 0002-7863 .
- ↑ Перейти обратно: Перейти обратно: а б Росс, Джеймс А.; Сейдерс, Реджинальд П.; Лемаль, Дэвид М. (1 июля 1976 г.). «Чрезвычайно легкая аутомеризация сульфоксида». Журнал Американского химического общества . 98 (14): 4325–4327. дои : 10.1021/ja00430a060 . ISSN 0002-7863 .
- ^ Бушвеллер, К. Хакетт; Росс, Джеймс А.; Лемаль, Дэвид М. (1 января 1977 г.). «Автомеризация тиофена Дьюара и его экзо-S-оксида. Резкий контраст». Журнал Американского химического общества . 99 (2): 629–631. дои : 10.1021/ja00444a063 . ISSN 0002-7863 .
- ^ Снайдер, Джеймс П.; Халгрен, Томас А. (1 апреля 1980 г.). «Сераорганические механизмы. 11. [1,3]-Сигматропные сдвиги для 5-X-бицикло[2.1.0]пент-2-енов. Оценка псевдоперициклической модели». Журнал Американского химического общества . 102 (8): 2861–2863. дои : 10.1021/ja00528a069 . ISSN 0002-7863 .
- ↑ Перейти обратно: Перейти обратно: а б Бирни, Дэвид М.; Вагенселлер, П. Юджин (1 июля 1994 г.). «Изучение реакционной способности формилкетена ab initio. Возвращение к псевдоперициклическим реакциям». Журнал Американского химического общества . 116 (14): 6262–6270. дои : 10.1021/ja00093a028 . ISSN 0002-7863 .
- ^ Ванцлик, Х.-В.; Шикора, Э. (21 июля 1960 г.). «Новый подход к химии карбенов». Прикладная химия . 72 (14): 494. Бибкод : 1960АнгЧ..72..494Вт . дои : 10.1002/anie.19600721409 . ISSN 1521-3757 .
- ^ Лемаль, Дэвид М.; Ловалд, Роджер А.; Кавано, Кеннет И. (1 июня 1964 г.). «Тетрааминоэтилены. Вопрос диссоциации». Журнал Американского химического общества . 86 (12): 2518–2519. дои : 10.1021/ja01066a044 . ISSN 0002-7863 .
- ^ Ардуенго, Энтони Дж.; Харлоу, Ричард Л.; Клайн, Майкл (1 января 1991 г.). «Стабильный кристаллический карбен». Журнал Американского химического общества . 113 (1): 361–363. дои : 10.1021/ja00001a054 . ISSN 0002-7863 .
- ^ Денк, Майкл К.; Хатано, Кен; Ма, Мартин (12 марта 1999 г.). «Нуклеофильные карбены и равновесие Ванцлика: повторное исследование». Буквы тетраэдра . 40 (11): 2057–2060. дои : 10.1016/S0040-4039(99)00164-1 .
- ^ Лю, Юфа; Лемаль, Дэвид М. (29 января 2000 г.). «О «равновесии Ванцлика» ». Буквы тетраэдра . 41 (5): 599–602. дои : 10.1016/S0040-4039(99)02161-9 .
- ^ Лю, Юфа; Линднер, Патрик Э.; Лемаль, Дэвид М. (1 ноября 1999 г.). «Термодинамика равновесия диаминокарбен-тетрааминоэтилен». Журнал Американского химического общества . 121 (45): 10626–10627. дои : 10.1021/ja9922678 . ISSN 0002-7863 .
- ^ Лаганис, Эван Д.; Лемаль, Дэвид М. (08 октября 1980 г.). «Стереоспецифическое 1,3-диполярное циклоэлиминирование в напряженных пиразолинах». Журнал Американского химического общества . 102 (21): 6634–6636. дои : 10.1021/ja00541a076 . ISSN 0002-7863 .
- ^ Петерссон, Э. Джеймс; Фануэле, Джейсон С.; Нимлос, Марк Р.; Лемаль, Дэвид М.; Эллисон, Дж. Барни; Радзишевский, Дж. Джордж (1 ноября 1997 г.). «Непланарность тетрафторциклобутадиена». Журнал Американского химического общества . 119 (45): 11122–11123. дои : 10.1021/ja971930u . ISSN 0002-7863 .
- ^ Джераче, MJ; Лемаль, Д.М.; Эртл, Х. (1 сентября 1975 г.). «Тетрафторциклобутадиен». Журнал Американского химического общества . 97 (19): 5584–5586. дои : 10.1021/ja00852a046 . ISSN 0002-7863 .
- ^ Такенака, Натали Э.; Хэмлин, Роберт; Лемаль, Дэвид М. (1 августа 1990 г.). «Гексафторбензолоксид и гексафтороксепин». Журнал Американского химического общества . 112 (18): 6715–6716. дои : 10.1021/ja00174a043 . ISSN 0002-7863 .
- ^ Химия синтетического фтора . Уайли. 11 августа 1992 г. ISBN 978-0-471-54370-1 .
- ^ Джанк, CP, докторская диссертация, Дартмутский колледж, 2000, стр. 51–54, 94, 95.
- ^ Лемаль, Дэвид М.; Акаши, Марк; Лу, Ян; Кумар, Вивек (20 декабря 2013 г.). «Тетрафтортиофен S,S-диоксид: перфторированный строительный блок». Журнал органической химии . 78 (24): 12330–12337. дои : 10.1021/jo402373x . ISSN 0022-3263 . ПМИД 24313897 .
- ^ Босиком, кондиционер; Сондерс, штат Вашингтон; Бузби, Джон М.; Грейстон, штат Вашингтон; Лемаль, Д.М. (1 октября 1980 г.). «Конфигурации и химия перфтортрицикло[4.2.0.02,5]окта-3,7-диенов». Журнал органической химии . 45 (22): 4292–4295. дои : 10.1021/jo01310a008 . ISSN 0022-3263 .
- ^ Он, Йиганг; Джанк, Кристофер П.; Коули, Джон Дж.; Лемаль, Дэвид М. (1 мая 2003 г.). «Замечательный [2.2.2] Пропеллан». Журнал Американского химического общества . 125 (19): 5590–5591. дои : 10.1021/ja030077y . ISSN 0002-7863 . ПМИД 12733871 .
- ^ Грейстон, штат Вашингтон; Сондерс, штат Вашингтон; Лемаль, ДМ (1 января 1980 г.). «Перфторциклопентадиенон». Журнал Американского химического общества . 102 (1): 413–414. дои : 10.1021/ja00521a088 . ISSN 0002-7863 .
- ^ Лемаль, Дэвид М.; Бузби, Джон М.; Босиком, Олдос К.; Грейстон, Майкл В.; Лаганис, Эван Д. (1 июля 1980 г.). «Новый синтез перфторциклооктатетраена». Журнал органической химии . 45 (15): 3118–3120. дои : 10.1021/jo01303a037 . ISSN 0022-3263 .
- ^ Ралли, Филип; Чжан, Инь; Лемаль, Дэвид М. (22 декабря 2008 г.). «Перфторбаррелен». Буквы тетраэдра . 49 (52): 7349–7351. дои : 10.1016/j.tetlet.2008.10.017 .
- ^ Смит, Джошуа Р.; Лемаль, Дэвид М. (01 марта 2000 г.). «Синтетические подходы к фторированному тетраэдрану» . Журнал химии фтора . 102 (1–2): 323–332. Бибкод : 2000JFluC.102..323S . дои : 10.1016/S0022-1139(99)00297-3 .