Комиссия по изотопному содержанию и атомному весу
 | |
| Аббревиатура | CIAW |
|---|---|
| Формирование | 1899 год |
| Тип | Международная научная организация |
| Цель | Предоставить рекомендованные на международном уровне значения изотопного состава и атомных весов элементов. |
Обслуживаемый регион | По всему миру |
Официальный язык | Английский |
Стул | Йоханна Ирргехер |
Секретарь | Йохен Фогль |
Головная организация | ИЮПАК (с 1920 г.) |
| Веб-сайт | www |
Комиссия по изотопному содержанию и атомному весу ( CIAAW ) — международный научный комитет Международного союза теоретической и прикладной химии (IUPAC) в рамках его отдела неорганической химии . С 1899 г. ему поручается периодическая критическая оценка атомных масс химических элементов и других родственных данных, например изотопного состава элементов. [1] CIAAW, публикуемые раз в два года, Стандартные атомные веса считаются авторитетным научным источником и появляются во всем мире на настенных диаграммах с таблицами Менделеева. [2]
Использование стандартных атомных весов CIAAW также требуется по закону, например, при расчете теплоты сгорания природного газа ( ISO 6976:1995) или при гравиметрической подготовке первичных эталонных стандартов в газовом анализе (ISO 6142:2006). Кроме того, до 2019 года определение кельвина , единицы измерения термодинамической температуры в системе СИ, напрямую относилось к изотопному составу кислорода и водорода, как рекомендовано CIAAW. [3] Последний отчет CIAAW был опубликован в мае 2022 года. [4]
Учреждение
[ редактировать ]- Фрэнк В. Кларк (США)
(показано слева) - Сэр Эдвард Торп (Великобритания)
(показано справа) - Карл Зойберт (Германия)
Хотя атомный вес принял концепцию постоянной природы, такой как скорость света , отсутствие согласия по общепринятым ценностям создавало трудности в торговле. Количества, измеренные с помощью химического анализа, не были переведены в вес одинаково всеми сторонами, и стандартизация стала неотложным вопросом. [5] Поскольку сообщалось о таком большом количестве различных значений, Американское химическое общество (ACS) в 1892 году назначило постоянный комитет для составления стандартной таблицы атомных весов для принятия Обществом. Кларк, который тогда был главным химиком Геологической службы США , был назначен комитетом из одного человека для подготовки отчета. Он представил первый отчет на ежегодном собрании 1893 года и опубликовал его в январе 1894 года. [6]
В 1897 году Немецкое химическое общество по предложению Германа Эмиля Фишера назначило рабочий комитет из трех человек для составления отчетов по атомным весам. В состав комитета входили председатель профессор Ганс Х. Ландольт (Берлинский университет), профессор Вильгельм Оствальд (Лейпцигский университет) и профессор Карл Зойберт (Ганноверский университет). Этот комитет опубликовал свой первый отчет в 1898 году, в котором комитет предложил желательность создания международного комитета по атомным весам. 30 марта 1899 года Ландольт, Оствальд и Зойберт направили приглашение другим национальным научным организациям назначить делегатов в Международный комитет по атомным весам. Пятьдесят восемь членов были назначены в Большой международный комитет по атомным весам, включая Фрэнка Кларка . [7] Большой комитет вел свою работу посредством переписки с Ландольтом, что создавало трудности и задержки, связанные с перепиской между пятьюдесятью восемью членами. В результате 15 декабря 1899 года немецкий комитет попросил членов Интернационала выбрать небольшой комитет из трех-четырех членов. [8] В 1902 году были избраны профессор Франк В. Кларк (США), профессор Карл Зойберт (Германия) и профессор Томас Эдвард Торп (Великобритания), а Международный комитет по атомным весам опубликовал свой первый отчет в 1903 году под председательством Профессор Кларк. [9]
Функция
[ редактировать ]С 1899 года Комиссия периодически и критически оценивает опубликованную научную литературу и составляет Таблицу стандартных атомных весов. В последнее время Таблица стандартных атомных весов публикуется раз в два года. Каждое рекомендуемое стандартное значение атомного веса отражает лучшие знания оцененных опубликованных данных. Рекомендуя стандартные атомные массы, CIAAW обычно не пытается оценить средний или составной изотопный состав Земли или какой-либо подгруппы земных материалов. Вместо этого Комиссия стремится найти единое значение и симметричную неопределенность, которая включала бы почти все вещества, которые могут встретиться. [10]
Примечательные решения
[ редактировать ]За свою историю Комиссия приняла множество заметных решений. Некоторые из них выделены ниже.

Международная единица атомного веса: H=1 или O=16.
[ редактировать ]Хотя Дальтон предложил установить атомный вес водорода равным единице в 1803 году, многие другие предложения были популярны на протяжении всего XIX века. К концу XIX века широкую поддержку получили две шкалы: H=1 и O=16. Такая ситуация была нежелательна для науки, и в октябре 1899 года первой задачей Международной комиссии по атомным весам было принятие решения в международном масштабе, и кислородная шкала стала международным стандартом. [11] Одобрение кислородной шкалы вызвало значительную негативную реакцию в химическом сообществе, и поэтому первый отчет об атомных весах был опубликован с использованием обеих шкал. Вскоре от этой практики отказались, и кислородная шкала оставалась международным стандартом на десятилетия вперед. Тем не менее, когда Комиссия присоединилась к ИЮПАК в 1920 году, ее попросили вернуться к шкале H=1, которую она отвергла.
Современный агрегат: 12 С=12
[ редактировать ]С открытием изотопов кислорода в 1929 году возникла ситуация, когда химики основывали свои расчеты на средней атомной массе (атомном весе) кислорода, тогда как физики использовали массу преобладающего изотопа кислорода кислорода-16. Это несоответствие стало нежелательным, и возникла необходимость объединения химии и физики. [12] На встрече в Париже в 1957 году Комиссия выдвинула предложение о шкале углерода-12. [13] Шкала углерода-12 для атомных весов и масс нуклидов была одобрена IUPAP (1960) и IUPAC (1961) и до сих пор используется во всем мире. [14]
Неопределенность атомного веса
[ редактировать ]В начале 20 века измерения атомного веса свинца показали значительные различия в зависимости от происхождения образца. Эти различия считались исключением, приписываемым изотопам свинца, являющимся продуктами естественных цепочек радиоактивного распада урана. Однако в 1930-х годах Малкольм Доул сообщил, что атомный вес кислорода в воздухе немного отличается от атомного веса в воде. [15] Вскоре после этого Альфред Нир сообщил о естественных изменениях изотопного состава углерода. Стало ясно, что атомные веса не являются константами природы. На заседании Комиссии в 1951 году было признано, что изменение изотопного содержания серы оказывает значительное влияние на международно признанное значение атомного веса. Чтобы указать диапазон значений атомного веса, который может применяться к сере из различных природных источников, к атомному весу серы было присвоено значение ± 0,003. К 1969 году Комиссия присвоила неопределенности всем значениям атомного веса.
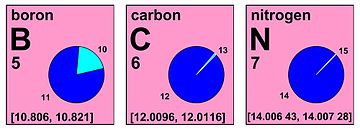
Интервальное обозначение
[ редактировать ]На своем заседании в 2009 году в Вене Комиссия решила выразить стандартный атомный вес водорода, углерода, кислорода и других элементов таким образом, чтобы четко указать, что эти значения не являются константами природы. [16] [17] Например, запись стандартного атомного веса водорода как [1,007 84, 1,008 11] показывает, что атомный вес любого нормального материала будет больше или равен 1,007 84 и будет меньше или равен 1,008 11. [18]
Принадлежность и имя
[ редактировать ]- Международный союз теоретической и прикладной химии (ИЮПАК) с 1920 г. [19]
- Международная ассоциация химических обществ (IACS) с 1913 по 1919 год.
Комиссия по содержанию изотопов и атомному весу претерпела множество изменений названия:
- Большой международный комитет по атомным весам (1899-1902)
- Международный комитет по атомным весам (1902-1920)
- Комиссия ИЮПАК по атомным весам (1920–1922)
- Комиссия ИЮПАК по химическим элементам (1922-1930)
- Комиссия ИЮПАК по атомным весам (1930–1979)
- Комиссия ИЮПАК по атомному весу и содержанию изотопов (1979–2002)
- Комиссия ИЮПАК по содержанию изотопов и атомному весу (2002 – настоящее время)
Известные участники
[ редактировать ]
С момента ее создания членами Комиссии были многие известные химики. Примечательно, что в состав Комиссии входили восемь нобелевских лауреатов: Анри Муассан (1903–1907), Вильгельм Оствальд (1906–1916), Фрэнсис Уильям Астон , Фредерик Содди , Теодор Уильям Ричардс , Нильс Бор , Отто Хан и Мария Кюри .
Ричардс был удостоен Нобелевской премии по химии 1914 года «в знак признания его точного определения атомного веса большого числа химических элементов». [20] пока он был членом Комиссии. [21] Точно так же Фрэнсис Астон был членом Комиссии, когда ему была присуждена Нобелевская премия по химии 1922 года за работу по изотопным измерениям. [22] Кстати, отчет об атомных весах 1925 года подписали три нобелевских лауреата. [23]
Среди других известных ученых, работавших в Комиссии, были Жорж Урбен (открыватель лютеция , хотя приоритет оспаривался с Карлом Ауэром фон Вельсбахом ), Андре-Луи Дебьерн (открыватель актиния , хотя приоритет оспаривался с Фридрихом Оскаром Гизелем ), Маргарита Перей (открыватель франция ), Георгий Флёров (тезка элемента флеровия ), [24] Роберт Уитлоу-Грей (первый выделил радон ) и Арне Оландер (секретарь и член Нобелевского комитета по химии ).
Председатели Комиссии
[ редактировать ]С момента создания председателями Комиссии были:
- Ганс Х. Ландольт
 (1899-1901)
(1899-1901) - Фрэнк В. Кларк
 (1902-1921)
(1902-1921) - Жорж Урбан
 (1922-1929)
(1922-1929) - Грегори П. Бакстер
 (1930-1949)
(1930-1949) - Эдвард Уичерс
 (1950-1959)
(1950-1959) - Томас Батуэкас
 (1960-1963)
(1960-1963) - Эдвард Уичерс
 (1964-1969)
(1964-1969) - Норман Гринвуд
 (1970-1975)
(1970-1975) - Этьен Рот
 (1976-1979)
(1976-1979) - Норман Э. Холден
 (1980-1983)
(1980-1983) - Раймонд Л. Мартин
 (1984-1987)
(1984-1987) - Джон де Лаэтер
 (1988-1991)
(1988-1991) - Клаус Г. Хойманн
 (1992-1995)
(1992-1995) - Людольф Шульц
 (1996-2001)
(1996-2001) - Филип Тейлор
 (2002-2003)
(2002-2003) - Чаевые Дин
 (2004-2007)
(2004-2007) - Роберто Гонфиантини
 (2008-2009)
(2008-2009) - Вилли А. Брэнд
 (2010-2013)
(2010-2013) - Юрис Мейя
 (2014-2021)
(2014-2021) - Йоханна Ирргехер
 (2022-настоящее время)
(2022-настоящее время)
В 1950 году испанский химик Энрике Молес стал первым секретарем Комиссии, когда была создана эта должность.
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ «Нобелевская премия по химии 1914 года — Вручение» . Нобелевская премия.org. 11 ноября 1915 года. Архивировано из оригинала 30 июня 2017 года.
- ^ «ИЮПАК, Оксфордский справочник» . Архивировано из оригинала 22 сентября 2013 г.
{{cite journal}}: Для цитирования журнала требуется|journal=( помощь ) - ^ «Уточнение определения кельвина, единицы термодинамической температуры» (PDF) . МБМВ. 2005. Архивировано (PDF) из оригинала 26 июня 2013 г.
- ^ Томас Прохаска; Йоханна Ирргехер; Жаклин Бенефилд; Джон Карл Бельке; Лесли Чессон; Тайлер Б. Коплен; Типинг Дин; Филип Дж. Х. Данн; Манфред Грёнинг; Норман Э. Холден; Харро А.Дж. Мейер; Хайко Муссен; Антонио Поссоло; Ёсио Такахаши; Йохен Фогль; Томас Вальчик; Цзюнь Ван; Майкл Визер; Сигекадзу Ёнеда; Сянкунь Чжу; Юрис Мейя (2022). «Стандартные атомные веса элементов 2021 (Технический отчет ИЮПАК)» . Чистое приложение. хим. 94 (5): 573–600. дои : 10.1515/pac-2019-0603 .
- ^ Э. Кроуфорд (1992). Национализм и интернационализм в науке, 1880-1939 (с. 40) . Издательство Кембриджского университета. ISBN 9780521524742 . Архивировано из оригинала 9 мая 2016 г.
- ^ «Атомные веса и Международный комитет — исторический обзор» . Химия Интернэшнл. 2004. Архивировано из оригинала 9 июля 2017 г.
- ^ LM Деннис, Фрэнк Вигглсворт Кларк (Национальная академия наук, 1932) на стр. 143. Архивировано 15 октября 2012 г. в Wayback Machine.
- ^ Х. Ландольт; В. Оствальд; К. Зойберт (1900). «Второй отчет Комиссии по определению атомного веса». Бер. 22 (2): 1847–1883. дои : 10.1002/cber.19000330270 .
- ^ Ф. В. Кларк (1903). «Отчет Международного комитета по атомным весам» . Дж. Ам. хим. Соц. 25 (1): 1–5. дои : 10.1021/ja02003a001 .
- ^ Майкл Э. Визер; Майкл Берглунд (2009). «Атомные веса элементов 2007 (Технический отчет ИЮПАК)» (PDF) . Чистое приложение. хим. 81 (11): 2131–2156. CiteSeerX 10.1.1.540.9258 . doi : 10.1351/PAC-REP-09-08-03 . S2CID 98084907 . Архивировано (PDF) из оригинала 4 марта 2016 г.
- ^ Ричардс, Теодор Уильям (1900). «Международные атомные веса». Труды Американской академии искусств и наук . 36 (10): 171–176. дои : 10.2307/20020992 . JSTOR 20020992 .
- ^ ФВ Астон (1931). «Единица атомного веса» . Природа . 128 (3234): 731. Бибкод : 1931Natur.128..731. . дои : 10.1038/128731a0 . S2CID 4134425 .
- ^ Эдвард Уичерс (1958). «Отчет об атомных весах за 1956–1957 годы». Дж. Ам. хим. Соц. 80 (16): 4121–4124. дои : 10.1021/ja01549a001 .
- ↑ Британская энциклопедия. Архивировано 8 марта 2013 г. в Wayback Machine.
- ^ Малькольм Доул (1935). «Относительный атомный вес кислорода в воде и воздухе». Дж. Ам. хим. Соц. 57 (12): 2731. doi : 10.1021/ja01315a511 .
- ^ «Массовая миграция: химики пересматривают атомные массы 10 элементов» . Научный американец . 16 декабря 2010 г. Архивировано из оригинала 30 декабря 2011 г.
- ^ «Атомные веса изменяются, отражая естественные вариации» . Химический мир . 2010. Архивировано из оригинала 23 сентября 2013 г.
- ^ Тайлер Б. Коплен; Норман Э. Холден (2011). «Атомные веса: больше не константы природы» . Химия Интернэшнл . Архивировано из оригинала 14 июня 2013 г.
- ^ «Детали тела» . ИЮПАК | Международный союз теоретической и прикладной химии . Проверено 16 марта 2024 г.
- ^ «Нобелевская премия по химии 1914 года» . Архивировано из оригинала 29 июня 2017 г.
- ^ «Нобелевская премия Ричардсу; премия по химии за 1914 год достается исследователю Гарварда» . Нью-Йорк Таймс . 13 ноября 1915 г. Архивировано из оригинала 22 сентября 2013 г.
- ^ ФВ Астон; и др. (1923). «Отчет Международного комитета по химическим элементам: 1923 г.». Дж. Ам. хим. Соц. 45 (4): 867–874. дои : 10.1021/ja01657a001 .
- ^ ФВ Астон; и др. (1925). «Международные атомные веса 1925 года» . Дж. Ам. хим. Соц. 47 (3): 597–601. дои : 10.1021/ja01680a001 .
- ^ «Сводка о прошлом и настоящем членстве, CIAAW» . Архивировано из оригинала 15 октября 2014 г.

