Перфторэфир
Перфторэфиры представляют собой класс фторорганических соединений, содержащих одну или несколько эфирных функциональных групп . В целом эти соединения структурно аналогичны родственным эфирам углеводородов, за исключением отличительных свойств фторуглеродов .
Введение эфирной функции в цепь перфторполимера также придает полимеру термопластичные свойства, делая возможным термическое формование. Это большое технологическое преимущество для производства самых разнообразных форм (например, стаканов, воронок, колб для лабораторного использования и т. д.) и позволяет экструзией трубок с высокой химической стойкостью. Это также придает полимеру полупрозрачный вид. [ 1 ]
Низкомолекулярные фторированные эфиры
[ редактировать ]
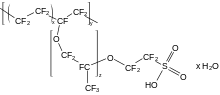
Ациклические перфторэфиры являются аналогами диэтилового эфира , например O(C 2 F 5 ) 2 , например перфтор(2-этоксиэтан)сульфоновой кислоты (PFEESA).
Более интересными и полезными являются циклические эфиры, особенно эпоксиды . Оксид тетрафторэтилена и оксид гексафторпропилена — два простейших циклических перфторэфира. Это предшественники перфтор(метилвинилового эфира) (CF 2 =CFOCF 3 ) и перфтор(пропилвинилового эфира), [ 2 ] и используются в качестве сомономеров с тетрафторэтиленом.
Полимерные перфторэфиры
[ редактировать ]Перфторалкоксиалканы (ПФА) представляют собой фторполимеры со свойствами, близкими к политетрафторэтилену (ПТФЭ). Метилфторалкокси (MFA) представляет собой перфторметилвиниловый эфир политетрафторэтилена, полученный с другим соотношением мономеров ПТФЭ и МВЭ по сравнению с тем, которое используется для PFA. В этих материалах эфирные группы являются подвесными к основной цепи полимера.
Krytox — смазка, получаемая в результате полимеризации оксида гексафторпропилена. Его химическая формула : F-(CF(CF 3 )-CF 2 -O) n -CF 2 CF 3 . Эфирные группы являются неотъемлемой частью полимерной цепи. [ 3 ]
Нафион представляет собой перфторированный полиэфир с боковыми группами сульфоновой кислоты (RSO 3 H).
Меры предосторожности
[ редактировать ]При высоких температурах или при пожаре перфторэфиры разлагаются и могут выделять фтористый водород . С любыми остатками необходимо обращаться, используя защитное оборудование.
Ссылки
[ редактировать ]- ^ Гюнтер Зигемунд; Вернер Швертфегер; Эндрю Фейринг; Брюс Смарт; Фред Бер; Гервард Фогель; Блейн МакКьюсик (2002). «Соединения фтора органические». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a11_349 . ISBN 3-527-30673-0 .
- ^ Патент США 3180895A , Джон Фергюсон Харрис-младший и Дональд Ирвин МакКейн, «Эфиры фторуглеродов», выдан 27 апреля 1965 г.
- ^ Майкл Г. Костелло; Ричард М. Флинн; Джон Г. Оуэнс (2001). «Фторэфиры и фторамины». Энциклопедия химической технологии Кирка-Отмера . Вайнштейн: Wiley-VCH. дои : 10.1002/0471238961.0612211506122514.a01.pub2 . ISBN 0-471-23896-1 .