Механизм отскока кислорода
В биохимии механизм отскока кислорода — это путь гидроксилирования органических соединений железосодержащими оксигеназами . Многие ферменты осуществляют гидроксилирование углеводородов как средство биосинтеза, детоксикации, регуляции генов и других функций. Эти ферменты часто используют центры Fe-O , которые преобразуют связи CH в группы C-OH. Механизм отскока кислорода начинается с отрыва H от углеводорода с образованием органического радикала и гидроксида железа. На стадии отскока органический радикал атакует центр Fe-OH, образуя спиртовую группу, которая связана с Fe в качестве лиганда. Диссоциация спирта от металла позволяет циклу начаться заново. Этот механистический сценарий является альтернативой прямому внедрению О-центра в связь CH. Этот путь является примером активации CH . [1] [2]
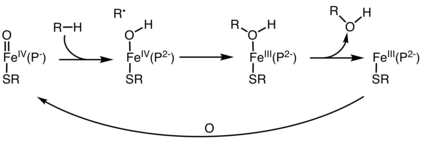
Тремя основными классами этих ферментов являются цитохром P450 , альфа-кетоглутарат-зависимые гидроксилазы и негем-дижелезогидроксилазы.
Ссылки
[ редактировать ]- ^ Хуанг, X.; Гроувс , Джей Ти (2017). «Помимо гидроксилирования, опосредованного феррилом: 40 лет механизма отскока и активации C – H» . Журнал биологической неорганической химии . 22 (2–3): 185–207. дои : 10.1007/s00775-016-1414-3 . ПМК 5350257 . ПМИД 27909920 .
- ^ Реакции оксигенации высоковалентными оксо-разновидностями железа представляют собой реакции «активации C – H» в широком смысле этого слова. Некоторые авторы назвали бы это функционализацией C–H , а не «активацией» (в узком смысле), поскольку связь металл–углерод не участвует в процессе разрыва связи C–H.