Полевой эффект (химия)
Эффект поля это поляризация молекулы — в пространстве. Эффект является результатом электрического поля , создаваемого локализацией заряда в молекуле. [1] Это поле, которое зависит от заместителя и конформации , может влиять на структуру и реакционную способность, манипулируя расположением электронной плотности в связях и/или молекуле в целом. [2] Поляризация молекулы через ее связи — это отдельное явление, известное как индукция . [3] Эффекты поля относительно слабы и быстро уменьшаются с расстоянием, но все же обнаружено, что они изменяют молекулярные свойства, такие как кислотность. [1]

Источники поля
[ редактировать ]

Полевые эффекты могут возникать из-за электрического дипольного поля связи, содержащей электроотрицательный атом или электроноакцепторный заместитель, а также из-за атома или заместителя, несущего формальный заряд. [1] молекулы Направленность диполя и концентрация заряда могут определять форму электрического поля , которое будет манипулировать локализацией электронной плотности по направлению к интересующим участкам или от них, например, к кислому водороду. Эффекты поля обычно связаны с выравниванием дипольного поля относительно реакционного центра. [5] Поскольку это пространственные эффекты, важным фактором является трехмерная структура молекулы. Поле может быть прервано другими связями или атомами, прежде чем распространиться на интересующий реактивный центр. [6] Атомы с разной электроотрицательностью могут приближаться друг к другу, что приводит к поляризации связей в пространстве, что имитирует индуктивный эффект через связи. [6] Бициклогептан и бициклооктан (на фото слева) — два соединения, в которых изменение кислотности при замещении объясняется эффектом поля. [4] Диполь CX ориентирован от группы карбоновой кислоты и может отводить электронную плотность, поскольку центр молекулы пуст и имеет низкую диэлектрическую проницаемость , поэтому электрическое поле может распространяться с минимальным сопротивлением. [5]
Полезность эффекта
[ редактировать ]Диполь может выравниваться, чтобы стабилизировать или дестабилизировать образование или потерю заряда, тем самым уменьшая (если стабилизирован) или увеличивая (если дестабилизирован) активационный барьер для химического события. [1] Таким образом, эффекты поля могут регулировать кислотность или основность связей внутри их полей, жертвуя или удаляя плотность заряда. [5] Что касается кислотности, следует отметить общую тенденцию: с индуктивной точки зрения электроноакцепторный заместитель вблизи кислого протона будет понижать pKa (т.е. увеличивать кислотность) и, соответственно, электронодонорный заместитель будет повышать pKa. . [7] Реорганизация заряда за счет эффектов поля будет иметь тот же результат. Поле электрического диполя, распространяющееся через пространство вокруг или в середине молекулы в направлении кислого протона, уменьшит кислотность, а направленный в сторону диполь увеличит кислотность и одновременно удлинит связь XH. [8] Таким образом, эти эффекты могут помочь настроить кислотность/основность молекулы для протонирования/депротонирования определенного соединения или повысить способность донора водородных связей для молекулярного распознавания или приложений по обнаружению анионов. [9] [10] Также было показано, что эффекты поля в замещенных аренах доминируют на картах электростатического потенциала, которые представляют собой карты электронной плотности, используемые для объяснения межмолекулярных взаимодействий. [2]
Доказательства полевых эффектов
[ редактировать ]
Локализованные электронные эффекты представляют собой комбинацию индуктивных и полевых эффектов. Из-за сходства этих эффектов трудно разделить их вклады в электронную структуру молекулы. Однако существует большой объем литературы, посвященной развитию понимания относительной значимости эффектов индукции и поля путем анализа родственных соединений в попытке количественно оценить каждый эффект на основе имеющихся заместителей и молекулярной геометрии. [4] [12] [13] [14] [15] Например, три соединения справа, все октаны , различаются только количеством линкеров между электроноакцепторной группой X и кислотной функциональной группой, которые находятся примерно на одинаковом пространственном расстоянии друг от друга в каждом соединении. [11] Известно, что электроноакцепторный заместитель индуктивно снижает рКа данного протона (т.е. увеличивает кислотность). [7] Если индукция была доминирующим эффектом в этих соединениях, кислотность должна увеличиваться линейно с количеством доступных индуктивных путей (линкеров). Однако экспериментальные данные показывают, что влияние на кислотность родственных октанов и кубанов очень похоже, и поэтому доминирующее влияние должно быть через пространство. [11]


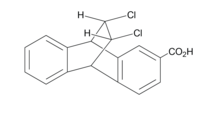
изомерах цис-11,12-дихлор-9,10-дигидро-9,10-этано-2-антроевой кислоты, В син- и анти- показанных ниже и слева, хлоры обеспечивают эффект поля. Концентрация отрицательного заряда каждого хлора имеет эффект сквозного пространства, который можно увидеть в относительных значениях pKa. [16] Когда хлоры направлены над группой карбоновой кислоты, pKa выше, поскольку потеря протона менее благоприятна из-за увеличения отрицательного заряда в этой области. Потеря протона приводит к образованию отрицательного заряда, который менее стабилен, если уже существует собственная концентрация электронов. [17] Это можно объяснить эффектом поля, поскольку в том же соединении, где хлоры направлены в сторону от кислотной группы, рКа ниже, и если бы эффект был индуктивным, конформационное положение не имело бы значения. [16]

Ссылки
[ редактировать ]- ^ Jump up to: а б с д Анслин, Эрик В., Догерти, Деннис А. (2006). Современная физическая органическая химия . Саусалито, Калифорния: Университетская наука. ISBN 9781891389313 . OCLC 55600610 .
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Jump up to: а б Уилер, Стивен Э.; Хоук, КН (2009). «Пространственные эффекты заместителей доминируют над молекулярными электростатическими потенциалами замещенных аренов» . Журнал химической теории и вычислений . 5 (9): 2301–2312. дои : 10.1021/ct900344g . ISSN 1549-9618 . ПМК 2806064 . ПМИД 20161573 .
- ^ Л., Патрик, Грэм (1997). Начало органической химии . Оксфорд: Издательство Оксфордского университета. ISBN 978-0198559368 . ОСЛК 37293506 .
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Jump up to: а б с д Уилкокс, Чарльз Ф.; Люнг, Констанс (1968). «Передача эффектов заместителей. Доминирование эффектов поля». Журнал Американского химического общества . 90 (2): 336–341. дои : 10.1021/ja01004a023 . ISSN 0002-7863 .
- ^ Jump up to: а б с Дьюар, Майкл Дж.С.; Грисдейл, Патрик Дж. (1962). «Эффекты-заместители. I. Введение». Журнал Американского химического общества . 84 (18): 3539–3541. дои : 10.1021/ja00877a023 . ISSN 0002-7863 .
- ^ Jump up to: а б Дейли, Ричард Ф., Дейли, Салли Дж. (2005). Органическая химия (1,3 изд.). Дэйли Пресс.
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Jump up to: а б Сигель, Мишель РФ; Штрейтвизер, Эндрю; Томас, Т. Дарра. (1988). «Роль резонансных и индуктивных эффектов в кислотности карбоновых кислот». Журнал Американского химического общества . 110 (24): 8022–8028. дои : 10.1021/ja00232a011 . ISSN 0002-7863 .
- ^ Парвин, Сальма; Чандра, Асит К.; Зегерс-Хюйскенс, Тереза (2009). «Теоретическое исследование взаимодействия фторированных диметиловых эфиров (nF = 1-5) с водой: роль кислотности и основности в конкуренции между водородными связями OH···O и CH···O». Журнал физической химии А. 113 (21): 6182–6191. Бибкод : 2009JPCA..113.6182P . дои : 10.1021/jp902244j . ISSN 1089-5639 . ПМИД 19422184 .
- ^ Молина, Педро; Сапата, Фабиола; Кабальеро, Антонио (2017). «Стратегии распознавания анионов, основанные на комбинированных нековалентных взаимодействиях». Химические обзоры . 117 (15): 9907–9972. doi : 10.1021/acs.chemrev.6b00814 . ISSN 0009-2665 . ПМИД 28665114 .
- ^ Треска, Блейкли В.; Хансен, Райан Дж.; Чау, Кэлвин В.; Хэй, Бенджамин П.; Захаров Лев Н.; Хейли, Майкл М.; Джонсон, Даррен В. (2015). «Эффекты заместителей во взаимодействиях водородных связей CH: линейные соотношения свободной энергии и влияние анионов» . Журнал Американского химического общества . 137 (47): 14959–14967. дои : 10.1021/jacs.5b08767 . ISSN 0002-7863 . ПМК 4977030 . ПМИД 26539974 .
- ^ Jump up to: а б с д и Коул, Томас В.; Майерс, Кэролайн Дж.; Сток, Леон М. (1974). «Химия бицикло[2.2.2]октанов. XV. Константы диссоциации 4-замещенных кубан-1-карбоновых кислот. Доказательства полевой модели полярного эффекта». Журнал Американского химического общества . 96 (14): 4555–4557. дои : 10.1021/ja00821a032 . ISSN 0002-7863 .
- ^ Прогресс в физико-органической химии, том 13 - Интернет-библиотека Wiley . Успехи физико-органической химии. 1981. doi : 10.1002/9780470171929 . ISBN 9780470171929 .
- ^ Сток, Леон М. (1972). «Происхождение индуктивного эффекта». Журнал химического образования . 49 (6): 400. Бибкод : 1972ЖЧЭд..49..400С . дои : 10.1021/ed049p400 . ISSN 0021-9584 .
- ^ Ханш, Корвин; Лео, А.; Тафт, Р.В. (1991). «Обзор констант заместителей Гаммета, а также параметров резонанса и поля». Химические обзоры . 91 (2): 165–195. дои : 10.1021/cr00002a004 . ISSN 0009-2665 .
- ^ Дьюар, Майкл Дж.С.; Грисдейл, Патрик Дж. (1962). «Эффекты заместителя. IV.1 Количественная теория». Журнал Американского химического общества . 84 (18): 3548–3553. дои : 10.1021/ja00877a026 . ISSN 0002-7863 .
- ^ Jump up to: а б с д Граббс, Э.Дж.; Фицджеральд, Р.; Филлипс, RE; Петти, Р. (1971). «Передача эффектов заместителя в изомерных дихлорэтаномостиковых производных антрацена». Тетраэдр . 27 (5): 935–944. дои : 10.1016/s0040-4020(01)92492-5 .
- ^ Пирсон, Ральф Г. (1963). «Твердые и мягкие кислоты и основания». Журнал Американского химического общества . 85 (22): 3533–3539. дои : 10.1021/ja00905a001 . ISSN 0002-7863 .