Наногель
Наногель субмикронного представляет собой основе полимера сшитую частицу гидрогеля на масштаба . [ 1 ] [ 2 ] [ 3 ] Эти сложные сети полимеров открывают уникальные возможности в области доставки лекарств на стыке наночастиц и синтеза гидрогелей. [ 1 ] [ 2 ] [ 3 ] Наногели могут быть натуральными, синтетическими или комбинацией этих двух и иметь высокую степень настраиваемости с точки зрения их размера, формы, поверхностной функционализации и механизмов деградации. [ 1 ] [ 2 ] [ 3 ] Учитывая эти присущие им характеристики, а также их биосовместимость и способность инкапсулировать небольшие лекарства и молекулы, наногели являются многообещающей стратегией лечения заболеваний и дисфункций, выступая в качестве средств доставки, способных преодолевать сложные физиологические барьеры внутри организма. [ 1 ] [ 2 ] [ 3 ]
Наногели не следует путать с Nanogel аэрогелем , легким теплоизолятором, или с нанокомпозитными гидрогелями (NC-гелями) , которые представляют собой наполненные наноматериалами гидратированные полимерные сети, которые демонстрируют более высокую эластичность и прочность по сравнению с гидрогелями, изготовленными традиционным способом.
Синтез
[ редактировать ]Синтез наногелей может быть достигнут с использованием широкого спектра различных методов. Однако в каждый метод обычно входят два важнейших этапа: полимеризация и сшивание, причем наиболее распространенными являются физическое и химическое сшивание. [ 4 ] Эти этапы могут выполняться одновременно или последовательно в зависимости от метода синтеза и возможного применения наногеля. [ 4 ] Здесь кратко описаны несколько различных механизмов синтеза.

Десольватация/коацервация и осаждение
[ редактировать ]При десольватации или коацервации к гомогенному раствору полимера добавляется нерастворитель для получения индивидуальных наноразмерных полимерных комплексов, диспергированных в том же растворе. [ 3 ] Затем эти комплексы подвергаются сшиванию с образованием наногелей, при этом функционализация поверхности является необязательным следующим шагом. [ 3 ]
При осаждении к гомогенному раствору мономера добавляют инициаторы и сшивающие агенты, чтобы вызвать реакцию полимеризации. [ 4 ] Когда полимерная цепь достигает желаемой длины, реакция останавливается и образуется коллоидная суспензия полимера. [ 2 ] [ 3 ] Поверхностно-активные вещества являются последней добавкой для производства наноразмерных полимеров. [ 2 ] [ 3 ]
Электростатические и гидрофобные взаимодействия.
[ редактировать ]Электростатические взаимодействия могут образовывать наногели за счет сочетания анионных и катионных полимеров в водном растворе. [ 3 ] Размер и поверхностный заряд полученных наногелей можно модулировать путем изменения молекулярной массы или соотношения зарядов двух разных полимеров. [ 3 ] Ионотропное гелеобразование также может использовать электростатические взаимодействия между многовалентными анионами и катионами для образования наногелей. [ 3 ]
Гидрофобные взаимодействия в значительной степени зависят от физического сшивания с образованием наногелей. [ 3 ] В этом методе гидрофобные группы добавляются к гидрофильным полимерам в водном растворе, чтобы вызвать их самосборку в наногели. [ 3 ] Когда для этого процесса получения используются тиолированные полимеры ( тиомеры ), наногели могут быть дополнительно стабилизированы за счет образования меж- и внутрицепочечных дисульфидных связей вследствие окисления . В дальнейшем можно даже удалить противоположно заряженные олиго- или полимеры. [ 5 ] [ 6 ]
обратная эмульсия
[ редактировать ]Обратная эмульсия, или обратная миниэмульсия, требует органического растворителя и поверхностно-активного вещества или эмульгатора. [ 3 ] [ 4 ] Наноразмерные капли образуются, когда водный раствор мономера диспергируется в органическом растворителе в присутствии поверхностно-активного вещества или эмульгатора. [ 3 ] [ 4 ] При удалении органического растворителя и дальнейшем химическом и физическом сшивании капель образуются наногели. [ 3 ] [ 4 ] Размер наногелей, синтезированных этим методом, может сильно варьироваться в зависимости от типа используемого ПАВ и реакционной среды. [ 3 ] Очистка наногелей, полученных с использованием эмульгатора, также может представлять собой проблему. [ 3 ]
Микротемплатная полимеризация
[ редактировать ]Добавление раствора предшественника мономера и сшивающего агента в микрошаблон или устройство типа пресс-формы может инициировать полимеризацию и образование наногелей. [ 4 ] Этот метод можно использовать для создания наногелей определенной формы и наполнения их различными небольшими молекулами. [ 4 ] Полимеризация литографических микрошаблонов — это аналогичный процесс, в котором используется фотоинициатор и свет для запуска образования наногелей. [ 4 ] Литографическая полимеризация микрошаблонов позволяет производить наногели меньшего размера с длиной менее 200 нм, что имеет более высокое разрешение по сравнению с полимеризацией микрошаблонов, не требующей фотоинициатора. [ 4 ]
Сшивающие мицеллы
[ редактировать ]Мицеллы на основе полимеров, которые подвергаются реакциям сшивки, могут индуцировать образование наногелей. [ 3 ] [ 7 ] Сшивка ядра или оболочки ранее существовавших мицелл позволяет синтезировать наногели с «высокой степенью пространственной организации». [ 3 ] [ 7 ]
Состав и структура
[ редактировать ]Материалы
[ редактировать ]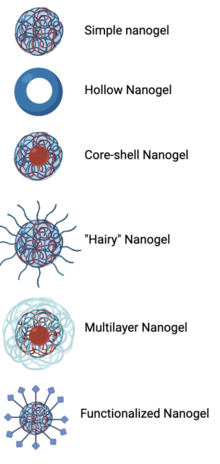
Поскольку биоразлагаемость является важной характеристикой наногелей, эти гидрогели обычно состоят из природных или разлагаемых синтетических полимеров. [ 3 ] Полисахариды и белки в значительной степени доминируют в природных формах полимеров, используемых для синтеза наногелей. [ 2 ] [ 3 ] Благодаря использованию тиолированных полисахаридов ( тиомеров ), таких как тиолированный хитозан или тиолированная гиалуроновая кислота. [ 8 ] [ 9 ] наногели можно стабилизировать за счет внутри- и межкаиновых дисульфидных связей. Преимущества наногелей на основе природных полимеров включают биосовместимость и способность к разложению за счет клеточных механизмов in vivo. [ 3 ] Природные полимеры также имеют тенденцию быть нетоксичными и биоактивными, поэтому они с большей вероятностью будут вызывать биологические сигналы, управляющие различными аспектами клеточного поведения. [ 3 ] Однако полимеры природного происхождения по-прежнему могут вызывать иммунный ответ и обладают другими недостатками, такими как переменная скорость разложения и гетерогенная структура. [ 3 ] И наоборот, полимеры на синтетической основе имеют более определенную структуру, повышенную стабильность и контролируемую скорость разложения. [ 3 ] По сравнению с полимерами природного происхождения, синтетическим полимерам не хватает биологических сигналов, которые могут быть необходимы для конкретных терапевтических применений. [ 3 ] Учитывая, что природные и синтетические полимеры имеют свой собственный набор преимуществ и недостатков, текущая область исследований направлена на создание композитных гидрогелей для синтеза наногелей, которые сочетают в себе синтетические и природные полимеры для использования преимуществ обоих в одной рецептуре наногеля. [ 3 ]

Структура
[ редактировать ]Структура наногеля зависит от механизма синтеза и его применения. Простые или традиционные наногели представляют собой сшитые полимерные сети размером с наночастицы, которые набухают в воде. [ 3 ] [ 10 ] Полые наногели, состоящие только из внешней оболочки, позволяют увеличить количество загружаемого на платформу груза. [ 3 ] [ 10 ] В других структурах наногеля внутреннее ядро и внешняя оболочка могут быть изготовлены из двух разных материалов, например, гидрофобного внутреннего ядра, окружающего лекарства или другие небольшие молекулы, и гидрофильной внешней оболочки, которая взаимодействует с внешней средой. [ 2 ] [ 3 ] Добавление второго линейного мономера, сшитого к наногелю, считается «волосатым наногелем». [ 2 ] [ 7 ] Различные методы синтеза наногелей могут быть выполнены последовательно для создания многослойных наногелей, например, начиная с ионотропного гелеобразования, а затем объединяя анионные и катионные полимеры в водном растворе. [ 7 ] [ 10 ] Функционализированные наногели, в которых нацеливающие лиганды или чувствительные к стимулам функциональные группы сопряжены с внешней оболочкой наногеля, также важны для некоторых применений наногелей. [ 2 ] [ 3 ] [ 7 ] [ 10 ]
Стимул-чувствительные наногели
[ редактировать ]Наногели могут быть разработаны так, чтобы реагировать на различные стимулы, включая изменения pH и температуры или наличие окислительно-восстановительных и световых сигналов. Тщательно разработанные наногели, реагирующие на стимулы, можно использовать для транспортировки и высвобождения различных типов грузов в определенные ткани организма с увеличением пространственно-временного разрешения.

pH-чувствительные наногели
[ редактировать ]Чувствительные к pH наногели представляют собой привлекательную форму технологии наногелей из-за различных уровней pH в организме. Здоровые ткани имеют pH 7,4, тогда как в опухолях он может достигать 6,5, а в желудке — всего 1,0. [ 10 ] Протонирование или депротонирование определенных функциональных групп может изменить скорость набухания и стабильность наногеля, что приводит к высвобождению инкапсулированного груза при воздействии различных диапазонов pH. [ 2 ] [ 10 ] Например, анионные наногели с группами карбоновой кислоты разрушаются при воздействии pH, который меньше, чем pKa полимера наногеля. [ 2 ] [ 10 ] Аналогично, катионные наногели с концевыми аминогруппами станут протонированными, если pH среды меньше, чем pKa гидрогеля. [ 2 ] [ 10 ] При этом скорость набухания наногеля изменится и он станет более гидрофильным. [ 2 ] [ 10 ] Другие группы также ранее сшивали pH-чувствительные гидразонные связи с наногелями на основе полисахаридов, которые высвобождали полезную нагрузку в кислой среде. [ 11 ]
Температурно-чувствительные наногели
[ редактировать ]Использование термочувствительных полимеров в синтезе наногелей позволяет этим системам реагировать на изменения температуры. [ 1 ] В зависимости от присутствующих химических групп термочувствительные полимеры могут реагировать либо на понижение температуры, либо на повышение температуры. [ 10 ] Как гидрофобные, так и гидрофильные группы обычно присутствуют в термочувствительных полимерных наногелях, которые реагируют на понижение температуры, тогда как наногели, реагирующие на повышение температуры, часто приходится готовить методом наслаивания водородных связей. [ 10 ] Температурно-чувствительные наногели являются потенциальной стратегией, когда терапевтическое средство воздействует на кожу, имеющую естественный температурный градиент, или на область, где наблюдается воспаление. [ 1 ] [ 2 ] [ 10 ]
Редокс-чувствительные наногели
[ редактировать ]Редокс-чувствительные наногели обычно содержат поперечные связи, образованные дисульфидными связями. [ 12 ] или специфические сшивающие агенты. [ 3 ] [ 10 ] Также можно использовать наногели из биоразлагаемых и бифункциональных мономеров. В присутствии восстановителей, таких как глутатион, тиоредоксин и пероксиредоксин, эти наногели реагируют высвобождением своего груза. [ 10 ] [ 13 ] Учитывая, что эти и некоторые другие восстановители обнаруживаются в больших концентрациях внутри клеток по сравнению с их внешней средой, окислительно-восстановительные наногели являются многообещающей стратегией для адресной внутриклеточной доставки. [ 10 ]
Светочувствительные наногели
[ редактировать ]Светочувствительные наногели могут высвобождать свой груз под воздействием света определенной длины волны. [ 10 ] Эти наногели синтезируются так, чтобы содержать специфические связи на основе акрила или кумарина, которые расщепляются во время фотореакции. [ 10 ] Благодаря возможности настройки длины волны света, энергии и времени облучения светочувствительные наногели могут инициировать деградацию с повышенным контролем над плотностью сшивки. [ 10 ] Например, было обнаружено, что набухание и размер светочувствительных наногелей с винильными группами уменьшаются и обеспечивают замедленное высвобождение лекарств после облучения УФ-светом. [ 10 ]
Физиологические реакции на наногели
[ редактировать ]
Биосовместимость, биоразлагаемость и биораспределение
[ редактировать ]Одной из основных проблем, связанных с любой формой системы доставки лекарств, включая наногели, являются потенциальные побочные эффекты и повреждение здоровых тканей, а также негативный иммунный ответ при введении инородного вещества. [ 3 ] [ 7 ] Это должно быть сбалансировано с необходимостью оставаться в обращении в течение достаточного периода времени для доставки груза и оказания терапевтического эффекта. [ 3 ] [ 7 ] Для борьбы со значительным иммунным ответом типичным стандартом являются разлагаемые наногели, поскольку они считаются менее токсичными по сравнению с неразлагаемыми наногелями. [ 3 ] [ 7 ] Податливость и небольшой размер разлагаемых наногелей также позволяют им проходить через кровеносные сосуды и достигать целевой области до потребления иммунными клетками или фильтрации печенью и селезенкой. [ 3 ] [ 7 ]
Механизмы клеточного поглощения
[ редактировать ]После того как наногели выходят из сосудистой сети, они диффундируют через интерстициальное пространство в ткань-мишень. [ 7 ] На клеточном уровне наногели могут интернализоваться посредством большого количества различных типов эндоцитоза, которые зависят от размера, формы и свойств поверхности частиц. [ 3 ] [ 7 ] Эндоцитоз — наиболее распространенный механизм, который начинается с поглощения наногелей клеточной мембраной. [ 3 ] [ 7 ] Наногели транспортируются во внутриклеточных везикулах для доставки в эндосомы, которые в конечном итоге объединяются с лизосомами. [ 3 ] [ 7 ] Как только лизосомы попадают в цитозоль клетки, они немедленно доставляют свой груз или перемещаются в соответствующий клеточный отсек. [ 3 ] [ 7 ]
Приложения
[ редактировать ]Потенциальные применения наногелей включают агенты доставки лекарств , [ 14 ] [ 15 ] [ 16 ] [ 17 ] контрастные вещества для медицинской визуализации или 19 F МРТ , трассеры [ 18 ] наноактюаторы и сенсоры. [ 19 ]
Доставка лекарств
[ редактировать ]Терапия рака
[ редактировать ]В 2022 году только в США прогнозируется более 1,9 миллиона новых случаев рака. [ 20 ] Наногели являются привлекательным решением для доставки лекарств, позволяющим повысить как эффективность лечения рака, так и его локализацию в раковых клетках. Наногели в настоящее время исследуются для лечения различных типов рака, несколько примеров из которых перечислены здесь.
В одном исследовании наногели на основе хитозана, загруженные химиотерапевтическим препаратом доксорубицином, с положительным поверхностным зарядом, продемонстрировали более низкую жизнеспособность клеток колоректального рака по сравнению с контрольными группами и аналогично загруженным наногелем с отрицательным поверхностным зарядом. [ 21 ] Другая группа конъюгировала фолиевую кислоту с наногелями, загруженными цисплатином или доксорубицином, и доставила эти терапевтические средства в клетки рака яичников, которые сверхэкспрессируют рецептор фолиевой кислоты, связывающийся с фолиевой кислотой. [ 22 ] Эти конъюгированные наногели вызвали значительное снижение роста опухоли в мышиной модели по сравнению с контрольной группой носителя и продемонстрировали модель доставки наногелей в сайт-специфическую область, которая может быть эффективной при других типах рака с повышенным уровнем экспрессии фолатных рецепторов. [ 22 ] Интересно, что наногели на основе желатина, загруженные цисплатином и конъюгированные с лигандами рецептора эпидермального фактора роста (EGFR), успешно воздействуют на клетки рака легких как in vitro, так и in vivo, при этом дополнительные исследования подтверждают эффективность этих наногелей при трансформации в аэрозольные частицы. . [ 23 ]

Молекулы на основе нуклеиновых кислот
[ редактировать ]Наногели являются выгодными носителями небольших молекул на основе нуклеиновых кислот, которые можно использовать для лечения различных заболеваний. Здесь обсуждаются примеры трех различных типов молекул, попадающих в эту категорию: олигонуклеотиды, микроРНК и аналоги нуклеозидов.
В одном исследовании катионные синтетические наногели, модифицированные инсулином и трансферрином, были синтезированы для транспортировки олигонуклеотидов, возможного терапевтического и диагностического инструмента нейродегенеративных заболеваний, в мозг. [ 25 ] Эти наногели успешно локализовались на модели гематоэнцефалического барьера in vitro и накапливались в мозге на мышиной модели. [ 25 ] Принимая во внимание лечение сердечно-сосудистых заболеваний, наногели на основе полисахаридов были функционализированы фукоиданом для воздействия на сверхэкспрессированные рецепторы P-селектина на тромбоцитах и эндотелиальных клетках. [ 26 ] После загрузки микроРНК эти наногели связывались с тромбоцитами и интернализовались линией эндотелиальных клеток. [ 26 ] Наногели также использовались для инкапсулирования фосфорилированных аналогов нуклеозидов или активных форм противораковых препаратов. В одном исследовании наногели, наполненные нуклеозид-5'-трифосфатами, претерпели поверхностные модификации и успешно связались со сверхэкспрессированными рецепторами фолиевой кислоты на клетках рака молочной железы. [ 27 ] Эти наногели затем усваивались клетками и вызывали значительное увеличение цитотоксичности по сравнению с контрольными группами. [ 27 ]
Стимул-чувствительные наногели для доставки лекарств
[ редактировать ]Наногели, которые реагируют на различные стимулы, включая изменения pH и температуры или наличие окислительно-восстановительных и световых сигналов, оказались полезными инструментами для доставки лекарств. Один из таких чувствительных наногелей был разработан для переключения с поверхностного отрицательного заряда на поверхностный положительный заряд при воздействии снижения pH внутри опухоли. [ 28 ] При загрузке химиотерапевтического агента эта технология вызывала более низкую жизнеспособность 3D-сфероидов опухоли по сравнению с контрольными группами. [ 28 ] Было обнаружено, что другой тип наногеля, наполненный противовоспалительными препаратами при остеоартрите, значительно увеличивает количество препарата, транспортируемого после местного нанесения на кожу и воздействия ее естественной повышенной температуры. [ 29 ] Одна группа сообщила о методе контроля скорости высвобождения антитромбоцитарного препарата из наногеля с помощью УФ-излучения для изменения плотности сшивки полимера и последующего изменения скорости набухания. [ 30 ] Кроме того, были синтезированы другие наногели, включающие расщепляемые дисульфидами полимеры, которые реагируют на восстановительные сигналы в окружающей среде. [ 31 ] Один такой наногель был загружен химиотерапевтическим агентом и продемонстрировал снижение жизнеспособности клеток по сравнению с бесплатной версией того же агента. [ 31 ]
Визуализация и диагностика
[ редактировать ]Помимо приложений для доставки лекарств, наногели использовались в качестве метода визуализации, поскольку они могут инкапсулировать небольшие красители и другие репортерные молекулы. [ 7 ]

МРТ-изображения
[ редактировать ]Типичные контрастные вещества для МРТ, содержащие гадолиний и марганец, быстро выводятся из организма и несут в себе риск повышенной токсичности. [ 33 ] [ 34 ] Наногели призваны обойти эти ограничения, инкапсулируя эти агенты и повышая их релаксацию или чувствительность. [ 7 ] [ 35 ] В одном исследовании гадолиний-III инкапсулировали в наногель и наблюдали значительное усиление релаксации по сравнению с клинически доступным составом гадолиния-III. [ 36 ] Другая группа разработала pH-чувствительные наногели, содержащие как оксид марганца, так и суперпарамагнитные наночастицы оксида железа, которые успешно визуализировали небольшие опухоли, где pH был более кислым по сравнению с окружающими здоровыми тканями. [ 32 ] Фторсодержащие наногели также можно использовать в качестве индикаторов для 19 F МРТ , поскольку их агрегация и связывание с тканями оказывают лишь незначительное влияние на их 19 F Сигнал МРТ. Более того, они могут переносить лекарства, а их физико-химические свойства полимеров можно сильно модулировать. [ 18 ] [ 37 ] [ 38 ]
ПЭТ-визуализация
[ редактировать ]Подобно МРТ-изображениям, радионуклиды металлов можно загружать в наногели и сшивать для получения радиоиндикаторов ПЭТ для визуализации. [ 7 ] [ 39 ] Наногели, содержащие изотопы меди, обычно используемые для ПЭТ-визуализации, продемонстрировали общую стабильность и накопление в опухолях, что давало более высокий сигнал по сравнению с близлежащими тканями. [ 39 ] В других исследованиях изучались аналогичные технологии с использованием окислительно-восстановительных наногелей, наполненных изотопом галлия и других трехвалентных металлов, для визуализации ПЭТ. [ 40 ] Наногели, состоящие из декстрана, также были разработаны для визуализации опухолеассоциированных макрофагов с помощью радионуклидов и воздействия на кости. [ 41 ] [ 42 ]
Другая оптическая визуализация
[ редактировать ]Для оптической визуализации на основе флуоресценции in vivo наиболее эффективны красители, излучающие волны ближнего ИК-диапазона >700 нм, такие как индоцианин зеленый, но сталкиваются с ограничениями, связанными с уменьшением времени циркуляции и неспецифическим взаимодействием с другими биологическими факторами, влияющими на флуоресценцию. [ 7 ] pH-чувствительные наногели с функционализированными поверхностными рецепторами, нацеленными на раковые клетки, были загружены флуоресцентным красителем, который высвобождался только при эндоцитозе. [ 43 ] Эти наногели успешно генерировали флуоресцентный сигнал изнутри раковых клеток, и многие другие группы разработали аналогичные технологии. [ 7 ] [ 43 ]
Регенеративная медицина
[ редактировать ]
Заживление ран
[ редактировать ]Наногели — это многообещающая технология, которая исследуется для облегчения процесса заживления ран. [ 44 ] Учитывая их способность инкапсулировать различные типы грузов, наногели могут стратегически доставлять противовоспалительные агенты, противомикробные препараты и необходимые факторы роста, чтобы способствовать росту новых тканей и образованию кровеносных сосудов. [ 44 ] В предыдущих исследованиях наногели на основе хитозана продемонстрировали улучшенный эффект заживления ран. [ 44 ] [ 45 ] [ 46 ] Наногели на основе хитозана, инкапсулирующие интерлейкин-2, успешно использовались для стимуляции иммунной системы и ускорения процесса заживления ран. [ 45 ] Кроме того, в одном исследовании in vivo было обнаружено, что наногели на основе хитозана, содержащие антибиотик сульфадиазин серебра, уменьшают размер ожогов второй степени. [ 46 ] В другом исследовании наногели с содержанием серебра были синтезированы в растворе на основе природного полимера, содержащем алоэ вера, и присутствие алоэ вера приводило к ускорению заживления и уменьшению размера ран. [ 47 ] С целью предотвращения инфекции и ускорения процесса заживления одна группа также опубликовала новую конструкцию наногеля, состоящую из инкапсулирующей сердцевины и функциональной внешней поверхности, способной воздействовать на бактерии, присутствующие в ранах. [ 48 ]
Регенерация тканей
[ редактировать ]Для восстановления и регенерации поврежденных тканей были исследованы наногели, которые не только инкапсулируют лекарства и факторы роста для местного введения, но и служат пористыми каркасами в месте имплантации ткани. [ 44 ] Борсодержащие термочувствительные наногели образовывали твердый каркас при инъекции в критический дефект кости и продолжали индуцировать выработку новых клеток остеобластов. [ 49 ] Для лечения последствий инфаркта миокарда в одном исследовании in vivo в термочувствительные наногели вводили сердечные стволовые клетки и наблюдали улучшение сердечной функции за счет увеличения выброса левого желудочка. [ 50 ] Кровеносные сосуды были успешно регенерированы на модели ишемии in vivo с использованием наногелей для инкапсуляции факторов роста эндотелия сосудов. [ 51 ] Наногели на основе гепарина, наполненные факторами роста, также были протестированы при регенерации мышц уретры, вызывающих недержание мочи. [ 52 ]
Другие приложения
[ редактировать ]Датчики
[ редактировать ]Был разработан флуоресцентный наногелевый термометр для измерения температуры в живых клетках с точностью до 0,5 ° C (0,90 ° F). Клетка поглощает воду, когда она холоднее, и выжимает ее, когда ее внутренняя температура повышается; относительное количество воды маскирует или усиливает флуоресценцию наногеля. [ 53 ]
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж Куджино, Хулио Сезар; Бланко, Эрнесто Рафаэль Осорио; Гульотта, Луис Марселино; Альварес Игарсабаль, Сесилия Инес; Кальдерон, Марсело (август 2019 г.). «Преодоление биологических барьеров с помощью наногелей для улучшения доставки лекарств» . Журнал контролируемого выпуска . 307 : 221–246. дои : 10.1016/j.jconrel.2019.06.005 . ПМИД 31175895 . S2CID 182947913 .
- ^ Jump up to: а б с д и ж г час я дж к л м н тот Сухайль, Мухаммед; Розенхольм, Джессика М; Минхас, Мухаммад Усман; Бадшах, Сайед Фейсал; Наим, Абид; Хан, Кифаят Улла; Фахад, Мухаммед (01 ноября 2019 г.). «Наногели как системы доставки лекарств: всесторонний обзор» . Терапевтическая доставка . 10 (11): 697–717. дои : 10.4155/tde-2019-0010 . ISSN 2041-5990 . ПМИД 31789106 . S2CID 208536874 .
- ^ Jump up to: а б с д и ж г час я дж к л м н тот п д р с т в v В х и С аа аб и объявление но из в ах есть также и аль являюсь а к Ли, Юлин; Масиэль, Дина; Родригес, Джон; Ши, Сянъян; Томас, Хелена (26 августа 2015 г.). «Биоразлагаемые полимерные наногели для доставки лекарств/нуклеиновых кислот» . Химические обзоры . 115 (16): 8564–8608. дои : 10.1021/cr500131f . ISSN 0009-2665 . ПМИД 26259712 . S2CID 1651110 .
- ^ Jump up to: а б с д и ж г час я дж Ли, Цуйся; Обиредди, Шрикант Редди; Лай, Вин-Фу (01 января 2021 г.). «Приготовление и использование наногелей в качестве носителей лекарственных средств» . Доставка лекарств . 28 (1): 1594–1602. дои : 10.1080/10717544.2021.1955042 . ISSN 1071-7544 . ПМЦ 8317930 . ПМИД 34308729 .
- ^ Грейндл, М; Бернкоп-Шнурх, А (2006). «Разработка нового метода получения наночастиц тиолированной полиакриловой кислоты». Фарм Рес . 23 (9): 2183–9. дои : 10.1007/s11095-006-9087-1 . ПМИД 16952008 . S2CID 23769149 .
- ^ Бернкоп-Шнурх, А; Генрих, А; Греймель, А (2006). «Разработка нового метода получения субмикронных частиц на основе тиолированного хитозана». Eur J Pharm Биофарм . 63 (2): 166–72. дои : 10.1016/j.ejpb.2006.01.002 . ПМИД 16527469 .
- ^ Jump up to: а б с д и ж г час я дж к л м н тот п д р с Сони, Крути С.; Десейл, Свапнил С.; Бронич, Татьяна К. (октябрь 2016 г.). «Наногели: обзор свойств, биомедицинских применений и препятствий для клинического внедрения» . Журнал контролируемого выпуска . 240 : 109–126. дои : 10.1016/j.jconrel.2015.11.009 . ПМЦ 4862943 . ПМИД 26571000 .
- ^ Федерер, К; Курпирс, М; Бернкоп-Шнурх, А (2021). «Тиолированные хитозаны: универсальный класс полимеров для различных применений» . Биомакромолекулы . 22 (1): 24–56. doi : 10.1021/acs.biomac.0c00663 . ПМК 7805012 . ПМИД 32567846 .
- ^ Гриссер, Дж; Хетеньи, Г; Бернкоп-Шнурх, А (2018). «Тиолированная гиалуроновая кислота как универсальный мукоадгезивный полимер: от химии к разработке продуктов - каковы возможности?» . Полимеры . 10 (3): 243. doi : 10.3390/polym10030243 . ПМК 6414859 . ПМИД 30966278 .
- ^ Jump up to: а б с д и ж г час я дж к л м н тот п д р с Хаджеби, Сакине; Раби, Навид; Багерзаде, Моджтаба; Ахмади, Сепиде; Рабие, Мухаммед; Рогани-Мамакани, Хосейн; Тахрири, Мохаммадреза; Тайеби, Лобат; Хэмблин, Майкл Р. (июль 2019 г.). «Стимул-чувствительные полимерные наногели как умные системы доставки лекарств» . Акта Биоматериалы . 92 : 1–18. doi : 10.1016/j.actbio.2019.05.018 . ПМК 6661071 . ПМИД 31096042 .
- ^ Алканавати, Мохаммад Шафи; Мачтакова Марина; Ландфестер, Катарина; Терьен-Обен, Элоиза (12 июля 2021 г.). «Биоортогональные наногели для мультиреактивного высвобождения» . Биомакромолекулы . 22 (7): 2976–2984. doi : 10.1021/acs.biomac.1c00378 . ISSN 1525-7797 . ПМЦ 8278386 . ПМИД 34129319 .
- ^ Хок, Н; Раканиелло, ГФ; Аспиналл, С; Денора, Н.; Хуторянский, В; Бернкоп-Шнурх, А (2022). «Тиолированные наночастицы для биомедицинских применений: имитация «рабочих лошадок» нашего тела» . Adv Sci (Вейн) . 9 (1): 2102451. doi : 10.1002/advs.202102451 . ПМЦ 8728822 . ПМИД 34773391 .
- ^ Хок, Н; Раканиелло, ГФ; Аспиналл, С; Денора, Н.; Хуторянский, В; Бернкоп-Шнурх, А (2022). «Тиолированные наночастицы для биомедицинских применений: имитация «рабочих лошадок» нашего тела» . Adv Sci (Вейн) . 9 (1): 2102451. doi : 10.1002/advs.202102451 . ПМЦ 8728822 . ПМИД 34773391 .
- ^ Кабанов Александр Владимирович; Виноградов, Сергей В. (2009). «Наногели как фармацевтические носители: конечные сети бесконечных возможностей» . Angewandte Chemie, международное издание . 48 (30): 5418–29. дои : 10.1002/anie.200900441 . ПМЦ 2872506 . ПМИД 19562807 .
- ^ Виноградов, Сергей В (2010). «Наногели в гонке за доставку лекарств». Наномедицина . 5 (2): 165–8. дои : 10.2217/nnm.09.103 . ПМИД 20148627 .
- ^ Наногели для биомедицинских применений, Редакторы: Арти Вашист, Аджит К Кошик, Шариф Ахмад, Мадхаван Наир, Королевское химическое общество, Кембридж, 2018, https://pubs.rsc.org/en/content/ebook/978-1-78801 -048-1
- ^ О, Чон Квон; Драмрайт, Рэй; Зигварт, Дэниел Дж.; Матияшевский, Кшиштоф (2008). «Разработка микрогелей/наногелей для доставки лекарств». Прогресс в науке о полимерах . 33 (4): 448–77. doi : 10.1016/j.progpolymsci.2008.01.002 .
- ^ Jump up to: а б Колоучова Кристина; Жирак, Дэниел; Гроборз, Ондрей; Седлачек, Ондрей; Циолковская, Наталья; Вит, Мартин; Стикова, Ева; Галисова, Андреа; Свец, Павел; Трусил, Иржи; Хаек, Милан; Груби, Мартин (2020). «Имплантатообразующий полимерный МРТ-индикатор 19F с регулируемым растворением». Журнал контролируемого выпуска . 327 : 50–60. дои : 10.1016/j.jconrel.2020.07.026 . ISSN 0168-3659 . ПМИД 32730953 . S2CID 220889066 .
- ^ Рэмдонк, Коэн; Демистер, Джозеф; Де Смедт, Стефан (2009). «Передовая наногелевая инженерия для доставки лекарств». Мягкая материя . 5 (4): 707–715. Стартовый код : 2009SMat....5..707R . дои : 10.1039/b811923f .
- ^ Сигел, Ребекка Л.; Миллер, Кимберли Д.; Фукс, Ханна Э.; Джемаль, Ахмедин (январь 2022 г.). «Статистика рака, 2022» . CA: Журнал рака для врачей . 72 (1): 7–33. дои : 10.3322/caac.21708 . ISSN 0007-9235 . ПМИД 35020204 . S2CID 245878846 .
- ^ Фэн, Чао; Ли, Цзин; Конг, Мин; Лю, Я; Ченг, Сяо Цзе; Ли, Ян; Пак, Хён Джин; Чен, Си Гуан (апрель 2015 г.). «Влияние поверхностного заряда на мукоадгезию наногелей на основе хитозана для местной доставки лекарств против колоректального рака» . Коллоиды и поверхности B: Биоинтерфейсы . 128 : 439–447. дои : 10.1016/j.colsurfb.2015.02.042 . ПМИД 25769283 .
- ^ Jump up to: а б Нуколова Наталья Владимировна; Оберой, Хардип С.; Коэн, Сэмюэл М.; Кабанов Александр Владимирович; Бронич, Татьяна К. (01 августа 2011 г.). «Наногели, декорированные фолатами, для таргетной терапии рака яичников» . Биоматериалы . 32 (23): 5417–5426. doi : 10.1016/j.bimaterials.2011.04.006 . ISSN 0142-9612 . ПМЦ 3255291 . ПМИД 21536326 .
- ^ Ценг, Чинг-Ли; Су, Вэнь-Юнь; Йен, Ко-Чунг; Ян, Кай-Чан; Линь, Фэн-Хуэй (1 июля 2009 г.). «Использование носителя наночастиц желатина, модифицированного биотинилированным ЭФР, для усиления накопления цисплатина в раковых легких путем ингаляции» . Биоматериалы . 30 (20): 3476–3485. doi : 10.1016/j.bimaterials.2009.03.010 . ISSN 0142-9612 . ПМИД 19345990 .
- ^ Нуколова Наталья Владимировна; Оберой, Хардип С.; Коэн, Сэмюэл М.; Кабанов Александр Владимирович; Бронич, Татьяна К. (август 2011 г.). «Наногели, декорированные фолатом, для таргетной терапии рака яичников» . Биоматериалы . 32 (23): 5417–5426. doi : 10.1016/j.bimaterials.2011.04.006 . ISSN 0142-9612 . ПМЦ 3255291 . ПМИД 21536326 .
- ^ Jump up to: а б Vinogradov, Serguei V.; Batrakova, Elena V.; Kabanov, Alexander V. (2004-01-01). "Nanogels for Oligonucleotide Delivery to the Brain" . Bioconjugate Chemistry . 15 (1): 50–60. doi : 10.1021/bc034164r . ISSN 1043-1802 . PMC 2837941 . PMID 14733583 .
- ^ Jump up to: а б Мораес, Фернанда Дж.; Марсело Фореро Рамирес, Лаура; Айде, Рашида; Бенадда, Самира; Мэр Мюриэль; Шовьер, Седрик; Антунес, Джоана К.; Шобе, Фредерик; Летурнер, Дидье (март 2021 г.). «P-селектин, нацеленный на наногели на основе полисахаридов, для доставки микроРНК» . Международный фармацевтический журнал . 597 : 120302. doi : 10.1016/j.ijpharm.2021.120302 . ПМИД 33540032 . S2CID 231821009 .
- ^ Jump up to: а б Виноградов С; Земан, А; Батракова Е; Кабанов, А (20 сентября 2005 г.). «Композиции Полиплекс Наногель для доставки препаратов цитотоксических аналогов нуклеозидов» . Журнал контролируемого выпуска . 107 (1): 143–157. дои : 10.1016/j.jconrel.2005.06.002 . ПМЦ 1357595 . ПМИД 16039001 .
- ^ Jump up to: а б Ли, Синь; Ли, Хелин; Чжан, Чанчан; Пич, Андрей; Син, Линси; Ши, Сянъян (октябрь 2021 г.). «Интеллектуальные наногели с самоадаптирующейся реакцией для улучшения доставки противоопухолевых лекарств и усиления химиотерапии» . Биоактивные материалы . 6 (10): 3473–3484. doi : 10.1016/j.bioactmat.2021.03.021 . ПМК 8024537 . ПМИД 33869898 .
- ^ Завгородня, Александра; Кармона-Моран, Карлос А.; Козловская Вероника; Лю, Фэй; Уик, Тимоти М.; Харлампиева, Евгения (ноябрь 2017 г.). «Температурно-чувствительные многослойные наногели поли(N-винилкапролактама) для местной доставки лекарств» . Журнал коллоидной и интерфейсной науки . 506 : 589–602. Бибкод : 2017JCIS..506..589Z . дои : 10.1016/j.jcis.2017.07.084 . ПМИД 28759859 .
- ^ Он, Цзе; Тонг, Ся; Чжао, Юэ (14 июля 2009 г.). «Фотореактивные наногели на основе фотоуправляемых сшивок» . Макромолекулы . 42 (13): 4845–4852. Бибкод : 2009МаМол..42.4845H . дои : 10.1021/ma900665v . ISSN 0024-9297 .
- ^ Jump up to: а б Ли, Пей-Юань; г-н Му, Хо-Йи; Сяо, Ли-Вэнь; Ху, Цзинь-Цзя; Ян, Дженг-Шиунг (апрель 2017 г.). «Наногели, содержащие восстанавливающе-расщепляемые полимеры для индуцированной глутатионом внутриклеточной доставки куркумина» . Журнал исследований полимеров . 24 (5): 66. дои : 10.1007/s10965-017-1207-6 . ISSN 1022-9760 . S2CID 89633225 .
- ^ Jump up to: а б , Ся, Декао, Бао, Сун; Лю, Сяохан, Шэнцзянь; Ван, Циган (июнь 2015 г.). Ван «Отзывчивые магнитно-резонансные » вещества контрастные 53 349–357 : . 10.1016/ . PMID 25890733 j.bimaterials.2015.02.101
- ^ Сяо, Дж.; Тянь, XM; Ян, К.; Лю, П.; Луо, Северная Каролина; Лян, Ю.; Ли, Х.Б.; Чен, Д.Х.; Ван, CX; Ли, Л.; Ян, GW (05 декабря 2013 г.). «Сверхвысокая релаксация и безопасные зонды наночастиц оксида марганца для визуализации in vivo» . Научные отчеты . 3 (1): 3424. Бибкод : 2013NatSR...3E3424X . дои : 10.1038/srep03424 . ISSN 2045-2322 . ПМК 4070373 . ПМИД 24305731 .
- ^ Эме, Сильвио; Караван, Питер (декабрь 2009 г.). «Биораспределение контрастных веществ на основе гадолиния, включая отложение гадолиния» . Журнал магнитно-резонансной томографии . 30 (6): 1259–1267. дои : 10.1002/jmri.21969 . ПМЦ 2822463 . ПМИД 19938038 .
- ^ Жак, Винсент; Дюма, Стефан; Сунь, Вэй-Чуань; Тротон, Джеффри С.; Гринфилд, Мэтью Т.; Караван, Питер (октябрь 2010 г.). «Высокорелаксирующие контрастные вещества для магнитно-резонансной томографии. Часть 2: Оптимизация релаксации внутренней и второй сферы» . Исследовательская радиология . 45 (10): 613–624. дои : 10.1097/RLI.0b013e3181ee6a49 . ISSN 0020-9996 . ПМК 3024144 . ПМИД 20808234 .
- ^ Сулеймани, Абдолрасул; Мартинес, Франциско; Экономопулос, Василики; Фостер, Паула Дж.; Шолль, Тимоти Дж.; Гиллис, Элизабет Р. (23 января 2013 г.). «Сшивание полимеров: подход наногеля к усилению релаксации контрастных веществ для МРТ» . Журнал химии материалов Б. 1 (7): 1027–1034. дои : 10.1039/C2TB00352J . ISSN 2050-7518 . ПМИД 32262367 .
- ^ Бабука, Дэвид; Колоучова Кристина; Гроборз, Ондрей; Тоснер, Зденек; Жигунов Александр; Степанек, Петр; Груби, Мартин (2020). «Внутренняя структура термочувствительного физически сшитого наногеля поли[N-(2-гидроксипропил)метакриламид]-блок-поли[N-(2,2-дифторэтил)акриламид], известный индикатор 19F для МРТ» . Наноматериалы . 10 (11): 2231. дои : 10.3390/nano10112231 . ISSN 2079-4991 . ПМЦ 7698257 . ПМИД 33182714 .
- ^ Бабука, Дэвид; Колоучова Кристина; Хруби, Мартин; Гроборз, Ондрей; Тоснер, Зденек; Жигунов Александр; Степанек, Петр (2019). «Исследование внутренней структуры термочувствительных наночастиц диблочного сополимера поли(2-метил-2-оксазолин)-b-поли[N-(2,2-дифторэтил)акриламида]». Европейский журнал полимеров . 121 : 109306. doi : 10.1016/j.eurpolymj.2019.109306 . ISSN 0014-3057 . S2CID 208729238 .
- ^ Jump up to: а б Люкс, Жак; Белый, Александр Г.; Чан, Минни; Андерсон, Кэролайн Дж.; Альмутаири, Ада (2015). «Наногели из металл-хелатирующих сшивающих агентов как универсальные платформы, применяемые для ПЭТ-визуализации опухолей и метастазов с медью-64» . Тераностика . 5 (3): 277–288. дои : 10.7150/thno.10904 . ISSN 1838-7640 . ПМК 4279191 . ПМИД 25553115 .
- ^ Сингх, Смрити; Бингёль, Бахар; Моргенрот, Агнешка; Моттаги, Феликс М.; Мёллер, Мартин; Шмальйоханн, Йорн (12 апреля 2013 г.). «Радиомеченные наногели для ядерной молекулярной визуализации» . Макромолекулярная быстрая связь . 34 (7): 562–567. дои : 10.1002/marc.201200744 . ПМИД 23423755 .
- ^ Келихер, Эдмунд Дж.; Йоу, Чонсу; Нарендорф, Матиас; Льюис, Джейсон С.; Маринелли, Бретт; Ньютон, Андита; Питтет, Микаэль Дж.; Вайсследер, Ральф (2011). «Наночастицы декстрана, меченные 89Zr, позволяют визуализировать макрофаги vivo» . Биоконъюгатная химия . 22 (12): 2383–9. дои : 10.1021/bc200405d . ПМК 3244512 . ПМИД 22035047 .
- ^ Хеллер, Дэниел А.; Леви, Яир; Пелет, Джейса М.; Долофф, Джошуа К.; Уоллас, Жасмин; Пратт, Джордж В.; Цзян, Шан; Сахай, Гаурав; Шредер, Ави; Шредер, Джош Э.; Чьян, Йеу; Зуренко, Кристофер; Кербес, Уильям; Мансано, Мигель; Кохане, Дэниел С.; Лангер, Роберт; Андерсон, Дэниел Г. (2013). «Модульные наногели, нацеленные на кость, с эффектом «защелкивания в эмульсии»» (PDF) . Продвинутые материалы . 25 (10): 1449–54. Бибкод : 2013AdM....25.1449H . дои : 10.1002/adma.201202881 . ПМЦ 3815631 . ПМИД 23280931 .
- ^ Jump up to: а б Пак, Хе Сон; Ли, Чон Ын; Чо, Ми Ён; Хон, Джи Хён; Чо, Сан Хи; Лим, Ён Тайк (26 сентября 2012 г.). «Полимерные наногели гиалуроновой кислоты/поли(β-аминоэфира) для переключения NIR-флуоресценции, специфичного для раковых клеток» . Макромолекулярная быстрая связь . 33 (18): 1549–1555. дои : 10.1002/marc.201200246 . ПМИД 22753358 .
- ^ Jump up to: а б с д Гримаудо, Мария Аврора; Коншейру, Анхель; Альварес-Лоренцо, Кармен (ноябрь 2019 г.). «Наногели для регенеративной медицины» . Журнал контролируемого выпуска . 313 : 148–160. дои : 10.1016/j.jconrel.2019.09.015 . ПМИД 31629040 . S2CID 204799512 .
- ^ Jump up to: а б Аслан, Джанан; Челеби, Невин; Дегим, И. Тунцер; Атак, Айшегюль; Озер, Чигдем (май 2017 г.). «Разработка наногелей на основе хитозана, нагруженных интерлейкином-2, с использованием искусственных нейронных сетей и исследование влияния на заживление ран у крыс» . AAPS PharmSciTech . 18 (4): 1019–1030. дои : 10.1208/s12249-016-0662-4 . ISSN 1530-9932 . ПМИД 27853994 . S2CID 4728172 .
- ^ Jump up to: а б Эль-Феки, Джина С.; Эль-Банна, Салли Т.; Эль-Бахи, Г.С.; Абдельразек, ЕМ; Камаль, Мустафа (декабрь 2017 г.). «Хитозановый наногель с альгинатным покрытием для контролируемой местной доставки сульфадиазина серебра» . Углеводные полимеры . 177 : 194–202. дои : 10.1016/j.carbpol.2017.08.104 . ПМИД 28962758 .
- ^ Анджум, Садия; Гупта, Амлан; Шарма, Дипика; Гаутам, Дипти; Бхан, Сурья; Шарма, Анупама; Капил, Арти; Гупта, Бхуванеш (июль 2016 г.). «Разработка новых систем ухода за ранами на основе наносеребра, наногидрогелей полиметакриловой кислоты с алоэ вера и куркумином» . Материаловедение и инженерия: C . 64 : 157–166. дои : 10.1016/j.msec.2016.03.069 . ПМИД 27127040 .
- ^ Аль-Авади, Мохаммед Дж.; Фоше, Аделаида; Гринуэй, Джиллиан М.; Паунов, Веселин Н. (04 октября 2017 г.). «Усиленное антимикробное действие берберина в наногелевых носителях с катионной поверхностной функциональностью» . Журнал химии материалов Б. 5 (38): 7885–7897. дои : 10.1039/C7TB02262J . ISSN 2050-7518 . ПМИД 32264390 . S2CID 55012690 .
- ^ Чжан, Цяо; Чен, Сяохуэй; Гэн, Шинан; Вэй, Линфэй; Мирон, Ричард Дж.; Чжао, Яньбин; Чжан, Юфэн (апрель 2017 г.). «Скаффолды на основе наногеля, изготовленные для регенерации кости с мезопористым биоактивным стеклом и стронцием: характеристика in vitro и in vivo: БИОАКТИВНЫЕ МАШИНЫ ДЛЯ РЕПАРАТА КОСТНЫХ ДЕФЕКТОВ» . Журнал исследований биомедицинских материалов, часть A. 105 (4): 1175–1183. дои : 10.1002/jbm.a.35980 . ПМИД 27998017 .
- ^ Тан, Цзюньнань; Цуй, Сяолинь; Каранасос, Томас Г.; Хенсли, М. Тейлор; Вандергрифф, Адам С.; Хартанто, Юсак; Шен, Делян; Чжан, Ху; Чжан, Цзинин; Ченг, Кэ (24 октября 2017 г.). «Восстановление сердца с использованием инкапсулированных в наногель человеческих сердечных стволовых клеток у мышей и свиней с инфарктом миокарда» . АСУ Нано . 11 (10): 9738–9749. дои : 10.1021/acsnano.7b01008 . ISSN 1936-0851 . ПМК 5656981 . ПМИД 28929735 .
- ^ Ян, Хан На; Чхве, Чон Хун; Пак, Джи Сон; Чон, Су Ён; Пак, Ки Дон; Пак, Гын-Хонг (май 2014 г.). «Дифференциация эндотелиальных клеток-предшественников в эндотелиальные клетки с помощью модифицированных гепарином супрамолекулярных плюроновых наногелей, инкапсулирующих bFGF и образующих комплекс с генами VEGF165» . Биоматериалы . 35 (16): 4716–4728. doi : 10.1016/j.bimaterials.2014.02.038 . ПМИД 24630837 .
- ^ Пак, Кён Мин; Сын Джу Ён; Чхве, Чон Хун; Ким, Ин Гюль; Ли, Юнки; Ли, Джи Юль; Пак, Ки Дон (9 июня 2014 г.). «Композит макро/наногеля как инъекционный и биоактивный наполнитель для лечения недержания мочи» . Биомакромолекулы . 15 (6): 1979–1984. дои : 10.1021/bm401787u . ISSN 1525-7797 . ПМИД 24739122 .
- ^ Гота, Чи; Окабе, Коки; Фунацу, Такаши; Харада, Йоши; Утияма, Сейичи (2009). «Гидрофильный флуоресцентный наногелевый термометр для внутриклеточной термометрии». Журнал Американского химического общества . 131 (8): 2766–7. дои : 10.1021/ja807714j . ПМИД 19199610 .
Дальнейшее чтение
[ редактировать ]- Да, Яньци; Ю, Цзичэн; Гу, Чжэнь (2015). «Универсальные белковые наногели, полученные полимеризацией in situ». Макромолекулярная химия и физика . 217 (3): 333–343. дои : 10.1002/macp.201500296 .
- Ян, Мин; Ге, Джун; Лю, Чжэн; Оуян, Пинкай (2006). «Инкапсуляция одного фермента в наногель с повышенной биокаталитической активностью и стабильностью». Журнал Американского химического общества . 128 (34): 11008–9. дои : 10.1021/ja064126t . ПМИД 16925402 .
- Риз, Чад Э.; Михонин Александр Владимирович; Каменицкий, Марта; Тихонов, Александр; Ашер, Сэнфорд А. (2004). «Наногель-наносекундное фотонно-кристаллическое оптическое переключение». Журнал Американского химического общества . 126 (5): 1493–6. дои : 10.1021/ja037118a . ПМИД 14759207 .
- Ли, Ын Сон; Ким, Донгин; Ён, Ю Сок; О, Кён Тэк; Пэ, Ю Хан (2008). «Вирус-миметический наногель» . Angewandte Chemie, международное издание . 47 (13): 2418–21. дои : 10.1002/anie.200704121 . ПМК 3118583 . ПМИД 18236507 .
- Хасэгава, Урара; Номура, Син-Ичиро М.; Каул, Сунил К.; Хирано, Такаши; Акиёси, Казунари (2005). «Гибридные наночастицы наногель-квантовые точки для визуализации живых клеток». Связь с биохимическими и биофизическими исследованиями . 331 (4): 917–21. дои : 10.1016/j.bbrc.2005.03.228 . ПМИД 15882965 .
- Ду, Цзинь-Чжи; Сунь, Тянь-Мэн; Сун, Вэнь-Цзин; Ву, Хуан; Ван, июнь (2010). «Наногель с преобразованием заряда, активируемый опухолевой кислотностью, как интеллектуальное средство для стимулирования поглощения опухолевыми клетками и доставки лекарств». Angewandte Chemie, международное издание . 49 (21): 3621–6. дои : 10.1002/anie.200907210 . ПМИД 20391548 .