Нитрон-олефиновое (3+2) циклоприсоединение
Реакция циклоприсоединения нитрон -олефин (3+2) представляет собой комбинацию нитрона с алкеном или алкином с образованием изоксазолина или изоксазолидина посредством процесса (3+2) циклоприсоединения . [ 1 ] Эта реакция представляет собой 1,3-диполярное циклоприсоединение , в котором нитрон выступает в роли 1,3-диполя , а алкен или алкин — в роли диполярофила.
Механизм и стереохимия
[ редактировать ]При соединении нитронов с алкенами или алкинами циклоприсоединение (3+2) приводит к образованию нового Связь C–C и новая связь C–O. Циклоприсоединения стереоспецифичны по отношению к конфигурации алкен; однако диастереоселективность в реакциях С-замещенных нитронов часто бывает низкой. [ 2 ] Региоселективность контролируются доминирующими граничными орбиталями, взаимодействующими в ходе реакции, и субстратами с электронными отдельные заместители имеют тенденцию реагировать с высокой региоселективностью. Использовались внутримолекулярные варианты реакции. синтезировать сложные поликлинные углеродные каркасы. Восстановление связи N–O приводит к образованию 1,3-аминоспиртов.

Само (3+2) циклоприсоединение представляет собой согласованное, перициклический процесс, региохимия которого контролируются граничными молекулярными орбиталями на нитрон (диполь) и диполярофил. [ 3 ] Когда R' представляет собой электронодонорную группу, алкил, или арил, доминирующими FMO являются ВЗМО диполярофил и НСМО нитрона. Таким образом, соединяя атомы, коэффициенты которых на этих орбиталях самые большие 5-замещенные Предполагается, что изоксазолидин будет преобладать. На с другой стороны, когда диполярофил беден электронами, ВЗМО- нитрон -ЛЮМО- диполярофил взаимодействие является наиболее важным, и 4-замещенный продукт имеет преимущество.

Область применения и ограничения
[ редактировать ]Алкильные и арильные концевые алкены реагируют с высокой региоселективностью с образованием 5-замещенных изоксазолидинов. Этот результат согласуется с пограничным молекулярно-орбитальным (кинетическим) контролем распределения изомеров: кислород нитрона, который обладает наибольшим орбитальным коэффициентом в ВЗМО нитрона, образует связь с внутренним углеродом алкена, который обладает наибольшим орбитальным коэффициентом в ВЗМО нитрона. орбитальный коэффициент в НСМО алкена. [ 4 ]

Конфигурация 1,2-дизамещенных алкенов сохраняется в продуктах циклоприсоединения. В соответствии с контролем реакции FMO, более электроноакцепторный заместитель на этих субстратах оказывается в 4-м положении продукта. Иными словами, углерод с наибольшим коэффициентом НСМО в диполярофиле (удаленный от электроноакцепторной группы) образует связь с кислородом нитрона, который обладает наибольшим коэффициентом ВЗМО в нитроне. [ 5 ]

Алкины также могут выступать в роли диполярофилов в этой реакции. Правила прогнозирования продуктов циклоприсоединения алкенов на основе соответствующих FMO применимы и к замещенным алкинам: алкины с низким содержанием электронов имеют тенденцию давать 4-замещенные продукты, тогда как богатые электронами, алкильные и арилалкины дают 5-замещенные продукты. [ 6 ]

Внутримолекулярные варианты реакции весьма полезны для синтеза сложных полициклических каркасов. Эти реакции обычно протекают при гораздо более низких температурах, чем межмолекулярные циклоприсоединения. Региохимию сложнее предсказать для внутримолекулярных реакций: могут образовываться либо мостиковые, либо конденсированные продукты, как цис- , так и трансконденсированные кольца. возможны [ 7 ]

Существующий стереоцентр в связке между алкеном и нитроном часто приводит к образованию единственного диастереомера продукта. В этом примере более объемный фенильный заместитель оказывается на экзо -грани бициклической кольцевой системы. [ 8 ]

Синтетические приложения
[ редактировать ]Синтез (±)-люпинина
[ редактировать ]2,3,4,5-Тетрагидропиридин-1-оксид может быть использован для создания плавленых гетероциклы в алкалоидах и других природных продуктах. Синтез (±) -люпинина использует расширяющий кольцо перегруппировка мезилата, обеспечивающая быстрый доступ к мишени. [ 9 ]

Синтез гидроксикотинина
[ редактировать ]Структура гидроксикотинина, человеческого метаболита никотина, была подтверждена независимыми исследованиями. синтез с использованием нитрон-олефинового циклоприсоединения. [ 10 ]

Синтез (+)-порантеридина
[ редактировать ]Перегруппировка (3+2) циклоаддукта дает (+)-порантеридин. [ 11 ] Циклоаддукт подвергается гидрирование, кислотный гидролиз, окисление, основной гидролиз и циклизация с получением цели.

Реакция Кинугасы с образованием β-лактамов
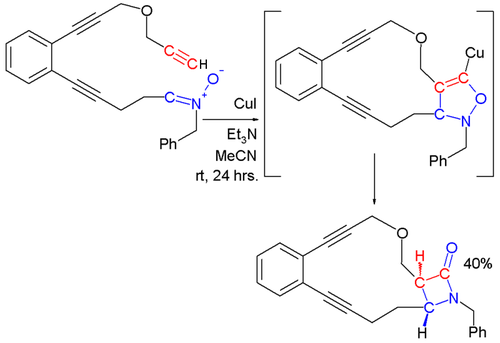
[ редактировать ]В реакции Кинугаса нитрон и меди ацетилид реагируют с образованием β-лактама . [ 12 ] [ 13 ] На первой стадии этой реакции в результате реакции концевого алкина с солью меди образуется ацетилид металла. 1,3-диполярное циклоприсоединение нитрона к ацетилиду металла приводит к образованию 5-членного кольца, которое перегруппировывается с образованием β-лактама.
Другие реакции
[ редактировать ]Другим примером циклоприсоединения (3+2) является то, при котором аддукт Бейлиса-Хиллмана является диполярофилом. Он реагирует с C-фенил-N-метилнитроном с образованием изоксазолидина . [ 14 ]
Ссылки
[ редактировать ]- ^ Конфалоне, ПН; Сегодня EM Org. Реагировать. 1988 , 36 , 1. два : 10.1002/0471264180.or036.01
- ^ Туфариелло, Джей Джей; Али, ЮАР; Клингеле. HO J. Org. хим. 1979 , 44 , 4213.
- ^ Хоук, KN J. Am. Ткань. Соц. 1972 , 94 , 8953.
- ^ Huisgen, R.; Hauck, H.; Grashey, R.; Seidl, H. Chem. Ber. 1968 , 101 , 2568.
- ^ Жукла, М. Тетраэдр 1973 , 29 , 2315.
- ^ Винтерфельдт, Э.; Крон, В.; Штраке, H. Chem. 1969 , 102 , 2346.
- ^ LeBel, N. A.; Post, M. E.; Whang, J. J. J. Am. Chem. Soc. 1964 , 86 , 3759–3767. два : 10.1021/ja01072a031
- ^ Виник, Ф.Дж.; Фенглер, IE; Гшвенд, HW J. Org. хим. 1977 , 42 , 2936.
- ^ Туфариелло, Джей Джей; Тегелер, Дж. Дж. Тетраэдр Летт. , 1976 , 4037–4040. два : 10.1016/S0040-4039(00)92569-3
- ^ Дань, Э.; Кастаньоли-младший, Нью- Джерси Мед. хим. 1972 , 15 , 356–360. два : 10.1021/jm00274a005
- ^ Госсинджер, Э. Тетраэдр Летт. 1980 , 21 , 2229.
- ^ Реакции фенилацетилида меди (I) с нитронами Манабу Кинугаса и Сидзунобу Хасимото J. Chem. Соц., хим. Коммун., 1972 , 466 – 467, два : 10.1039/C39720000466
- ^ Новый синтез циклических ендиинов, слитых с β-лактамами, с помощью внутримолекулярной реакции Кинугасы Runa Pal и Amit Basak Chem. Общий. , 2006 , 2992 - 2994, два : 10.1039/b605743h
- ^ Диастереоселективность 1,3-диполярного циклоприсоединения нитрона к аддуктам Бейлиса-Хиллмана Бранислав Дугович, Любор Фишера, Кристиан Хаметнер и Нада Пронайовац. Аркивок 2004 BS-834A Артикул