Значение

Значения A — это числовые значения, используемые при определении наиболее стабильной ориентации атомов в молекуле ( конформационный анализ ), а также для общего представления стерического объема . Значения A получены на основе измерений энергии различных конформаций циклогексана монозамещенного химического вещества циклогексана. [1] Заместители в циклогексановом кольце предпочитают располагаться в экваториальном положении, а не в аксиальном. Разница в свободной энергии Гиббса (ΔG) между конформацией с более высокой энергией (аксиальное замещение) и конформацией с более низкой энергией (экваториальное замещение) представляет собой значение A для этого конкретного заместителя.
Утилита
[ редактировать ]Значения A помогают предсказать конформацию циклогексановых колец. Наиболее стабильной конформацией будет та, которая имеет экваториальный заместитель или заместители. Когда принимаются во внимание несколько заместителей, предпочтительна конформация, в которой заместитель с наибольшим значением А является экваториальным.

Полезность значений A можно обобщить для использования за пределами конформаций циклогексана. Значения A могут помочь предсказать стерический эффект заместителя. В общем, чем больше значение А заместителя, тем больше стерический эффект этого заместителя. Метильная группа имеет значение A 1,74, а трет- бутильная группа имеет значение A ~5. Поскольку значение А трет -бутила выше, трет -бутил оказывает больший стерический эффект, чем метил. Эту разницу в стерических эффектах можно использовать для прогнозирования реакционной способности химических реакций.
Соображения о свободной энергии
[ редактировать ]Стерические эффекты играют важную роль в определении конфигураций циклогексанов. Можно использовать стерические препятствия, чтобы определить склонность заместителя находиться в аксиальной или экваториальной плоскости. Известно, что аксиальные связи более затруднены, чем соответствующие экваториальные связи. Это связано с тем, что заместители в аксиальном положении относительно близки к двум другим аксиальным заместителям. Это делает его очень скученным, когда объемистые заместители ориентированы в аксиальном положении. Эти типы стерических взаимодействий широко известны как 1,3-диаксиальные взаимодействия. [2] Эти типы взаимодействий отсутствуют с заместителями в экваториальном положении.
Обычно рассматриваются три основных вклада в конформационную свободную энергию : [3]
- Деформация Байера , определяемая как деформация, возникающая в результате деформации валентных углов.
- Деформация Питцера , определяемая как деформация кручения, возникающая в результате 1,2-взаимодействий между группами, прикрепленными к соседним атомам углерода,
- Взаимодействия Ван-дер-Ваальса , которые аналогичны 1,3-диаксиальным взаимодействиям.
Энтальпийные компоненты
[ редактировать ]При сравнении относительной стабильности взаимодействия 6- и 7-атомов можно использовать для аппроксимации различий в энтальпии между конформациями. Каждое взаимодействие 6 атомов стоит 0,9 ккал/моль (3,8 кДж/моль), а каждое взаимодействие 7 атомов — 4 ккал/моль (17 кДж/моль). [4]
Энтропийные компоненты
[ редактировать ]Энтропия также играет роль в предпочтении заместителем экваториального положения. Энтропийная составляющая определяется по следующей формуле:
Где σ равно количеству микросостояний, доступных для каждой конформации.

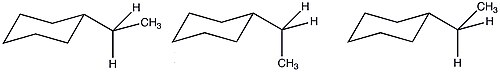
Из-за большего количества возможных конформаций этилциклогексана значение A снижается по сравнению с тем, которое можно было бы предсказать, исходя исключительно из энтальпийных показателей. Благодаря этим благоприятным энтропийным условиям стерическая значимость этильной группы аналогична стерической значимости метильного заместителя.
Таблица значений A
[ редактировать ]| заместитель | Значение А | заместитель | Значение А | заместитель | Значение А | ||
|---|---|---|---|---|---|---|---|
| Д | 0.006 | CH 2 Бр | 1.79 | ОСи(СН 3 ) 3 | 0.74 | ||
| Ф | 0.15 | СН(СН 3 ) 2 | 2.15 | ОЙ | 0.87 | ||
| кл. | 0.43 | сС 6 Ч 11 | 2.15 | ОЧ 3 | 0.6 | ||
| Бр | 0.38 | С(СН 3 ) 3 | >4 | ОКР 3 | 0.56 | ||
| я | 0.43 | Ph | 3 | OCH2CHOCH2CH3 | 0.9 | ||
| Китай | 0.17 | СО 2 Н | 1.35 | О-И | 0.6 | ||
| Северная Каролина | 0.21 | СО 2 − | 1.92 | О-ТФА | 0.68 | ||
| унтер-офицер | 0.51 | СО 2 СН 3 | 1.27 | ВОСЕМЬ | 0.27 | ||
| НКС | 0.28 | СО 2 Эт | 1.2 | О-Ц | 0.5 | ||
| Н=К=НР | 1 | СО 2 я Пр | 0.96 | ОНО 2 | 0.59 | ||
| СН 3 | 1.7 | COCl | 1.25 | НХ 2 | 1.6 | ||
| CFCF3 | 2.1 | КОЧ 3 | 1.17 | НХЧ 3 | 1 | ||
| CH2CHCH2CH3 | 1.75 | Ш.Х. | 0.9 | Н(СН 3 ) 2 | 2.1 [10] | ||
| СН=СН 2 | 1.35 | МСП | 0.7 | НХ 3 + | 1.9 | ||
| КСН | 0.41 | СПФ | 0.8 | НЕТ 2 | 1.1 | ||
| СН 2 т Этот | 2 | С − | 1.3 | HgBr | ~0 | ||
| Ч 2 ОЦ | 1.75 | СОФ | 1.9 | HgCl | 0.3 | ||
| СО 2 Ф. | 2.5 | Си(СН 3 ) 3 | 2.5 |
Приложения
[ редактировать ]Прогнозирование реактивности
[ редактировать ]Один из оригинальных экспериментов, проведенных Уинстоном и Холнессом, заключался в измерении скорости окисления транс- и цис-замещенных колец с использованием хромового катализатора. Используемая большая трет -бутильная группа фиксирует конформацию каждой молекулы, размещая ее экваториально (показано цис-соединение).

Было замечено, что цис-соединение подвергается окислению гораздо быстрее, чем транс-соединение. Предполагалось, что большая гидроксильная группа в аксиальном положении находится в невыгодном положении и легче образует карбонил, чтобы облегчить это напряжение. Транс-соединение имело скорости, идентичные тем, которые обнаружены в монозамещенном циклогексаноле.

Аппроксимация силы внутримолекулярной силы с использованием значений A
[ редактировать ]Используя значения A гидроксильной и изопропильной субъединицы, можно рассчитать энергетическую ценность благоприятной внутримолекулярной водородной связи. [11]

Ограничения
[ редактировать ]Значения A измерены с использованием монозамещенного циклогексанового кольца и являются показателем только стерических свойств, которые конкретный заместитель придает молекуле. Это приводит к проблеме, когда в другой системе возможны стабилизирующие электронные факторы. Заместитель карбоновой кислоты , показанный ниже, является аксиальным в основном состоянии, несмотря на положительное значение A. Из этого наблюдения становится ясно, что существуют и другие возможные электронные взаимодействия, которые стабилизируют аксиальную конформацию.

Другие соображения
[ редактировать ]Значения A не предсказывают физический размер молекулы, а только стерический эффект. Например, трет- бутильная группа (значение A = 4,9) имеет большее значение A, чем триметилсилильная группа (значение A = 2,5), однако трет -бутильная группа фактически занимает меньше места. Это различие можно объяснить большей длиной связи углерод–кремний по сравнению со связью углерод–углерод -бутильной группы трет . Более длинная связь позволяет меньше взаимодействовать с соседними заместителями, что эффективно делает триметилсилильную группу менее стерически затрудненной, тем самым снижая ее A-значение. [2] Это также можно увидеть при сравнении галогенов . Бром, йод и хлор имеют одинаковые значения А, хотя их атомные радиусы различаются. [4] Тогда значения A предсказывают кажущийся размер заместителя, а относительные кажущиеся размеры определяют различия в стерических эффектах между соединениями. Таким образом, значения A являются полезными инструментами при определении реакционной способности соединений в химических реакциях.
Ссылки
[ редактировать ]- ^ Мюллер, П. (1994). «Словарь терминов, используемых в физической органической химии (Рекомендации ИЮПАК, 1994 г.)» . Чистая и прикладная химия . 66 (5): 1077–1184. дои : 10.1351/pac199466051077 . S2CID 195819485 .
- ^ Jump up to: а б Хоффман, Роберт В. (2004). Органическая химия [ Промежуточный текст ] (второе изд.). Нью-Джерси: John Wiley and Sons, Inc., с. 167. ИСБН 978-0-471-45024-5 .
- ^ Андерсон, Дж. Эдгар (1974). Динамическая химия [ Темы современной химии ]. Темы современной химии. Достижения в химических исследованиях. Том 45. Спрингер Верлаг. п. 139. дои : 10.1007/3-540-06471-0 . ISBN 978-3-540-06471-8 .
- ^ Jump up to: а б Анслин, Эрик В.; Догерти, Деннис А. (2006). Современная физико-органическая химия . Саусалито, Калифорния: Университетские научные книги. С. 104–105 . ISBN 978-1-891389-31-3 .
- ^ Примечание: измерено в различных условиях.
- ^ Элиэль, Эль; Вилен, Ш.; Мандер, Л.Н. (1994). Стереохимия органических соединений . Нью-Йорк: Уайли. ISBN 81-224-0570-3 .
- ^ Элиэль, Эль; Аллинджер, Нидерланды; Ангьял, С.Дж.; Джорджия, Моррисон (1965). Конформационный анализ . Нью-Йорк: Издательство Interscience.
- ^ Хирш, Дж. А. (1967). Темы стереохимии (первое изд.). Нью-Йорк: John Wiley & Sons, Inc., с. 199.
- ^ Ромерс, К.; Альтона, К.; Покупает, HR; Хавинга, Э. (1969). Темы стереохимии (четвертое изд.). Нью-Йорк: John Wiley & Sons, Inc., с. 40.
- ^ «Таблица значений A» (PDF) . Высшая органическая химия 330 . Университет Британской Колумбии. 21 ноября 2012 г. Архивировано (PDF) из оригинала 22 января 2021 г.
- ^ Хуанг, Китай; Кэбелл, Луизиана; Анслин, Э.В. (1994). «Молекулярное распознавание циклитов нейтральными полиаза-водородными рецепторами: сила и влияние внутримолекулярных водородных связей между вицинальными спиртами». Журнал Американского химического общества . 116 (7): 2778–2792. дои : 10.1021/ja00086a011 .


