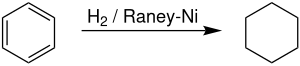Циклогексан
| |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК Циклогексан [2] | |||
| Другие имена Гексанафтен (архаичный) [1] | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| 3DMeet | |||
| 1900225 | |||
| ЧЭБИ | |||
| ЧЕМБЛ | |||
| ХимическийПаук | |||
| Лекарственный Банк | |||
| Информационная карта ECHA | 100.003.461 | ||
| 1662 | |||
| КЕГГ | |||
ПабХим CID | |||
| номер РТЭКС |
| ||
| НЕКОТОРЫЙ | |||
| Число | 1145 | ||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| С 6 Ч 12 | |||
| Молярная масса | 84.162 g·mol −1 | ||
| Появление | Бесцветная жидкость | ||
| Запах | Сладкий, бензин похожий на | ||
| Плотность | 0,7739 г/мл (жидкость); 0,996 г/мл (твердый) | ||
| Температура плавления | 6,47 ° С (43,65 ° F; 279,62 К) | ||
| Точка кипения | 80,74 ° С (177,33 ° F; 353,89 К) | ||
| несмешиваемый | |||
| Растворимость | Растворим в эфире , спирте , ацетоне. | ||
| Давление пара | 78 мм рт.ст. (20 °С) [3] | ||
| −68.13·10 −6 см 3 /моль | |||
Показатель преломления ( n D ) | 1.42662 | ||
| Вязкость | 1,02 сП при 17 °C | ||
| Опасности | |||
| СГС Маркировка : | |||
    | |||
| Опасность | |||
| Х225 , Х304 , Х315 , Х336 | |||
| P210 , P233 , P240 , P241 , P242 , P243 , P261 , P264 , P271 , P273 , P280 , P301+P310 , P302+P352 , P303+P361+P353 , P304+P340 , P312 , П331 21 , П332 , +П313 , П362 , П370+П378 , П391 , П403+П233 , П403+П235 , П405 , П501 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | -20 ° C (-4 ° F; 253 К) | ||
| 245 ° С (473 ° F; 518 К) | |||
| Взрывоопасные пределы | 1.3–8% [3] | ||
| Летальная доза или концентрация (LD, LC): | |||
ЛД 50 ( средняя доза ) | 12705 мг/кг (крыса, перорально) 813 мг/кг (мыши, перорально) [4] | ||
LC Lo ( самый низкий из опубликованных ) | 17 142 частей на миллион (мышь, 2 часа ) 26 600 частей на миллион (кролик, 1 час) [4] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
МЕХ (Допускается) | TWA 300 частей на миллион (1050 мг/м 3 ) [3] | ||
РЕЛ (рекомендуется) | TWA 300 частей на миллион (1050 мг/м 3 ) [3] | ||
IDLH (Непосредственная опасность) | 1300 частей на миллион [3] | ||
| Термохимия | |||
Стандартная энтальпия образование (Δ f H ⦵ 298 ) | −156 кДж/моль | ||
Стандартная энтальпия горение (Δ c H ⦵ 298 ) | −3920 кДж/моль | ||
| Родственные соединения | |||
Родственные циклоалканы | Циклопентан Циклогептан | ||
Родственные соединения | Циклогексен Бензол | ||
| Страница дополнительных данных | |||
| Циклогексан (страница данных) | |||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Циклогексан представляет собой циклоалкан с молекулярной формулой С 6 Ч 12 . Циклогексан неполярен . Циклогексан представляет собой бесцветную легковоспламеняющуюся жидкость с характерным запахом моющего средства , напоминающим чистящие средства (в которых он иногда используется). используется для промышленного производства адипиновой кислоты и капролактама , которые являются предшественниками нейлона Циклогексан в основном . [5]
Циклогексил ( C 6 H 11 ) представляет собой алкильный заместитель циклогексана и обозначается сокращенно Cy . [6]
Производство
[ редактировать ]Современный
[ редактировать ]получают гидрированием бензола В промышленных масштабах циклогексан в присутствии никелевого катализатора Ренея . [7] На производителей циклогексана приходится примерно 11,4% мирового спроса на бензол. [8] Реакция сильно экзотермична, ΔH(500 К) = -216,37 кДж/моль. Дегидрирование начинается заметно выше 300 ° C, что отражает благоприятную энтропию для дегидрирования. [9]
Рано
[ редактировать ]В отличие от бензола , циклогексан не встречается в природных ресурсах, таких как уголь. По этой причине первые исследователи синтезировали образцы циклогексана. [10]
Отказ
[ редактировать ]- В 1867 году Марселлен Бертло восстановил бензол при иодистоводородной кислотой повышенных температурах. [11] [12]
- В 1870 году Адольф фон Байер повторил реакцию. [13] и произнес тот же продукт реакции как «гексагидробензол».
- В 1890 году Владимир Марковников полагал, что ему удалось перегнать то же самое соединение из кавказской нефти , назвав свою смесь «гексанафтеном». [ нужна ссылка ]
Удивительно, но их циклогексаны кипели на 10 °C выше, чем гексагидробензол или гексанафтен, но эта загадка была решена в 1895 году Марковниковым, Н.М. Кишнером и Николаем Зелинским , когда они переназначили «гексагидробензол» и «гексанафтен» на метилциклопентан , что стало результатом неожиданного открытия. реакция перегруппировки .
Успех
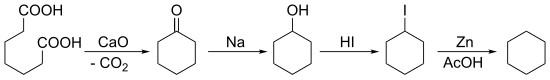
[ редактировать ]В 1894 году Байер синтезировал циклогексан, начав с кетонизации пимелиновой кислоты с последующим множественным восстановлением:
В том же году Э. Хаворт и У. Х. Перкин-младший (1860–1929) получили его реакцией Вюрца с 1,6-дибромгексаном.
Реакции и использование
[ редактировать ]Хотя циклогексан довольно нереакционноспособен, он подвергается каталитическому окислению с образованием циклогексанона и циклогексанола . Смесь циклогексанона и циклогексанола, называемая « масло КА », является сырьем для производства адипиновой кислоты и капролактама , предшественников нейлона . Ежегодно производится несколько миллионов килограммов циклогексанона и циклогексанола. [9]
Он используется в качестве растворителя в некоторых марках корректирующих жидкостей. Циклогексан иногда используется в качестве неполярного органического растворителя, хотя н-гексан более широко для этой цели используется . Его часто используют в качестве растворителя для перекристаллизации , поскольку многие органические соединения хорошо растворяются в горячем циклогексане и плохо растворяются при низких температурах.
Циклогексан также используется для калибровки приборов дифференциальной сканирующей калориметрии (ДСК) из-за удобного перехода кристалл-кристалл при -87,1 ° C. [14]
Пары циклогексана используются в вакуумных печах цементации, при производстве оборудования для термообработки.
Телосложение
[ редактировать ]Кольцо с 6 вершинами не соответствует форме идеального шестиугольника . Конформация плоского двумерного плоского шестиугольника имеет значительную угловую деформацию, поскольку угол его связей не составляет 109,5 градусов; деформация кручения также будет значительной, потому что все связи будут затмеваться связями . Поэтому, чтобы уменьшить деформацию кручения , циклогексан принимает трехмерную структуру, известную как конформация стула , которая быстро взаимопревращается при комнатной температуре посредством процесса, известного как переворот стула . Во время переворота стула встречаются три другие промежуточные формы: полустул, являющийся наиболее нестабильной конформацией, более устойчивая форма лодочки и твист-лодочка, которая более устойчива, чем лодка, но все же гораздо менее устойчива. устойчивее, чем стул. Стул и лодочка представляют собой минимумы энергии и, следовательно, являются конформерами, тогда как полукресло и лодочка являются переходными состояниями и представляют собой максимумы энергии. Идея о том, что конформация кресла является наиболее стабильной структурой циклогексана, была впервые предложена еще в 1890 году Германом Заксе, но получила широкое признание лишь намного позже. В новой конформации атомы углерода располагаются под углом 109,5°. Половина атомов водорода находится в плоскости кольца ( экваториальный ), а другая половина перпендикулярна плоскости ( осевой ). Эта конформация обеспечивает наиболее стабильную структуру циклогексана. Существует еще одна конформация циклогексана, известная как конформация лодочки , но она преобразуется в несколько более стабильное образование стула. Если циклогексан монозамещен большим заместителем , то заместитель, скорее всего, будет присоединен в экваториальном положении, поскольку это несколько более стабильная конформация .
Циклогексан имеет наименьшую угловую и крутильную деформацию из всех циклоалканов; в результате циклогексан был признан нулевым по общей деформации кольца.
Твердые фазы
[ редактировать ]Циклогексан имеет две кристаллические фазы. Высокотемпературная фаза I, стабильная в диапазоне от 186 К до температуры плавления 280 К, представляет собой пластичный кристалл , что означает, что молекулы сохраняют некоторую степень свободы вращения. Низкотемпературная (ниже 186 К) фаза II упорядочена. Две другие низкотемпературные (метастабильные) фазы III и IV были получены применением умеренных давлений выше 30 МПа, где фаза IV возникает исключительно в дейтерированном циклогексане (приложение давления увеличивает значения всех температур перехода). [15]
| Нет | Симметрия | Космическая группа | а (Å) | б(Å) | с (Å) | С | Т (К) | П (МПа) |
|---|---|---|---|---|---|---|---|---|
| я | Кубический | FM3m | 8.61 | 4 | 195 | 0.1 | ||
| II | Моноклиника | С2/с | 11.23 | 6.44 | 8.20 | 4 | 115 | 0.1 |
| III | орторомбический | Пмнн | 6.54 | 7.95 | 5.29 | 2 | 235 | 30 |
| IV | Моноклиника | P12(1)/n1 | 6.50 | 7.64 | 5.51 | 4 | 160 | 37 |
Здесь Z — количество единиц структуры числа на элементарную ячейку ; константы элементарной ячейки a, b и c были измерены при заданных температуре T и давлении P.
См. также
[ редактировать ]- Катастрофа во Фликсборо — крупная промышленная авария, вызванная взрывом циклогексана.
- Гексан
- Кольцо флип
- Циклогексан (страница данных)
Ссылки
[ редактировать ]- ^ «Гексанафтен» . словарь.com . Архивировано из оригинала 12 февраля 2018 г.
- ^ «Фронт материи». Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга) . Кембридж: Королевское химическое общество . 2014. стр. P001–P004. дои : 10.1039/9781849733069-FP001 . ISBN 978-0-85404-182-4 .
- ^ Jump up to: а б с д и Карманный справочник NIOSH по химическим опасностям. «#0163» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Jump up to: а б «Циклогексан» . Непосредственно опасные для жизни и здоровья концентрации (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Кэмпбелл, М. Ларри (2011). «Циклогексан». Энциклопедия промышленной химии Ульмана . дои : 10.1002/14356007.a08_209.pub2 . ISBN 978-3527306732 .
- ^ «Стандартные сокращения и акронимы» (PDF) . Журнал органической химии.
- ^ Фред Фан Чжан; Томас ван Рейнман; Джи Су Ким; Аллен Ченг (2008). «О современных методах гидрирования ароматических соединений с 1945 г. по настоящее время». Лундсская техническая школа .
- ^ Цересана. «Бензол – Исследование: рынок, анализ, тенденции 2021 – Ceresana» . www.ceresana.com . Архивировано из оригинала 21 декабря 2017 года . Проверено 4 мая 2018 г.
- ^ Jump up to: а б Майкл Таттл Массер (2005). «Циклогексанол и Циклогексанон». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a08_217 . ISBN 978-3527306732 .
- ^ Варнхофф, EW (1996). «Любопытно переплетенные истории бензола и циклогексана». Дж. Хим. Образование. 73 (6): 494. Бибкод : 1996JChEd..73..494W . дои : 10.1021/ed073p494 .
- ^ Бертоле (1867). «Новые применения методов восстановления в органической химии» . Бюллетень Парижского химического общества (на французском языке). ряд 2 (7): 53–65.
- ^ Бертоле (1868). «Универсальный метод восстановления и насыщения органических соединений водородом» . Бюллетень Парижского химического общества (на французском языке). ряд 2 (9): 8–31.
Действительно, бензин, нагретый до 280° в течение 24 часов с холодным насыщенным водным раствором иодистоводородной кислоты, в 80 раз превышающим его вес, почти полностью превращается в гексиленгидрид C 12 H 14 , связывая водород, в 4 раза превышающий его объем: C 12. H 6 + 4H 2 = C 12 H 14 … Новый карбид, образованный бензином, представляет собой уникальное и определенное тело: он кипит при 69° и обладает всеми свойствами и составом гексиленгидрида, извлеченного из масел.
[Фактически, бензол, нагретый до 280° в течение 24 часов с водным раствором холодной насыщенной иодистоводородной кислоты, в 80 раз превышающим его вес, почти полностью превращается в гидрид гексилена C 12 H 14 . [Примечание: эта формула для гексана ( C 6 H 14 ) неверно, потому что химики в то время использовали неверную атомную массу углерода.] путем фиксации [т. е. соединения с] 4-кратным его объемом водорода: C 12 H 6 + 4H 2 = C 12 H 14 Новое углеродное соединение, образуемое бензолом, представляет собой уникальное и четко определенное вещество: оно кипит при 69° и обладает всеми свойствами и составом гидрида гексилена, извлеченного из нефти.)] - ^ Адольф Байер (1870). «О восстановлении ароматических соединений иодидом фосфония [H 4 IP]». Анналы химии и фармации . 55 : 266-281.
При восстановлении амальгамой натрия или иодофосфонием объединяются не более шести атомов водорода и образуются производные, производные углеводорода C 6 H 12 . Этот углеводород, скорее всего, представляет собой замкнутое кольцо, поскольку его производные, гексагидромезитилен и гексагидромеллитовая кислота, легко превращаются обратно в производные бензола.
[При восстановлении [бензола] амальгамой натрия или йодидом фосфония в крайнем случае присоединяется шесть атомов водорода и возникают производные, которые происходят из углеводорода C 6 H 12 . Этот углеводород, по всей вероятности, представляет собой замкнутое кольцо, поскольку его производные — гексагидромезитилен [1,3,5-триметилциклогексан] и гексагидромеллитовая кислота [циклогексан-1,2,3,4,5,6-гексакарбоновая кислота] — могут превращаться с легкостью снова в производные бензола.] - ^ Прайс, DM (1995). «Температурная калибровка дифференциальных сканирующих калориметров». Журнал термического анализа . 45 (6): 1285–1296. дои : 10.1007/BF02547423 . S2CID 97402835 .
- ^ Jump up to: а б Майер, Дж.; Урбан, С.; Хабрило, С.; Холдерна, К.; Натканец, И.; Вюрфлингер, А.; Заяк, В. (1991). «Исследование нейтронного рассеяния циклогексана C6H12 и C6D12 под высоким давлением». Физический статус Solidi B. 166 (2): 381. Бибкод : 1991ПССБР.166..381М . дои : 10.1002/pssb.2221660207 .
Внешние ссылки
[ редактировать ]- Международная карта химической безопасности 0242
- Национальный реестр загрязнителей – информационный бюллетень по циклогексану
- Карманный справочник NIOSH по химическим опасностям
- Циклогексан@3Dchem
- Герман Заксе и первое предложение конструкции стула.
- Банк данных по опасным веществам NLM – Циклогексан
- Метанол обнаружен в космосе
- Расчет давления пара , плотности жидкости , динамической вязкости жидкости , поверхностного натяжения циклогексана .
- Технологическая схема производства циклогексана, технология гидрирования бензола