Гексан
 | |
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК Гексан [2] | |
| Другие имена Секстан, [1] гексакарбан | |
| Идентификаторы | |
3D model ( JSmol ) | |
| 1730733 | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| ХимическийПаук | |
| Лекарственный Банк | |
| Информационная карта ECHA | 100.003.435 |
| Номер ЕС |
|
| 1985 | |
| КЕГГ | |
| МеШ | н-гексан |
ПабХим CID | |
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
| Число | 1208 |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 6 Ч 14 | |
| Молярная масса | 86.178 g·mol −1 |
| Появление | Бесцветная жидкость |
| Запах | бензин |
| Плотность | 0,6606 г мл −1 [3] |
| Температура плавления | от −96 до −94 °С; от −141 до −137 ° F; от 177 до 179 К |
| Точка кипения | от 68,5 до 69,1 °С; от 155,2 до 156,3 °F; от 341,6 до 342,2 К |
| 9,5 мг л −1 | |
| войти P | 3.764 |
| Давление пара | 17,60 кПа (при 20,0 °C) |
Закон Генри постоянная ( k H ) | 7,6 нмоль Па −1 кг −1 |
| УФ-видимое излучение (λ макс .) | 200 нм |
| −74.6·10 −6 см 3 /моль | |
Показатель преломления ( n D ) | 1.375 |
| Вязкость | 0,3 мПа·с |
| 0,08 Д | |
| Термохимия | |
Теплоемкость ( С ) | 265,2 ДжК −1 моль −1 |
Стандартный моляр энтропия ( S ⦵ 298 ) | 296.06 ДжК −1 моль −1 |
Стандартная энтальпия образование (Δ f H ⦵ 298 ) | −199,4–−198,0 кДж моль −1 |
Стандартная энтальпия горение (Δ c H ⦵ 298 ) | −4180–−4140 кДж моль −1 |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности | Репродуктивная токсичность – после аспирации , отек легких , пневмонит. [4] |
| СГС Маркировка : | |
    | |
| Опасность | |
| Х225 , Х302 , Х305 , Х315 , Х336 , Х361фд , Х373 , Х411 | |
| P201 , P202 , P210 , P233 , P235 , P240 , P241 , P242 , P243 , P260 , P264 , P271 , P273 , P280 , P281 , P301+P330+P331 , P302+P352 , P303+P 361+П353 , П304+П340 , P308+P313 , P310 , P312 , P314 , P332+P313 , P363 , P370+P378 , P391 , P403+P233 , P405 , P501 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | -26,0 ° C (-14,8 ° F; 247,2 К) |
| 234,0 ° С (453,2 ° F; 507,1 К) | |
| Взрывоопасные пределы | 1.2–7.7% |
| Летальная доза или концентрация (LD, LC): | |
ЛД 50 ( средняя доза ) | 25 г кг −1 (оральный, крыса) 28710 мг/кг (крыса, перорально) [6] |
LD Lo ( самый низкий опубликованный ) | 56137 мг/кг (крыса, перорально) [6] |
| NIOSH (пределы воздействия на здоровье в США): | |
МЕХ (Допускается) | TWA 500 частей на миллион (1800 мг/м 3 ) [5] |
РЕЛ (рекомендуется) | СВВ 50 частей на миллион (180 мг/м 3 ) [5] |
IDLH (Непосредственная опасность) | 1100 частей на миллион [5] |
| Родственные соединения | |
Родственные алканы | |
| Страница дополнительных данных | |
| Гексан (страница данных) | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Гексан ( / ˈ h ɛ k s eɪ n / ) или н -гексан — органическое соединение с прямой цепью , алкан с шестью атомами углерода и молекулярной формулой C 6 H 14 . [7]
Гексан представляет собой бесцветную жидкость без запаха в чистом виде и с температурой кипения около 69 ° C (156 ° F). Он широко используется как дешевый, относительно безопасный, в значительной степени инерционный и легко испаряющийся неполярный растворитель , а современные бензиновые смеси содержат около 3% гексана. [8]
Термин «гексаны» относится к смеси , состоящей в основном (>60%) из н -гексана с различными количествами изомерных соединений 2-метилпентана и 3-метилпентана и, возможно, меньшими количествами неизомерных C 5 , C 6 и C. 7 (цикло)алканы. Эти смеси «гексанов» дешевле, чем чистый гексан, и часто используются в крупномасштабных операциях, не требующих одного изомера (например, в качестве очищающего растворителя или для хроматографии ).
Изомеры
[ редактировать ]| Общее имя | Название ИЮПАК | Текстовая формула | Скелетная формула |
|---|---|---|---|
| Обычный гексан , н -Гексан | Гексан | СН 3 (СН 2 ) 4 СН 3 | |
| изогексан | 2-метилпентан | (СН 3 ) 2 СН(СН 2 ) 2 СН 3 | 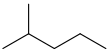 |
| 3-Метилпентан | СН 3 СН 2 СН(СН 3 )СН 2 СН 3 | 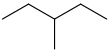 | |
| 2,3-Диметилбутан | (СН 3 ) 2 СНСН(СН 3 ) 2 | 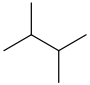 | |
| Неогексан | 2,2-Диметилбутан | (СН 3 ) 3 ССН 2 СН 3 | 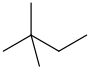 |
Использование
[ редактировать ]В промышленности гексаны используются в рецептурах клеев для обуви, изделий из кожи , кровли. Они также используются для извлечения кулинарных масел (таких как масло канолы или соевое масло ) из семян, для очистки и обезжиривания различных предметов, а также в текстильном производстве.
Типичным лабораторным применением гексанов является извлечение масляных и жировых загрязнений из воды и почвы для анализа. [9] Поскольку гексан нелегко депротонировать , его используют в лаборатории для реакций, в которых участвуют очень сильные основания, например, при получении литийорганических соединений . Например, бутиллитий обычно поставляется в виде раствора в гексане. [10]
Гексаны обычно используются в хроматографии в качестве неполярного растворителя. Высшие алканы, присутствующие в качестве примесей в гексанах, имеют такое же время удерживания, что и растворитель, а это означает, что фракции, содержащие гексан, также будут содержать эти примеси. При препаративной хроматографии концентрация большого объема гексанов может привести к тому, что образец будет значительно загрязнен алканами. Это может привести к получению твердого соединения в виде масла , а алканы могут помешать анализу.
Производство
[ редактировать ]Гексан в основном получают при переработке сырой нефти . Точный состав фракции во многом зависит от источника нефти (сырая или риформинговая) и ограничений переработки. [11] Промышленный продукт (обычно около 50% по массе изомера с прямой цепью) представляет собой фракцию, кипящую при 65–70 ° C (149–158 ° F).
Физические свойства
[ редактировать ]Все алканы бесцветны. [12] [13] Точки кипения различных гексанов в некоторой степени схожи и, как и у других алканов, обычно ниже для более разветвленных форм. Точки плавления совершенно разные, и тенденция не очевидна. [14]
| изомер | МП (°С) | МП (°F) | АД (°С) | АД (°F) |
|---|---|---|---|---|
| н -гексан | −95.3 | −139.5 | 68.7 | 155.7 |
| 3-метилпентан | −118.0 | −180.4 | 63.3 | 145.9 |
| 2-метилпентан (изогексан) | −153.7 | −244.7 | 60.3 | 140.5 |
| 2,3-диметилбутан | −128.6 | −199.5 | 58.0 | 136.4 |
| 2,2-диметилбутан (неогексан) | −99.8 | −147.6 | 49.7 | 121.5 |
Гексан имеет значительное давление паров при комнатной температуре:
| Температура (°С) | Температура (°F) | Давление пара ( мм рт.ст. ) | Давление пара ( кПа ) |
|---|---|---|---|
| −40 | −40 | 3.36 | 0.448 |
| −30 | −22 | 7.12 | 0.949 |
| −20 | −4 | 14.01 | 1.868 |
| −10 | 14 | 25.91 | 3.454 |
| 0 | 32 | 45.37 | 6.049 |
| 10 | 50 | 75.74 | 10.098 |
| 20 | 68 | 121.26 | 16.167 |
| 25 | 77 | 151.28 | 20.169 |
| 30 | 86 | 187.11 | 24.946 |
| 40 | 104 | 279.42 | 37.253 |
| 50 | 122 | 405.31 | 54.037 |
| 60 | 140 | 572.76 | 76.362 |
Реактивность
[ редактировать ]Как и большинство алканов, гексаны характеризуются низкой реакционной способностью и являются подходящими растворителями для реакционноспособных соединений. Однако коммерческие образцы н-гексана часто содержат метилциклопентан , который имеет третичные связи CH, несовместимые с некоторыми радикальными реакциями. [15]
Безопасность
[ редактировать ]Вдыхание н -гексана в концентрации 5000 ppm в течение 10 минут вызывает выраженное головокружение; 2500-1000 ppm в течение 12 часов вызывают сонливость , утомляемость , потерю аппетита и парестезии в дистальных конечностях; 2500–5000 ppm вызывают мышечную слабость, холодную пульсацию в конечностях, нечеткость зрения, головную боль и анорексию . [16] хроническое профессиональное воздействие повышенных уровней н Было продемонстрировано, что -гексана связано с периферической невропатией у автомехаников в США и нейротоксичностью у рабочих типографий, обувных и мебельных фабрик в Азии, Европе и Северной Америке. [17]
США Национальный институт безопасности и гигиены труда (NIOSH) установил рекомендуемый предел воздействия (REL) для изомеров гексана (не н -гексана) на уровне 100 частей на миллион (350 мг/м2). 3 (0,15 г/куб. футов)) в течение 8-часового рабочего дня. [18] Однако для н -гексана текущее значение REL NIOSH составляет 50 частей на миллион (180 мг/м3). 3 (0,079 г/куб футов)) в течение 8-часового рабочего дня. [19] Этот предел был предложен в качестве допустимого предела воздействия (PEL) Управлением по безопасности и гигиене труда в 1989 году; однако этот PEL был отменен в судах США в 1992 году. [20] Текущий PEL н-гексана в США составляет 500 частей на миллион (1800 мг/м3). 3 (0,79 г/куб футов)). [19]
Гексан и другие летучие углеводороды ( петролейный эфир ) представляют опасность при аспирации . [21] н- Гексан иногда используется как денатурант спирта и как чистящее средство в текстильной , мебельной и кожевенной промышленности. Его постепенно заменяют другими растворителями. [22]
Как и бензин, гексан очень летуч и может взорваться. в 1981 году Взрывы канализационных сетей в Луисвилле , разрушившие более 13 миль (21 км) канализационных линий и улиц в Кентукки, были вызваны возгоранием паров гексана, которые незаконно сбрасывались с завода по переработке соевых бобов , принадлежащего Ralston-Purina . Гексан был назван причиной взрыва, произошедшего в Национальном университете Рио-Куарто , Аргентина, 5 декабря 2007 года из-за разлива гексана возле тепловыделяющей машины, которая взорвалась, вызвав пожар, в результате которого погиб один студент и были ранены еще 24 человека. .
Инциденты
[ редактировать ]Производственное отравление гексаном произошло у японских рабочих-сандалистов, итальянских рабочих-обувщиков, [23] Тайваньские работники по проверке печати и другие. [24] Анализ тайваньских рабочих показал профессиональное воздействие веществ, включая н -гексан. [25] Сообщалось, что в 2010–2011 годах китайские рабочие, производившие iPhone, отравились гексаном. [26] [27]
Биотрансформация
[ редактировать ]н- биотрансформируется в 2-гексанол и далее в 2,5-гександиол Гексан в организме . Превращение катализируется ферментом цитохромом P450, использующим кислород воздуха. 2,5-гександиол может далее окисляться до 2,5-гександиона , который нейротоксичен и вызывает полиневропатию . [22] Учитывая такое поведение, замена н обсуждалась -гексана в качестве растворителя. н -Гептан является возможной альтернативой. [28]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Хофманн, Август Вильгельм Фон (1 января 1867 г.). «I. О действии трихлорида фосфора на соли ароматических моноаминов». Труды Лондонского королевского общества . 15 : 54–62. дои : 10.1098/rspl.1866.0018 . S2CID 98496840 .
- ^ «Н-гексан – Краткое описание соединений» . Пабхим соединение . США: Национальный центр биотехнологической информации. 16 сентября 2004 г. Идентификация и соответствующие записи. Архивировано из оригинала 8 марта 2012 года . Проверено 31 декабря 2011 г.
- ^ Уильям М. Хейнс (2016). Справочник CRC по химии и физике (97-е изд.). Бока-Ратон: CRC Press. стр. 3–298. ISBN 978-1-4987-5429-3 .
- ^ Классификация СГС на [PubChem]
- ^ Перейти обратно: а б с Карманный справочник NIOSH по химическим опасностям. «#0322» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Перейти обратно: а б «н-Гексан» . Непосредственно опасные для жизни и здоровья концентрации (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ ПабХим. «н-ГЕКСАН» . pubchem.ncbi.nlm.nih.gov . Проверено 3 ноября 2023 г.
- ^ «Н-Гексан – опасные вещества» . Карта опасности . Проверено 7 июля 2022 г.
- ^ Использование озоноразрушающих веществ в лабораториях . Kbh: Совет министров Северных стран. 2003. ISBN 92-893-0884-2 . OCLC 474188215 . Архивировано из оригинала 16 июля 2012 года.
- ^ Швиндеман, Джеймс А.; Вольтерманн, Крис Дж.; Летчфорд, Роберт Дж. (1 мая 2002 г.). «Безопасное обращение с литийорганическими соединениями в лаборатории» . Химическое здоровье и безопасность . 9 (3): 6–11. дои : 10.1016/s1074-9098(02)00295-2 . ISSN 1074-9098 .
- ^ Ле Ван Мао, Р.; Мелансон, С.; Готье-Кэмпбелл, К.; Клетниекс, П. (1 мая 2001 г.). «Процесс селективного глубокого каталитического крекинга (SDCC) нефтяного сырья для производства легких олефинов. I. Эффект Катлевера, полученный с помощью системы с двумя реакционными зонами, при конверсии н-гексана» . Письма о катализе . 73 (2): 181–186. дои : 10.1023/А:1016685523095 . ISSN 1572-879X . S2CID 98167823 .
- ^ «Органическая химия-I» (PDF) . Nsdl.niscair.res.in. Архивировано из оригинала (PDF) 29 октября 2013 года . Проверено 17 февраля 2014 г.
- ^ «13. Углеводороды | Учебники» . Учебник.s-anand.net. Архивировано из оригинала 6 октября 2014 года . Проверено 17 февраля 2014 г.
- ^ Уильям Д. Маккейн (1990). Свойства нефтяных жидкостей . ПеннНу. ISBN 978-0-87814-335-1 .
- ^ Кох, Х.; Хааф, В. (1973). «1-адамантанкарбоновая кислота» . Органические синтезы ; Сборник томов , т. 5, с. 20 .
- ^ «Н-ГЕКСАН» . Сеть токсикологических данных Банк данных об опасных веществах . Национальная медицинская библиотека . Архивировано из оригинала 4 сентября 2015 года.
- ^ Центры по контролю и профилактике заболеваний (CDC) (16 ноября 2001 г.). «Периферическая невропатия, связанная с н-гексаном, у автомехаников - Калифорния, 1999–2000». ММВР. Еженедельный отчет о заболеваемости и смертности . 50 (45): 1011–1013. ISSN 0149-2195 . ПМИД 11724159 .
- ^ «CDC - Карманный справочник NIOSH по химическим опасностям - изомеры гексана (исключая н-гексан)» . cdc.gov . Архивировано из оригинала 31 октября 2015 года . Проверено 3 ноября 2015 г.
- ^ Перейти обратно: а б CDC (28 марта 2018 г.). «н-Гексан» . Центры по контролю и профилактике заболеваний . Проверено 3 мая 2020 г.
- ^ «Приложение G: Проект обновления данных о загрязнителях воздуха 1989 года – пределы воздействия НЕ действуют» . www.cdc.gov . 20 февраля 2020 г. Проверено 3 мая 2020 г.
- ^ Гад, Шейн С. (2005), «Нефтяные углеводороды», Энциклопедия токсикологии , том. 3 (2-е изд.), Elsevier, стр. 377–379.
- ^ Перейти обратно: а б Клаф, Стивен Р.; Малхолланд, Лейна (2005). «Гексан». Энциклопедия токсикологии . Том. 2 (2-е изд.). Эльзевир. стр. 522–525.
- ^ Риццуто, Н; Де Грандис, Д; Ди Трапани, Дж; Пасинато, Э (1980). «Н-гексановая полинейропатия. Профессиональное заболевание сапожников». Европейская неврология . 19 (5): 308–15. дои : 10.1159/000115166 . ПМИД 6249607 .
- ^ н-гексан , Критерии гигиены окружающей среды , Всемирная организация здравоохранения, 1991 г., заархивировано из оригинала 19 марта 2014 г.
- ^ Лю, CH; Хуанг, Китай; Хуанг, CC (2012). «Профессиональные нейротоксические заболевания на Тайване» . Безопасность и здоровье на работе . 3 (4): 257–67. дои : 10.5491/SHAW.2012.3.4.257 . ПМК 3521924 . ПМИД 23251841 .
- ^ «Рабочие отравились при изготовлении iPhone – ABC News (Австралийская радиовещательная корпорация)» . Австралийская радиовещательная корпорация. 26 октября 2010 года. Архивировано из оригинала 8 апреля 2011 года . Проверено 17 марта 2015 г.
- ^ Дэвид Барбоза (22 февраля 2011 г.). «Работники поставщика Apple в Китае заболели» . Нью-Йорк Таймс . Архивировано из оригинала 7 апреля 2015 года . Проверено 17 марта 2015 г.
- ^ Фильзер Дж.Г., Чанади Г.А., Дитц В., Кесслер В., Кройцер П.Е., Рихтер М., Штёрмер А. (1996). «Сравнительная оценка нейротоксического риска н-гексана и н-гептана у крыс и человека на основе образования метаболитов 2,5-гександиона и 2,5-гептандиона». Биологические реактивные интермедиаты V . Достижения экспериментальной медицины и биологии. Том. 387. стр. 411–427. дои : 10.1007/978-1-4757-9480-9_50 . ISBN 978-1-4757-9482-3 . ПМИД 8794236 .
Внешние ссылки
[ редактировать ]- Международная карта химической безопасности 1262 (2-метилпентан)
- Паспорт безопасности материала для гексана
- Национальный реестр загрязнителей – по н- гексану информационный бюллетень
- Запись в базе данных фитохимических веществ
- Центр по контролю и профилактике заболеваний
- Предупреждение Совета национальной безопасности «ОБЫЧНЫЕ ХИМИЧЕСКИЕ ВЛИЯНИЯ НА АВТОМЕХАНИКУ»
- Австралийского национального реестра загрязнителей (NPI) Страница
- «EPA не считает н-гексан канцерогеном для человека». Федеральный реестр / Том. 66, № 71 / Четверг, 12 апреля 2001 г. / Правила и положения
