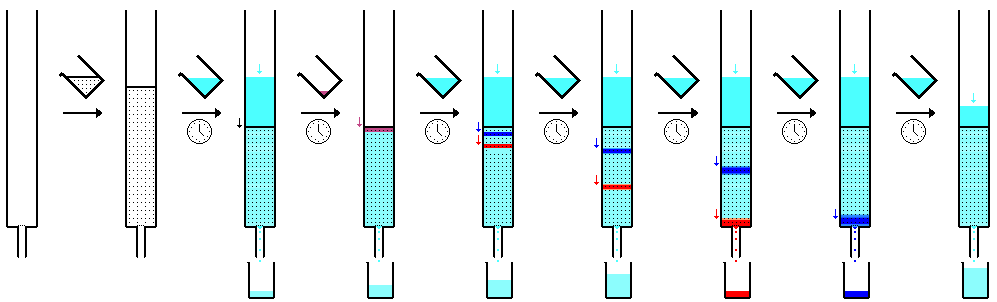
Хроматография
| Часть серии о |
| Механика сплошных сред |
|---|
| Часть серии о |
| Химия |
|---|
 |
|

В анализе химическом хроматография это лабораторный метод разделения на смеси — компоненты. Смесь растворяется в жидком растворителе (газе или жидкости), называемом подвижной фазой , который переносит ее через систему (колонку, капиллярную трубку, пластину или лист), на которой материал, называемый неподвижной фазой закреплен . Поскольку различные компоненты смеси имеют разное сродство к неподвижной фазе и удерживаются в течение разного времени в зависимости от их взаимодействия с поверхностными участками, компоненты перемещаются в подвижной жидкости с разными кажущимися скоростями, что приводит к их разделению. Разделение основано на дифференциальном разделении подвижной и неподвижной фаз. соединения Незначительные различия в коэффициенте распределения приводят к различному удержанию на неподвижной фазе и, таким образом, влияют на разделение. [1]
Хроматография может быть препаративной и аналитической . Целью препаративной хроматографии является разделение компонентов смеси для последующего использования и, таким образом, это форма очистки . [2] [3] Этот процесс связан с более высокими затратами из-за способа его производства. [4] [5] Аналитическая хроматография обычно проводится с меньшими количествами материала и предназначена для установления присутствия или измерения относительных пропорций аналитов в смеси. Эти два типа не являются взаимоисключающими. [6]
Этимология и произношение [ править ]
Хроматография, произносится как / ˌ k r oʊ m ə ˈ t ɒ ɡ r ə f i / , происходит от греческого χρῶμα chroma , что означает « цвет », и γράφεινgraphein , что означает «писать». Комбинация этих двух терминов была непосредственно унаследована от изобретения метода, впервые использованного для разделения биологических пигментов . [7]
История [ править ]
Хроматография была впервые изобретена в Казанском университете русским учёным итальянского происхождения Михаилом Цветом в 1900 году. [8] [9] Он разработал эту технику и ввел термин хроматография в первом десятилетии 20-го века, в первую очередь для разделения растительных пигментов, таких как хлорофилл , каротины и ксантофиллы . Поскольку эти компоненты разделены полосами разного цвета (зеленого, оранжевого и желтого соответственно), они напрямую послужили источником названия техники. Новые типы хроматографии, разработанные в 1930-х и 1940-х годах, сделали этот метод полезным для многих процессов разделения . [10]
Техника хроматографии существенно развилась в результате работ Арчера Джона Портера Мартина и Ричарда Лоуренса Миллингтона Синджа в 1940-х и 1950-х годах, за которые они получили Нобелевскую премию по химии 1952 года . [11] Они установили принципы и основные методы распределительной хроматографии, а их работа способствовала быстрому развитию нескольких хроматографических методов: бумажной хроматографии , газовой хроматографии и того, что впоследствии стало известно как высокоэффективная жидкостная хроматография . С тех пор технология быстро развивалась. Исследователи обнаружили, что основные принципы хроматографии Цвета можно применять по-разному, в результате чего были созданы различные разновидности хроматографии, описанные ниже. Достижения постоянно улучшают технические характеристики хроматографии, позволяя разделять все более похожие молекулы.
Условия [ править ]
- Аналит – вещество, которое необходимо разделить при хроматографии. Это также обычно то, что требуется от смеси.
- Аналитическая хроматография – использование хроматографии для определения наличия и, возможно, концентрации аналита(ов) в образце .
- Связанная фаза – неподвижная фаза, которая ковалентно связана с частицами носителя или с внутренней стенкой трубок колонки.
- Хроматограмма – визуальный результат хроматографа. В случае оптимального разделения разные пики или узоры на хроматограмме соответствуют разным компонентам разделяемой смеси.
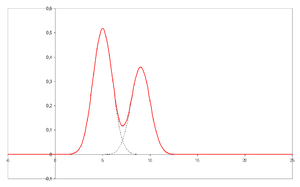
 По оси X отложено время удерживания, а по оси Y — сигнал (например, полученный спектрофотометром , масс -спектрометром или рядом других детекторов), соответствующий отклику, создаваемому аналитами, выходящими из системы. В случае оптимальной системы сигнал пропорционален концентрации конкретного отделяемого аналита.
По оси X отложено время удерживания, а по оси Y — сигнал (например, полученный спектрофотометром , масс -спектрометром или рядом других детекторов), соответствующий отклику, создаваемому аналитами, выходящими из системы. В случае оптимальной системы сигнал пропорционален концентрации конкретного отделяемого аналита. - Хроматограф – прибор, позволяющий проводить сложное разделение, например, газовой хроматографией или жидкостной хроматографией.
- Хроматография – физический метод разделения, при котором компоненты распределяются между двумя фазами, одна из которых неподвижна (неподвижная фаза), а другая (подвижная фаза) движется в определенном направлении.
- Элюент (иногда пишется как элюент ) — растворитель или растворитель, используемый в элюционной хроматографии и является синонимом подвижной фазы . [12]
- Элюат – смесь растворенного вещества (см. Элюит) и растворителя (см. Элюент), выходящая из колонки. [12]
- Эфлюент – поток, выходящий из хроматографической колонки. На практике он используется как синоним элюата , но более точно этот термин относится к потоку, независимому от происходящего разделения. [12]
- Элюит – более точный термин для растворенного вещества или аналита . Это компонент пробы, покидающий хроматографическую колонку. [12]
- Элюотропный ряд – список растворителей, ранжированный по их элюирующей способности.
- Иммобилизованная фаза – неподвижная фаза, иммобилизованная на частицах носителя или на внутренней стенке трубок колонки.
- Подвижная фаза – фаза, которая движется в определенном направлении. Это может быть жидкость (ЖХ и капиллярная электрохроматография , КЭХ), газ (ГХ) или сверхкритическая жидкость (сверхкритическая жидкостная хроматография, СФХ). Подвижная фаза состоит из разделяемой/анализируемой пробы и растворителя, который перемещает пробу через колонку. В случае ВЭЖХ подвижная фаза состоит из неполярного растворителя(ов), такого как гексан в нормальной фазе, или полярного растворителя, такого как метанол, в обращенно-фазовой хроматографии, и разделяемого образца. Подвижная фаза проходит через хроматографическую колонку (неподвижная фаза), где образец взаимодействует с неподвижной фазой и отделяется.
- Препаративная хроматография – использование хроматографии для очистки достаточного количества вещества для дальнейшего использования, а не для анализа.
- Время удерживания – характерное время, необходимое конкретному аналиту для прохождения через систему (от входа в колонку до детектора) при заданных условиях. См. Также: Индекс удержания Коваца.
- Проба – вещество, анализируемое с помощью хроматографии. Он может состоять из одного компонента или представлять собой смесь компонентов. Когда образец обрабатывается в ходе анализа, фаза или фазы, содержащие интересующие аналиты, называются образцом, тогда как все, что представляет интерес, отделенное от образца до или в ходе анализа, называется образцом. как отходы .
- Растворенное вещество – компоненты пробы в распределительной хроматографии.
- Растворитель – любое вещество, способное растворять другое вещество, особенно жидкую подвижную фазу в жидкостной хроматографии.
- Стационарная фаза – вещество, зафиксированное для процедуры хроматографии. Примеры включают слой кремнезема в тонкослойной хроматографии.
- Детектор – прибор, используемый для качественного и количественного обнаружения аналитов после разделения.
Хроматография основана на понятии коэффициента распределения. Любые перегородки растворенного вещества между двумя несмешивающимися растворителями. Когда один растворитель делают неподвижным (путем адсорбции на твердой матрице носителя), а другой подвижным, это приводит к наиболее распространенным применениям хроматографии. Если матричный носитель или неподвижная фаза полярны (например, целлюлоза , диоксид кремния и т. д.), то это прямофазовая хроматография. неполярная стационарная фаза (например, неполярная производная C-18 В противном случае этот метод известен как обращенная фаза, где используется ).
Методика по форме хроматографического слоя [ править ]
Колоночная хроматография [ править ]
Колоночная хроматография — это метод разделения, при котором неподвижный слой находится внутри пробирки. Частицы твердой неподвижной фазы или носителя, покрытого жидкой неподвижной фазой, могут заполнять весь внутренний объем трубки (насадочной колонны) или концентрироваться на внутренней стенке трубки или вдоль нее, оставляя открытый, неограниченный путь для подвижной фазы в средняя часть трубки (открытая трубчатая колонна). Различия в скоростях движения через среду рассчитаны для разного времени удерживания образца. [13] [14] В 1978 году У. Кларк Стилл представил модифицированную версию колоночной хроматографии, названную флэш-колоночной хроматографией (флэш-хроматографией). [15] [16] Этот метод очень похож на традиционную колоночную хроматографию, за исключением того, что растворитель прогоняется через колонку под положительным давлением. Это позволило выполнить большинство разделений менее чем за 20 минут, при этом разделение было улучшено по сравнению со старым методом. Современные системы флэш-хроматографии продаются в виде предварительно упакованных пластиковых картриджей, через которые прокачивается растворитель. Системы также могут быть связаны с детекторами и коллекторами фракций, обеспечивающими автоматизацию. Внедрение градиентных насосов привело к более быстрому разделению и меньшему использованию растворителя.
При адсорбции в расширенном слое используется псевдоожиженный слой, а не твердая фаза, образованная насадочным слоем. Это позволяет пропустить начальные этапы очистки, такие как центрифугирование и фильтрация, для культуральных бульонов или суспензий разрушенных клеток.
Хроматография фосфоцеллюлозы использует аффинность связывания многих ДНК-связывающих белков с фосфоцеллюлозой. Чем сильнее взаимодействие белка с ДНК, тем выше концентрация соли, необходимая для элюирования этого белка. [17]
Планарная хроматография [ править ]
Планарная хроматография — это метод разделения, при котором неподвижная фаза присутствует в виде плоскости или на ней. Плоскость может представлять собой бумагу, выступающую в качестве таковой или пропитанную веществом в качестве неподвижного слоя ( бумажная хроматография ) или слой твердых частиц, нанесенный на подложку, например стеклянную пластинку ( тонкослойная хроматография ). Различные соединения в смеси образцов перемещаются на разные расстояния в зависимости от того, насколько сильно они взаимодействуют с неподвижной фазой по сравнению с подвижной фазой. Конкретный коэффициент удерживания (R f ) каждого химического вещества можно использовать для идентификации неизвестного вещества.
Бумажная хроматография


Бумажная хроматография – это метод, который предполагает размещение небольшой точки или линии раствора образца на полоске хроматографической бумаги . Бумагу помещают в емкость с неглубоким слоем растворителя и запечатывают. Когда растворитель поднимается через бумагу, он встречается со смесью пробы, которая вместе с растворителем начинает перемещаться вверх по бумаге. Эта бумага сделана из целлюлозы , полярного вещества , и соединения в смеси перемещаются дальше, если они менее полярны. Более полярные вещества быстрее связываются с целлюлозной бумагой и, следовательно, не перемещаются так далеко.
Тонкослойная хроматография (ТСХ) [ править ]

Тонкослойная хроматография (ТСХ) – это широко используемый лабораторный метод, используемый для разделения различных биохимических веществ на основе их относительного притяжения к неподвижной и подвижной фазам. Это похоже на бумажную хроматографию . Однако вместо использования неподвижной фазы бумаги он включает в себя неподвижную фазу тонкого слоя адсорбента , такого как силикагель , оксид алюминия или целлюлоза , на плоской инертной подложке . ТСХ очень универсален; несколько образцов можно разделить одновременно на одном слое, что делает его очень полезным для скрининговых приложений, таких как тестирование уровня наркотиков и чистоты воды. [18]
Возможность перекрестного загрязнения невелика, поскольку каждое разделение выполняется на новом слое. По сравнению с бумагой она имеет преимущество в более быстром анализе, лучшем разделении, лучшем количественном анализе и возможности выбора между различными адсорбентами. Для еще большего разрешения и более быстрого разделения с использованием меньшего количества растворителя высокопроизводительную ТСХ можно использовать . Более раннее популярное использование заключалось в дифференциации хромосом путем наблюдения за расстоянием в геле (разделение было отдельным этапом).
Вытеснительная хроматография [ править ]
Основной принцип вытеснительной хроматографии заключается в следующем:Молекула с высоким сродством к хроматографической матрице (вытеснитель) эффективно конкурирует за места связывания и, таким образом, вытесняет все молекулы с меньшим сродством. [19] Существуют явные различия между вытеснительной и элюционной хроматографией. В режиме элюирования вещества обычно выходят из колонки в виде узких гауссовских пиков. Для максимальной очистки желательно широкое разделение пиков, предпочтительно до базовой линии. Скорость, с которой любой компонент смеси перемещается по колонке в режиме элюирования, зависит от многих факторов. Но для того, чтобы два вещества двигались с разной скоростью и, таким образом, растворялись, должны существовать существенные различия во взаимодействии между биомолекулами и хроматографической матрицей. Рабочие параметры корректируются так, чтобы максимизировать эффект этой разницы. Во многих случаях разделение пиков по базовой линии может быть достигнуто только при градиентном элюировании и низкой загрузке колонки. Таким образом, двумя недостатками элюционной хроматографии, особенно в препаративном масштабе, являются сложность эксплуатации из-за градиентной перекачки растворителя и низкая пропускная способность из-за низкой загрузки колонки. Вытесняющая хроматография имеет преимущества перед элюционной хроматографией в том, что компоненты разделяются на последовательные зоны чистых веществ, а не на «пики». Поскольку этот процесс использует преимущества Из-за нелинейности изотерм на данной колонке можно разделить большее количество сырья, при этом очищенные компоненты извлекаются в значительно более высоких концентрациях.
Методики по физическому состоянию подвижной фазы [ править ]
Газовая хроматография [ править ]
Газовая хроматография (ГХ), также иногда известная как газожидкостная хроматография (ГЖХ), представляет собой метод разделения, в котором подвижной фазой является газ. Газохроматографическое разделение всегда проводят в колонке, которая обычно является «насадочной» или «капиллярной». Насадочные колонки — это обычные рабочие лошадки газовой хроматографии, они дешевле и проще в использовании и часто дают адекватную производительность. Капиллярные колонки обычно дают гораздо более высокое разрешение и, хотя и более дорогие, становятся широко используемыми, особенно для сложных смесей. Кроме того, капиллярные колонки можно разделить на три класса: открытые трубчатые колонки с пористым слоем (PLOT), открытые трубчатые колонки со стенками (WCOT) и открытые трубчатые колонки с опорным покрытием (SCOT). Колонки PLOT уникальны тем, что неподвижная фаза адсорбируется на стенках колонки, тогда как колонки WCOT имеют неподвижную фазу, химически связанную со стенками. Колонки SCOT в некотором смысле представляют собой комбинацию двух упомянутых типов в том смысле, что частицы носителя приклеены к стенкам колонны, но на этих частицах химически связана жидкая фаза. [20] Оба типа колонок изготовлены из неадсорбирующих и химически инертных материалов. Нержавеющая сталь и стекло являются обычными материалами для насадочных колонок, а кварц или кварцевый кварц – для капиллярных колонок.
Газовая хроматография основана на равновесии распределения аналита между твердой или вязкой жидкой неподвижной фазой (часто жидким материалом на основе силикона) и подвижным газом (чаще всего гелием). Неподвижная фаза прилипает к внутренней части стеклянной трубки небольшого диаметра (обычно внутренний диаметр 0,53–0,18 мм) или трубки из плавленого кварца (капиллярная колонка) или к твердой матрице внутри металлической трубки большего размера (насадочная колонка). Он широко используется в аналитической химии ; хотя высокие температуры, используемые в ГХ, делают его непригодным для высокомолекулярных биополимеров или белков (тепло денатурирует их), часто встречающихся в биохимии , он хорошо подходит для использования в нефтехимии , мониторинге и восстановлении окружающей среды , а также в промышленной химии . Он также широко используется в химических исследованиях.
Жидкостная хроматография [ править ]
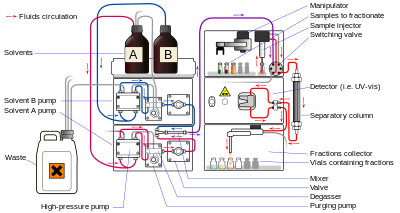
Жидкостная хроматография (ЖХ) – это метод разделения, при котором подвижной фазой является жидкость. Его можно выполнять как в колонне, так и в плоскости. Современная жидкостная хроматография, в которой обычно используются очень мелкие насадочные частицы и относительно высокое давление, называется высокоэффективной жидкостной хроматографией .
При ВЭЖХ образец проталкивается жидкостью под высоким давлением (подвижная фаза) через колонку, заполненную неподвижной фазой, состоящей из частиц неправильной или сферической формы, пористого монолитного слоя или пористой мембраны. Монолиты - это «губчатые хроматографические среды». [21] и состоят из бесконечного блока органических или неорганических частей. ВЭЖХ исторически делится на два разных подкласса в зависимости от полярности подвижной и стационарной фаз. Методы, в которых неподвижная фаза более полярна, чем подвижная фаза (например, толуол в качестве подвижной фазы, диоксид кремния в качестве неподвижной фазы), называются нормально-фазовой жидкостной хроматографией (НЖХ), а противоположные методы (например, смесь воды и метанола в качестве подвижной фазы). фаза и C18 ( октадецилсилил ) в качестве неподвижной фазы) называется жидкостной хроматографией с обращенной фазой (RPLC).
жидкостная Сверхкритическая хроматография
Сверхкритическая жидкостная хроматография — это метод разделения, в котором подвижной фазой является жидкость, температура и давление которой выше и относительно близки к ее критической температуре.
Конкретные методы, относящиеся к этому широкому заголовку, перечислены ниже.
Аффинная хроматография [ править ]
Аффинная хроматография [22] основан на избирательном нековалентном взаимодействии между аналитом и конкретными молекулами. Это очень специфично, но не очень надежно. [23] Его часто используют в биохимии для очистки белков, связанных с метками. Эти слитые белки помечены такими соединениями, как His-метки , биотин или антигены , которые специфически связываются с неподвижной фазой. После очистки эти метки обычно удаляются и получается чистый белок.
Аффинная хроматография часто использует сродство биомолекулы к катионам металла (Zn, Cu, Fe и т. д.). Колонки часто готовятся вручную и могут быть разработаны специально для интересующих белков. Традиционные аффинные колонки используются в качестве подготовительного этапа для удаления нежелательных биомолекул или в качестве основного этапа анализа белка с неизвестными физическими свойствами. [24]
Однако существуют методы жидкостной хроматографии, которые используют свойства аффинной хроматографии. Аффинная хроматография с иммобилизованными металлами (IMAC) [25] [26] полезно разделить вышеупомянутые молекулы на основе относительного сродства к металлу. Часто эти колонки могут быть загружены различными металлами для создания колонки с заданным сродством. [27]
Техники по механизму разделения [ править ]
Ионообменная хроматография [ править ]
Ионообменная хроматография (обычно называемая ионной хроматографией) использует механизм ионного обмена для разделения аналитов на основе их соответствующих зарядов. Обычно это выполняется в столбцах, но может быть полезно и в плоском режиме. Ионообменная хроматография использует заряженную неподвижную фазу для разделения заряженных соединений, включая анионы , катионы , аминокислоты , пептиды и белки . В традиционных методах неподвижной фазой является ионообменная смола , несущая заряженные функциональные группы , которые удерживаются при взаимодействии с противоположно заряженными группами соединения. Существует два типа ионообменной хроматографии: катионообменная и анионообменная. В катионообменной хроматографии неподвижная фаза имеет отрицательный заряд, а обменный ион представляет собой катион, тогда как в анионообменной хроматографии неподвижная фаза имеет положительный заряд, а обменный ион представляет собой анион. [28] Ионообменная хроматография обычно используется для очистки белков с использованием FPLC .
Эксклюзионная хроматография [ править ]
Эксклюзионная хроматография (SEC) также известна как гель-проникающая хроматография (GPC) или гель-фильтрационная хроматография и разделяет молекулы в соответствии с их размером (или, точнее, в соответствии с их гидродинамическим диаметром или гидродинамическим объемом).Молекулы меньшего размера способны проникать в поры носителя и, следовательно, молекулы улавливаются и удаляются из потока подвижной фазы. Среднее время пребывания в порах зависит от эффективного размера молекул аналита. Однако молекулы, размер которых превышает средний размер пор насадки, исключаются и, таким образом, практически не удерживаются; такие виды элюируются первыми. Обычно это метод хроматографии низкого разрешения, поэтому его часто используют для заключительного, «полирующего» этапа очистки. Он также полезен для определения третичной и четвертичной структуры очищенных белков, тем более что его можно проводить в условиях нативного раствора.
разделение в расширенном слое Адсорбционное хроматографическое
Колонна хроматографической адсорбции с расширенным слоем (EBA) для процесса биохимического разделения включает распределитель жидкости для выравнивания давления, имеющий функцию самоочистки под пористой блокирующей ситовой пластиной в нижней части расширенного слоя, узел сопла в верхней части, имеющий функцию очистки обратной промывкой. в верхней части расширенного слоя лучшее распределение исходного раствора, добавленного в расширенный слой, обеспечивает то, что жидкость, проходящая через слой расширенного слоя, демонстрирует состояние поршневого потока. Слой расширенного слоя отображает состояние поршневого потока. Хроматографическая разделительная колонна с расширенным слоем имеет преимущества, заключающиеся в повышении эффективности разделения расширенного слоя.
Адсорбционная хроматография в расширенном слое (EBA) — удобный и эффективный метод улавливания белков непосредственно из неосветленной пробы сырой нефти. В хроматографии EBA осевший слой сначала расширяется восходящим потоком уравновешивающего буфера. Сырой корм, представляющий собой смесь растворимых белков, примесей, клеток и клеточного мусора, затем подается вверх через расширенный слой. Целевые белки захватываются адсорбентом, а частицы и загрязнения проходят сквозь него. Замена буфера для элюирования при сохранении восходящего потока приводит к десорбции целевого белка в режиме расширенного слоя. Альтернативно, если поток повернуть вспять, адсорбированные частицы быстро осядут, и белки можно будет десорбировать с помощью элюирующего буфера. Режим, используемый для элюирования (расширенный слой или осевший слой), зависит от характеристик сырья. После элюирования адсорбент очищают заранее заданным раствором для безразборной мойки (CIP), после очистки следует либо регенерация колонки (для дальнейшего использования), либо хранение.
Специальные техники [ править ]
Обратно-фазовая хроматография [ править ]
Обращенно-фазовая хроматография (RPC) — это любая процедура жидкостной хроматографии, в которой подвижная фаза значительно более полярна, чем неподвижная фаза. Она названа так потому, что в нормально-фазовой жидкостной хроматографии подвижная фаза значительно менее полярна, чем неподвижная. Гидрофобные молекулы в подвижной фазе имеют тенденцию адсорбироваться на относительно гидрофобной неподвижной фазе. Гидрофильные молекулы в подвижной фазе будут стремиться элюироваться первыми. Разделительные колонки обычно содержат углеродную цепь C8 или C18, связанную с подложкой из частиц диоксида кремния.
Хроматография гидрофобного взаимодействия
Хроматография гидрофобного взаимодействия (HIC) — это метод очистки и анализа, который разделяет аналиты, такие как белки, на основе гидрофобных взаимодействий между этим аналитом и хроматографической матрицей. Он может обеспечить неденатурирующий ортогональный подход к обращенно-фазовому разделению, сохраняя нативные структуры и потенциально активность белка. В хроматографии гидрофобного взаимодействия материал матрицы слегка заменяется гидрофобными группами. Эти группы могут варьироваться от метильных, этильных, пропильных, бутильных, октильных или фенильных групп. [29] При высоких концентрациях соли неполярные боковые цепи на поверхности белков «взаимодействуют» с гидрофобными группами; то есть оба типа групп исключаются полярным растворителем (гидрофобные эффекты усиливаются за счет увеличения ионной силы). Таким образом, образец наносится на колонку в высокополярном буфере, что приводит к ассоциации гидрофобных участков аналита с неподвижной фазой. Элюент обычно представляет собой водный буфер с уменьшающейся концентрацией соли, увеличивающейся концентрацией детергента (который нарушает гидрофобные взаимодействия) или изменениями pH. Решающее значение имеет тип используемой соли: более космотропные соли, определенные в ряду Хофмайстера, обеспечивают наибольшее структурирование воды вокруг молекулы и, как следствие, гидрофобное давление. Для этой цели часто используют сульфат аммония. Добавление органических растворителей или других менее полярных компонентов может способствовать улучшению разрешения.
В целом, хроматография гидрофобного взаимодействия (HIC) предпочтительна, если образец чувствителен к изменению pH или к агрессивным растворителям, обычно используемым в других типах хроматографии, но не к высоким концентрациям солей. Обычно варьируется количество соли в буфере. В 2012 году Мюллер и Францреб описали влияние температуры на HIC, используя бычий сывороточный альбумин (БСА) с четырьмя различными типами гидрофобных смол. В ходе исследования изменялась температура, чтобы повлиять на аффинность связывания BSA с матрицей. Был сделан вывод, что циклическое повышение температуры от 50 до 10 градусов будет недостаточным для эффективного вымывания всего БСА из матрицы, но может быть очень эффективным, если колонку использовать всего несколько раз. [30] Использование температуры для изменения температуры позволяет лабораториям сократить расходы на покупку соли и сэкономить деньги.
Если нужно избежать высоких концентраций соли и колебаний температуры, можно использовать более гидрофобный раствор, чтобы конкурировать с образцом за его элюирование. Этот так называемый солевой независимый метод HIC продемонстрировал прямое выделение человеческого иммуноглобулина G (IgG) из сыворотки с удовлетворительным выходом и использовал β-циклодекстрин в качестве конкурента для вытеснения IgG из матрикса. [31] Это в значительной степени открывает возможность использования HIC с образцами, чувствительными к соли, поскольку мы знаем, что высокие концентрации соли осаждают белки.
Гидродинамическая хроматография [ править ]
Гидродинамическая хроматография (ГДХ) основана на наблюдаемом явлении, заключающемся в том, что большие капли движутся быстрее, чем маленькие. [32] В колонне это происходит потому, что центр масс более крупных капель не может находиться так близко к краям колонны, как более мелкие капли, из-за их большего общего размера. [33] Капли большего размера будут элюироваться первыми из середины колонки, а капли меньшего размера прилипнут к боковым частям колонки и элюируются последними. Эта форма хроматографии полезна для разделения аналитов по молярной массе (или молекулярной массе), размеру, форме и структуре при использовании в сочетании с светорассеяния детекторами , вискозиметрами и рефрактометрами . [34] Двумя основными типами HDC являются открытые пробирки и насадочные колонки . Открытая трубка обеспечивает быстрое разделение мелких частиц, тогда как насадочная колонка HDC может повысить разрешение и лучше подходит для частиц со средней молекулярной массой более Дальтоны . [35] HDC отличается от других типов хроматографии тем, что разделение происходит только в промежуточном объеме, который представляет собой объем, окружающий частицы и между ними в насадочной колонке. [36]
HDC использует тот же порядок элюирования, что и эксклюзионная хроматография (SEC), но эти два процесса по-прежнему во многом различаются. [35] В исследовании, сравнивающем два типа разделения, Изенберг, Брюэр, Коте и Стригель использовали оба метода для определения характеристик полисахаридов и пришли к выводу, что HDC в сочетании с многоугловым рассеянием света (MALS) обеспечивает более точное распределение молярной массы по сравнению с автономным MALS, чем SEC в значительно более короткие сроки. [37] Во многом это связано с тем, что ЭХ является более деструктивным методом из-за пор в колонке, которые разрушают аналит во время разделения, что имеет тенденцию влиять на массовое распределение. [37] Однако основным недостатком HDC является низкое разрешение пиков аналитов, что делает SEC более жизнеспособным вариантом при использовании с химическими веществами, которые трудно разлагаются и где быстрое элюирование не важно. [38]
HDC играет особенно важную роль в области микрофлюидики . Первое успешное устройство для системы HDC-на-чипе было предложено Чмелой и др. в 2002 году. [39] Их конструкция позволила добиться разделения с использованием канала длиной 80 мм за время 3 минуты для частиц диаметром от 26 до 110 нм, но авторы выразили необходимость улучшить параметры удерживания и дисперсии . [39] В публикации Джеллемы, Маркестейна, Вестервила и Верпоорте в 2010 году внедрение HDC с рециркулирующим двунаправленным потоком привело к разделению с высоким разрешением и размером по размеру с каналом длиной всего 3 мм. [40] Наличие такого короткого канала и высокого разрешения было расценено как особенно впечатляющее, учитывая, что в предыдущих исследованиях использовались каналы длиной 80 мм. [39] Что касается биологического применения, в 2007 году Huh et al. предложил микрофлюидное сортировочное устройство на основе HDC и гравитации, которое было полезно для предотвращения попадания потенциально опасных частиц диаметром более 6 микрон в кровоток при введении контрастных веществ при ультразвуковом исследовании . [41] Это исследование также способствовало обеспечению экологической устойчивости в микрофлюидике из-за отсутствия внешней электроники, управляющей потоком, что стало преимуществом использования устройства на основе гравитации.

Двумерная хроматография [ править ]
В некоторых случаях селективность, обеспечиваемая использованием одной колонки, может оказаться недостаточной для обеспечения разделения аналитов в сложных пробах. Двумерная хроматография направлена на увеличение разрешения этих пиков за счет использования второй колонки с другими физико-химическими ( химическими классификационными ) свойствами. [42] [43] можно разделить соединения Поскольку механизм удерживания на этом новом твердом носителе отличается от механизма первого измерения, с помощью двумерной хроматографии , которые неотличимы при одномерной хроматографии. Более того, разделение во втором измерении происходит быстрее, чем в первом измерении. [42] Примером двумерного разделения ТСХ является то, что образец наносится на один угол квадратной пластины, проявляется, сушится на воздухе, затем поворачивается на 90° и обычно повторно проявляется во второй системе растворителей. Двумерная хроматография может применяться для разделения с помощью ГХ или ЖХ. [42] [43] Этот метод разделения также может быть использован в душераздирающем подходе, [44] когда конкретные области интереса по первому измерению выбираются для разделения по второму измерению или при комплексном подходе, [42] [43] где все аналиты из первого измерения подвергаются разделению во втором измерении.
слоем с подвижным Имитированная хроматография
Метод имитации движущегося слоя (SMB) представляет собой вариант высокоэффективной жидкостной хроматографии; он используется для разделения частиц и/или химических соединений, которые другим способом было бы трудно или невозможно разделить. Это увеличенное разделение достигается за счет конструкции клапана и колонны, которая используется для неограниченного удлинения стационарной фазы.В методе препаративной хроматографии с подвижным слоем подача сырья и извлечение аналита происходят одновременно и непрерывно, но из-за практических трудностей с непрерывно движущимся слоем был предложен метод имитации движущегося слоя. В методе имитации движущегося слоя вместо перемещения слоя положения входа пробы и выхода аналита постоянно перемещаются, создавая впечатление движущегося слоя.Настоящая хроматография с подвижным слоем (TMBC) – это всего лишь теоретическая концепция. Его имитация SMBC достигается за счет использования множества последовательно соединенных колонн и сложной конструкции клапанов. Такое расположение клапанов обеспечивает подачу пробы и растворителя, а также отбор аналита и отходов в соответствующих местах любой колонки, при этом он позволяет через регулярные промежутки времени переключать подачу пробы в одном направлении, подачу растворителя в противоположном направлении, одновременно меняя отбор аналита и отходов. позиции также соответствующие.
газовая Пиролизная хроматография
Пиролиз-газовая хроматография-масс-спектрометрия — это метод химического анализа, при котором образец нагревается до разложения с образованием более мелких молекул, которые разделяются газовой хроматографией и обнаруживаются с помощью масс-спектрометрии.
Пиролиз — это термическое разложение материалов в инертной атмосфере или вакууме. Образец приводят в непосредственный контакт с платиновой проволокой или помещают в кварцевую пробирку и быстро нагревают до 600–1000 °C. В зависимости от применения используются даже более высокие температуры. В реальных пиролизёрах используются три различных метода нагрева: изотермическая печь, индукционный нагрев (нить точки Кюри) и резистивный нагрев с использованием платиновых нитей. Большие молекулы расщепляются в самых слабых местах и образуют более мелкие и летучие фрагменты. Эти фрагменты можно разделить с помощью газовой хроматографии. Хроматограммы пиролизной ГХ обычно сложны, поскольку образуется широкий спектр различных продуктов разложения. Данные можно использовать либо в качестве отпечатков пальцев для подтверждения идентичности материала, либо данные ГХ/МС используются для идентификации отдельных фрагментов и получения структурной информации. Для повышения летучести полярных фрагментов перед пиролизом в образец можно добавлять различные метилирующие реагенты.
Помимо использования специальных пиролизеров, пиролизную ГХ твердых и жидких образцов можно проводить непосредственно в инжекторах испарителя с программируемой температурой (PTV), которые обеспечивают быстрый нагрев (до 30 °C/с) и высокие максимальные температуры 600–650 °C. Этого достаточно для некоторых применений пиролиза. Основное преимущество заключается в том, что не требуется приобретать специальный инструмент, а пиролиз можно проводить как часть рутинного ГХ-анализа. В этом случае необходимо использовать кварцевые входные лайнеры для ГХ. Могут быть получены количественные данные, а также опубликованы хорошие результаты дериватизации внутри инжектора PTV.
жидкостная белков Быстрая хроматография
Быстрая жидкостная хроматография белков (FPLC) — это форма жидкостной хроматографии, которая часто используется для анализа или очистки смесей белков. Как и в других формах хроматографии, разделение возможно, поскольку разные компоненты смеси имеют разное сродство к двум материалам: движущейся жидкости («подвижная фаза») и пористому твердому веществу (неподвижная фаза). В FPLC подвижная фаза представляет собой водный раствор или «буфер». Расход буфера контролируется поршневым насосом и обычно поддерживается постоянным, в то время как состав буфера можно изменять путем отбора жидкостей в разных пропорциях из двух или более внешних резервуаров. Неподвижная фаза представляет собой смолу, состоящую из шариков, обычно из сшитой агарозы , упакованных в цилиндрическую стеклянную или пластиковую колонку. Смолы FPLC доступны в широком диапазоне размеров гранул и поверхностных лигандов в зависимости от применения.
Противоточная хроматография [ править ]
Противоточная хроматография (CCC) — это тип жидкостно-жидкостной хроматографии, в котором как неподвижная, так и подвижная фазы являются жидкостями, а жидкая неподвижная фаза удерживается в застое под действием сильной центробежной силы. [45]
Гидродинамическая противоточная хроматография (CCC) [ править ]
Принцип работы прибора CCC предполагает наличие колонки, состоящей из открытой трубки, намотанной на катушку. Шпулька вращается по двойной оси (кардиоида), что приводит к воздействию переменного гравитационного поля (G) на колонну во время каждого вращения. Это движение приводит к тому, что колонка совершает один шаг разделения за один оборот, и компоненты образца разделяются в колонке из-за их коэффициента разделения между двумя используемыми несмешивающимися жидкими фазами. Сегодня существует множество типов CCC. К ним относятся HSCCC (высокоскоростной CCC) и HPCCC (высокопроизводительный CCC). HPCCC — это новейшая и наиболее эффективная версия инструмента, доступного в настоящее время.
Центробежная распределительная хроматография (ЦПХ) [ править ]
В приборе CPC (центробежная распределительная хроматография или гидростатическая противоточная хроматография) колонка состоит из ряда ячеек, соединенных между собой каналами, прикрепленными к ротору. Этот ротор вращается вокруг своей центральной оси, создавая центробежное поле, необходимое для удержания неподвижной фазы на месте. Процесс разделения в CPC регулируется исключительно разделением растворенных веществ между неподвижной и подвижной фазами, механизм которого можно легко описать с помощью коэффициентов разделения ( K D ) растворенных веществ. Приборы CPC коммерчески доступны для лабораторного, пилотного и промышленного разделения с колонками разного размера, от 10 миллилитров до 10 литров по объему.
противоточная хроматография Периодическая
В отличие от противоточной хроматографии (см. выше), периодическая противоточная хроматография (ПХХ) использует твердую неподвижную фазу и только жидкую подвижную фазу. Таким образом, она гораздо больше похожа на обычную аффинную хроматографию, чем на противоточную хроматографию. PCC использует несколько столбцов, которые на этапе загрузки соединяются в линию. Этот режим позволяет перегрузить первую колонку этой серии без потери продукта, который уже прорывается через колонку до полного насыщения смолы. Продукт прорыва фиксируется в последующих колонках. На следующем этапе колонки отключаются друг от друга. Первую колонку промывают и элюируют, в то время как другие колонки все еще загружаются. Как только (первоначально) первая колонка снова уравновешивается, она снова вводится в поток загрузки, но уже как последняя колонка. Далее процесс продолжается циклически.
Хиральная хроматография [ править ]
Хиральная хроматография предполагает разделение стереоизомеров . В случае энантиомеров они не имеют никаких химических или физических различий, кроме трехмерного зеркального отображения. Чтобы обеспечить возможность хирального разделения, либо подвижная фаза, либо неподвижная фаза сами должны быть хиральными, что обеспечивает различное сродство между аналитами. Колонки для хиральной хроматографии ВЭЖХ (с хиральной неподвижной фазой) как в нормальной, так и в обращенной фазе коммерчески доступны.
Обычная хроматография не способна разделить рацемические смеси энантиомеров. Однако в некоторых случаях нерацемические смеси энантиомеров могут быть неожиданно разделены с помощью обычной жидкостной хроматографии (например, ВЭЖХ без хиральной подвижной фазы или неподвижной фазы). [46] [47]
-фазовая нормально Водная хроматография
Водная нормально-фазовая (ANP) хроматография характеризуется элюирующим поведением классического нормально-фазового режима (т.е. когда подвижная фаза значительно менее полярна, чем неподвижная фаза), в котором вода является одним из компонентов системы растворителей подвижной фазы. Она отличается от жидкостной хроматографии с гидрофильным взаимодействием (HILIC) тем, что механизм удерживания обусловлен адсорбцией, а не разделением. [48]
Приложения [ править ]
Хроматография используется во многих областях, включая фармацевтическую промышленность , пищевую промышленность , , химическую промышленность , судебную медицину окружающей среды анализ и больницы . [49]
См. также [ править ]
- Аффинная хроматография
- Водная нормально-фазовая хроматография
- Селективность связывания
- Хиральный анализ
- хроматофокусирование
- Хроматография при обработке крови
- Программное обеспечение для хроматографии
- Глюматография
- Многоколоночная противоточная градиентная очистка растворителей (MCSGP)
- Уравнение Пурнелла
- Уравнение Ван Деемтера
Ссылки [ править ]
- ^ Макмерри Дж. (2011). Органическая химия: с биологическими приложениями (2-е изд.). Бельмонт, Калифорния: Брукс/Коул. стр. 395 . ISBN 9780495391470 .
- ^ Гонсалес-Гонсалес М., Майоло-Делойза К., Рито-Паломарес М. (1 января 2020 г.), Матте А (ред.), «Глава 5 - Последние достижения в монолитной хроматографии на основе антител для терапевтического применения», Подходы к очистке, анализу и характеристика терапии на основе антител , Elsevier, стр. 105–116, doi : 10.1016/b978-0-08-103019-6.00005-9 , ISBN 978-0-08-103019-6 , S2CID 226450210
- ^ Альтернативные операции биоразделения: жизнь за пределами хроматографии с насадочным слоемTM Przybycien, NS Pujar и LM SteeleCurr Opin Biotechnol, 15 (5) (2004), стр. 469-478.
- ^ Онкудон СМ, Кансил Т, Вонг С (2014). «Проблемы и стратегии получения монолитных хроматографических адсорбентов на основе полимеров большого объема» . Журнал науки о разделении . 37 (5): 455–464. дои : 10.1002/jssc.201300995 . ISSN 1615-9314 . ПМИД 24376196 .
- ^ Гонсалес-Гонсалес М., Майоло-Делойза К., Рито-Паломарес М. (1 января 2020 г.), Матте А (ред.), «Глава 5 - Последние достижения в монолитной хроматографии на основе антител для терапевтического применения», Подходы к очистке, анализу и характеристика терапии на основе антител , Elsevier, стр. 105–116, doi : 10.1016/b978-0-08-103019-6.00005-9 , ISBN 978-0-08-103019-6 , S2CID 226450210
- ^ Хостеттманн К., Марстон А., Хостеттманн М. (1998). Применение методов препаративной хроматографии при выделении натуральных продуктов (второе изд.). Берлин, Гейдельберг: Springer Berlin Heidelberg. п. 50. ISBN 9783662036310 .
- ^ Харпер Д. «Хроматография» . Интернет-словарь этимологии .
- ^ Эттре Л.С., Златкис А., ред. (26 августа 2011 г.). 75 лет хроматографии: исторический диалог . Эльзевир. ISBN 978-0-08-085817-3 .
- ^ Эттре Л.С. (май 2003 г.). «М. С. Цветт и изобретение хроматографии» (PDF) . LCGC Северная Америка . 21 (5): 458–467.
- ^ Эттре Л.С., Сакодинский К.И. (март 1993 г.). «М. С. Цветт и открытие хроматографии II: Завершение развития хроматографии (1903–1910)». Хроматография . 35 (5–6): 329–338. дои : 10.1007/BF02277520 . S2CID 97052560 .
- ^ «Нобелевская премия по химии 1952 года» . nobelprize.org . Проверено 25 августа 2016 г.
- ^ Jump up to: Перейти обратно: а б с д Борман С (1987). «Элюент, сточные воды, элюат и элюит». Аналитическая химия . 59 (2): 99А. дои : 10.1021/ac00129a735 .
- ^ Эттре Л.С. (1993). «Номенклатура хроматографии (Рекомендации ИЮПАК 1993 г.)» . Чистая и прикладная химия . 65 (4): 819–872. дои : 10.1351/pac199365040819 .
- ^ Маниш Т. «Как работает колоночная хроматография?» . БрайтМагс. Архивировано из оригинала 21 апреля 2017 года . Проверено 7 апреля 2017 г.
- ^ Still WC, Кан М, Митра А (1978). «Быстрая хроматографическая техника препаративного разделения с умеренным разрешением». Дж. Орг. хим. 43 (14): 2923–2925. CiteSeerX 10.1.1.476.6501 . дои : 10.1021/jo00408a041 .
- ^ Харвуд Л.М., Муди С.Дж. (1989). Экспериментальная органическая химия: принципы и практика (Иллюстрированное издание). Уайли Блэквелл. стр. 180–185 . ISBN 978-0-632-02017-1 .
- ^ Буржуа С., Пфаль М. (1976). «Репрессоры». В Anfinsen CB, Edsall JT, Richards FM (ред.). Достижения в области химии белков . Том. 30. Академическая пресса. стр. 6–7. дои : 10.1016/S0065-3233(08)60478-7 . ISBN 978-0-12-034230-3 . ПМИД 779429 .
- ^ Бернард Ф (2003). Справочник по тонкослойной хроматографии . Марселя Деккера Inc. ISBN 978-0824748661 . OCLC 437068122 .
- ^ Вытесняющая хроматография 101. Архивировано 15 сентября 2008 г. в Wayback Machine . Sachem, Inc. Остин, Техас 78737
- ^ Рахман М., Эль-Ати А., Чой Дж. Х., Шин Х. К., Шин СК, Шим Дж. Х. (ноябрь 2015 г.). «Глава 3. Основной обзор колонок для газовой хроматографии». Аналитическая наука о разделении . Джон Уайли и сыновья. стр. 823–834. ISBN 9783527333745 .
- ^ Гонсалес-Гонсалес М., Майоло-Делойза К., Рито-Паломарес М. (1 января 2020 г.), Матте А (ред.), «Глава 5 - Последние достижения в монолитной хроматографии на основе антител для терапевтического применения», Подходы к очистке, анализу и характеристика терапии на основе антител , Elsevier, стр. 105–116, doi : 10.1016/b978-0-08-103019-6.00005-9 , ISBN 978-0-08-103019-6 , S2CID 226450210
- ^ Вилчек М., Чайкен I (2000). «Обзор аффинной хроматографии». В Bailon P, Эрлих Г.К., Фунг В.Дж., Бертольд В. (ред.). Аффинная хроматография . Методы молекулярной биологии. Том. 147. Хумана Пресс. стр. 1–6. дои : 10.1007/978-1-60327-261-2_1 . ISBN 978-1-60327-261-2 . ПМИД 10857080 .
- ^ Урх М, Симпсон Д., Чжао К. (2009). «Глава 26. Аффинная хроматография» . Руководство по очистке белков, 2-е издание . Методы энзимологии. Том. 463. стр. 417–438. дои : 10.1016/S0076-6879(09)63026-3 . ISBN 9780123745361 . ПМИД 19892186 .
- ^ Марквелл Дж. (сентябрь 2009 г.). «Фундаментальные лабораторные подходы к биохимии и биотехнологии, 2-е издание» . Образование в области биохимии и молекулярной биологии . 37 (5): 317–318. дои : 10.1002/bmb.20321 . ISSN 1470-8175 .
- ^ Сингх Н.К., Д.Суза Р.Н., Биби Н.С., Фернандес-Лахор М. (2015). «Прямой захват белков, меченных His6, с использованием мегапористых криогелей, разработанных для металл-ионной аффинной хроматографии». В Райхельте С. (ред.). Аффинная хроматография . Методы молекулярной биологии. Том. 1286. стр. 201–12. дои : 10.1007/978-1-4939-2447-9_16 . ISBN 978-1-4939-2447-9 . ПМИД 25749956 .
- ^ Габерц-Порекар В., Менарт В. (октябрь 2001 г.). «Перспективы аффинной хроматографии с иммобилизованными металлами». Журнал биохимических и биофизических методов . 49 (1–3): 335–60. дои : 10.1016/S0165-022X(01)00207-X . ПМИД 11694288 .
- ^ Махмуди Гомари М., Сарайгорд-Афшари Н., Фарсимадан М., Ростами Н., Агамири С., Фарахоллахи М.М. (декабрь 2020 г.). «Возможности и проблемы методов очистки белков с помощью меток: применение в фармацевтической промышленности» . Достижения биотехнологии . 45 : 107653. doi : 10.1016/j.biotechadv.2020.107653 . ISSN 0734-9750 . ПМИД 33157154 . S2CID 226276355 .
- ^ Нинфа Эй Джей (2009). Фундаментальные лабораторные подходы к биохимии и биотехнологии . ISBN 978-0-470-47131-9 .
- ^ Нинфа А.Дж., Баллу Д.П., Бенор М. (2010). Фундаментальные лабораторные подходы к биохимии и биотехнологии . Хобокен, Нью-Джерси: Джон Уайли.
- ^ Мюллер Т.К., Францреб М. (октябрь 2012 г.). «Пригодность коммерческих сорбентов гидрофобного взаимодействия для терморегулируемой жидкостной хроматографии белков в условиях низкого содержания солей». Журнал хроматографии А. 1260 : 88–96. дои : 10.1016/j.chroma.2012.08.052 . ПМИД 22954746 .
- ^ Рен Дж, Яо П, Чен Дж, Цзя Л (ноябрь 2014 г.). «Солевая гидрофобно-вытеснительная хроматография для очистки антител с использованием циклодекстрина в качестве надмолекулярного вытеснителя». Журнал хроматографии А. 1369 : 98–104. дои : 10.1016/j.chroma.2014.10.009 . ПМИД 25441076 .
- ^ Сонг Х, Тайс Дж.Д., Исмагилов Р.Ф. (февраль 2003 г.). «Микрофлюидная система для управления реакционными сетями во времени». Ангеванде Хеми . 42 (7): 768–72. дои : 10.1002/anie.200390203 . ПМИД 12596195 .
- ^ Смолл Х., Лангхорст, Массачусетс (1 июля 1982 г.). «Гидродинамическая хроматография». Аналитическая химия . 54 (8): 892А–898А. дои : 10.1021/ac00245a724 . ISSN 0003-2700 .
- ^ Брюэр А.К., Стригель А.М. (апрель 2011 г.). «Характеристика коллоидного кремнезема с жемчужной нитью с помощью многодетекторной гидродинамической хроматографии и сравнение с многодетекторной эксклюзионной хроматографией, автономным многоугловым статическим рассеянием света и просвечивающей электронной микроскопией». Аналитическая химия . 83 (8): 3068–75. дои : 10.1021/ac103314c . ПМИД 21428298 .
- ^ Jump up to: Перейти обратно: а б Стегеман Г., ван Астен А.С., Краак Дж.К., Поппе Х., Тейссен Р. (1994). «Сравнение разрешающей способности и времени разделения при термическом фракционировании в полевом потоке, гидродинамической хроматографии и эксклюзионной хроматографии» . Аналитическая химия . 66 (7): 1147–1160. дои : 10.1021/ac00079a033 . ISSN 0003-2700 .
- ^ Смолл H (1 июля 1974 г.). «Гидродинамическая хроматография – метод анализа размеров коллоидных частиц». Журнал коллоидной и интерфейсной науки . 48 (1): 147–161. Бибкод : 1974JCIS...48..147S . дои : 10.1016/0021-9797(74)90337-3 . ISSN 0021-9797 .
- ^ Jump up to: Перейти обратно: а б Айзенберг С.Л., Брюэр А.К., Коте Г.Л., Стригель А.М. (сентябрь 2010 г.). «Характеристика альтернана по сравнению с эксклюзионной хроматографией и сравнение с автономным MALS». Биомакромолекулы . 11 (9): 2505–11. дои : 10.1021/bm100687b . ПМИД 20690593 .
- ^ Стригель А.М., Брюэр А.К. (19 июля 2012 г.). «Гидродинамическая хроматография». Ежегодный обзор аналитической химии . 5 (1): 15–34. Бибкод : 2012ARAC....5...15S . doi : 10.1146/annurev-anchem-062011-143107 . ПМИД 22708902 .
- ^ Jump up to: Перейти обратно: а б с Чмела Э., Тейссен Р., Блом М.Т., Гарденьерс Х.Дж., ван ден Берг А. (июль 2002 г.). «Чиповая система для разделения макромолекул и частиц по размеру методом гидродинамической хроматографии» (PDF) . Аналитическая химия . 74 (14): 3470–5. дои : 10.1021/ac0256078 . ПМИД 12139056 . S2CID 6948037 .
- ^ Джеллема Л.Дж., Маркестейн А.П., Вестервел Дж., Верпорте Э. (май 2010 г.). «Перестраиваемая гидродинамическая хроматография микрочастиц, локализованных в коротких микроканалах». Аналитическая химия . 82 (10): 4027–35. дои : 10.1021/ac902872d . ПМИД 20423105 .
- ^ Ху Д., Банг Дж. Х., Линг Ю., Вэй Х. Х., Крипфганс О. Д., Фаулкс Дж. Б. и др. (февраль 2007 г.). «Устройство гравитационной микрожидкостной сортировки частиц с гидродинамическим усилением разделения» . Аналитическая химия . 79 (4): 1369–76. дои : 10.1021/ac061542n . ПМЦ 2527745 . ПМИД 17297936 .
- ^ Jump up to: Перейти обратно: а б с д Пребихало С.Э., Берье К.Л., Фрей CE, Бахагигат Х.Д., Мур Н.Р., Пинкертон Д.К., Synovec RE (январь 2018 г.). «Многомерная газовая хроматография: достижения в области приборостроения, хемометрики и приложений». Аналитическая химия . 90 (1): 505–532. дои : 10.1021/acs.analchem.7b04226 . ПМИД 29088543 .
- ^ Jump up to: Перейти обратно: а б с Столл Д.Р., Карр П.В. (январь 2017 г.). «Двумерная жидкостная хроматография: современное учебное пособие». Аналитическая химия . 89 (1): 519–531. дои : 10.1021/acs.analchem.6b03506 . ПМИД 27935671 .
- ^ Транчида PQ, Шарроне Д., Дуго П., Монделло Л. (февраль 2012 г.). «Сердцераздирающая многомерная газовая хроматография: обзор недавней эволюции, применения и будущих перспектив» . Аналитика Химика Акта . Подборка докладов, представленных на 12-м Международном симпозиуме по технологиям добычи (ExTech 2010). 716 : 66–75. Бибкод : 2012AcAC..716...66T . дои : 10.1016/j.aca.2011.12.015 . ПМИД 22284880 .
- ^ Бертод А., Марютина Т., Спиваков Б., Шпигун О., Сазерленд И.А. (1 января 2009 г.). «Противоточная хроматография в аналитической химии (Технический отчет ИЮПАК)» . Чистая и прикладная химия . 81 (2): 355–387. doi : 10.1351/PAC-REP-08-06-05 . ISSN 1365-3075 .
- ^ Юрген Мартенс, Бхушан, Р. , Мечислав Саевич, Тереза Ковальска Дж. Хроматогр. наук. 2017 , Том 55, 748–749. ( doi : 10.1093/chromsci/bmx031 )
- ^ Юрген Мартенс, Рави Бхушан, Хелв. Хим. Акта 2014 , Том. 97, 161–187. ( два : 10.1002/hlca.201300392 )
- ^ Кулсинг С., Нолвачай Ю., Марриотт П.Дж., Бойсен Р.И., Матыска М.Т., Песек Дж.Дж., Хирн М.Т. (февраль 2015 г.). «Понимание происхождения селективности разделения с помощью адсорбентов на основе гидрида кремния». Журнал физической химии Б. 119 (7): 3063–9. дои : 10.1021/jp5103753 . ПМИД 25656442 .
- ^ «Хроматография: определение, работа и значение в различных отраслях» . www.researchdive.com . Проверено 25 февраля 2022 г.