Колоночная хроматография

Колоночная хроматография в химии — это метод хроматографии, используемый для выделения одного химического соединения из смеси. Хроматография способна разделять вещества на основе дифференциальной адсорбции соединений на адсорбенте; соединения движутся через колонку с разной скоростью, что позволяет разделить их на фракции. Этот метод широко применим, поскольку можно использовать множество различных адсорбентов (нормально-фазовых, обращенно-фазовых и т. д.) с широким спектром растворителей. Методику можно использовать на весах от микрограммов до килограммов. Основным преимуществом колоночной хроматографии является относительно низкая стоимость и одноразовость неподвижной фазы используемой в процессе . Последнее предотвращает перекрестное загрязнение и деградацию неподвижной фазы в результате переработки. Колоночную хроматографию можно проводить с использованием силы тяжести для перемещения растворителя или с использованием сжатого газа для проталкивания растворителя через колонку.
Тонкослойный хроматограф может показать, как поведет себя смесь соединений при очистке колоночной хроматографией. Разделение сначала оптимизируют с помощью тонкослойной хроматографии, а затем проводят колоночную хроматографию.
Подготовка колонки
[ редактировать ]Колонку готовят путем упаковки твердого адсорбента в цилиндрическую стеклянную или пластиковую трубку. Размер будет зависеть от количества изолируемого соединения. В основании пробирки находится фильтр, пробка из ваты или стекловаты, или стеклянная фритта для удержания твердой фазы на месте. Резервуар для растворителя может быть прикреплен к верхней части колонны.
Для подготовки колонки обычно используются два метода: сухой и мокрый. При использовании сухого метода колонку сначала наполняют сухим порошком неподвижной фазы, после чего добавляют подвижную фазу, которую промывают через колонку до тех пор, пока она полностью не станет влажной, и с этого момента никогда не допускается ее высыхание. [1] Для мокрого метода суспензию с порошком неподвижной фазы готовят из элюента , которую затем осторожно выливают в колонку. Верхняя часть кремнезема должна быть плоской, а верхнюю часть кремнезема можно защитить слоем песка. Элюент медленно пропускают через колонку для продвижения органического материала.
Отдельные компоненты удерживаются неподвижной фазой по-разному и отделяются друг от друга при прохождении с разной скоростью через колонку с элюентом. В конце колонки они элюируются по одному. В течение всего процесса хроматографии элюент собирается в ряд фракций . Фракции могут собираться автоматически с помощью коллекторов фракций. Производительность хроматографии можно повысить, пропуская несколько колонок одновременно. В этом случае используются многопоточные коллекторы. Состав потока элюента можно контролировать, и каждую фракцию анализировать на наличие растворенных соединений, например, с помощью аналитической хроматографии, УФ-спектров поглощения или флуоресценции . Цветные соединения (или флюоресцентные соединения при помощи УФ-лампы) можно увидеть сквозь стеклянную стену в виде движущихся полос.
Стационарная фаза
[ редактировать ]
Неподвижная фаза или адсорбент в колоночной хроматографии представляет собой твердое вещество. Наиболее распространенной неподвижной фазой для колоночной хроматографии является силикагель , следующим по распространенности является оксид алюминия . целлюлозный В прошлом часто использовался порошок. Доступен широкий спектр неподвижных фаз для проведения ионообменной хроматографии , обращенно-фазовой хроматографии (RP), аффинной хроматографии или адсорбции в расширенном слое (EBA). Неподвижные фазы обычно представляют собой тонкоизмельченные порошки или гели и/или имеют микропористую структуру для увеличения поверхности, хотя в ЭВА используется псевдоожиженный слой. Существует важное соотношение между массой стационарной фазы и сухой массой смеси аналитов, которую можно нанести на колонку. Для колоночной хроматографии на силикагеле это соотношение лежит в пределах от 20:1 до 100:1 в зависимости от того, насколько близко друг к другу элюируются компоненты аналита. [2]
Подвижная фаза (элюент)
[ редактировать ]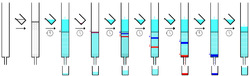
Подвижная фаза или элюент представляет собой растворитель или смесь растворителей, используемых для перемещения соединений через колонку. Его выбирают таким образом, чтобы значение коэффициента удерживания интересующего соединения составляло примерно около 0,2–0,3, чтобы минимизировать время и количество элюента для проведения хроматографии. Элюент также был выбран таким образом, чтобы можно было эффективно разделить различные соединения. Элюент оптимизируется в небольших предварительных испытаниях, часто с использованием тонкослойной хроматографии (ТСХ) с одной и той же неподвижной фазой и растворителями разной полярности, пока не будет найдена подходящая система растворителей. Распространенные растворители подвижной фазы, в порядке возрастания полярности, включают гексан , дихлорметан , этилацетат , ацетон и метанол . [3] Обычная система растворителей представляет собой смесь гексана и этилацетата, пропорции которых корректируют до тех пор, пока коэффициент удерживания целевого соединения не составит 0,2–0,3. Вопреки распространенному заблуждению, сам по себе метанол можно использовать в качестве элюента для высокополярных соединений, и он не растворяет силикагель.
Для каждого конкретного разделения существует оптимальная скорость потока . Более высокая скорость потока элюента минимизирует время, необходимое для работы колонки, и тем самым минимизирует диффузию, что приводит к лучшему разделению. Однако максимальная скорость потока ограничена, поскольку аналиту требуется конечное время для установления равновесия между стационарной и подвижной фазами, см. уравнение Ван Димтера . Простая лабораторная колонка работает самотеком . Скорость потока такой колонки можно увеличить, вытянув колонку, заполненную свежим элюентом, над верхней частью неподвижной фазы, или уменьшить с помощью крана управления. Более высоких скоростей потока можно достичь, используя насос или используя сжатый газ (например, воздух, азот или аргон ) для подачи растворителя через колонку (флэш-хроматография на колонке). [4] [5]

Размер частиц неподвижной фазы обычно меньше при флэш-хроматографии на колонке, чем при гравитационной колоночной хроматографии. Например, одним из наиболее широко используемых сортов силикагеля в первом методе является меш 230–400 (40–63 мкм), тогда как для второго метода обычно требуется силикагель 70–230 меш (63–200 мкм). [6]
Была разработана электронная таблица, которая помогает успешно разрабатывать флеш-колонки. В электронной таблице оцениваются удерживаемый объем и объем полосы аналитов, номера фракций, которые, как ожидается, будут содержать каждый аналит, а также разрешение между соседними пиками. Эта информация позволяет пользователям выбирать оптимальные параметры для препаративного разделения еще до того, как будет использована флэш-колонка. [7]
Автоматизированные системы
[ редактировать ]
Колоночная хроматография является чрезвычайно трудоемким этапом в любой лаборатории и может быстро стать узким местом для любой технологической лаборатории. Многие производители, такие как Biotage, Buchi, Interchim и Teledyne Isco, разработали автоматизированные системы флэш-хроматографии (обычно называемые LPLC, жидкостная хроматография низкого давления, около 350–525 кПа или 50,8–76,1 фунтов на квадратный дюйм), которые сводят к минимуму участие человека в процессе очистки. Автоматизированные системы будут включать в себя компоненты, обычно встречающиеся в более дорогих системах высокоэффективной жидкостной хроматографии (ВЭЖХ), такие как градиентный насос, порты для ввода проб, УФ-детектор и коллектор фракций для сбора элюента. Обычно эти автоматизированные системы могут отделять пробы массой от нескольких миллиграммов до многих килограммов промышленного масштаба и предлагают гораздо более дешевое и быстрое решение для выполнения множественных инъекций в системах препаративной ВЭЖХ.
Разрешение (или способность разделять смесь) в системе ВЭЖХ всегда будет ниже по сравнению с ВЭЖХ, поскольку насадочный материал в колонке ВЭЖХ может быть намного меньше, обычно всего 5 микрометров, что увеличивает площадь поверхности неподвижной фазы и увеличивает поверхностное взаимодействие. и обеспечивая лучшее разделение. Однако использование этой небольшой насадочной среды приводит к высокому противодавлению, поэтому ее называют жидкостной хроматографией высокого давления. Колонки LPLC обычно заполнены кремнеземом размером около 50 микрометров, что снижает противодавление и разрешение, но также устраняет необходимость в дорогостоящих насосах высокого давления. В настоящее время производители начинают переходить на системы флэш-хроматографии более высокого давления и называют их системами жидкостной хроматографии среднего давления (MPLC), которые работают при давлении выше 1 МПа (150 фунтов на квадратный дюйм).
Расчет разрешения колоночной хроматограммы
[ редактировать ]
Обычно колоночная хроматография включает перистальтические насосы, проточные буферы и пробу раствора через верхнюю часть колонки. Растворы и буферы проходят через колонку, где коллектор фракций в конце установки колонки собирает элюированные образцы. Перед сбором фракций образцы, элюированные из колонки, проходят через детектор, такой как спектрофотометр или масс-спектрометр, чтобы можно было определить концентрацию разделенных образцов в смеси растворов проб.
Например, если вам нужно отделить два разных белка с разной способностью связывания на колонке из образца раствора, хорошим типом детектора будет спектрофотометр, использующий длину волны 280 нм. Чем выше концентрация белка, который проходит через элюированный раствор через колонку, тем выше поглощение этой длины волны.
Поскольку колоночная хроматография предполагает постоянный поток элюированного раствора, проходящего через детектор с различными концентрациями, детектор должен отображать концентрацию элюированного образца с течением времени. Этот график зависимости концентрации образца от времени называется хроматограммой.
Конечная цель хроматографии — разделение различных компонентов из смеси растворов. Разрешение выражает степень разделения компонентов смеси. Чем выше разрешение хроматограммы, тем лучше степень разделения проб дает колонка. Эти данные являются хорошим способом определения свойств разделения колонки для конкретного образца. Разрешение можно рассчитать по хроматограмме.
Отдельные кривые на диаграмме представляют различные профили концентрации элюируемых образцов с течением времени в зависимости от их сродства к смоле колонки. Для расчета разрешения необходимы время удерживания и ширина кривой.
Время удерживания — это время от начала обнаружения сигнала детектором до высоты пика профиля концентрации элюирования каждого отдельного образца.
Ширина кривой – это ширина кривой профиля концентрации различных образцов на хроматограмме в единицах времени.
Упрощенный метод расчета разрешения хроматограммы заключается в использовании модели пластинки. [8] Тарелочная модель предполагает, что колонну можно разделить на определенное количество секций или тарелок и рассчитать баланс массы для каждой отдельной тарелки. Этот подход аппроксимирует типичную кривую хроматограммы кривой распределения Гаусса . При этом ширина кривой оценивается как 4-кратное стандартное отклонение кривой, 4σ. Время удерживания — это время от начала регистрации сигнала до момента достижения пиковой высоты кривой Гаусса.
Из переменных на рисунке выше разрешение, количество тарелок и высоту тарелок модели тарелки колонны можно рассчитать с помощью уравнений:
Разрешение (Р с ):
- R s = 2(t RB – t RA )/(w B + w A ),
где:
- t RB = время удерживания растворенного вещества B
- t RA = время удерживания растворенного вещества A
- w B = ширина кривой Гаусса растворенного вещества B
- w A = ширина кривой Гаусса растворенного вещества A
Номер пластины (N):
- Н = (т р ) 2 /(с/4) 2
Высота пластины (H):
- Н = Л/Н
где L — длина столбца. [8]
Адсорбционное равновесие колонки
[ редактировать ]В адсорбционной колонке смола колонки (неподвижная фаза) состоит из микрошариков. Даже более мелкие частицы, такие как белки, углеводы, ионы металлов или другие химические соединения, конъюгируются с микрошариками. Можно предположить, что каждая связывающая частица, прикрепленная к микрогранулам, связывается в соотношении 1:1 с образцом растворенного вещества, проходящим через колонку, которую необходимо очистить или отделить.
Связывание между целевой молекулой, которую нужно разделить, и связывающей молекулой на шариках колонки можно смоделировать с помощью простой равновесной реакции K eq = [CS]/([C][S]), где K eq — константа равновесия , [C] и [S] представляют собой концентрации целевой молекулы и связывающей молекулы на смоле колонки соответственно. [CS] — концентрация комплекса целевой молекулы, связанной со смолой колонки. [8]
Используя это в качестве основы, для описания динамики связывания колоночной хроматографии можно использовать три разные изотермы: линейную, Ленгмюра и Фрейндлиха.
Линейная изотерма возникает, когда концентрация растворенного вещества, которую необходимо очистить, очень мала по сравнению с связывающей молекулой. Таким образом, равновесие можно определить как:
- [CS] = К экв [С].
При использовании в промышленных масштабах необходимо учитывать общее количество связывающих молекул на шариках смолы колонки, поскольку необходимо учитывать незанятые участки. и Изотерма Ленгмюра изотерма Фрейндлиха полезны для описания этого равновесия. Изотерма Ленгмюра определяется формулой:
- [CS] = (K eq S tot [C])/(1 + K eq [C]), где S tot представляет собой общее количество связывающих молекул на гранулах.
Изотерма Фрейндлиха определяется формулой:
- [CS] = К экв [С] 1/н
Изотерма Фрейндлиха используется, когда колонка может связываться со многими различными образцами в растворе, который необходимо очистить. Поскольку многие разные образцы имеют разные константы связывания с гранулами, существует много разных K- экв . Следовательно, изотерма Ленгмюра в данном случае не является хорошей моделью связывания. [8]
См. также
[ редактировать ]- Быстрая жидкостная хроматография белков (FPLC) – разделение белков с помощью колоночной хроматографии.
- Высокоэффективная жидкостная хроматография (ВЭЖХ) – колоночная хроматография под высоким давлением.
Ссылки
[ редактировать ]- ^ Шустерман, AJ; Макдугал, П.Г.; Гласфельд, А. (1997). «Сухая колоночная флэш-хроматография». J Chem Educ . 74 (10): 1222. Бибкод : 1997ЖЧЭд..74.1222С . дои : 10.1021/ed074p1222 . ISSN 0021-9584 .
- ^ «Как настроить колонку с силикагелем для флэш-хроматографии и действительно добиться успеха в разделении» . www.reachdevices.com . REACH Devices, ООО . Проверено 3 января 2019 г.
- ^ Фернисс, Брайан С.; Ханнафорд, Энтони, Дж.; Смит, Питер У.Г.; Тэтчелл, Остин С. (1989). Учебник практической органической химии Фогеля . Лонгман научно-технический. п. 203. ИСБН 978-0582462366 .
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Тем не менее, туалет; Кан, М; Митра, А (1978). «Быстрая хроматографическая техника препаративного разделения с умеренным разрешением». J Орг. хим . 43 (14). ОКС : 2923–2925. дои : 10.1021/jo00408a041 .
- ^ Харвуд Л.М., Муди CJ (13 июня 1989 г.). Экспериментальная органическая химия: принципы и практика (Иллюстрированное издание). Лондон: Блэквелл. стр. 180–185 . ISBN 978-0-632-02017-1 . ОСЛК 1079261960 .
- ^ «Сбор силикагеля для нормально-фазовой колоночной хроматографии» . Материальный урожай. 2008 год . Проверено 3 января 2019 г.
- ^ Фэйр, Джей Ди; Кормос, CM (2008). «Колоночные флэш-хроматограммы, рассчитанные на основе данных тонкослойной хроматографии». Дж Хроматогр А. 1211 (1–2): 49–54. дои : 10.1016/j.chroma.2008.09.085 . ISSN 0021-9673 . ПМИД 18849041 .
- ^ Jump up to: а б с д Харрисон Р.Г., Тодд П.В., Радж С.Р., Петридес Д.П. (2003). Биоразделение науки и техники (2-е изд.). Нью-Йорк, штат Нью-Йорк: Издательство Оксфордского университета . ISBN 9780190213732 . OCLC 899240244 .