Нажмите химия
| Часть серии о |
| Химия |
|---|
 |
|
В химическом синтезе клик -химия представляет собой класс простых реакций с экономией атомов , обычно используемых для соединения двух выбранных молекулярных образований. Клик-химия — это не одна конкретная реакция, а описание способа получения продуктов, соответствующих примерам в природе , при котором также образуются вещества путем соединения небольших модульных единиц. Во многих приложениях реакции щелчка соединяют биомолекулу и репортерную молекулу . Щелчковая химия не ограничивается биологическими условиями: концепция реакции «щелчка» использовалась в хемопротеомных , фармакологических, биомиметических и молекулярных механизмах . [1] Однако они оказались особенно полезными для обнаружения, локализации и квалификации биомолекул.
Реакции щелчка происходят в одном сосуде , не разрушаются водой , производят минимальные и безвредные побочные продукты и являются «подпружиненными» — характеризуются высокой термодинамической движущей силой, которая быстро и необратимо приводит к высокому выходу одного продукта реакции, при этом высокая специфичность реакции (в некоторых случаях как регио-, так и стереоспецифичность). Эти качества делают реакцию щелчка особенно подходящей для решения проблемы выделения и нацеливания молекул в сложных биологических средах. Соответственно, в таких средах продукты должны быть физиологически стабильными, а любые побочные продукты должны быть нетоксичными (для in vivo систем ).
Разработав специфические и контролируемые биоортогональные реакции, ученые открыли возможность поражения определенных целей в сложных клеточных лизатах . Недавно ученые адаптировали химию щелчков для использования в живых клетках, например, используя зонды из небольших молекул, которые находят и прикрепляются к своим мишеням с помощью реакций щелчка. Несмотря на проблемы клеточной проницаемости, биоортогональности, фоновой маркировки и эффективности реакции, реакции щелчка поколения уже доказали свою полезность в экспериментах нового (в которых конкретные мишени могут быть выделены с использованием, например, репортерных молекул, которые связываются с определенной колонкой). и флуоресцентная спектрометрия (при которой флуорофор прикрепляют к интересующей мишени, а мишень определяют количественно или определяют ее местоположение). Совсем недавно стали использоваться новые методы для включения партнеров реакции щелчка в биомолекулы , включая включение неприродных аминокислот, содержащих реакционноспособные группы, в белки и модификацию нуклеотиды . Эти методы представляют собой часть области химической биологии , в которой химия щелчков играет фундаментальную роль, намеренно и целенаправленно соединяя модульные единицы для различных целей.
Термин «химия кликов» был придуман женой К. Барри Шарплесса , Джен Дьюзер. [2] в 1998 году и впервые был полностью описан Шарплессом, Хартмутом К. Колбом и М.Г. Финном из Исследовательского института Скриппса в 2001 году. [3] [4] В 2022 году Нобелевская премия по химии была присуждена совместно Кэролайн Р. Бертоцци , Мортену П. Мелдалу и К. Барри Шарплессу «за разработку клик-химии и биоортогональной химии ». [5]
Предыстория [ править ]
Клик-химия — это метод прикрепления интересующего зонда или субстрата к конкретной биомолекуле, процесс, называемый биоконъюгацией . [6] Возможность присоединения флуорофоров и других репортерных молекул сделала клик-химию очень мощным инструментом для идентификации, локализации и характеристики как старых, так и новых биомолекул.
Одним из самых ранних и наиболее важных методов биоконъюгации было экспрессирование репортера в той же открытой рамке считывания, что и интересующая биомолекула. Примечательно, что зеленый флуоресцентный белок (GFP) впервые был (и до сих пор экспрессируется) таким образом на N- или C-конце многих белков. Однако этот подход сопряжен с рядом трудностей. Например, GFP представляет собой очень большую единицу и часто может влиять на сворачивание интересующего белка. Более того, экспрессируясь на любом конце, аддукт GFP также может влиять на нацеливание и экспрессию желаемого белка . Наконец, с помощью этого метода GFP можно прикрепить только к белкам, а не посттрансляционно, оставляя другие важные биомолекулярные классы ( нуклеиновые кислоты , липиды , углеводы и т. д.) вне досягаемости.
Чтобы преодолеть эти проблемы, химики решили продолжить идентификацию пар биоортогональных партнеров реакции, что позволяет использовать небольшие экзогенные молекулы в качестве биомолекулярных зондов. К одному из этих зондов можно прикрепить флуорофор, чтобы давать сигнал флуоресценции при связывании репортерной молекулы с мишенью — точно так же, как флуоресцирует GFP, когда он экспрессируется с мишенью.
Теперь возникают ограничения из химии зонда по отношению к его цели. Чтобы этот метод был полезен в биологических системах, клик-химия должна работать в биологических условиях или близких к ним, производить мало и (в идеале) нетоксичных побочных продуктов, иметь (предпочтительно) отдельные и стабильные продукты в тех же условиях и быстро переходить к высокая урожайность в одном горшке . Существующие реакции, такие как лигирование Штаудингера и 1,3-диполярное циклоприсоединение Хейсгена , были модифицированы и оптимизированы для таких условий реакции. Сегодня исследования в этой области касаются не только понимания и разработки новых реакций, а также перепрофилирования и переосмысления известных реакций, но и расширения методов, используемых для включения партнеров реакции в живые системы, разработки новых партнеров реакции и разработки приложений для биоконъюгации.
Биотехнологическая компания Shasqi — это компания, использующая химию щелчков на людях. [7] [8]
Реакция [ править ]
Чтобы реакция считалась реакцией щелчка, она должна удовлетворять определенным характеристикам: [9]
- модульность
- нечувствительность к параметрам растворителя
- высокие химические выходы
- нечувствительность к кислороду и воде
- региоспецифичность и стереоспецифичность
- большая термодинамическая движущая сила (>20 ккал / моль ), способствующая реакции с одним продуктом реакции. Отчетливая экзотермическая реакция делает реагент «подпружиненным».
Предпочтительно, чтобы этот процесс:
- имеют простые условия реакции
- использовать легкодоступные исходные материалы и реагенты
- не используйте растворитель или используйте безвредный или легко удаляемый растворитель (предпочтительно воду)
- обеспечить простое выделение продукта нехроматографическими методами ( кристаллизацией или дистилляцией )
- имеют высокую атомную экономику .
Многие критерии клик-химии являются субъективными, и даже если можно будет согласовать измеримые и объективные критерии, маловероятно, что какая-либо реакция будет идеальной для каждой ситуации и применения. Однако было выявлено несколько реакций, которые лучше других соответствуют этой концепции: [ нужны разъяснения ]
- [3+2] циклоприсоединения , такие как 1,3-диполярное циклоприсоединение Хейсгена , в частности ступенчатый вариант, катализируемый Cu(I), [10] часто называют просто реакциями щелчка.
- Тиол-еновая реакция [11] [12]
- Реакция Дильса-Альдера и обратная потребность электронов. Реакция Дильса-Альдера. [13] [14]
- [4+1] циклоприсоединения между изонитрилами (изоцианидами) и тетразинами [15]
- нуклеофильное замещение, особенно в небольших напряженных кольцах, таких как эпоксидная смола. [16] и азиридины
- карбонильнохимическое образование мочевин , а не реакции альдольного типа из-за низкой термодинамической движущей силы.
- реакции присоединения к двойным углерод-углеродным связям , такие как дигидроксилирование или алкины в реакции тиол-ин . [9]
- Сера (VI) Фторидный обмен
медью(I) (CuAAC катализируемое Азид-алкиновое циклоприсоединение , )
Классический [17] [18] клик-реакция - это катализируемая медью реакция азида с алкином с образованием 5-членного гетероатомного кольца: катализируемое Cu (I) азид-алкиновое циклоприсоединение (CuAAC). О первом синтезе триазола из диэтилацетилендикарбоксилата и фенилазида сообщил Артур Майкл в 1893 году. [19] Позже, в середине 20-го века, это семейство 1,3-диполярных циклоприсоединения получило имя Рольфа Хейсгена после исследования кинетики и условий их реакций.
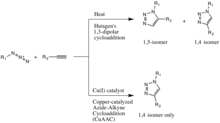
Медь(I)-катализ 1,3-диполярного циклоприсоединения Хьюсгена был открыт одновременно и независимо группами Валерия В. Фокина и К. Барри Шарплесса в Исследовательском институте Скриппса в Калифорнии. [20] и Мортен Мелдал в лаборатории Carlsberg , Дания. [21] Версия этой реакции, катализируемая медью, дает только 1,4-изомер, тогда как некатализируемое 1,3-диполярное циклоприсоединение Хейсгена дает как 1,4-, так и 1,5-изомеры, является медленным и требует температуры 100 градусов Цельсия. [19]

Более того, этот катализируемый медью «щелчок» не требует наличия лигандов на металле, хотя сообщалось об ускоряющих лигандах, таких как трис (триазолил)метиламинные лиганды с различными заместителями, которые с успехом использовались в водных растворах. [19] Другие лиганды, такие как PPh3 и TBIA, также могут быть использованы, хотя PPh 3 подвержен лигированию по Штаудингеру с азидным заместителем. Было обнаружено, что Cu 2 O в воде при комнатной температуре также катализирует ту же реакцию за 15 минут с выходом 91%. [22]
Первый предложенный механизм реакции включал один каталитический атом меди; но изотопные, кинетические и другие исследования показали, что димедный механизм может быть более актуальным. [23] [24] [25] [26] [27] Несмотря на то, что эта реакция эффективно протекает в биологических условиях, медь в этом диапазоне дозировок является цитотоксичной. Были представлены решения этой проблемы, такие как использование водорастворимых лигандов на меди для улучшения проникновения катализатора в клетки и тем самым снижения необходимой дозировки. [28] [29] [30] или использовать хелатирующие лиганды для дальнейшего увеличения эффективной концентрации Cu(I) и тем самым снижения фактической дозировки. [31] [32] [33]
Хотя о варианте, катализируемом Cu(I), впервые сообщили Мелдал и его коллеги для синтеза пептидотриазолов на твердом носителе, их условия были далеки от истинного духа клик-химии и были вытеснены более признанным в обществе Шарплессом. Мелдал и его коллеги также решили не называть этот тип реакции «химией кликов», из-за чего их открытие, как утверждается, было в значительной степени проигнорировано основным химическим обществом. Фокин и Шарплесс независимо друг от друга описали его как надежный каталитический процесс, предлагающий «беспрецедентный уровень селективности, надежности и возможностей для тех усилий по органическому синтезу, которые зависят от создания ковалентных связей между различными строительными блоками».
Об аналогичной реакции RuAAC, катализируемой рутением вместо меди, сообщили группы Цзя и Фокина в 2005 году, и она позволяет селективно получать 1,5-изомеры. [34]
штаммом азид-алкиновое циклоприсоединение ( Промотируемое SPAAC )
Группа Бертоцци развила одну из реакций щелчка Хейсгена без меди, чтобы преодолеть цитотоксичность реакции CuAAC. [35] Вместо использования Cu(I) для активации алкина, алкин вводится в напряженный дифтороктин (DIFO), в котором электроноакцепторные пропаргиловые гем-фторы действуют вместе с кольцевой деформацией, значительно дестабилизируя алкин. [36] Эта дестабилизация увеличивает движущую силу реакции и стремление циклоалкина ослабить напряжение своего кольца.

Эта реакция протекает как согласованное [3+2]-циклоприсоединение к тройной связи в циклооктине по тому же механизму, что и 1,3-диполярное циклоприсоединение Хейсгена. В циклооктине также допускаются заместители, отличные от фтора, такие как бензольные кольца.
Эту реакцию успешно использовали для исследования азидов в живых системах, хотя скорость реакции несколько ниже, чем у CuAAC. Более того, поскольку синтез циклооктинов часто дает низкий выход, разработка зондов для этой реакции не была такой быстрой, как для других реакций. Но производные циклооктина, такие как DIFO, дибензилциклооктин (DIBO) и биарилазациклооктинон (BARAC), успешно используются в реакции SPAAC для исследования азидов в живых системах. [37] [38] [39]
штаммом алкин-нитронное циклоприсоединение ( Промотируемое SPANC )
Диарил-напряженные циклооктины, включая дибензилциклооктин (DIBO), также использовались для реакции с 1,3-нитронами в промотируемых штаммом алкин-нитронных циклоприсоединениях (SPANC) с получением N-алкилированных изоксазолинов. [40]
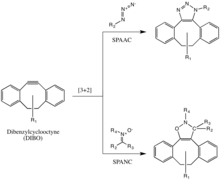
Поскольку эта реакция не содержит металлов и протекает с быстрой кинетикой (k2 со скоростью 60 1/Мс, быстрее, чем CuAAC или SPAAC), SPANC можно использовать для мечения живых клеток. Более того, допускается замещение как атомов углерода, так и азота нитрон-диполя, а также ациклических и эндоциклических нитронов. Этот большой допуск обеспечивает большую гибкость при установке нитронной ручки или зонда. [41]
Однако изоксазолиновый продукт не так стабилен, как триазольный продукт CuAAC и SpAAC, и может подвергаться перегруппировке в биологических условиях. Несмотря на это, эта реакция по-прежнему очень полезна, поскольку она имеет особенно быструю кинетику реакции. [40]
Применение этой реакции включает мечение белков, содержащих серин в качестве первого остатка: серин окисляется до альдегида с помощью NaIO 4 , а затем превращается в нитрон с помощью п-метоксибензолтиола, N-метилгидроксиламина и п-ансидина и, наконец, инкубируется с циклооктином с получением нажмите продукт. SPANC также допускает мультиплексную маркировку. [42] [43]
Реакции напряженных алкенов [ править ]
Напряженные алкены также используют снятие напряжения в качестве движущей силы, которая позволяет им участвовать в реакциях щелчка. Транс-циклоалкены (обычно циклооктены) и другие напряженные алкены, такие как оксанорборнадиен, реагируют в реакциях щелчка с рядом партнеров, включая азиды, тетразины и тетразолы. Эти партнеры реакции могут специфически взаимодействовать с напряженным алкеном, оставаясь биоортогональными эндогенным алкенам, обнаруженным в липидах, жирных кислотах, кофакторах и других натуральных продуктах. [42]
Алкеновое и азидное [3+2] циклоприсоединение [ править ]
Оксанорборнадиен (или другой активированный алкен) реагирует с азидами, давая в качестве продукта триазолы. Однако эти триазольные продукты не являются ароматическими, как в реакциях CuAAC или SPAAC, и в результате не так стабильны. Активированная двойная связь в оксаноборнадиене образует промежуточный триазолин, который впоследствии самопроизвольно подвергается ретрореакции Дильса-Альдера с высвобождением фурана и образованием 1,2,3- или 1,4,5-триазолов. Несмотря на то, что эта реакция протекает медленно, она полезна, поскольку синтезировать оксабордиен относительно просто. Однако реакция не является полностью хемоселективной. [44]
Алкен и тетразин с обратным спросом Альдера - Дильса

Напряженные циклооктены и другие активированные алкены реагируют с тетразинами в реакции Дильса-Альдера с обратной электронной потребностью с последующим ретро-[4+2]-циклоприсоединением (см. рисунок). [45] Как и другие реакции транс-циклооктена, движущей силой этой реакции является снятие напряжения кольца. Таким образом, трехчленные и четырехчленные циклоалкены из-за высокой деформации кольца являются идеальными алкеновыми субстратами. [45]
Подобно другим [4+2] циклоприсоединениям, электронодонорные заместители в диенофиле и электроноакцепторные заместители в диене ускоряют реакцию Дильса-Альдера с обратным спросом. Диен, тетразин, благодаря наличию дополнительных атомов азота является хорошим диеном для этой реакции. Диенофил, активированный алкен, часто может быть присоединен к электронодонорным алкильным группам на целевых молекулах, что делает диенофил более подходящим для реакции. [46]
и Фотоклик реакция - тетразола алкена
Реакция «фотоклика» тетразол-алкена представляет собой еще одно диполярное присоединение, которое Хьюсген впервые представил в конце 1960-х годов ChemBioChem 2007, 8, 1504. (68) Clovis, JS; Экелл, А.; Хейсген, Р.; Сустманн, Р. Хим. Бер. 1967, 100, 60.) Тетразолы с амино- или стириловыми группами, которые могут активироваться УФ-светом с длиной волны 365 нм (365 не повреждает клетки), реагируют быстро (так что УФ-свет не приходится включать в течение длительного времени, обычно около 1–4 минут) для получения флюорогенных пиразолиновых продуктов. Эта схема реакции хорошо подходит для мечения живых клеток, поскольку УФ-свет с длиной волны 365 нм минимально повреждает клетки. Более того, реакция протекает быстро, так что УФ-свет можно применять в течение короткого времени. Квантовые выходы коротковолнового УФ-излучения могут превышать 0,5. Это позволяет избирательно использовать тетразолы по длине волны в сочетании с другой реакцией фотолигирования, где при короткой длине волны протекает почти исключительно реакция лигирования тетразола, а при более длинной длине волны протекает исключительно другая реакция (связывание через о-хинодиметаны). [47] Наконец, нефлуорогенные реагенты дают флуорогенный продукт, что обеспечивает реакцию встроенной спектрометрической ручкой.
И тетразолы, и алкеновые группы были включены в качестве белковых маркеров в качестве неприродных аминокислот, но это преимущество не уникально. Вместо этого фотоиндуцируемость реакции делает ее главным кандидатом на пространственно-временную специфичность в живых системах. Проблемы включают присутствие эндогенных алкенов, хотя обычно они (как и в жирных кислотах) могут реагировать с активированным тетразолом. [48]
Возможные применения [ править ]
Click Chemistry — мощный инструмент для исследования клеточной локализации малых молекул. Знание того, куда попадают небольшие молекулы в клетке, дает глубокое понимание механизмов их действия. [49] Этот подход использовался в многочисленных исследованиях, и открытия включают в себя то, что салиномицин локализуется в лизосомах, инициируя ферроптоз в раковых стволовых клетках. [50] и что производные метформина накапливаются в митохондриях, образуя хелат меди(II), влияя на метаболизм и эпигенетические изменения ниже по ходу воспалительных макрофагов. [51]
Коммерческий потенциал клик-химии огромен. Флуорофор и родамин связывался с норборненом вступал в реакцию с тетразином в живых системах. [52] В других случаях SPAAC между модифицированным циклооктином флуорофором и белками, меченными азидом, позволял отбирать эти белки в клеточных лизатах. [53]
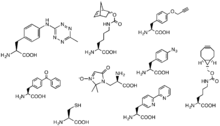
Методы включения партнеров реакции щелчка в системы in и ex vivo расширяют спектр возможных реакций. Развитие процесса включения неприродных аминокислот рибосомами позволило включить партнеров реакции щелчка в качестве неприродных боковых групп этих неприродных аминокислот. Например, UAA с азидной боковой группой обеспечивает удобный доступ циклоалкинов к белкам, меченным этой неприродной аминокислотой «AHA». [54] В другом примере «CpK» имеет боковую группу, включающую циклопропановую альфа-амидную связь, которая служит партнером по реакции тетразина в обратной реакции Дильса-Альдера. [55]
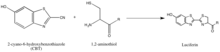
Синтез люциферина является примером другой стратегии выделения партнеров реакции, которая заключается в использовании редко встречающихся природных групп, таких как 1,2-аминотиол, который появляется только тогда, когда цистеин является последней N'-аминокислотой в белке. Таким образом, их естественная селективность и относительная биоортогональность важны для разработки зондов, специфичных для этих меток. Вышеупомянутая реакция происходит между 1,2-аминотиолом и 2-цианобензотиазолом с образованием люциферина, который является флуоресцентным. Эту флуоресценцию люциферина можно затем количественно оценить с помощью спектрометрии после промывки и использовать для определения относительного присутствия молекулы, несущей 1,2-аминотиол. Если желательно количественное определение белка, не содержащего 1,2-аминотиол, интересующий белок можно расщепить с получением фрагмента с N'-Cys, который уязвим для 2-CBT. [56]
Дополнительные приложения включают в себя:
- двумерным гель-электрофорезом разделение [57]
- препаративный органический синтез 1,4-замещенных триазолов
- модификация функции пептида триазолами
- модификация натуральных продуктов и фармацевтических препаратов
- натуральных продуктов открытие [58]
- открытие лекарств
- макроциклизации с использованием триазольных реакций, катализируемых Cu (I)
- модификация ДНК и нуклеотидов путем лигирования триазола
- супрамолекулярная химия : каликсарены , ротаксаны и катенаны.
- дендримерный дизайн
- углеводные кластеры и конъюгация углеводов с помощью реакций лигирования триазола, катализируемых Cu (1)
- полимеры и биополимеры [59]
- поверхности [60]
- материаловедение
- нанотехнологии, [61]
- биоконъюгация, например, азидокумарином и
- биоматериалы [62]
В сочетании с комбинаторной химией , высокопроизводительным скринингом и созданием химических библиотек клик-химия ускорила открытие новых лекарств, сделав каждую реакцию в многоэтапном синтезе быстрой, эффективной и предсказуемой.
Лицензия на технологию [ править ]
Научно-исследовательский институт Скриппса имеет портфель патентов на клик-химию. [63] В число лицензиатов входят Invitrogen , [64] Аллозин , [65] Элерон, [66] Комплексная диагностика, [67] и биотехнологическая компания Baseclick, [68] дочерняя компания BASF, созданная для продажи продуктов, изготовленных с использованием клик-химии. [69] Кроме того, Baseclick владеет эксклюзивной во всем мире лицензией на рынок исследований и диагностики в области нуклеиновых кислот.Флуоресцентные азиды и алкины также производятся такими компаниями, как Cyandye. [70]
Ссылки [ править ]
- ^ Кэрролл, GT; Лондон, Г.; Фернандес-Ландалус, Т.; Рудольф, П.; Феринга, БЛ (2011). «Адгезия фотонных молекулярных двигателей к поверхностям посредством 1,3-диполярных циклоприсоединений: влияние межфазных взаимодействий на молекулярное движение» (PDF) . АСУ Нано . 5 (1): 622–630. дои : 10.1021/nn102876j . ПМИД 21207983 . S2CID 39105918 .
- ^ Лекция Нобелевской премии: Барри Шарплесс, Нобелевская премия по химии 2022 г. , получено 4 января 2024 г.
- ^ ХК Колб; МГ Финн; КБ Шарплесс (2001). «Клик-химия: разнообразные химические функции из нескольких хороших реакций». Angewandte Chemie, международное издание . 40 (11): 2004–2021. doi : 10.1002/1521-3773(20010601)40:11<2004::AID-ANIE2004>3.0.CO;2-5 . ПМИД 11433435 .
- ^ Р.А. Эванс (2007). «Появление азидо-алкинового 1,3-диполярного циклоприсоединения «клик» и его применение в науке о полимерах и модификации поверхности». Австралийский химический журнал . 60 (6): 384–395. дои : 10.1071/CH06457 .
- ^ «Нобелевская премия по химии 2022» . NobelPrize.org . Проверено 5 октября 2022 г.
- ^ Б. Стамп (2022). «Биоконъюгация по клику: модификация белков с помощью химии, подобной клику». ХимБиоХим . 23 (16): e202200016. дои : 10.1002/cbic.202200016 . ПМИД 35491526 . S2CID 248494718 .
- ^ «Биоортогональная революция» . Химический мир . Проверено 11 ноября 2022 г.
- ^ « Химические партнеры «фазы медового месяца» доставляют токсичное лекарство в опухоли» . Откройте для себя журнал . Проверено 11 ноября 2022 г.
- ^ Jump up to: Перейти обратно: а б Ван, Сифань; Шмидт, Франциска; Ханаор, Дориан; Камм, Пол Х.; Ли, Шуан; Гурло, Александр (6 мая 2019 г.). «Аддитивное производство керамики из прекерамических полимеров: универсальный стереолитографический подход с использованием тиол-еновой клик-химии». Аддитивное производство . 27 : 80–90. arXiv : 1905.02060 . дои : 10.1016/j.addma.2019.02.012 . S2CID 104470679 .
- ^ Спитери, Кристиан; Моисей, Джон Э. (2010). «Медь-катализируемое азид-алкиновое циклоприсоединение: региоселективный синтез 1,4,5-тризамещенных 1,2,3-триазолов». Angewandte Chemie, международное издание . 49 (1): 31–33. дои : 10.1002/anie.200905322 . ПМИД 19921729 .
- ^ Хойл, Чарльз Э.; Боуман, Кристофер Н. (2010). «Химия тиол-енового клика». Angewandte Chemie, международное издание . 49 (9): 1540–1573. дои : 10.1002/anie.200903924 . ПМИД 20166107 .
- ^ Лоу, AB Polymer Chemistry 2010 , 1 (1), 17–36. DOI: 10.1039/B9PY00216B
- ^ Блэкман, Мелисса Л.; Ройзен Максим; Фокс, Джозеф М. (2008). «Лигирование тетразина: быстрая биоконъюгация на основе реакции Дильса-Альдера с обратной потребностью в электронах» . Журнал Американского химического общества . 130 (41): 13518–13519. дои : 10.1021/ja8053805 . ПМК 2653060 . ПМИД 18798613 .
- ^ Деварадж, Нил К.; Вайсследер Ральф и Хильдербранд, Скотт А. (2008). «Циклоприсоединения на основе тетразина: применение для предварительной маркировки живых клеток» . Биоконъюгатная химия . 19 (12): 2297–2299. дои : 10.1021/bc8004446 . ПМЦ 2677645 . ПМИД 19053305 .
- ^ Штёкманн, Хеннинг; Невес, Андре; Лестница, Шон; Бриндл, Кевин; Липер, Финиан (2011). «Изучение клик-химии на основе изонитрила для лигирования биомолекул». Органическая и биомолекулярная химия . 9 (21): 7303–5. дои : 10.1039/C1OB06424J . ПМИД 21915395 .
- ^ Кашемиров Борис А.; Бала, Джой Л.Ф.; Чен, Сяолань; Эбетино, FH; Ся, Чжидао; Рассел, Р. Грэм Г.; Коксон, Фрейзер П.; Рулофс, Анке Дж.; Роджерс Майкл Дж.; Маккенна, Чарльз Э. (2008). «Флуоресцентно меченный ризедронат и родственные аналоги: синтез «магического линкера». Биоконъюгатная химия . 19 (12): 2308–2310. дои : 10.1021/bc800369c . ПМИД 19032080 .
- ^ Грегори К., Паттон (8 ноября 2004 г.). «Разработка и применение клик-химии» (PDF) . Кафедра химии. Колледж свободных искусств и наук Университета Иллинойса в Урбана-Шампейн. Архивировано из оригинала (PDF) 9 июля 2010 г.
{{cite journal}}: Для цитирования журнала требуется|journal=( помощь ) - ^ Колб, ХК; Шарплесс, Б.К. (2003). «Растущее влияние клик-химии на открытие лекарств» . Обнаружение наркотиков сегодня . 8 (24): 1128–1137. дои : 10.1016/S1359-6446(03)02933-7 . ПМИД 14678739 .
- ^ Jump up to: Перейти обратно: а б с Л. Лян и Д. Астрюк: «Реакция «щелчка» алкин-азидного циклоприсоединения (CuAAC), катализируемая медью (I), и ее применение. Обзор», 2011; 255, 23–24, 2933–2045, с. 2934
- ^ Ростовцев Всеволод Васильевич; Грин, Люк Дж.; Фокин Валерий Владимирович; Шарплесс, К. Барри (2002). «Пошаговый процесс циклоприсоединения Хьюсгена: катализируемое медью (I) региоселективное «связывание» азидов и терминальных алкинов». Angewandte Chemie, международное издание . 41 (14): 2596–2599. doi : 10.1002/1521-3773(20020715)41:14<2596::aid-anie2596>3.0.co;2-4 . ПМИД 12203546 .
- ^ Торное, CW; Кристенсен, К.; Мелдал, М. (2002). «Пептидотриазолы на твердой фазе: [1,2,3]-триазолы путем региоспецифического катализируемого медью (I) 1,3-диполярного циклоприсоединения терминальных алкинов к азидам» . Журнал органической химии . 67 (9): 3057–3064. дои : 10.1021/jo011148j . ПМИД 11975567 . S2CID 11957672 .
- ^ К. Ван, X. Би, С. Син, П. Ляо, З. Фанг, X. Мэн, К. Чжан, К. Лю, Ю. Цзи Green Chem. , 13 (2011), с. 562
- ^ Б.Т. Уоррелл, Дж.А. Малик, В.В. Фокин 2013, 340, 457–459; Дж. Э. Хейн, В. В. Фокин, Хим. Соц. Замри. 39 (2010) 1302.
- ^ Родионов Валентин О.; Фокин Валерий Владимирович; Финн, МГ (8 апреля 2005 г.). «Механизм безлигандной реакции циклоприсоединения азида-алкина, катализируемой CuI». Angewandte Chemie, международное издание . 44 (15): 2210–2215. дои : 10.1002/anie.200461496 . ISSN 1521-3773 . ПМИД 15693051 .
- ^ Якобуччи, Клаудио; Реале, Саманта; Галь, Жан-Франсуа; Де Анджелис, Франческо (2 марта 2015 г.). «Двуядерные промежуточные соединения меди в катализируемом медью (I) азид-алкиновом циклоприсоединении, непосредственно наблюдаемом с помощью масс-спектрометрии с ионизацией электрораспылением». Angewandte Chemie, международное издание . 54 (10): 3065–3068. дои : 10.1002/anie.201410301 . ISSN 1521-3773 . ПМИД 25614295 .
- ^ Озкилыч, Йылмаз; Тюзюн, Нуркан Ш. (22 августа 2016 г.). «Исследование методом ДПФ биядерной реакции CuAAC: механизм в свете новых экспериментов». Металлоорганические соединения . 35 (16): 2589–2599. doi : 10.1021/acs.organomet.6b00279 . ISSN 0276-7333 .
- ^ Зиглер, Мика С.; Лакшми, К.В.; Тилли, Т. Дон (19 апреля 2017 г.). «Двумедные комплексы Cu(I)Cu(I) и Cu(I)Cu(II) в катализируемом медью азидно-алкиновом циклоприсоединении» (PDF) . Журнал Американского химического общества . 139 (15): 5378–5386. дои : 10.1021/jacs.6b13261 . ISSN 0002-7863 . ПМИД 28394586 .
- ^ Браттон, Вашингтон; Майклс, штат Ха; Симмонс, Джей Ти; Кларк, Р.Дж.; Далал, Н.С.; Чжу, Л. Орг. Летт. 2009, 11, 4954.
- ^ Куанг, Г.-К.; Майклс, штат Ха; Симмонс, Джей Ти; Кларк, Р.Дж.; Чжу, L" J. Org. Chem. 2010; 75, 6540.
- ^ Уттамапинант, К.; Тангпирачайкул, А.; Грециан, С.; Кларк, С.; Сингх, У.; Слэйд, П.; Ну и дела, КР; Ting, AY" Angew. Chem. Int. Ed. 2012; 51, 5852.
- ^ Алдер, К.; Штейн, Г.; Финценхаген, Х. Юстус Либигс Ann.Chem 1931, 485, 211.
- ^ Алдер, К.; Штейн, Г. Юстус Либигс Энн. хим. 1933, 501, 1.
- ^ Виттиг, Г.; Кребс, А. Хим. 1961, 94, 3260.
- ^ Чжан, Ли; Чен, Синго; Сюэ, Пэн; Солнце, Герман HY; Уильямс, Ян Д.; Шарплесс, К. Барри; Фокин Валерий Владимирович; Цзя, Гочен (ноябрь 2005 г.). «Рутений-катализируемое циклоприсоединение алкинов и органических азидов» . Журнал Американского химического общества . 127 (46): 15998–15999. дои : 10.1021/ja054114s . ПМИД 16287266 .
- ^ Хьюсген, Р. Ангью. хим. Межд. Эд. англ. 1963, 2, 565
Агард, Нью-Джерси; Баскин, Дж. М.; Прешер, Дж. А.; Ло, А.; Бертоцци, ЧР (2006). «Сравнительное исследование биоортогональных реакций с азидами». АКС хим. Биол . 1 (10): 644–648. дои : 10.1021/cb6003228 . ПМИД 17175580 .
- ^ Агард, Нью-Джерси; Баскин, Дж. М.; Прешер, Дж. А.; Ло, А.; Бертоцци, ЧР (2006). «Сравнительное исследование биоортогональных реакций с азидами». АКС хим. Биол . 1 (10): 644–648. дои : 10.1021/cb6003228 . ПМИД 17175580 .
- ^ Коделли, Дж. А.; Баскин, Дж. М.; Агард, Нью-Джерси; Бертоцци, ЧР (2008). «Дифторированные циклооктины второго поколения для клик-химии, не содержащей меди» . Дж. Ам. хим. Соц . 130 (34): 11486–11493. дои : 10.1021/ja803086r . ПМЦ 2646667 . ПМИД 18680289 .
- ^ Нин, X.; Го, Дж.; Вольферт, Массачусетс; Бунс, Г.-Ж. (2008). «Визуализация метаболически меченных гликоконъюгатов живых клеток с помощью не содержащих меди и быстрых циклоприсоединений Хейсгена» . Энджью. хим. Межд. Эд . 47 (12): 2253–2255. дои : 10.1002/anie.200705456 . ПМЦ 2835304 . ПМИД 18275058 .
- ^ Гордон, CG; Макки, Дж. Л.; Джуэтт, Дж. К.; Слеттен, Э.М.; Хоук, КН; Бертоцци, ЧР (2012). «Реакционная способность биарилазациклооктинонов в безмедийной клик-химии» . Дж. Ам. хим. Соц . 134 (22): 9199–9208. дои : 10.1021/ja3000936 . ПМЦ 3368396 . ПМИД 22553995 .
- ^ Jump up to: Перейти обратно: а б Маккензи, округ Колумбия; Шерратт, Арканзас; Чигринова М; Чунг, LL; Пезацки, JP (август 2014 г.). «Стимулируемые штаммом циклоприсоединения с участием нитронов и алкинов - быстрые настраиваемые реакции биоортогонального мечения». Curr Opin Chem Biol . 21 : 81–8. дои : 10.1016/j.cbpa.2014.05.023 . ПМИД 25022431 .
- ^ (64) (а) Нин, X.; Темминг, Р.П.; Доммерхольт, Дж.; Го, Дж.; Аня, Д.Б.; Дебец, МФ; Вольферт, Массачусетс; Бунс, Г.-Ж.; van Delft, F.L. Angew. Chem. Int. Ed. 2010; 49, 3065. (b) McKay, CS; Moran, J.; Pezacki, JP Chem. Commun. (Кембридж, Великобритания) 2010, 46, 931. (c) Дебетс, М.Ф., Дж.; Диркс, FPJT, FL Acc., M., Blake, J.P. Org., 2012, 10, 3066.
- ^ Jump up to: Перейти обратно: а б Ланг, К.; Чин, Дж. (2014). «Биоортогональные реакции для мечения белков». АКС хим. Биол . 9 (1): 16–20. дои : 10.1021/cb4009292 . ПМИД 24432752 .
- ^ Маккензи, округ Колумбия; Пезацкий, JP (2014). «Кинетические исследования быстрого стимулируемого штаммом [3+2] циклоприсоединения нитронов с бицикло[6.1.0]нонином». Может ли J Chem . 92 (4): 337–340. дои : 10.1139/cjc-2013-0577 .
- ^ (67) (а) ван Беркель, СС; Диркс, ATJ; Меувиссен, Южная Каролина; Пинг, DLL; Бурман, О.К.; Лаверман, П.; Ван Делфт, Флорида; Корнелиссен, JJLM; Рутьес, FPJT ChemBioChem 2008, 9, 1805. (б) ван Беркель, СС; Диркс, ATJ; Дебет, МФ; Ван Делфт, Флорида; Корнелиссен, JJLM; Нолте, RJM; Рутьес, FPJT ChemBioChem 2007, 8, 150.
- ^ Jump up to: Перейти обратно: а б Лю, Фанг; Патон, Роберт С.; Ким, Сона; Лян, Юн; Хоук, КН (2013). «Реакционная способность Дильса-Альдера напряженных и ненапряженных циклоалкенов с диенами с нормальной и обратной потребностью в электронах: активационные барьеры и анализ искажений/взаимодействий». Дж. Ам. хим. Соц . 135 (41): 15642–15649. дои : 10.1021/ja408437u . ПМИД 24044412 .
- ^ Ридер, Ульрике; Людтке, Натан В. (25 августа 2014 г.). «Алкен-тетразиновое лигирование для визуализации клеточной ДНК». Angew Chem Int Ed Engl . 53 (35): 9168–9172. дои : 10.1002/anie.201403580 . ПМИД 24981416 .
- ^ Мензель, Ян П.; Файст, Флориан; Тутен, Брайан; Вейль, Таня; Блинко, Джеймс П.; Барнер-Коволлик, Кристофер (2019). «Управляемое светом образование ортогональной ковалентной связи на двух разных длинах волн» . Angewandte Chemie, международное издание . 58 (22): 7470–7474. дои : 10.1002/anie.201901275 . hdl : 21.11116/0000-0003-99B4-5 . ПМИД 30916368 .
- ^ Рамиль, Карло П; Линь, Цин (август 2014 г.). , запускаемая флюорогенным светом in vivo «Химия Photoclick: реакция лигирования » . Современное мнение в области химической биологии . 21 : 89–95. дои : 10.1016/j.cbpa.2014.05.024 . ПМЦ 4149939 . ПМИД 25022432 .
- ^ Каньеке, Татьяна; Мюллер, Себастьян; Родригес, Рафаэль (2018). «Визуализация биологически активных малых молекул в клетках с помощью клик-химии» . Обзоры природы Химия . 2 (9): 202–215. дои : 10.1038/s41570-018-0030-x . S2CID 91366817 .
- ^ Май, Транг Тхи; Хамаи, Ахмед; Хинцш, Антье; Каньеке, Татьяна; Мюллер, Себастьян; Вичински, Жюльен; Кабо, Оливье; Лерой, Кристина; Дэвид, Амандин; Асеведо, Вероника; Ре, Акихидэ; Жинестье, Кристоф; Бирнбаум, Дэниел; Шараф-Жофре, Эммануэль; Кодоньо, Патрис; Мехпур, Марьям; xРодригес, Рафаэль Родригес (октябрь 2017 г.). «Салиномицин убивает раковые стволовые клетки, связывая железо в лизосомах» . Природная химия . 9 (10): 1025–1033. дои : 10.1038/nchem.2778 . ПМК 5890907 . ПМИД 28937680 .
- ^ Солье, Стефани; Мюллер, Себастьян; Татьяна, Каньеке; Антуан, Версини; Арно, Мансар; Фабьен, Синдикубвабо; Лирой, барон; Лейла, Эмам; Пьер, Гестрауд; Г. Дан, Пантош; Винсент, Гандон; Кристина, Гайе; Тинг-Ди, Ву; Флоран, Дингли; Дамарис, Лоу; Сильвен, Бауланд; Сильвер, Дюран; Валентин, Сенсио; Сирил, Робиль; Франсуа, Троттен; Давид, Перикат; Эммануэль, Нэсер; Селин, Когоюль; Этьен, Менье; Анн-Лора, заика; Элен, Лосось; Николя, Манель; Ален, Пюизье; Сара, Ватсон; Марк А., Доусон; Николас, слуга; Гвидо, Кремер; Джиллали, Аннан; Рафаэль, Родригес (2023). «Лекарственный сигнальный путь меди, вызывающий воспаление» . Природа . 617 (7960): 386–394. дои : 10.1038/s41586-023-06017-4 . ПМЦ 10131557 . ПМИД 37100912 .
- ^ Деварадж, Нил К.; Вайсследер, Ральф; Хильдербранд, Скотт А. (декабрь 2008 г.). «Циклоприсоединения на основе тетразина: применение для предварительной визуализации живых клеток» . Биоконъюгат, хим . 19 (12): 2297–2299. дои : 10.1021/bc8004446 . ПМЦ 2677645 . ПМИД 19053305 .
- ^ Дин, Х.; Демпл, Б. (2000). «Прямая передача сигнала оксида азота посредством нитрозилирования железо-серных центров в активаторе транскрипции SoxR» . Учеб. Натл. акад. наук. США . 97 (10): 5146–5150. Бибкод : 2000PNAS...97.5146D . дои : 10.1073/pnas.97.10.5146 . ПМК 25796 . ПМИД 10805777 .
- ^ Дитрих; и др. (2007). «Метка, обнаружение и идентификация вновь синтезированных протеомов с биоортогональной неканонической аминокислотной маркировкой». Протоколы природы . 2 (3): 532–540. дои : 10.1038/nprot.2007.52 . ПМИД 17406607 . S2CID 2833184 .
- ^ Ю; и др. (2012). «Генетически закодированный циклопропен управляет быстрой маркировкой белков, опосредованной фотощелчковой химией, в клетках млекопитающих» . Angew Chem Int Ed Engl . 51 (42): 10600–10604. дои : 10.1002/anie.201205352 . ПМК 3517012 . ПМИД 22997015 .
- ^ (а) Лян, Г.; Рен, Х.; Рао, Дж. Нат. хим. 2010, 2, 54. (б) Рен, Х.; Сяо, Ф.; Жан, К.; Ким, Ю.-П.; Се, Х.; Ся, З.; Рао, Дж. Angew.Chem., Int. Эд. 2009, 48, 9658.
- ^ Ilya A. Osterman; Alexey V. Ustinov; Denis V. Evdokimov; Vladimir A. Korshun; Petr V. Sergiev; Marina V. Serebryakova; Irina A. Demina; Maria A. Galyamina; Vadim M. Govorun; Olga A. Dontsova (January 2013). "A nascent proteome study combining click chemistry with 2DE" (PDF) . Proteomics . 13 (1): 17–21. doi : 10.1002/pmic.201200393 . PMID 23161590 . S2CID 9002232 . Archived from the original (PDF) on 2015-06-30 . Retrieved 2015-02-11 .
- ^ Кокс, Кортни Л.; Титц, Джонатан И.; Соколовский, Кароль; Мелби, Джоэл О.; Дорогази, Джеймс Р.; Митчелл, Дуглас А. (17 июня 2014 г.). «Нуклеофильные 1,4-добавки для открытия натуральных продуктов» . АКС Химическая биология . 9 (9): 2014–2022. дои : 10.1021/cb500324n . ПМК 4168802 . ПМИД 24937678 .
- ^ Майкл Флорос; Алсидес Леан; Суреш Нарине (2014). «Растворитель, полученный из растительного масла, и термопластичные политриазолы «Click Chemistry», не содержащие катализаторов» . БиоМед Исследования Интернэшнл . 2014 : 1–14. дои : 10.1155/2014/792901 . ПМК 4085725 . ПМИД 25032224 .
- ^ Лондон, Габор; Чен, Куан-Йен; Кэрролл, Грегори Т.; Феринга, Бен Л. (2013). «На пути к динамическому контролю смачиваемости с помощью функционализированных высотных молекулярных двигателей на твердых поверхностях» . Химия: Европейский журнал . 19 (32): 10690–10697. дои : 10.1002/chem.201300500 . ПМИД 23784916 . S2CID 5759186 .
- ^ Джон Э. Мозес; Адам Д. Мурхаус (2007). «Растущее применение клик-химии». хим. Соц. Откр. 36 (8): 1249–1262. дои : 10.1039/b613014n . ПМИД 17619685 .
- ^ Жан-Франсуа Лутц; Зоя Зарафшани (2008). «Эффективное создание терапевтических средств, биоконъюгатов, биоматериалов и биоактивных поверхностей с использованием азид-алкиновой химии «щелчка». Обзоры расширенной доставки лекарств . 60 (9): 958–970. дои : 10.1016/j.addr.2008.02.004 . ПМИД 18406491 .
- ^ «Нажмите Химия» . Архивировано из оригинала 15 мая 2012 г. Проверено 5 июня 2012 г.
- ^ «Invitrogen эксклюзивно лицензирует новые химические анализы пролиферации клеток Click от Гарвардского университета (NASDAQ:LIFE)» . Архивировано из оригинала 17 декабря 2012 г. Проверено 5 июня 2012 г.
- ^ «Xconomy: аллозиновые лицензии, химия Скриппса» . 15 июля 2010 г.
- ^ «Xconomy: чернильная сделка по элеронам и Скриппсу» . 30 ноября 2010 г.
- ^ «Лицензии на комплексную диагностику «Click Chemistry» от Научно-исследовательского института Скриппса, укрепление партнерской сети» . Архивировано из оригинала 30 апреля 2012 г. Проверено 5 июня 2012 г.
- ^ "baseclick GmbH :: Мы обеспечиваем биоконъюгацию мечения нуклеиновых кислот" . Компания «Бейсклик ГмбХ» . Проверено 21 марта 2022 г.
- ^ http://www.basf.com/group/pressrelease/P-10-427 [ постоянная мертвая ссылка ]
- ^ «ЦИАНДИ» . 03.10.2018. Архивировано из оригинала 3 октября 2018 года . Проверено 21 марта 2022 г.
Внешние ссылки [ править ]
- Нажмите Химия: краткий обзор и новейшая литература
- Национальный научный фонд: статья «Жизнь с Click Chemistry»
- Новости химии и техники: тема «Химия кликов in-situ»
- Новости химии и техники: статья «Клик-химия без меди»
- Обзор химии безметаллового клика
- Click Chemistry – тематический выпуск Chem Soc Rev , посвященный новейшим применениям клик-химии, приглашенные редакторы MG Finn и Валерий Фокин. Опубликовано Королевским химическим обществом.