Морская химия
| Компонент | Концентрация (моль/кг) |
|---|---|
| ЧАС 22О |
53.6 |
| кл. − |
0.546 |
| Уже + |
0.469 |
| мг 2+ |
0.0528 |
| ТАК 2− 4 |
0.0282 |
| Что 2+ |
0.0103 |
| К + |
0.0102 |
| С Т | 0.00206 |
| Бр − |
0.000844 |
| B T (общий бор) | 0.000416 |
| старший 2+ |
0.000091 |
| Ф − |
0.000068 |
Морская химия , также известная как химия океана или химическая океанография , представляет собой изучение химического состава морской среды под влиянием тектоники плит и распространения морского дна , мутности , течений , отложений , pH уровней , атмосферных составляющих, метаморфической активности и экологии . Морская жизнь адаптировалась к химическому составу, уникальному для океанов Земли , а морские экосистемы чувствительны к изменениям в химическом составе океана.
Воздействие человеческой деятельности на химию океанов Земли со временем усилилось, при этом загрязнение от промышленности и различных методов землепользования существенно повлияло на океаны. Более того, повышение уровня углекислого газа в атмосфере Земли привело к закислению океана , что оказывает негативное воздействие на морские экосистемы. Международное сообщество согласилось с тем, что восстановление химического состава океанов является приоритетом, и усилия по достижению этой цели отслеживаются как часть Цели устойчивого развития 14 .
Химическая океанография — это изучение химии Земли океанов . Химические океанографы, являясь междисциплинарной областью, изучают распределение и реакции как природных, так и антропогенных химических веществ от молекулярного до глобального масштаба. [2]
Из-за взаимосвязанности океана химики-океанографы часто работают над проблемами, имеющими отношение к физической океанографии , геологии и геохимии , биологии и биохимии , а также науке об атмосфере . Многие химики-океанографы исследуют биогеохимические циклы , и морской углеродный цикл, в частности, вызывает значительный интерес из-за его роли в секвестрации углерода и закислении океана . [3] Другие важные темы, представляющие интерес, включают аналитическую химию океанов, загрязнение морской среды и антропогенное изменение климата .
Органические соединения в океанах [ править ]
По оценкам, цветное растворенное органическое вещество (CРОВ) составляет 20–70% содержания углерода в океанах, причем его содержание выше у устьев рек и ниже в открытом океане. [4]
Морская жизнь во многом схожа по биохимии с наземными организмами, за исключением того, что они обитают в соленой среде. Одним из последствий их адаптации является то, что морские организмы являются наиболее богатым источником галогенированных органических соединений . [5]
Химическая экология экстремофилов [ править ]
Океан является домом для множества морских организмов, известных как экстремофилы – организмов, которые процветают в экстремальных условиях температуры, давления и доступности света. Экстремофилы населяют множество уникальных мест обитания в океане, таких как гидротермальные источники , черные курильщики, холодные просачивания , гиперсоленые регионы и карманы с рассолом морского льда . Некоторые ученые предполагают, что жизнь могла возникнуть из гидротермальных источников в океане.
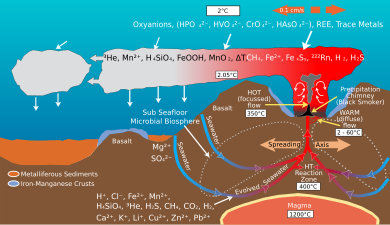
В гидротермальных жерлах и подобных средах многие экстремофилы приобретают энергию посредством хемоавтотрофии , используя в качестве источников энергии химические соединения, а не свет, как при фотоавтотрофии . Гидротермальные источники обогащают окружающую среду такими химическими веществами, как элементарная сера , H 2 , H 2 S , Fe. 2+ и метан . Хемоавтотрофные организмы, в первую очередь прокариоты, получают энергию из этих химических веществ посредством окислительно-восстановительных реакций . Эти организмы затем служат источниками питания для более высоких трофических уровней , образуя основу уникальных экосистем.
В экосистемах гидротермальных жерл присутствует несколько различных процессов метаболизма. Многие морские микроорганизмы, в том числе Thiomicrospira , Halothiobacillus и Beggiatoa , способны окислять соединения серы, включая элементарную серу и часто токсичное соединение H 2 S. H 2 S в изобилии присутствует в гидротермальных жерлах, образующихся в результате взаимодействия морской воды и горных пород при высоких температурах. температура внутри вентиляционных отверстий. Это соединение является основным источником энергии, составляющим основу круговорота серы в экосистемах гидротермальных жерл. В более холодных водах, окружающих жерла, может происходить окисление серы с использованием кислорода в качестве акцептора электронов ; ближе к вентиляционным отверстиям организмы должны использовать альтернативные метаболические пути или использовать другой акцептор электронов, например нитрат. Некоторые виды Thiomicrospira могут использовать тиосульфат в качестве донора электронов, производя элементарную серу. Кроме того, многие морские микроорганизмы способны окислять железо, например Mariprofundus Ferrooxydans . Окисление железа может быть кислородным, происходящим в богатых кислородом частях океана, или бескислородным, требующим либо акцептора электронов, такого как нитрат, либо энергии света. При окислении железа Fe(II) используется в качестве донор электронов ; и наоборот, восстановители железа используют Fe (III) в качестве акцептора электронов. Эти два метаболизма составляют основу окислительно-восстановительного цикла железа и, возможно, способствовали образованию полосчатого железа .
Другой крайностью является то, что некоторые морские экстремофилы обитают в карманах с рассолом морского льда, где температура очень низкая, а соленость очень высокая. Организмы, запертые в замерзшем морском льду, должны адаптироваться к быстрому изменению солености, которая в 3 раза превышает соленость обычной морской воды, а также к быстрому изменению солености обычной морской воды при таянии льда. Большинство организмов, обитающих в рассолах, являются фотосинтезирующими, поэтому эта микросреда может стать гипероксической, что может быть токсичным для ее обитателей. Таким образом, эти экстремофилы часто производят высокие уровни антиоксидантов. [6]
Тектоника плит [ править ]

Морское дно, распространяющееся на срединно-океанические хребты, систему глобального масштаба представляет собой ионообменную . [7] Гидротермальные жерла в центрах распространения приносят в океан различные количества железа , серы , марганца , кремния и других элементов, часть из которых перерабатывается в океанскую кору . Гелий-3 , изотоп, который сопровождает вулканизм в мантии, выбрасывается гидротермальными жерлами и может быть обнаружен в шлейфах в океане. [8]
Скорость распространения на срединно-океанических хребтах колеблется от 10 до 200 мм/год. Быстрые скорости распространения вызывают повышенную реакцию базальта с морской водой. Соотношение магний / кальций будет ниже, поскольку больше ионов магния удаляется из морской воды и поглощается породой, а больше ионов кальция удаляется из породы и попадает в морскую воду. Гидротермальная деятельность на гребне хребта эффективна для удаления магния. [9] Более низкое соотношение Mg/Ca благоприятствует осаждению полиморфных модификаций с карбоната кальция низким содержанием Mg ( кальцитовые моря ). [7]
Медленное распространение на срединно-океанических хребтах имеет противоположный эффект и приведет к более высокому соотношению Mg/Ca, что будет способствовать осаждению арагонита и полиморфных модификаций карбоната кальция с высоким содержанием магния ( арагонитовые моря ). [7]
Эксперименты показывают, что большинство современных кальцитовых организмов с высоким содержанием магния в прошлых кальцитовых морях представляли собой кальцит с низким содержанием магния. [10] это означает, что соотношение Mg/Ca в скелете организма зависит от соотношения Mg/Ca в морской воде, в которой он был выращен.
Таким образом, минералогия рифообразующих и производящих отложения организмов регулируется химическими реакциями, происходящими вдоль срединно-океанического хребта, скорость которых контролируется скоростью расширения морского дна. [9] [10]
Человеческое воздействие [ править ]
Загрязнение морской среды [ править ]
Загрязнение морской среды происходит, когда вещества, используемые или распространяемые людьми, такие как промышленные , сельскохозяйственные и бытовые отходы , частицы , шум , избыток углекислого газа или инвазивные организмы, попадают в океан и вызывают там вредные последствия. Большая часть этих отходов (80%) образуется в результате наземной деятельности, хотя морской транспорт . значительный вклад вносит и [11] Это сочетание химикатов и мусора, большая часть которого поступает из наземных источников и смывается или выбрасывается в океан. Это загрязнение наносит ущерб окружающей среде, здоровью всех организмов и экономическим структурам во всем мире. [12] Поскольку большая часть выбросов поступает с суши через реки , сточные воды или атмосферу, это означает, что континентальные шельфы более уязвимы к загрязнению. Загрязнение воздуха также является фактором, уносящим железо, углекислоту, азот , кремний, серу, пестициды или частицы пыли. в океан [13] Загрязнение часто происходит из неточечных источников, таких как сельскохозяйственные стоки , переносимый ветром , мусор , и пыль. Эти неточечные источники в основном возникают из-за стока, который попадает в океан через реки, но переносимый ветром мусор и пыль также могут сыграть свою роль, поскольку эти загрязнители могут оседать в водные пути и океаны. [14] Пути загрязнения включают прямой сброс, сток с земель, загрязнение с судов , загрязнение трюмами , загрязнение атмосферы и, возможно, глубоководную добычу полезных ископаемых .
Типы загрязнения морской среды можно сгруппировать как загрязнение морским мусором , пластиковое загрязнение , включая микропластик , закисление океана , загрязнение биогенными веществами , токсины и подводный шум. Пластиковое загрязнение океана — это тип загрязнения морской среды пластиком , размер которого варьируется от крупных исходных материалов, таких как бутылки и пакеты, до микропластика, образующегося в результате фрагментации пластикового материала. Морской мусор – это в основном выброшенный человеком мусор, который плавает или находится во взвешенном состоянии в океане. Пластиковое загрязнение вредно для морской жизни .климата Изменение
Повышенный уровень углекислого газа , в основном из-за сжигания ископаемого топлива , меняет химический состав океана. Глобальное потепление и изменения солености [15] имеют значительные последствия для экологии морской среды . [16]
Подкисление [ править ]
Закисление океана — это продолжающееся снижение pH земного океана . За последние 200 лет быстрый рост антропогенного производства CO 2 (углекислого газа) привел к повышению кислотности океанов Земли. В период с 1950 по 2020 год средний pH поверхности океана упал примерно с 8,15 до 8,05. [17] Выбросы углекислого газа в результате деятельности человека являются основной причиной закисления океана: уровень углекислого газа (CO 2 ) в атмосфере превышает 410 частей на миллион (в 2020 году). CO 2 из атмосферы поглощается океанами. В результате этой химической реакции образуется угольная кислота ( H 2 CO 3 ), который диссоциирует на ион бикарбоната ( HCO - 3 ) и ион водорода ( ЧАС + ). Наличие свободных ионов водорода ( ЧАС + ) понижает pH океана, повышая кислотность (это не значит, что морская вода еще кислая; она все еще щелочная , с pH выше 8). Морские кальцифицирующие организмы , такие как моллюски и кораллы , особенно уязвимы, поскольку они полагаются на карбонат кальция для построения раковин и скелетов. [18]
Изменение pH на 0,1 представляет собой увеличение концентрации ионов водорода в Мировом океане на 26% (шкала pH логарифмическая, поэтому изменение на единицу в единицах pH эквивалентно десятикратному изменению концентрации ионов водорода). Уровень pH морской поверхности и насыщенность карбонатами варьируются в зависимости от глубины и местоположения океана. Воды более холодных и более высоких широт способны поглощать больше CO 2 . Это может привести к повышению кислотности, снижению pH и уровня насыщения карбонатами в этих областях. Существует несколько других факторов, влияющих на обмен CO 2 между атмосферой и океаном и, следовательно, на локальное закисление океана. К ним относятся океанские течения и зоны апвеллинга , близость к крупным континентальным рекам, покрытие морским льдом и обмен атмосферы азотом и серой в результате сжигания ископаемого топлива и сельского хозяйства . [19] [20] [21]Деоксигенация [ править ]

Деоксигенация океана — это уменьшение содержания кислорода в различных частях океана в результате деятельности человека. [23] [24] Есть две области, где это происходит. Во-первых, это происходит в прибрежных зонах , где эвтрофикация привела к довольно быстрому (за несколько десятилетий) снижению содержания кислорода до очень низкого уровня. [23] Этот тип деоксигенации океана также называют мертвыми зонами . Во-вторых, деоксигенация океана происходит и в открытом океане. В этой части океана в настоящее время наблюдается постоянное снижение уровня кислорода. В результате естественные области с низким содержанием кислорода (так называемые зоны кислородного минимума (ОМЗ)) теперь медленно расширяются. [25] Это расширение происходит в результате антропогенного изменения климата . [26] [27] Возникающее в результате снижение содержания кислорода в океанах представляет угрозу для морской жизни , а также для людей, чье питание или средства к существованию зависят от морской жизни. [28] [29] [30] Снижение уровня кислорода в океане влияет на продуктивность океана , на то, как питательные вещества и перемещаются углерод , а также на функционирование морской среды обитания . [31] [32]
Поскольку океаны становятся теплее, это увеличивает потерю кислорода в океанах. Это происходит потому, что более высокие температуры увеличивают стратификацию океана . Причина этого кроется в множественных связях между эффектами плотности и растворимости, возникающими в результате потепления. [33] [34] В качестве побочного эффекта снижается доступность питательных веществ для морской жизни, что приводит к дополнительному стрессу для морских организмов .
Повышение температуры в океанах также приводит к снижению растворимости кислорода в воде, что может объяснить около 50% потерь кислорода в верхних слоях океана (>1000 м). Более теплая океанская вода содержит меньше кислорода и обладает большей плавучестью, чем более холодная вода. Это приводит к уменьшению смешивания насыщенной кислородом воды у поверхности с более глубокой водой, которая, естественно, содержит меньше кислорода. Более теплая вода также повышает потребность живых организмов в кислороде; в результате для морской жизни доступно меньше кислорода. [35]
Исследования показали, что океаны уже потеряли 1-2% кислорода с середины 20-го века. [36] [37] в мировом океане на 7% а модельное моделирование предсказывает снижение содержания O 2 в течение следующих ста лет. По прогнозам, снижение содержания кислорода будет продолжаться еще тысячу лет или даже больше. [38]История [ править ]
Этот раздел нуждается в дополнительных цитатах для проверки . ( апрель 2021 г. ) |

Ранние исследования морской химии обычно касались происхождения солености океана, включая работы Роберта Бойля . Современная химическая океанография началась как область с Челленджера экспедиции 1872–1876 годов , которая провела первые систематические измерения химии океана.
Инструменты [ править ]
Этот раздел нуждается в дополнительных цитатах для проверки . ( апрель 2021 г. ) |
Океанографы-химики собирают и измеряют химические вещества в морской воде, используя стандартный набор инструментов аналитической химии , а также такие инструменты, как pH-метры , измерители электропроводности , флуориметры и измерители растворенного CO₂. Большая часть данных собирается посредством судовых измерений, а также с автономных поплавков или буев , но дистанционное зондирование также используется . На океанографическом исследовательском судне CTD для сбора морской воды для анализа используется для измерения электропроводности , температуры и давления и часто устанавливается на розетке бутылок Нансена . Отложения обычно изучаются с помощью коробчатого керна или отстойника , а более старые отложения могут быть извлечены с помощью научного бурения .
Морская химия на других планетах спутниках их и
Химический состав подземного океана Европы может быть похож на земной. [39] Подземный океан Энцелада выбрасывает в космос водород и углекислый газ. [40]
См. также [ править ]
- Глобальный проект анализа океанических данных
- Океанография
- Физическая океанография
- Атлас Мирового океана
- Морская вода
- проект RISE
Ссылки [ править ]
- ^ МЭ (1994). «5» (PDF) . В А. Г. Диксоне; К. Гойе (ред.). Справочник методов анализа различных параметров углекислотной системы морской воды . 2. ОРНЛ/CDIAC-74. Архивировано 18 июля 2015 г. в Wayback Machine.
- ^ Дарнелл, Резнит. Американское море: естественная история Мексиканского залива .
- ^ Гиллис, Джастин (2 марта 2012 г.). «Темпы закисления океана не имеют аналогов за последние 300 миллионов лет, говорится в статье» . Зеленый блог . Проверено 28 апреля 2020 г.
- ^ Кобл, Паула Г. (2007). «Морская оптическая биогеохимия: химия цвета океана». Химические обзоры . 107 (2): 402–418. дои : 10.1021/cr050350+ . ПМИД 17256912 .
- ^ Гриббл, Гордон В. (2004). «Природные органогалогены: новый рубеж для лекарственных средств?». Журнал химического образования . 81 (10): 1441. Бибкод : 2004JChEd..81.1441G . дои : 10.1021/ed081p1441 .
- ^ «Хемоавтотрофия в глубоководных жерлах: прошлое, настоящее и будущее | Океанография» . tos.org . дои : 10.5670/oceanog.2012.21 . Проверено 8 февраля 2024 г.
- ↑ Перейти обратно: Перейти обратно: а б с Стэнли, С.М.; Харди, Луизиана (1999). «Гиперкальцификация: палеонтология связывает тектонику плит и геохимию с седиментологией». ГСА сегодня . 9 (2): 1–7.
- ^ Луптон, Джон (15 июля 1998 г.). «Гидротермальные гелиевые шлейфы в Тихом океане» . Журнал геофизических исследований: Океаны . 103 (С8): 15853–15868. Бибкод : 1998JGR...10315853L . дои : 10.1029/98jc00146 . ISSN 0148-0227 .
- ↑ Перейти обратно: Перейти обратно: а б Коггон, РМ; Тигл, DAH; Смит-Дюк, CE; Альт, Дж.К.; Купер, MJ (26 февраля 2010 г.). «Реконструкция прошлой морской воды Mg/Ca и Sr/Ca из жил карбоната кальция на флангах срединно-океанических хребтов». Наука . 327 (5969): 1114–1117. Бибкод : 2010Sci...327.1114C . дои : 10.1126/science.1182252 . ISSN 0036-8075 . ПМИД 20133522 . S2CID 22739139 .
- ↑ Перейти обратно: Перейти обратно: а б Райс, Джастин Б. (2004). «Влияние соотношения Mg/Ca в окружающей среде на фракционирование Mg у известковых морских беспозвоночных: запись океанического соотношения Mg/Ca в фанерозое». Геология . 32 (11): 981. Бибкод : 2004Geo....32..981R . дои : 10.1130/G20851.1 . ISSN 0091-7613 .
- ^ Шеппард, Чарльз, изд. (2019). Мировые моря: экологическая оценка . Том. III, Экологические проблемы и воздействие на окружающую среду (второе изд.). Лондон: Академическая пресса. ISBN 978-0-12-805204-4 . OCLC 1052566532 .
- ^ «Загрязнение морской среды» . Образование | Национальное географическое общество . Проверено 19 июня 2023 г.
- ^ Дуче, Роберт; Галлоуэй, Дж.; Лисс, П. (2009). «Воздействие атмосферных осаждений в океан на морские экосистемы и климат. Бюллетень ВМО, том 58 (1)» . Архивировано из оригинала 18 декабря 2023 года . Проверено 22 сентября 2020 г.
- ^ «Какой самый большой источник загрязнения океана?» . Национальная океаническая служба (США) . Силвер-Спринг, Мэриленд: Национальное управление океанических и атмосферных исследований . Проверено 21 сентября 2022 г.
- ^ «Соленость океана: изменение климата также меняет водный цикл» . usys.ethz.ch. Проверено 22 мая 2022 г.
- ^ Миллеро, Фрэнк Дж. (2007). «Морской неорганический углеродный цикл». Химические обзоры . 107 (2): 308–341. дои : 10.1021/cr0503557 . ПМИД 17300138 .
- ^ Терхаар, Йенс; Фрелихер, Томас Л.; Йоос, Фортунат (2023). «Закисление океана в сценариях стабилизации температуры, вызванных выбросами: роль TCRE и парниковых газов, не связанных с CO 2 » . Письма об экологических исследованиях . 18 (2): 024033. Бибкод : 2023ERL....18b4033T . дои : 10.1088/1748-9326/acaf91 . ISSN 1748-9326 . S2CID 255431338 .
Рисунок 1f
- ^ Закисление океана из-за увеличения содержания углекислого газа в атмосфере (PDF) . Королевское общество. 2005. ISBN 0-85403-617-2 .
- ^ Цзян, Ли-Цин; Картер, Брендан Р.; Фили, Ричард А.; Лаувсет, Сив К.; Олсен, Аре (2019). «РН поверхности океана и буферная емкость: прошлое, настоящее и будущее» . Научные отчеты . 9 (1): 18624. Бибкод : 2019NatSR...918624J . дои : 10.1038/s41598-019-55039-4 . ПМК 6901524 . ПМИД 31819102 .
 Текст был скопирован из этого источника, который доступен по международной лицензии Creative Commons Attribution 4.0. Архивировано 16 октября 2017 г. на Wayback Machine.
Текст был скопирован из этого источника, который доступен по международной лицензии Creative Commons Attribution 4.0. Архивировано 16 октября 2017 г. на Wayback Machine.
- ^ Чжан, Ю.; Ямамото-Каваи, М.; Уильямс, WJ (16 февраля 2020 г.). «Два десятилетия закисления океана в поверхностных водах круговорота Бофорта, Северный Ледовитый океан: последствия таяния и отступления морского льда в 1997–2016 годах» . Письма о геофизических исследованиях . 47 (3). дои : 10.1029/2019GL086421 . S2CID 214271838 .
- ^ Бопре-Лаперьер, Алексис; Муччи, Альфонсо; Томас, Хельмут (31 июля 2020 г.). «Современное состояние и изменчивость карбонатной системы Канадского Арктического архипелага и прилегающих бассейнов в условиях закисления океана» . Биогеонауки . 17 (14): 3923–3942. Бибкод : 2020BGeo...17.3923B . дои : 10.5194/bg-17-3923-2020 . S2CID 221369828 .
- ^ Брейтбург, Дениз; Левин, Лиза А.; Ошлис, Эндрю; Грегори, Марилора; Чавес, Франсиско П.; Конли, Дэниел Дж.; Боже, Вероника; Гилберт, Деннис; Гутьеррес, Дмитрий; Айзензее, Кирстен; Гиацинт, Гил С.; Лимбург, Карен Э.; Монтес, Ивонн; Накви, ЮВА; Питчер, Грант К.; Рабале, Нэнси Н.; Роман, Майкл Р.; Роуз, Кеннет А.; Сейбел, Брэд А.; Тельшевский, Мацей; Ясухара, Мориаки; Чжан, Цзин (2018). «Уменьшение содержания кислорода в мировом океане и прибрежных водах» . Наука 359 (6371): eaam7240. Бибкод : 2018Наука... 359M7240B дои : 10.1126/science.aam7240 . ПМИД 29301986 . S2CID 206657115 .
- ↑ Перейти обратно: Перейти обратно: а б Лаффоли, Д; Бакстер, Дж. М. (2019). Деоксигенация океана: проблема каждого . Швейцария: Гланд. п. 562. ИСБН 978-2-8317-2013-5 .
- ^ Лимбург, Карин Э.; Брейтбург, Дениз; Суони, Деннис П.; Хасинто, Хил (24 января 2020 г.). «Дезоксигенация океана: учебник для начинающих» . Одна Земля . 2 (1): 24–29. Бибкод : 2020OEart...2...24L . дои : 10.1016/j.oneear.2020.01.001 . ISSN 2590-3330 . S2CID 214348057 .
- ^ Ошлис, Андреас; Брандт, Питер; Страмма, Лотар; Шмидтко, Суньке (2018). «Драйверы и механизмы деоксигенации океана» . Природа Геонауки . 11 (7): 467–473. Бибкод : 2018NatGe..11..467O . дои : 10.1038/s41561-018-0152-2 . ISSN 1752-0894 . S2CID 135112478 .
- ^ Страмма, Л; Джонсон, GC; Принталл, Дж; Морхольц, В. (2008). «Расширение зон минимума кислорода в тропических океанах» . Наука . 320 (5876): 655–658. Бибкод : 2008Sci...320..655S . дои : 10.1126/science.1153847 . ПМИД 18451300 . S2CID 206510856 .
- ^ Мора, К; и др. (2013). «Биотическая и человеческая уязвимость к прогнозируемым изменениям в биогеохимии океана в 21 веке» . ПЛОС Биология . 11 (10): e1001682. дои : 10.1371/journal.pbio.1001682 . ПМК 3797030 . ПМИД 24143135 .
- ^ Кэррингтон (04 января 2018 г.). «Окружающая среда. Океаны задыхаются, поскольку огромные мертвые зоны увеличились в четыре раза с 1950 года, предупреждают ученые» . Хранитель . ISSN 0261-3077 . Проверено 4 июля 2023 г.
- ^ Лонг, Мэтью С.; Дойч, Кертис; Ито, Така (2016). «Обнаружение вынужденных тенденций содержания океанического кислорода» . Глобальные биогеохимические циклы . 30 (2): 381–397. Бибкод : 2016GBioC..30..381L . дои : 10.1002/2015GB005310 . ISSN 0886-6236 . S2CID 130885459 .
- ^ Пирс, Розамунд (15 июня 2018 г.). «Гостевой пост: Как глобальное потепление приводит к падению уровня кислорода в океане» . Карбоновое резюме . Проверено 4 июля 2023 г.
- ^ Харви, Фиона (07 декабря 2019 г.). «Океаны теряют кислород с беспрецедентной скоростью, предупреждают эксперты» . Хранитель . ISSN 0261-3077 . Проверено 7 декабря 2019 г.
- ^ Лаффоли, Д. и Бакстер, Дж. М. (ред.) (2019). Деоксигенация океана: проблема каждого – причины, последствия, последствия и решения . МСОП, Швейцария.
- ^ Беднаршек Н., Харви С.Дж., Каплан И.С., Фили Р.А. и Можина Дж. (2016) «Птероподы на грани: кумулятивные эффекты подкисления океана, потепления и деоксигенации». Прогресс в океанографии , 145: 1–24. два : 10.1016/j.pocean.2016.04.002
- ^ Килинг, Ральф Ф. и Эрнан Э. Гарсия (2002) «Изменение запасов O2 в океане, связанное с недавним глобальным потеплением». Труды Национальной академии наук , 99 (12): 7848–7853. два : 10.1073/pnas.122154899
- ^ «Дезоксигенация океана» . МСОП . 06.12.2019 . Проверено 2 мая 2021 г.
- ^ Бопп, Л; Респланди, Л; Орр, Дж.К.; Дони, Южная Каролина; Данн, JP; Гелен, М; Холлоран, П; Хайнце, К; Ильина, Т; Сефериан, Р; Чипутра, Дж (2013). «Множественные факторы стресса океанских экосистем в 21 веке: прогнозы с использованием моделей CMIP5» . Биогеонауки . 10 (10): 6625–6245. Бибкод : 2013BGeo...10.6225B . дои : 10.5194/bg-10-6225-2013 . hdl : 11858/00-001M-0000-0014-6A3A-8 .
- ^ Шмидтко, С; Страмма, Л; Висбек, М (2017). «Снижение содержания кислорода в океане за последние пять десятилетий» . Природа . 542 (7641): 335–339. Бибкод : 2017Natur.542..335S . дои : 10.1038/nature21399 . ПМИД 28202958 . S2CID 4404195 .
- ^ Ральф Ф. Килинг; Арне Корцингер; Николас Грубер (2010). «Дезоксигенация океана в условиях потепления» (PDF) . Ежегодный обзор морской науки . 2 : 199–229. Бибкод : 2010ARMS....2..199K . дои : 10.1146/annurev.marine.010908.163855 . ПМИД 21141663 . Архивировано из оригинала (PDF) 1 марта 2016 г.
- ^ Грейсиус, Тони (16 мая 2016 г.). «Океан Европы может иметь химический баланс, подобный земному» . НАСА . Проверено 22 мая 2022 г.
- ^ «Химия шлейфов Энцелада: жизнь или нет?» .