Океанический углеродный цикл

Океанический углеродный цикл (или морской углеродный цикл ) состоит из процессов обмена углеродом между различными резервуарами в океане, а также между атмосферой, недрами Земли и морским дном . Углеродный цикл — это результат взаимодействия множества сил в различных временных и пространственных масштабах, которые циркулируют углерод по планете, обеспечивая глобальную доступность углерода. Океанический углеродный цикл является центральным процессом глобального углеродного цикла и содержит как неорганический углерод (углерод, не связанный с живым существом, например углекислый газ), так и органический углерод (углерод, который включен или был включен в живое существо). . Часть морского углеродного цикла преобразует углерод между неживой и живой материей.
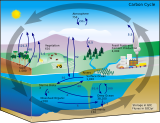
Три основных процесса (или насоса), составляющих морской углеродный цикл, переносят атмосферный углекислый газ (CO 2 ) в недра океана и распределяют его по океанам. Этими тремя насосами являются: (1) насос растворимости, (2) карбонатный насос и (3) биологический насос. Общий активный запас углерода на поверхности Земли в течение периода менее 10 000 лет составляет примерно 40 000 гигатонн С (Гт С, гигатонна равна одному миллиарду тонн, или вес примерно 6 миллионов синих китов ), и около 95% (~ 38 000 Гт C) хранится в океане, главным образом, в виде растворенного неорганического углерода . [1] [2] Видообразование [ нужны разъяснения ] растворенного неорганического углерода в морском углеродном цикле является основным регулятором кислотно-щелочной химии в океанах.
Земные растения и водоросли ( первичные производители ) ответственны за наибольшие ежегодные потоки углерода. Хотя количество запасаемого углерода в морской биоте (~3 ГтС) очень мало по сравнению с наземной растительностью (~610 ГтС), количество обмениваемого углерода (поток) этими группами примерно одинаково – около 50 ГтС каждая. [1] Морские организмы связывают циклы углерода и кислорода посредством таких процессов, как фотосинтез . [1] Морской углеродный цикл также биологически связан с циклами азота и фосфора почти постоянным стехиометрическим соотношением C:N:P 106:16:1, также известным как соотношение Редфилда Кетчума Ричардса (RKR) . [3] в котором говорится, что организмы имеют тенденцию поглощать азот и фосфор, включая новый органический углерод. Аналогичным образом, органические вещества, разлагаемые бактериями, выделяют фосфор и азот.
На основе публикаций НАСА , Всемирной метеорологической ассоциации, МГЭИК и Международного совета по исследованию моря , а также ученых из NOAA , Океанографического института Вудс-Хоул , Океанографического института Скриппса , CSIRO и Национальной лаборатории Ок-Ридж , человеческая воздействие на морской углеродный цикл является значительным. [4] [5] [6] [7] До промышленной революции океан был чистым источником CO 2 в атмосфере, тогда как сейчас большая часть углерода, попадающего в океан, поступает из атмосферного углекислого газа (CO 2 ). [8] Сжигание ископаемого топлива и производство цемента изменили баланс углекислого газа между атмосферой и океанами. [6] вызывая закисление океанов. [8] [9] Изменение климата, вызванное избытком CO 2 в атмосфере, привело к повышению температуры океана и атмосферы ( глобальное потепление ). [10] Замедление темпов глобального потепления, происходящее в 2000–2010 гг. [11] может быть объяснено наблюдаемым увеличением содержания тепла в верхних слоях океана . [12] [13]
| Часть серии о |
| Углеродный цикл |
|---|
 |
Морской углерод
[ редактировать ]
Углеродные соединения можно разделить на органические и неорганические, растворенные или дисперсные, в зависимости от их состава. Органический углерод образует основу ключевых компонентов органических соединений, таких как белки , липиды , углеводы и нуклеиновые кислоты . Неорганический углерод содержится преимущественно в простых соединениях, таких как диоксид углерода, угольная кислота, бикарбонат и карбонат (CO 2 , H 2 CO 3 , HCO 3 − , СО3 2− соответственно).
Морской углерод далее разделяется на твердую и растворенную фазы. Эти пулы оперативно определяются путем физического разделения: растворенный углерод проходит через фильтр с размером пор 0,2 мкм, а твердые частицы углерода — нет.
Неорганический углерод
[ редактировать ]В океанах встречаются два основных типа неорганического углерода. Растворенный неорганический углерод (DIC) состоит из бикарбоната (HCO 3 − ), карбонат (CO 3 2− ) и диоксид углерода (включая как растворенный CO 2 , так и угольную кислоту H 2 CO 3 ). DIC может быть преобразован в твердый неорганический углерод (PIC) путем осаждения CaCO 3 (биологическим или абиотическим путем). DIC также может быть преобразован в твердый органический углерод (POC) посредством фотосинтеза и хемоавтотрофии (т.е. первичного производства). ДВС увеличивается с глубиной по мере того, как частицы органического углерода тонут и выдыхаются. Свободный кислород уменьшается по мере увеличения ДВС-синдрома, поскольку кислород потребляется во время аэробного дыхания.
Частицы неорганического углерода (PIC) — это еще одна форма неорганического углерода, обнаруженная в океане. Большая часть PIC представляет собой CaCO 3 , входящий в состав раковин различных морских организмов, но также может образовываться при путассу . Морские рыбы также выделяют карбонат кальция во время осморегуляции . [14]
Некоторые из неорганических видов углерода в океане, такие как бикарбонат и карбонат , вносят основной вклад в щелочность , естественный буфер океана, который предотвращает резкие изменения кислотности (или pH ). Морской углеродный цикл также влияет на скорость реакций и растворения некоторых химических соединений, регулирует количество углекислого газа в атмосфере и температуру Земли. [15]
Органический углерод
[ редактировать ]Как и неорганический углерод, в океане встречаются две основные формы органического углерода (растворенный и твердый). Растворенный органический углерод (DOC) с практической точки зрения определяется как любая органическая молекула, которая может пройти через фильтр с размером пор 0,2 мкм. DOC может превращаться в твердый органический углерод посредством гетеротрофии, а также обратно в растворенный неорганический углерод (DIC) посредством дыхания.
Молекулы органического углерода, улавливаемые фильтром, называются твердыми частицами органического углерода (POC). ПОК состоит из организмов (мертвых или живых), их фекалий и детрита . дезагрегации молекул и экссудации фитопланктоном путем ПОУ может быть преобразовано в РОУ , например, . POC обычно превращается в DIC посредством гетеротрофии и дыхания.
Морские угольные насосы
[ редактировать ]Насос растворимости
[ редактировать ]Полная статья: Насос растворимости

Океаны хранят самый большой запас реактивного углерода на планете в виде DIC, который попадает в результате растворения атмосферного углекислого газа в морскую воду – насоса растворимости. [15] Концентрации водного CO 2 , угольной кислоты , бикарбонат-иона и карбонат-иона включают растворенный неорганический углерод (DIC). ДИК циркулирует по всему океану за счет термохалинной циркуляции , что способствует огромной емкости хранения ДИК в океане. [16] Приведенные ниже химические уравнения показывают реакции, которым подвергается CO 2 после того, как он попадает в океан и превращается в водную форму.

| ( 1 ) |
Угольная кислота быстро диссоциирует на свободные ионы водорода (технически гидроксоний ) и бикарбонат.
| ( 2 ) |
Свободный ион водорода встречается с карбонатом, уже присутствующим в воде в результате растворения CaCO 3 , и реагирует с образованием большего количества ионов бикарбоната.
| ( 3 ) |
Растворенные вещества в приведенных выше уравнениях, в основном бикарбонаты, составляют карбонатную щелочную систему, вносящую основной вклад в щелочность морской воды. [9]
Карбонатный насос
[ редактировать ]Карбонатный насос, иногда называемый карбонатным противонасосом, начинается с морских организмов на поверхности океана, производящих твердый неорганический углерод (PIC) в форме карбоната кальция ( кальцита или арагонита , CaCO 3 ). Этот CaCO 3 образует твердые части тела, такие как панцири . [15] Образование этих оболочек увеличивает содержание CO2 в атмосфере за счет производства CaCO3 . [9] в следующей реакции с упрощенной стехиометрией: [17]
| [18] | ( 4 ) |
Кокколитофоры , почти повсеместная группа фитопланктона, производящая раковины из карбоната кальция, вносят основной вклад в карбонатный насос. [15] Из-за своего обилия кокколитофоры оказывают существенное влияние на химию карбонатов в поверхностных водах, в которых они обитают, и в океане под ними: они обеспечивают крупный механизм нисходящего транспорта CaCO 3 . [19] из воздуха в море, Поток CO 2 вызванный морским биологическим сообществом, может быть определен по соотношению осадков – доле углерода из карбоната кальция по сравнению с углеродом из органического углерода в твердых частицах, оседающих на дно океана (PIC/POC). [18] Карбонатный насос действует как отрицательная обратная связь с CO 2 , поступающим в океан насосом растворимости. Это происходит с меньшей величиной, чем насос растворимости.
Биологический насос
[ редактировать ]Полная статья: Биологический насос
Органический углерод в виде частиц, созданный в результате биологического производства, может быть вынесен из верхних слоев океана в потоке, обычно называемом биологическим насосом, или вдыхаться (уравнение 6) обратно в неорганический углерод. В первом случае растворенный неорганический углерод биологически превращается в органическое вещество посредством фотосинтеза (уравнение 5) и других форм автотрофии. [15] затем он тонет и частично или полностью переваривается гетеротрофами. [20] Частицы органического углерода можно классифицировать в зависимости от того, насколько легко организмы могут расщеплять их для употребления в пищу, на лабильные , полулабильные или тугоплавкие. Фотосинтез фитопланктона является основным источником лабильных и полулабильных молекул и косвенным источником большинства тугоплавких молекул. [21] [22] Лабильные молекулы присутствуют в низких концентрациях вне клеток (в пикомолярном диапазоне) и имеют период полураспада всего несколько минут, когда они находятся в свободном состоянии в океане. [23] Они потребляются микробами в течение нескольких часов или дней после образования и обитают на поверхности океана. [22] где они составляют большую часть потока нестабильного углерода. [24] Полулабильные молекулы, которые гораздо труднее потреблять, способны достигать глубины в сотни метров под поверхностью, прежде чем метаболизироваться. [25] Тугоплавкое РОВ в основном состоит из сильно сопряженных молекул, таких как полициклические ароматические углеводороды или лигнин . [21] Огнеупорное РОВ может достигать глубины более 1000 м и циркулирует по океанам на протяжении тысячелетий. [26] [22] [27] поглощают около 20 гигатонн фотосинтетически закрепленного лабильного и полулабильного углерода В течение года гетеротрофы , тогда как потребляется менее 0,2 гигатонны тугоплавкого углерода. [22] Морское растворенное органическое вещество (РОВ) может хранить столько же углерода, сколько текущий запас CO 2 в атмосфере . [27] но промышленные процессы меняют баланс этого цикла. [28]
| ( 5 ) |
| ( 6 ) |
Входы
[ редактировать ]Вклады в морской углеродный цикл многочисленны, но основной вклад в чистом выражении поступает из атмосферы и рек. [1] Гидротермальные источники обычно поставляют углерод, равный тому количеству, которое они потребляют. [15]
Атмосфера
[ редактировать ]

До промышленной революции океан был источником CO 2 в атмосфере. [8] балансирование воздействия выветривания горных пород и земных частиц органического углерода; теперь он стал поглотителем избытка атмосферного CO 2 . [30] Углекислый газ поглощается из атмосферы на поверхности океана со скоростью обмена, которая варьируется локально. [31] но в среднем чистое поглощение океанами CO 2 составляет 2,2 Пг С в год. [31] Поскольку растворимость углекислого газа увеличивается при понижении температуры, холодные районы могут содержать больше CO 2 и при этом оставаться в равновесии с атмосферой; Напротив, повышение температуры поверхности моря снижает способность океанов поглощать углекислый газ. [32] [9] Северная Атлантика и Северные океаны имеют самое высокое поглощение углерода на единицу площади в мире. [33] а в Северной Атлантике глубокая конвекция переносит на глубину примерно 197 Тг в год неупорного углерода. [34]
Исследование 2020 года выявило значительно более высокий чистый поток углерода в океаны по сравнению с предыдущими исследованиями. В новом исследовании использовались спутниковые данные для учета небольшой разницы температур между поверхностью океана и глубиной в несколько метров, где проводятся измерения. [35] [36]
Скорость обмена углекислого газа между океаном и атмосферой
[ редактировать ]Скорость обмена CO 2 между океаном и атмосферой зависит от концентрации углекислого газа, уже присутствующего как в атмосфере, так и в океане, температуры, солености и скорости ветра. [37] Этот обменный курс можно аппроксимировать законом Генри и рассчитать как S = kP, где растворимость (S) углекислого газа пропорциональна количеству газа в атмосфере или его парциальному давлению . [1]
Фактор Ревелла
[ редактировать ]Поскольку потребление углекислого газа океаном ограничено, приток CO 2 также можно описать фактором Ревелля . [32] [9] Фактор Ревелля представляет собой отношение изменения содержания углекислого газа к изменению содержания растворенного неорганического углерода, которое служит индикатором растворения углекислого газа в перемешанном слое с учетом насоса растворимости. Фактор Ревелля представляет собой выражение, характеризующее термодинамическую эффективность пула DIC по поглощению CO 2 в бикарбонат. Чем ниже коэффициент Ревелля, тем выше способность океанской воды поглощать углекислый газ. Хотя Ревелль в свое время подсчитал коэффициент около 10, данные исследования 2004 года показали, что коэффициент Ревелля варьируется от примерно 9 в тропических регионах низких широт до 15 в южном океане недалеко от Антарктиды. [38]
Реки
[ редактировать ]Реки также могут переносить органический углерод в океан посредством выветривания или эрозии алюмосиликатных (уравнение 7) и карбонатных пород (уравнение 8) на суше.
| ( 7 ) |
| ( 8 ) |
или разложением жизни (уравнение 5, например, растительный и почвенный материал). [1] Реки вносят в океаны примерно одинаковое количество (~0,4 ГтУ/год) DIC и DOC. [1] По оценкам, примерно 0,8 ГтУ (DIC + DOC) ежегодно переносится из рек в океан. [1] Реки, впадающие в Чесапикский залив ( реки Саскуэханна , Потомак и Джеймс ), вносят примерно 0,004 Гт (6,5 х 10 10 молей) ДВС в год. [39] Общий перенос углерода реками составляет примерно 0,02% от общего количества углерода в атмосфере. [40] Хотя это кажется небольшим, в длительных временных масштабах (от 1000 до 10 000 лет) углерод, попадающий в реки (и, следовательно, не попадающий в атмосферу), служит стабилизирующей обратной связью для парникового потепления. [41]
Выходы
[ редактировать ]
Ключевыми результатами морской углеродной системы являются сохранение твердых частиц органических веществ (POC) и карбоната кальция (PIC), а также обратное выветривание . [1] Хотя существуют регионы с локальными потерями CO 2 в атмосферу и гидротермальными процессами, чистых потерь в цикле не происходит. [15]
Сохранение органических веществ
[ редактировать ]Седиментация является долгосрочным поглотителем углерода в океане, а также крупнейшей потерей углерода из океанической системы. [42] Глубоководные морские отложения и геологические образования важны, поскольку они обеспечивают тщательную запись жизни на Земле и являются важным источником ископаемого топлива. [42] Океанический углерод может выходить из системы в виде детрита, который тонет и закапывается на морском дне, не разлагаясь и не растворяясь полностью. на поверхности дна океана Отложения составляют 1,75x10 15 кг углерода в глобальном углеродном цикле [43] Максимум 4% твердых частиц органического углерода из эвфотической зоны Тихого океана, где происходит первичное производство с помощью света , захоронено в морских отложениях. [42] Тогда подразумевается, что, поскольку в океан поступает больше органического вещества, чем того, что захоранивается, большая часть его израсходуется или потребляется внутри.
Судьба тонущего органического углерода
[ редактировать ]Исторически отложения с самым высоким содержанием органического углерода часто обнаруживались в районах с высокой продуктивностью поверхностных вод или с низким содержанием кислорода в придонной воде. [44] 90% захоронения органического углерода приходится на отложения дельт , континентальных шельфов и верхних склонов; [45] отчасти это связано с коротким временем воздействия из-за меньшего расстояния до морского дна и состава органического вещества, которое уже отложено в этой среде. [46] Захоронение органического углерода также чувствительно к климатическим условиям: скорость накопления органического углерода была на 50% выше во время ледникового максимума по сравнению с межледниковьем . [47]
Деградация
[ редактировать ]| Часть серии о |
| Биогеохимические циклы |
|---|
 |
POC разлагается в результате ряда микробных процессов, таких как метаногенез и сульфатредукция, перед захоронением на морском дне. [48] [49] Деградация ВОУ также приводит к образованию микробного метана, который является основным газовым гидратом на окраинах континента. [50] Лигнин и пыльца по своей природе устойчивы к разложению , а некоторые исследования показывают, что неорганические матрицы также могут защищать органические вещества. [51] Скорость сохранения органического вещества зависит от других взаимозависимых переменных, которые нелинейно изменяются во времени и пространстве. [52] Хотя разложение органических веществ происходит быстро в присутствии кислорода, микробы, использующие различные химические соединения (посредством окислительно-восстановительных градиентов), могут разлагать органические вещества в бескислородных отложениях. [52] Глубина захоронения, на которой прекращается разложение, зависит от скорости седиментации, относительного содержания органического вещества в отложениях, типа захороненного органического вещества и множества других переменных. [52] В то время как разложение органического вещества может происходить в бескислородных отложениях, когда бактерии используют окислители, отличные от кислорода ( нитраты , сульфаты , Fe 3+ ), разложение имеет тенденцию заканчиваться до полной минерализации . [53] Это происходит из-за преимущественного распада лабильных молекул по сравнению с преломляющими молекулами. [53]
Похороны
[ редактировать ]Захоронение органического углерода является источником энергии для подземной биологической среды и может регулировать содержание кислорода в атмосфере в длительных временных масштабах (> 10 000 лет). [47] Захоронение может произойти только в том случае, если органический углерод попадет на морское дно, в результате чего континентальные шельфы и прибрежные окраины станут основным хранилищем органического углерода из первичной продукции на суше и в океане. Фьорды , или скалы, образовавшиеся в результате ледниковой эрозии, также были идентифицированы как области значительного захоронения углерода, уровень которого в сто раз превышает средний показатель по океану. [54] Частицы органического углерода захоронены в океанических отложениях, создавая путь между быстродоступным пулом углерода в океане и его хранилищем в геологических временных масштабах. Когда углерод связывается на морском дне, он считается голубым углеродом . Скорость захоронения можно рассчитать как разницу между скоростью оседания органического вещества и скоростью его разложения.
Консервация карбоната кальция
[ редактировать ]Осаждение карбоната кальция важно, поскольку оно приводит к потере щелочности, а также к выделению CO 2 (уравнение 4), и, следовательно, изменение скорости сохранения карбоната кальция может изменить парциальное давление CO 2 в земной атмосфере. атмосфера. [15] CaCO 3 перенасыщен недонасыщен в подавляющем большинстве поверхностных вод океана и на глубине. [9] это означает, что раковины с большей вероятностью растворятся, когда опускаются на глубины океана. CaCO 3 также может растворяться в результате метаболического растворения (т.е. может использоваться в пищу и выводиться из организма), и поэтому глубоководные отложения океана содержат очень мало карбоната кальция. [15] Осаждение и захоронение карбоната кальция в океане удаляет из океана частицы неорганического углерода и в конечном итоге образует известняк . [15] Во временных масштабах, превышающих 500 000 лет, климат Земли регулируется потоком углерода в литосферу и из нее . [55] Породы, образовавшиеся на морском дне океана, в результате тектоники плит возвращаются на поверхность и выветриваются или погружаются в мантию углерод выделяется вулканами , а . [1]
Человеческое воздействие
[ редактировать ]Океаны поглощают от 15 до 40% антропогенного CO 2 , [56] [57] и на сегодняшний день примерно 40% углерода от сжигания ископаемого топлива было поглощено океанами. [58] Поскольку фактор Ревелля увеличивается с увеличением CO 2 , меньшая часть антропогенного потока будет поглощаться океаном в будущем. [59] Текущий годовой прирост атмосферного CO 2 составляет примерно 4 гигатонны углерода. [60] Это вызывает изменение климата, которое приводит к концентрации углерода и процессам обратной связи между углеродом и климатом, которые изменяют циркуляцию океана , а также физические и химические свойства морской воды CO 2 . , что изменяет поглощение [61] [62] Чрезмерный вылов рыбы и загрязнение океанов пластиком способствуют ухудшению состояния крупнейшего в мире поглотителя углерода. [63] [64]
Закисление океана
[ редактировать ]Полная статья: Закисление океана
pH океанов снижается из-за поглощения атмосферного CO 2 . [65] Увеличение растворенного диоксида углерода снижает доступность карбонат-иона, снижая состояние насыщения CaCO 3 , что термодинамически затрудняет создание CaCO 3 . оболочки [66] Ионы карбоната преимущественно связываются с ионами водорода с образованием бикарбоната. [9] таким образом, уменьшение доступности карбонат-ионов увеличивает количество несвязанных ионов водорода и уменьшает количество образующегося бикарбоната (уравнения 1–3). pH — это измерение концентрации ионов водорода, где низкий pH означает, что в организме больше несвязанных ионов водорода. Таким образом, pH является индикатором образования карбонатов ( формата присутствующего углерода) в океанах и может использоваться для оценки того, насколько здоров океан. [66]
В список организмов, которые могут бороться с закислением океана, входят кокколитофоры и фораминиферы (основа морской пищевой цепи во многих регионах), источники пищи для человека, такие как устрицы и мидии , [67] и, пожалуй, самая примечательная структура, построенная организмами – коралловые рифы. [66] При нынешних траекториях выбросов большая часть поверхностных вод будет оставаться перенасыщенной по отношению к CaCO 3 (как кальциту, так и арагониту) в течение некоторого времени. [66] но организмы, которым необходим карбонат, вероятно, будут заменены во многих областях. [66] Коралловые рифы находятся под давлением чрезмерного вылова рыбы, загрязнения нитратами и потепления вод; закисление океана создаст дополнительную нагрузку на эти важные структуры. [66]
Железные удобрения
[ редактировать ]Полная статья: Железное удобрение
Железное удобрение — это аспект геоинженерии , который целенаправленно манипулирует климатической системой Земли, обычно в аспектах углеродного цикла или радиационного воздействия. В настоящее время интерес геоинженерии представляет возможность ускорения биологического насоса для увеличения экспорта углерода с поверхности океана. Этот увеличенный экспорт теоретически может удалить избыток углекислого газа из атмосферы для хранения в глубинах океана. Продолжаются исследования относительно искусственного оплодотворения. [68] Из-за масштабов океана и быстрого реагирования гетеротрофных сообществ на увеличение первичной продукции трудно определить, приводит ли ограничение удобрений к увеличению экспорта углерода. [68] Однако большая часть сообщества не считает такой подход разумным и жизнеспособным. [69]
Плотины и водохранилища
[ редактировать ]более 16 миллионов плотин . В мире [70] которые изменяют перенос углерода из рек в океаны. [71] Используя данные базы данных Global Reservoirs and Dams, которая содержит около 7000 водоемов, вмещающих 77% общего объема воды, удерживаемой плотинами (8000 км2). 3 ), по оценкам, поступление углерода в океан сократилось на 13% с 1970 года и, по прогнозам, достигнет 19% к 2030 году. [72] Избыток углерода, содержащийся в водоемах, может выбрасывать в атмосферу дополнительно ~0,184 Гт углерода в год. [73] и еще ~0,2 ГтС будут погребены в осадках. [72] До 2000 года Миссисипи , Нигер и на бассейны рек Ганг приходилось 25–31% всего захоронения углерода в резервуарах. [72] После 2000 года бассейны рек Парана (где находится 70 плотин) и Замбези (где находится крупнейшее водохранилище) превысили захоронение Миссисипи. [72] Другие крупные источники захоронения углерода, вызванного строительством плотин, происходят на реках Дунай , Амазонка , Янцзы , Меконг , Енисей и Токантинс . [72]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж г час я дж Шлезингер, Уильям Х.; Бернхардт, Эмили С. (2013). Биогеохимия: анализ глобальных изменений (3-е изд.). Уолтем, Массачусетс: Академическая пресса. ISBN 9780123858740 . OCLC 827935936 .
- ^ Фальковский, П.; Скоулз, Р.Дж.; Бойл, Э.; Канаделл, Дж.; Кэнфилд, Д.; Эльзер, Дж.; Грубер, Н.; Хиббард, К.; Хёгберг, П. (13 октября 2000 г.). «Глобальный углеродный цикл: проверка наших знаний о Земле как системе». Наука . 290 (5490): 291–296. Бибкод : 2000Sci...290..291F . дои : 10.1126/science.290.5490.291 . ISSN 0036-8075 . ПМИД 11030643 .
- ^ Редфилд, Альфред К. (1958). «Биологический контроль химических факторов окружающей среды». Американский учёный . 46 (3): 230А–221. JSTOR 27827150 . ПМИД 24545739 .
- ^ Холли, Рибик (16 июня 2011 г.). «Углеродный цикл: Тематические статьи» . Earthobservatory.nasa.gov . Проверено 30 ноября 2017 г.
- ^ «Опубликован новый отчет «Климат, углерод и коралловые рифы» . Всемирная метеорологическая организация . 5 ноября 2015 г. Архивировано из оригинала 18 декабря 2023 г. Проверено 30 ноября 2017 г.
- ^ Jump up to: а б «Пятый оценочный отчет – Изменение климата, 2013 г.» . www.ipcc.ch. Проверено 30 ноября 2017 г.
- ^ «Сабин и др. - Океанический поглотитель антропогенного CO2» . www.pmel.noaa.gov . Проверено 30 ноября 2017 г.
- ^ Jump up to: а б с Закисление океана из-за увеличения содержания углекислого газа в атмосфере (PDF) . Лондон: Королевское общество. 2005. ISBN 0-85403-617-2 . Проверено 17 ноября 2017 г.
- ^ Jump up to: а б с д и ж г Зибе, Р; Вольф-Гладроу, Д. (2001). CO2 в морской воде: равновесие, кинетика, изотопы . Эльзевир Наука. п. 360.
- ^ «Пятый оценочный отчет – Изменение климата, 2013 г.» . www.ipcc.ch. Проверено 26 ноября 2017 г.
- ^ Найт, Дж. (2009). «Глобальные океаны: фальсифицируют ли глобальные температурные тенденции за последнее десятилетие прогнозы климата?». Бюллетень Американского метеорологического общества . 90 : S56–S57.
- ^ «Глобальное тепло океана и содержание соли» . www.nodc.noaa.gov . Министерство торговли США, Национальные центры экологической информации NOAA . Проверено 26 ноября 2017 г.
- ^ Гемас, В; Доблас-Рейес, Ф; Андреу-Бурильо, я; Асиф, М (2013). «Ретроспективный прогноз замедления глобального потепления в последнее десятилетие» . Природа Изменение климата . 3 (7): 649–653. Бибкод : 2013NatCC...3..649G . дои : 10.1038/nclimate1863 . Архивировано из оригинала 25 ноября 2022 г. Проверено 10 декабря 2019 г.
- ^ Уилсон, RW; Миллеро, Ф.Дж.; Тейлор, младший; Уолш, Пи Джей; Кристенсен, В.; Дженнингс, С.; Гроселл, М. (16 января 2009 г.). «Вклад рыбы в морской цикл неорганического углерода». Наука . 323 (5912): 359–362. Бибкод : 2009Sci...323..359W . дои : 10.1126/science.1157972 . ISSN 0036-8075 . ПМИД 19150840 . S2CID 36321414 .
- ^ Jump up to: а б с д и ж г час я дж Эмерсон, Стивен (2008). Химическая океанография и морской углеродный цикл . Соединенное Королевство: Издательство Кембриджского университета. ISBN 978-0-521-83313-4 .
- ^ Фальковский, П.; Скоулз, Р.Дж.; Бойл, Э.; Канаделл, Дж.; Кэнфилд, Д.; Эльзер, Дж.; Грубер, Н.; Хиббард, К.; Хёгберг, П.; Линдер, С.; Маккензи, штат Форт; Мур III, Б.; Педерсен, Т.; Розенталь, Ю.; Зейтцингер, С.; Сметачек, В.; Стеффен, В. (2000). «Глобальный углеродный цикл: проверка наших знаний о Земле как системе». Наука . 290 (5490): 291–296. Бибкод : 2000Sci...290..291F . дои : 10.1126/science.290.5490.291 . ПМИД 11030643 .
- ^ «АСЛО: Лимнология и океанография: электронные книги» . aslo.org . Архивировано из оригинала 07.12.2017 . Проверено 28 ноября 2017 г.
- ^ Jump up to: а б Смит, СВ; Ки, GS (1 мая 1975 г.). «Углекислый газ и обмен веществ в морской среде1» . Лимнология и океанография . 20 (3): 493–495. Бибкод : 1975LimOc..20..493S . дои : 10.4319/lo.1975.20.3.0493 . ISSN 1939-5590 .
- ^ Рост, Бьёрн; Рибезель, Ульф (2004). «Кокколитофоры и биологический насос: реакция на изменения окружающей среды». Кокколитофоры . Шпрингер, Берлин, Гейдельберг. стр. 99–125. CiteSeerX 10.1.1.455.2864 . дои : 10.1007/978-3-662-06278-4_5 . ISBN 9783642060168 .
- ^ Ким, С; Крамер, Р; Хэтчер, П. (2003). «Графический метод анализа широкополосных масс-спектров природного органического вещества сверхвысокого разрешения, диаграмма Ван Кревелена». Аналитическая химия . 75 (20): 5336–5344. дои : 10.1021/AC034415P . ПМИД 14710810 .
- ^ Jump up to: а б Брофи, Дженнифер Э.; Карлсон, Дэвид Дж. (1989). «Производство биологически тугоплавкого растворенного органического углерода природными микробными популяциями морской воды». Глубоководные исследования. Часть A. Статьи океанографических исследований . 36 (4): 497–507. Бибкод : 1989DSRA...36..497B . дои : 10.1016/0198-0149(89)90002-2 .
- ^ Jump up to: а б с д Моран, М; Куявинский, Э; Стаббинс, А; Фатланд, Р; Алуихаре, Л; Бьюкен, А; Крамп, Б; Доррестейн, П; Дирман, С; Хесс, Н; Хау, Б; Лонгнекер, К; Медейрос, П; Ниггеманн, Дж; Оберностерер, я; Репета, Д; Вальдбауэр, Дж (2016). «Расшифровка содержания углерода в океане в меняющемся мире» . Труды Национальной академии наук Соединенных Штатов Америки . 113 (12): 3143–3151. Бибкод : 2016PNAS..113.3143M . дои : 10.1073/pnas.1514645113 . ПМЦ 4812754 . ПМИД 26951682 .
- ^ Азам, Ф; Малфатти, Ф (2007). «Микробное структурирование морских экосистем». Обзоры природы Микробиология . 5 (10): 782–791. дои : 10.1038/nrmicro1747 . ПМИД 17853906 . S2CID 10055219 .
- ^ Моран, X; Даклоу, Х; Эриксон, М. (2013). «Потоки углерода через эстуарные бактерии отражают взаимодействие с фитопланктоном» . Серия «Прогресс в области морской экологии» . 489 : 75–85. Бибкод : 2013MEPS..489...75M . дои : 10.3354/meps10428 .
- ^ Ханселл, Д; Карлсон, К. (1998). «Чистое общественное производство растворенного органического углерода» . Глобальные биогеохимические циклы . 12 (3): 443–453. Бибкод : 1998GBioC..12..443H . дои : 10.1029/98gb01928 .
- ^ Фоллетт, К; Репета, Д; Ротман, Д; Сюй, Л; Сантинелли, К. (2014). «Скрытый круговорот растворенного органического углерода в глубинах океана» . Труды Национальной академии наук Соединенных Штатов Америки . 111 (47): 16706–16711. Бибкод : 2014PNAS..11116706F . дои : 10.1073/pnas.1407445111 . ПМК 4250131 . ПМИД 25385632 .
- ^ Jump up to: а б Ханселл, Д. (2013). «Упорные фракции растворенного органического углерода». Ежегодный обзор морской науки . 5 (1): 421–445. doi : 10.1146/annurev-marine-120710-100757 . ПМИД 22881353 .
- ^ Дони, Скотт ; Рукельшауз, Мэри; Даффи, Эммет; Барри, Джеймс; Чан, Фрэнсис; английский, Чад; Галиндо, Хизер; Гребмайер, Жаклин ; Опустошенная, Энн; Ноултон, Нэнси; Половина, Джеффри; Рабале, Нэнси; Сайдман, Уильям; Тэлли, Линн (2012). «Влияние изменения климата на морские экосистемы». Ежегодный обзор морской науки . 4 (1): 11–37. Бибкод : 2012ARMS....4...11D . doi : 10.1146/annurev-marine-041911-111611 . ПМИД 22457967 . S2CID 35349779 .
- ^ Капелле, Дэвид В.; Кузык, Зоу Зоу А.; Папакириаку, Тим; Геген, Селин; Миллер, Лиза А.; Макдональд, Роби В. (2020). «Влияние наземного органического вещества на закисление океана и поток CO2 в арктическом шельфовом море» . Прогресс в океанографии . 185 : 102319. Бибкод : 2020Proce.18502319C . дои : 10.1016/j.pocean.2020.102319 . HDL : 1993/34767 .
 Материал был скопирован из этого источника, который доступен по международной лицензии Creative Commons Attribution 4.0 .
Материал был скопирован из этого источника, который доступен по международной лицензии Creative Commons Attribution 4.0 . - ^ Рэйвен, Дж.А.; Фальковски, П.Г. (2009). «Океанические поглотители атмосферного CO2» (PDF) . Глобальные биогеохимические циклы . 23 (1): GB1005. Бибкод : 2009GBioC..23.1005G . CiteSeerX 10.1.1.715.9875 . дои : 10.1029/2008gb003349 . hdl : 1912/3415 . S2CID 17471174 .
- ^ Jump up to: а б Такахаши, Т; Сазерленд, С; Суини, К; Пуассон, А; Мецль, Н. (2002). «Глобальный поток CO2 из моря в воздух, основанный на климатологических показателях pCO2 на поверхности океана, а также сезонных биологических и температурных эффектах». Глубоководные исследования, часть II: Актуальные исследования в океанографии . 49 (9–10): 1601–1622. Бибкод : 2002DSRII..49.1601T . дои : 10.1016/S0967-0645(02)00003-6 .
- ^ Jump up to: а б Ревель, Р; Зюсс, Х (1957). «Обмен углекислым газом между атмосферой и океаном и вопрос увеличения содержания CO2 в атмосфере за последние десятилетия». Теллус . 9 (1): 18–27. Бибкод : 1957Скажите....9...18R . дои : 10.1111/j.2153-3490.1957.tb01849.x .
- ^ Такахаши, Т; Сазерленд, С; Ваннинхоф, Р; и др. (2009). «Средние климатологические и десятилетние изменения pCO2 на поверхности океана и чистый поток CO2 из морского воздуха над мировыми океанами». Глубоководные исследования, часть II: Актуальные исследования в океанографии . 56 (8–10): 554–577. Бибкод : 2009DSRII..56..554T . дои : 10.1016/j.dsr2.2008.12.009 .
- ^ Фонтела, М; Гарсия-Ибанес, М; Ханселл, Д; Мерсье, Х; Перес, Ф (2016). «Растворенный органический углерод в меридиональной опрокидывающей циркуляции Северной Атлантики» . Природа . 6 : 26931. Бибкод : 2016NatSR...626931F . дои : 10.1038/srep26931 . ПМЦ 4886255 . ПМИД 27240625 .
- ^ «Поглощение углерода океаном сильно недооценено» . Физика.орг. 4 сентября 2020 г.
- ^ Уотсон, Эндрю Дж.; Шустер, Юте; Шатлер, Джейми Д.; Холдинг, Томас; Эштон, Ян Г.К.; Ландшютцер, Питер; Вульф, Дэвид К.; Годдейн-Мерфи, Лоннеке (4 сентября 2020 г.). «Пересмотренные оценки потока CO 2 из океана в атмосферу согласуются с данными о запасах углерода в океане» . Природные коммуникации . 11 (1): 4422. Бибкод : 2020NatCo..11.4422W . дои : 10.1038/s41467-020-18203-3 . ISSN 2041-1723 . ПМЦ 7474059 . PMID 32887875 .
 Текст и изображения доступны по международной лицензии Creative Commons Attribution 4.0 .
Текст и изображения доступны по международной лицензии Creative Commons Attribution 4.0 . - ^ Роббинс, LL; Хансен, Мэн; Клейпас, Дж.А.; Мейлан, Южная Каролина (2010). CO2calc — удобный калькулятор выбросов углерода в морской воде для Windows, Mac OS X и iOS (iPhone) . Открытый отчет Геологической службы США за 2010–1280 гг. п. 16.
- ^ Сабина, CL; Фили, РА; Грубер, Н; Ключ, РМ; Ли, К. (2004). «Океанический поглотитель антропогенного CO2» (PDF) . Наука . 305 (5682): 367–371. Бибкод : 2004Sci...305..367S . дои : 10.1126/science.1097403 . hdl : 10261/52596 . ПМИД 15256665 . S2CID 5607281 .
- ^ Вальдбуссер, Г; Пауэлл, Э; Манн, Р. (2013). «Экосистемные эффекты скоплений раковин и велосипедного движения в прибрежных водах: пример устричных рифов Чесапикского залива» . Экология . 94 (4): 895–903. дои : 10.1890/12-1179.1 .
- ^ Гали, Валье; Пойкер-Эренбринк, Бернхард; Эглинтон, Тимоти (2015). «Глобальный экспорт углерода из земной биосферы, контролируемый эрозией». Природа . 521 (7551): 204–207. Бибкод : 2015Natur.521..204G . дои : 10.1038/nature14400 . ПМИД 25971513 . S2CID 205243485 .
- ^ Велбель, Майкл Энтони (1 декабря 1993 г.). «Температурная зависимость силикатного выветривания в природе: насколько сильна отрицательная обратная связь на долговременное накопление атмосферного CO2 и глобальное парниковое потепление?». Геология . 21 (12): 1059–1062. Бибкод : 1993Geo....21.1059V . doi : 10.1130/0091-7613(1993)021<1059:TDOSWI>2.3.CO;2 . ISSN 0091-7613 . S2CID 747129 .
- ^ Jump up to: а б с Эмерсон, С; Хеджес, Дж. (октябрь 1988 г.). «Процессы контроля содержания органического углерода в отложениях открытого океана». Палеоокеанография . 3 (5): 621–634. Бибкод : 1988PalOc...3..621E . дои : 10.1029/pa003i005p00621 .
- ^ Сиа, Филипп; Сабина, Кристофер (2014). Изменение климата 2013: основы физической науки. Вклад Рабочей группы I в Пятый оценочный отчет Межправительственной группы экспертов по изменению климата (PDF) . Издательство Кембриджского университета. стр. 465–470.
- ^ Флеминг, Р.Х.; Ревель, Р. (1939). «Физические процессы в Мировом океане». В Траске, П.Д. (ред.). Современные морские отложения . Талса: Американская ассоциация геологов-нефтяников . стр. 48–141.
- ^ Бернер, Роберт А. (1 января 1989 г.). «Биогеохимические циклы углерода и серы и их влияние на атмосферный кислород в фанерозойское время». Палеогеография, Палеоклиматология, Палеоэкология . Долгосрочная стабильность системы Земли. 75 (1): 97–122. Бибкод : 1989PPP....75...97B . дои : 10.1016/0031-0182(89)90186-7 .
- ^ Хенрикс, Сьюзен (1992). «Ранний диагенез органического вещества в морских отложениях: прогресс и недоумение». Морская химия . 39 (1–3): 119–149. дои : 10.1016/0304-4203(92)90098-У .
- ^ Jump up to: а б Картапанис, Оливье; Бьянки, Даниэле; Жаккар, Самуэль; Гэлбрейт, Эрик (21 января 2016 г.). «Глобальные импульсы захоронения органического углерода в глубоководных отложениях во время ледниковых максимумов» . Природные коммуникации . 7 : 10796. Бибкод : 2016NatCo...710796C . дои : 10.1038/ncomms10796 . ПМЦ 4773493 . ПМИД 26923945 .
- ^ Клейпул, GE; Каплан, ИК (1974). Природные газы в морских отложениях . Пленум Пресс. стр. 99–139.
- ^ Д'Ондт, С; Резерфорд, С; Спивак, Эй Джей (2002). «Метаболическая активность подземной жизни в глубоководных отложениях». Наука . 295 (5562): 2067–2070. Бибкод : 2002Sci...295.2067D . дои : 10.1126/science.1064878 . ПМИД 11896277 . S2CID 26979705 .
- ^ Квенволден, Калифорния; Лоренсон, Т.Д. (2001). Чарльз К. Полл; Уильям П. Диллон (ред.). Гидраты природного газа: появление, распространение и обнаружение . Серия геофизических монографий. Том. 124. Американский геофизический союз. стр. 3–18. ISBN 978-0-875-90982-0 .
- ^ Уге, Карме; де Ланге, Герт Дж.; Густафссон, Орьян; Мидделбург, Джек Дж.; Синнингхе Дамсте, Яап С.; Схоутен, Стефан (15 декабря 2008 г.). «Селективное сохранение органического вещества почвы в окисленных морских отложениях (Абиссальная равнина Мадейры)». Geochimica et Cosmochimica Acta . 72 (24): 6061–6068. Бибкод : 2008GeCoA..72.6061H . дои : 10.1016/j.gca.2008.09.021 .
- ^ Jump up to: а б с Хеджес, Джон И.; Ху, Фэн Шэн; Девол, Аллан Х.; Хартнетт, Хилэри Э .; Цамакис, Элизабет; Кейл, Ричард Г. (1999). «Сохранение осадочных органических веществ: тест на избирательное разложение в кислородных условиях» . Американский научный журнал . 299 (7–9): 529. Бибкод : 1999AmJS..299..529H . дои : 10.2475/ajs.299.7-9.529 . ISSN 0002-9599 .
- ^ Jump up to: а б Кристенсен, Эрик; Ахмед, Сайед И.; Девол, Аллан Х. (1 декабря 1995 г.). «Аэробное и анаэробное разложение органических веществ в морских отложениях: что происходит быстрее?» . Лимнология и океанография . 40 (8): 1430–1437. Бибкод : 1995LimOc..40.1430K . дои : 10.4319/lo.1995.40.8.1430 . ISSN 1939-5590 .
- ^ Смит, Ричард; Бьянки, Томас; Эллисон, Мид; Сэвидж, Кандида; Гали, Валье (2015). «Высокие темпы захоронения органического углерода в отложениях фьордов во всем мире». Природа Геонауки . 8 (6): 450. Бибкод : 2015NatGe...8..450S . дои : 10.1038/ngeo2421 .
- ^ Кастинг, Дж. Ф.; Тун, О.Б.; Поллак, Дж. Б. (1 февраля 1988 г.). «Как развивался климат на планетах земной группы». Научный американец . 258 (2): 90–97. Бибкод : 1988SciAm.258b..90K . doi : 10.1038/scientificamerican0288-90 . ISSN 0036-8733 . ПМИД 11538470 .
- ^ Хативала, С; Примо, Ф; Холл, Т. (2009). «Реконструкция истории антропогенных концентраций CO2 в океане» . Природа . 462 (7271): 346–349. Бибкод : 2009Natur.462..346K . дои : 10.1038/nature08526 . ПМИД 19924213 . S2CID 2301279 .
- ^ Ле Кер, К; Андрес, Р; Боден, Т; Конвей, Т; Хоутон, Р; Хаус, Дж; Марланд, Дж; Питерс, Дж; ван дер Верф, Г; Альстрем, А; Эндрю, Р; Бопп, Л; Канаделл, Дж; Сиас, П; Дони, С; Энрайт, С; Фридлингстон, П; Хантингфорд, К; Джайн, А; Журден, К; Като, Э; Килинг, Р; Кляйн Гольдевейк, К; Левис, С; Леви, П; Ломас, М; Поултер, Б; Раупак, М; Швингер, Дж; Ситч, С; Стокер, Б; Виви, Н; Захле, С; Чжэн, Н. (2013). «Глобальный углеродный бюджет 1959–2011» . Данные науки о системе Земли . 5 (1): 165–185. Бибкод : 2013ESSD....5..165L . дои : 10.5194/essd-5-165-2013 . hdl : 10871/20993 .
- ^ Набережная, Вашингтон; Тилбрук, Б.; Вонг, CS (3 апреля 1992 г.). «Поглощение океаном ископаемого топлива CO2: данные об углероде-13». Наука . 256 (5053): 74–79. Бибкод : 1992Sci...256...74Q . дои : 10.1126/science.256.5053.74 . ISSN 0036-8075 . ПМИД 17802595 . S2CID 9289370 .
- ^ Ревелл, Роджер; Зюсс, Ганс Э. (1 февраля 1957 г.). «Обмен углекислым газом между атмосферой и океаном и вопрос увеличения содержания CO2 в атмосфере за последние десятилетия». Теллус . 9 (1): 18–27. Бибкод : 1957TellA...9...18R . дои : 10.1111/j.2153-3490.1957.tb01849.x . ISSN 2153-3490 .
- ^ Сиас, П; Сабина, К. (2014). «6» (PDF) . Углеродный и другие биогеохимические циклы в изменении климата, 2013: Физические научные основы . Кембридж и Нью-Йорк: Издательство Кембриджского университета. стр. 465–570. Архивировано из оригинала (PDF) 3 октября 2018 г. Проверено 24 ноября 2017 г.
- ^ Бур, Г; Арора, В. (2013). «Обратная связь в глобальных бюджетах углерода, обусловленных выбросами и концентрацией» . Журнал климата . 26 (10): 3326–3341. Бибкод : 2013JCli...26.3326B . дои : 10.1175/JCLI-D-12-00365.1 .
- ^ Грегори, Дж; Джонс, К; Кадуле, П; Фридлингштейн, П. (2009). «Количественная оценка обратной связи углеродного цикла» (PDF) . Журнал климата . 22 (19): 5232–5250. Бибкод : 2009JCli...22.5232G . дои : 10.1175/2009JCLI2949.1 . S2CID 59385833 .
- ^ Харви, Фиона (04 декабря 2019 г.). «Решение проблемы деградации океанов может смягчить климатический кризис – доклад» . Хранитель . ISSN 0261-3077 . Проверено 7 декабря 2019 г.
- ^ Харви, Фиона (07 декабря 2019 г.). «Океаны теряют кислород с беспрецедентной скоростью, предупреждают эксперты» . Хранитель . ISSN 0261-3077 . Проверено 7 декабря 2019 г.
- ^ Калдейра, Кен; Уикетт, Майкл Э. (25 сентября 2003 г.). «Океанография: антропогенный углерод и pH океана» . Природа . 425 (6956): 365. Бибкод : 2003Natur.425..365C . дои : 10.1038/425365a . ISSN 1476-4687 . ПМИД 14508477 . S2CID 4417880 .
- ^ Jump up to: а б с д и ж Гаттузо, Жан-Пьер; Ханссон, Лина (2011). Закисление океана . Оксфорд [Англия]: Издательство Оксфордского университета. ISBN 9780199591091 . OCLC 823163766 .
- ^ Бартон, Алан (2015). «Воздействие закисления прибрежных зон на индустрию моллюсков северо-западной части Тихого океана и стратегии адаптации, реализованные в ответ» (PDF) . Океанография . 25 (2): 146–159. дои : 10.5670/oceanog.2015.38 .
- ^ Jump up to: а б Омон, О.; Бопп, Л. (1 июня 2006 г.). «Глобализация результатов исследований железного удобрения океана in situ» . Глобальные биогеохимические циклы . 20 (2): GB2017. Бибкод : 2006GBioC..20.2017A . дои : 10.1029/2005gb002591 . ISSN 1944-9224 .
- ^ Чисхолм, С; Фальковский, П; Каллен, Дж (2001). «Дискредитация удобрения океана». Наука . 294 (5541): 309–310. дои : 10.1126/science.1065349 . ПМИД 11598285 . S2CID 130687109 .
- ^ Ленер, Б; Лирманн, К; Ревенга, К; Воросмарти, К; Фекете, Б; Крузе, П; Кукла, П; Эндежан, М; Френкен, К; Магоме, Дж; Нильссон, К; Робертсон, Дж; Родель, Р; Зиндорф, Н.; Виссер, Д. (2011). «Картирование мировых водохранилищ и плотин с высоким разрешением для устойчивого управления речным стоком» . Границы в экологии и окружающей среде . 9 (9): 494–502. дои : 10.1890/100125 .
- ^ Ренье, Пьер; Фридлингштейн, Пьер; Сиа, Филипп; и др. (2013). «Антропогенное возмущение потоков углерода с суши в океан» . Природа Геонауки . 6 (8): 597–607. Бибкод : 2013NatGe...6..597R . дои : 10.1038/ngeo1830 . hdl : 10871/18939 . S2CID 53418968 .
{{cite journal}}: CS1 maint: числовые имена: список авторов ( ссылка ) - ^ Jump up to: а б с д и Маавара, Т; Лауэрвальд, Р; Ренье, П; Ван Каппеллен, П. (2016). «Глобальное нарушение круговорота органического углерода из-за строительства плотин на реках» . Природа . 8 : 15347. Бибкод : 2017NatCo...815347M . дои : 10.1038/ncomms15347 . ПМЦ 5442313 . ПМИД 28513580 .
- ^ Баррос, Н.; Коул, Дж; Транвик, Л; Прейри, Ю; Баствикен, Д; Гузар, В; дель Джорджио, П; Роланд, Ф. (2011). «Выбросы углерода из гидроэлектрических водоемов связаны с возрастом и широтой водохранилища». Природа Геонауки . 4 (9): 593–596. Бибкод : 2011NatGe...4..593B . дои : 10.1038/ngeo1211 . S2CID 52245758 .




![{\displaystyle {\ce {{\underset {диоксид углерода}}{6CO2}}+{\underset {вода}{6H2O}}->[световая~энергия]{\underset {углевод}{C6H12O6}}+{\ ниже {кислорода}{6O2}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/cdcf64396a6289ac1a8f18afa8a4e15b47c13924)


