Аэробное производство метана

Аэробное производство метана является потенциальным биологическим путем производства атмосферного метана (CH 4 ) в условиях насыщения кислородом . Существование этого пути впервые было высказано в 2006 году. [1] Хотя существенные данные свидетельствуют о существовании этого пути, [1] [2] [3] [4] [5] он остается плохо изученным, и его существование вызывает споры. [2] [6] [7] Встречающийся в природе метан в основном производится в процессе метаногенеза — формы анаэробного дыхания , используемой микроорганизмами в качестве источника энергии. [8] Метаногенез обычно происходит только в бескислородных условиях. Напротив, аэробное считается, что производство метана происходит в насыщенной кислородом среде в условиях, близких к окружающей среде . Этот процесс включает немикробную генерацию метана из наземных растений . Считается, что температура и ультрафиолет являются ключевыми факторами в этом процессе. [1] Метан также может производиться в аэробных условиях в приповерхностных водах океана, и этот процесс, вероятно, включает в себя разложение метилфосфоната. [9]
Из наземных растений
[ редактировать ]
| Часть серии о |
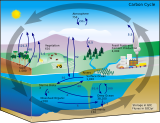
| Углеродный цикл |
|---|
 |
Первоначальное открытие
[ редактировать ]В 2005 году Франкенберг и др. опубликовали результаты глобального исследования распределения метана, в котором они использовали космическую спектроскопию поглощения в ближнем инфракрасном диапазоне . Исследование выявило значительно повышенные CH 4 соотношения смешивания в тропических регионах над вечнозелеными лесами. [10] Данные указывают на дополнительный тропический источник 30–40 Тг. [10] за период расследования (август-ноябрь). Этот вклад не может быть адекватно объяснен в рамках принятого в настоящее время глобального бюджета CH 4 . [10] Эти результаты побудили Кеплера и соавт. провести исследование по изучению возможности образования метана растительным материалом. Их исследование включало эксперименты по инкубации в стеклянных флаконах с оторванными листьями и эксперименты в камере из оргстекла с неповрежденными растениями. В обоих случаях материал герметизировали в контролируемой среде с воздухом, не содержащим CH 4 , для анализа образования CH 4 . Поскольку испытания проводились в аэробных условиях, маловероятно, что какой-либо образующийся CH 4 будет связан с метаногенными бактериями. [1] Эта возможность была дополнительно исключена путем измерения продукции CH 4 тканями листьев, стерилизованными γ-излучением . Они предположили, что «структурный компонент пектин играет важную роль в in situ образовании CH 4 в растениях». [1] но не смогли определить химический механизм производства CH 4 .
Дальнейшее изучение
[ редактировать ]Ван и др. (2008) обнаружили, что выбросы метана сильно различаются в зависимости от вида растений, отметив, что кустарниковые виды с гораздо большей вероятностью производят метан, чем травянистые виды. [4] Они также отметили, что среди травянистых видов, которые они тестировали, те, которые выделяли метан из стеблей, а не из отдельных листьев, в то время как виды кустарников обычно выделяли более высокие концентрации метана из отдельных листьев. [4] Последующее исследование Keppler et al. подтвердили свои более ранние выводы и нашли «однозначное изотопное доказательство того, что метоксильные группы пектина могут выступать в качестве источника атмосферного CH 4 в аэробных условиях», [3] но снова не удалось определить химический механизм.
Влияние температуры и света
[ редактировать ]Кепплер и др. . заметил, что высвобождение CH 4 «очень чувствительно к температуре - концентрации примерно удваиваются с увеличением на каждые 10 ° C в диапазоне 30–70 ° C, что указывает на неферментативный, а не ферментативный процесс ». [1] Они также отметили, что «обнаружено, что интенсивность выбросов резко возросла, в 3–5 раз (до 870 нг на г (сухого веса) ч). −1 ), когда камеры подвергались воздействию естественного солнечного света». [1] Вигано и др. . обнаружили, что «выбросы от УФ-облучения происходят почти мгновенно, что указывает на прямой фотохимический процесс ». [2]
Потенциальная экологическая значимость
[ редактировать ]Кепплер и др. . рассчитали «первую оценку» вновь созданного источника CH 4 . Их расчеты основывались на широких предположениях, которые, по их признанию, не учитывали «сложность наземных экосистем ». [1] По их оценкам, объем метана, выделяемого живой растительностью, находится в диапазоне 62–236 Тг в год. −1 (в среднем 149 Тг/год −1 ), при этом основной вклад отведен тропическим лесам и лугам. [1] Они полагали, что «обнаружение дополнительного источника такого масштаба, составляющего около 10–30% от нынешней годовой мощности источника, потребует пересмотра глобального бюджета CH 4 ». [1] Более поздние оценки с использованием Keppler et al. Данные США , а также данные, полученные в ходе более поздних исследований, предполагают меньшую глобальную значимость. [3] Одно исследование показало, что максимальные глобальные выбросы метана наземными растениями могут составлять всего лишь порядка 0,2–1,0 Тг CH 4 года. −1 по сравнению с общими глобальными выбросами 550 Тг CH 4 года −1 , существенно меньший вклад. [5]
Критика и противоречивые данные
[ редактировать ]После публикации Keppler et al. ( 2006 ), это вызвало существенную реакцию со стороны научного сообщества. Многие подвергли сомнению полученные результаты, указав на недостатки в работе Keppler et al. ' s методология. В частности, критике подвергся их метод масштабирования для расчета глобальных оценок выбросов метана наземными растениями. [2] В ряде последующих публикаций были представлены противоречивые данные, что привело к значительной неопределенности в отношении роли наземных растений в глобальном балансе метана.
Дуек и др. провели эксперименты, аналогичные экспериментам с камерами с неповрежденными растениями, проведенным Keppler et al. . Они не нашли «никаких доказательств значительных выбросов метана наземными растениями». [7] Они предположили, что предполагаемые выбросы, наблюдаемые Кепплером и др. возможно, было связано с «концентрацией метана в межклеточных воздушных пространствах и воздушных пространствах почвенной системы». [7] Вигано и др. позже ответил на эту критику, предположив, что, если УФ-свет действительно является важным фактором аэробных выбросов метана, «то неудивительно, что Дуек и др . (2007), которые использовали металлогалогенные лампы HPI-T, не обнаружили никаких выбросов. лампы и стеклянные камеры для их измерений». [2] Другие исследования показали, что обнаруженные выбросы метана были связаны с переносом растворенного метана из почвы в воду или со спонтанным распадом растительного вещества в определенных стрессовых условиях. [6]
В водной среде
[ редактировать ]Пересыщение метаном в насыщенных кислородом приповерхностных водах океанов, озер и рек — явление, которое широко наблюдалось, но до сих пор плохо изучено. [11] Метан часто перенасыщен на 10–75% в насыщенном кислородом поверхностном смешанном слое океанов и на 1000% в озерах, в результате чего водная среда вносит метан в атмосферу. [11] [12] [13]
Было идентифицировано несколько источников и механизмов производства метана в водной среде. Одним из таких источников является разложение метилфосфоната растворенной воды . [9] Важность разложения метилфосфоната при производстве CH4 в океане, вероятно, варьируется и может быть связана с наличием Fe , N и P в толще воды. [11] а также наличию и природе ферментативного механизма, обрабатывающего метилфосфонаты. [14]
Второй источник, который, по-видимому, не зависит ни от какого субстрата, — это выделение метана фитопланктоном (водорослями и цианобактериями) в процессе фотосинтеза. [15] [16]
Присутствие водорослей и цианобактерий во всех освещенных водных средах на Земле, вероятно, делает этот процесс значительным вкладом в выбросы водного метана. В последние десятилетия мы наблюдаем увеличение цветения цианобактерий и водорослей в результате антропогенного загрязнения и глобального потепления. [17] [18]
Поскольку атмосферный метан является очень мощным парниковым газом, была выдвинута гипотеза о петле обратной связи, в которой водоросли и цианобактерии производят метан, усиливают потепление и впоследствии усиливают цветение. [19] Диметилсульфониопропионат (ДМСП) — широко распространенное соединение в морской среде, используемое водорослями в качестве осмопротектора. Несколько исследований показали, что разложение ДМСП бактериями приводит к выделению метана. [20] [21]
Метиламины являются известным источником метана из бескислородной среды. В 2018 году Бизич и др. опубликованные результаты показывают, что разложение метиламинов приводит к выбросам метана даже в кислородных условиях. [22] Механизм, ответственный за этот процесс, позже был установлен Wang et al. и был приписан одному, очень распространенному гену. [23] [24]
С тех пор были признаны несколько других механизмов. В 2022 году Перес-Коронель и Беман проанализировали производство метана в пресной воде и обнаружили связь с «метаболизмом (бактериального) хлорофилла и фотосинтезом». [25] Кепплер и его коллеги определили механизм, посредством которого активные формы кислорода приводят к производству метана организмом, потенциально использующим кислород. [26] [27]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д и ж г час я дж Кепплер, Фрэнк; Гамильтон, Джон Т.Г.; Брасс, Марк; Рёкманн, Томас (12 января 2006 г.). «Выбросы метана наземными растениями в аэробных условиях». Природа . 439 (7073): 187–191. Бибкод : 2006Natur.439..187K . дои : 10.1038/nature04420 . ПМИД 16407949 . S2CID 2870347 .
- ^ Перейти обратно: а б с д и Вигано, И.; ван Вельден, Х.; Хольцингер, Р.; Кепплер, Ф.; Маклеод, А.; Рёкманн, Т. (26 июня 2008 г.). «Влияние УФ-излучения и температуры на выделение метана растительной биомассой и структурными компонентами» . Биогеонауки . 5 (3): 937–947. Бибкод : 2008BGeo....5..937V . дои : 10.5194/bg-5-937-2008 .
- ^ Перейти обратно: а б с Кепплер, Фрэнк; Гамильтон, Джон Т.Г.; МакРобертс, В. Колин; Вигано, Иван; Брасс, Марк; Рёкманн, Томас (июнь 2008 г.). «Метоксильные группы растительного пектина как предшественник атмосферного метана: данные исследований по маркировке дейтерием» . Новый фитолог . 178 (4): 808–814. дои : 10.1111/j.1469-8137.2008.02411.x . ПМИД 18346110 .
- ^ Перейти обратно: а б с Ван, ЗП; Хан, XG; Ван, Г.Г.; Песня, Ю; Галледж, Дж. (1 января 2008 г.). «Аэробная эмиссия метана растениями степи Внутренней Монголии». Экологические науки и технологии . 42 (1): 62–8. Бибкод : 2008EnST...42...62W . дои : 10.1021/es071224l . ПМИД 18350876 .
- ^ Перейти обратно: а б Блум, А. Энтони; Ли-Тейлор, Джулия; Мадронич, Саша; Мессенджер, Дэвид Дж.; Палмер, Пол И.; Рей, Дэвид С.; Маклеод, Энди Р. (июль 2010 г.). «Оценки глобальных выбросов метана в результате ультрафиолетового облучения листвы наземных растений» . Новый фитолог . 187 (2): 417–425. дои : 10.1111/j.1469-8137.2010.03259.x . ПМИД 20456057 .
- ^ Перейти обратно: а б Нисбет, RER; Фишер, Р.; Ниммо, Р.Х.; Бендалл, Д.С.; Крилл, премьер-министр; Гальего-Сала, А.В.; Хорнибрук, ERC; Лопес-Хуес, Э; Лоури, Д; Нисбет, PBR; Шакбург, EF; Шрискантараджа, С; Хау, CJ; Нисбет, Э.Г. (13 января 2009 г.). «Выбросы метана растениями» . Труды Королевского общества B: Биологические науки . 276 (1660): 1347–1354. дои : 10.1098/rspb.2008.1731 . ПМК 2660970 . ПМИД 19141418 .
- ^ Перейти обратно: а б с Дуек, штат Калифорния; де Виссер, Р.; Пуртер, Х; Персейн, С; Гориссен, А; де Виссер, В; Шапендонк, А; Верхаген, Дж; Быстрый, Дж; Харрен, Ф.Дж.; Нгай, А.К.; Ферстаппен, Ф; Бауместер, Х; Воесенек, Луизиана; ван дер Верф, А (2007). «Нет доказательств значительных аэробных выбросов метана наземными растениями: подход с маркировкой 13C» . Новый фитолог . 175 (1): 29–35. дои : 10.1111/j.1469-8137.2007.02103.x . ПМИД 17547664 .
- ^ Тауэр, РК (1998). «Биохимия метаногенеза: дань уважения Марджори Стивенсон» . Микробиология . 144 (9): 2377–2406. дои : 10.1099/00221287-144-9-2377 . ПМИД 9782487 .
- ^ Перейти обратно: а б Карл, Дэвид М.; Беверсдорф, Лукас; Бьоркман, Карин М.; Черч, Мэтью Дж.; Мартинес, Асунсьон; Делонг, Эдвард Ф. (29 июня 2008 г.). «Аэробное производство метана в море». Природа Геонауки . 1 (7): 473–478. Бибкод : 2008NatGe...1..473K . дои : 10.1038/ngeo234 .
- ^ Перейти обратно: а б с Франкенберг, К.; Мейринк, Дж. Ф.; ван Вил, М.; Платт, Ю.; Вагнер, Т. (13 мая 2005 г.). «Оценка выбросов метана по данным глобальных космических наблюдений». Наука . 308 (5724): 1010–1014. Бибкод : 2005Sci...308.1010F . дои : 10.1126/science.1106644 . ПМИД 15774724 . S2CID 14987357 .
- ^ Перейти обратно: а б с дель Валле, Д.А.; Карл, DM (2 октября 2014 г.). «Аэробное производство метана из растворенного в толще воды метилфосфоната и тонущих частиц в субтропическом круговороте северной части Тихого океана» . Водная микробная экология . 73 (2): 93–105. дои : 10.3354/ame01714 .
- ^ Розентретер, Джудит А.; Борхес, Альберто В.; Димер, Бриджит Р.; Хольгерсон, Мередит А.; Лю, Шаода; Сун, Чунлин; Мелак, Джон; Раймонд, Питер А.; Дуарте, Карлос М.; Аллен, Джордж Х.; Олефельдт, Дэвид; Поултер, Бенджамин; Баттин, Том И.; Эйр, Брэдли Д. (апрель 2021 г.). «Половина глобальных выбросов метана происходит из весьма изменчивых источников водных экосистем». Природа Геонауки . 14 (4): 225–230. Бибкод : 2021NatGe..14..225R . дои : 10.1038/s41561-021-00715-2 . hdl : 10754/668712 . S2CID 233030781 .
- ^ Гюнтель, Марко; Донис, Дафна; Кириллин Георгий; Ионеску, Дэнни; Бизич, Мина; Макгиннис, Дэниел Ф.; Гроссарт, Ганс-Петер; Тан, Кам В. (2 декабря 2019 г.). «Вклад производства кислородного метана в поверхностные выбросы метана в озерах и его глобальное значение» . Природные коммуникации . 10 (1): 5497. Бибкод : 2019NatCo..10.5497G . дои : 10.1038/s41467-019-13320-0 . ПМК 6888895 . ПМИД 31792203 .
- ^ Соса, Оскар А.; Кейси, Джон Р.; Карл, Дэвид М. (июль 2019 г.). «Окисление метилфосфоната в штамме прохлорококка MIT9301 способствует приобретению фосфатов, выделению формиатов и ассимиляции углерода в пурины» . Прикладная и экологическая микробиология . 85 (13). Бибкод : 2019ApEnM..85E.289S . дои : 10.1128/AEM.00289-19 . ПМК 6581173 . ПМИД 31028025 .
- ^ Уильямс, Р. (2020) Сине-зеленые водоросли производят метан, The Scientist Magazine®. Доступно по адресу: https://www.the-scientist.com/blue-green-algae-produce-mthan-66971 (дата обращения: 12 марта 2024 г.).
- ^ Клинч, Томас; Лангер, Джеральд; Нерке, Гернот; Виланд, Анна; Ленхарт, Катарина; Кепплер, Франк (28 октября 2019 г.). «Производство метана тремя широко распространенными видами морского фитопланктона: скорость выбросов, соединения-прекурсоры и потенциальное значение для окружающей среды» . Биогеонауки . 16 (20): 4129–4144. Бибкод : 2019BGeo...16.4129K . дои : 10.5194/bg-16-4129-2019 .
- ^ Потепление климата может усилить цветение водорослей, вызванное выбросом питательных веществ в отложения в озерах – управление должно адаптироваться (2023 г.) Окружающая среда. Доступно по адресу: https://environment.ec.europa.eu/news/climate-warming-may-increase-algal-blooms-caused-sediment-nutrient-release-lakes-management-must-2023-01-18_en (доступ : 12 марта 2024 г.).
- ^ Колм, Р. (2024) Агентство по охране окружающей среды: Сельское хозяйство является «основным фактором» цветения водорослей в сельских районах, Agriland.ie. Доступно по адресу: https://www.agriland.ie/farming-news/epa-agricultural-the-biggest-driver-of-algal-blooms-in-rural-areas (дата обращения: 12 марта 2024 г.).
- ^ Бизич, Мина (23 ноября 2021 г.). «Фотосинтез фитопланктона: неизведанный источник биогенной эмиссии метана из кислородной среды». Журнал исследований планктона . 43 (6): 822–830. дои : 10.1093/plankt/fbab069 .
- ^ Флорес-Лейва, Леннин; Дамм, Эллен; Фариас, Лаура (май 2013 г.). «Производство метана, вызванное диметилсульфидом в поверхностных водах апвеллинговой экосистемы» (PDF) . Прогресс в океанографии . 112–113: 38–48. Бибкод : 2013Proce.112...38F . дои : 10.1016/j.pocean.2013.03.005 .
- ^ Дамм, Э.; Киене, РП; Шварц, Дж.; Фальк, Э.; Дикманн, Г. (февраль 2008 г.). «Круговорот метана в арктических шельфовых водах и его связь с биомассой фитопланктона и DMSP». Морская химия . 109 (1–2): 45–59. Бибкод : 2008МартЧ.109...45Д . дои : 10.1016/j.marchem.2007.12.003 .
- ^ Бижич-Ионеску, Мина; Ионеску, Дэнни; Гюнтель, Марко; Тан, Кам В.; Гроссарт, Ханс-Петер (2018). «Круговорот кислородного метана: новые доказательства образования метана в воде кислородного озера». Биогенез углеводородов . стр. 1–22. дои : 10.1007/978-3-319-53114-4_10-1 . ISBN 978-3-319-53114-4 .
- ^ Государственный университет Монтаны (2021 г.) Исследовательская группа публикует революционное открытие синтеза метана, Phys.org - Новости и статьи по науке и технологиям. Доступно по адресу: https://phys.org/news/2021-07-team-publishes-groundbreaking-mthan-synthesis.amp (дата обращения: 13 марта 2024 г.).
- ^ Ван, Цянь; Аловаифер, Абдулла; Кернер, Патрисия; Баласубраманиан, Нараянаганеш; Паттерсон, Анджела; Кристиан, Уильям; Тарвер, Анджела; Дор, Джон Э.; Хаценпихлер, Роланд; Ботнер, Брайан; Макдермотт, Тимоти Р. (6 июля 2021 г.). «Аэробный бактериальный синтез метана» . Труды Национальной академии наук . 118 (27). Бибкод : 2021PNAS..11819229W . дои : 10.1073/pnas.2019229118 . ПМЦ 8271786 . ПМИД 34183407 .
- ^ Перес-Коронель, Элизабет; Майкл Беман, Дж. (29 октября 2022 г.). «Множественные источники производства аэробного метана в водных экосистемах включают бактериальный фотосинтез» . Природные коммуникации . 13 (1): 6454. Бибкод : 2022NatCo..13.6454P . дои : 10.1038/s41467-022-34105-y . ПМЦ 9617973 . ПМИД 36309500 .
- ^ Эрнст, Леонард; Стейнфельд, Бенедикт; Бараев Владимир; Клинч, Томас; Курт, Маркус; Гримм, Дирк; Дик, Тобиас П.; Ребелейн, Йоханнес Г.; Бишофс, Илька Б.; Кепплер, Франк (17 марта 2022 г.). «Образование метана, обусловленное активными формами кислорода во всех живых организмах». Природа . 603 (7901): 482–487. Бибкод : 2022Nature.603..482E . дои : 10.1038/s41586-022-04511-9 . PMID 35264795 .
- ^ Лю, Чанг; Чжан, Цзинъяо (17 марта 2022 г.). «Метан могут производить все живые организмы». Природа . 603 (7901): 396–397. Бибкод : 2022Natur.603..396L . дои : 10.1038/d41586-022-00206-3 . ПМИД 35264800 . S2CID 247362071 .