Осадки (химия)
В этой статье есть несколько проблем. Пожалуйста, помогите улучшить его или обсудите эти проблемы на странице обсуждения . ( Узнайте, как и когда удалять эти шаблонные сообщения )
|

В водном растворе осаждение — это «осаждение твердого материала (осадка) из жидкого раствора». [1] [2] Образовавшееся твердое вещество называется осадком . [3] В случае неорганической химической реакции, приводящей к осаждению, химический реагент, вызывающий образование твердого вещества, называется осадителем . [4]
Прозрачная жидкость, остающаяся над осажденной или центрифугированной твердой фазой, также называется надосадочной жидкостью или надосадочной жидкостью .
Понятие осаждения также можно распространить на другие области химии ( органическую химию и биохимию ) и даже применить к твердым фазам (например, металлургии и сплавам ), когда твердые примеси отделяются от твердой фазы.
Пересыщение [ править ]
Осаждение соединения может произойти, когда его концентрация превышает его растворимость . Это может быть связано с изменением температуры, испарением растворителя или смешиванием растворителей. Осаждение происходит быстрее из сильно пересыщенного раствора.
Образование осадка может быть вызвано химической реакцией. При хлорида бария взаимодействии раствора с серной кислотой белый осадок сульфата бария образуется . При йодида калия взаимодействии раствора с раствором нитрата свинца(II) желтый осадок йодида свинца(II) образуется .
Неорганическая химия [ править ]
Образование осадка полезно для определения типа катиона в соли . Для этого щелочь сначала реагирует с неизвестной солью с образованием осадка, представляющего собой гидроксид неизвестной соли. Для идентификации катиона отмечают цвет осадка и его растворимость в избытке. Подобные процессы часто используются последовательно - например, раствор нитрата бария вступает в реакцию с ионами сульфата с образованием твердого осадка сульфата бария , что указывает на вероятность присутствия ионов сульфата.
Типичным примером осаждения из водного раствора является хлорид серебра . При добавлении нитрата серебра (AgNO 3 ) к раствору хлорида калия (KCl) наблюдается осаждение белого твердого вещества (AgCl). [5] [6]
Ионное уравнение позволяет записать эту реакцию, детализируя диссоциированные ионы, присутствующие в водном растворе.
Восстановительные осадки [ править ]

Восстановитель Вальдена является иллюстрацией реакции восстановления, непосредственно сопровождающейся осаждением менее растворимого соединения из-за его более низкой химической валентности:
Восстановитель Вальдена, изготовленный из крошечных кристаллов серебра , полученных погружением медной проволоки в раствор нитрата серебра, используется для восстановления до более низкой валентности любого иона металла, расположенного выше пары серебра (Ag + + 1 и – → Ag) в шкале окислительно-восстановительного потенциала .
Коллоидные суспензии [ править ]
Без достаточных сил притяжения ( например , силы Ван-дер-Ваальса ) для агрегирования твердых частиц вместе и удаления их из раствора под действием силы тяжести ( осаждения ), они остаются во взвешенном состоянии и образуют коллоиды . Седиментацию можно ускорить с помощью высокоскоростного центрифугирования . Полученную таким образом компактную массу иногда называют «таблеткой».
и ускорение старения Пищеварение
Пищеварение, или старение осадка , происходит, когда свежеобразованный осадок остается, обычно при более высокой температуре , в растворе, из которого он выпадает. В результате получаются более чистые и крупные рекристаллизованные частицы. Физико-химический процесс, лежащий в основе пищеварения, называется оствальдовским созреванием . [7] [8]
Органическая химия [ править ]

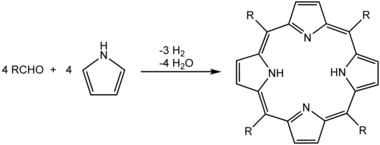
Хотя реакции осаждения можно использовать для изготовления пигментов , удаления ионов из раствора при очистке воды и в классическом качественном неорганическом анализе , осаждение также обычно используется для выделения продуктов органической реакции во время операций обработки и очистки. В идеале продукт реакции нерастворим в растворителе, используемом для реакции. Таким образом, он выпадает в осадок по мере образования, предпочтительно образуя чистые кристаллы . Примером этого может быть синтез порфиринов в кипящей пропионовой кислоте . При охлаждении реакционной смеси до комнатной температуры кристаллы порфирина осаждаются и собираются фильтрацией на фильтре Бюхнера, как показано на фотографии рядом: [9]
Осаждение также может происходить при добавлении антирастворителя (растворителя, в котором продукт нерастворим), что резко снижает растворимость желаемого продукта. После этого осадок можно легко отделить декантацией , фильтрованием или центрифугированием . Примером может служить синтез Cr 3+ хлорид тетрафенилпорфирина добавляют воду , и продукт выпадает в осадок. : к раствору диметилформамида (ДМФ) , в котором произошла реакция, [10] Осаждение полезно при очистке многих других продуктов: например , сырой bmim -Cl растворяется в ацетонитриле и по каплям в этилацетат , где он выпадает в осадок. [11]
Биохимия [ править ]
Очистку и разделение белков можно осуществлять методом осаждения при изменении природы растворителя или значения его относительной диэлектрической проницаемости ( например , путем замены воды на этанол ) или путем увеличения ионной силы раствора. Поскольку белки имеют сложную третичную и четвертичную структуру из-за их специфической укладки и различных слабых межмолекулярных взаимодействий ( например , водородных мостиков), эти сверхструктуры могут быть модифицированы, а белки денатурированы и преципитированы. применение антирастворителя — осаждение ДНК Другое важное этанолом .
Металлургия и сплавы [ править ]
В твердых фазах осаждение происходит, если концентрация одного твердого вещества превышает предел растворимости в твердом веществе-хозяине, например, из-за быстрого гашения или ионная имплантация , а температура достаточно высока, чтобы диффузия могла привести к сегрегации в осадки. Осаждение в твердых телах обычно используется для синтеза нанокластеров . [12]
В металлургии осаждение из твердого раствора также является способом упрочнения сплавов .
Выделение керамических фаз в металлических сплавах, таких как гидриды циркония, в циркалойной оболочке ядерных твэлов также может сделать металлические сплавы хрупкими и привести к их механическому разрушению. Поэтому правильное соблюдение точного температурно-барического режима при охлаждении отработавшего ядерного топлива имеет важное значение для предотвращения повреждения его оболочек и сохранения целостности отработавших твэлов на длительный срок в сухих контейнерах хранения и в условиях геологического захоронения.
Промышленные процессы
Осаждение гидроксидом, вероятно, является наиболее широко используемым промышленным процессом осаждения, при котором гидроксиды металлов образуются путем добавления гидроксида кальция ( гашеная известь ) или гидроксида натрия ( каустическая сода ) в качестве осадителя.
История [ править ]
Порошки, полученные в результате различных процессов осаждения, также исторически были известны как «цветы».
См. также [ править ]
- Соосаждение
- Вскипание , «стрелка вверх»
- Зона без осадков
- Засолка
- Высаливание
Ссылки [ править ]
- ^ «осадки» . Золотая книга ИЮПАК .
- ^ «Химическое осаждение» . Британская энциклопедия . Проверено 28 ноября 2020 г.
- ^ «осаждать» . Словарь Merriam-Webster.com . Проверено 28 ноября 2020 г.
- ^ «осадитель» . Словарь Merriam-Webster.com . Проверено 28 ноября 2020 г.
- ^ Зумдал, Стивен С.; ДеКост, Дональд Дж. (2012). Химические принципы . Cengage Обучение. ISBN 978-1-133-71013-4 .
- ^ Зумдал, Стивен С.; ДеКост, Дональд Дж. (2018). Вводная химия: основа . Cengage Обучение. ISBN 978-1-337-67132-3 .
- ^ Венгренович, Р.Д. (1982). «О теории созревания Оствальда». Акта Металлургика . 30 (6): 1079–1086. дои : 10.1016/0001-6160(82)90004-9 . ISSN 0001-6160 .
- ^ Вурхис, PW (1985). «Теория созревания Оствальда». Журнал статистической физики . 38 (1–2): 231–252. Бибкод : 1985JSP....38..231В . дои : 10.1007/BF01017860 . ISSN 0022-4715 . S2CID 14865117 .
- ^ А.Д. Адлер; Ф. Р. Лонго; Дж. Д. Финарелли; Дж. Гольдмахер; Дж. Ассур; Л. Корсаков (1967). «Упрощенный синтез мезо-тетрафенилпорфина». Дж. Орг. хим. 32 (2): 476. doi : 10.1021/jo01288a053 .
- ^ Алан Д. Адлер; Фредерик Р. Лонго; Фрэнк Кампас; Джин Ким (1970). «О получении металлопорфиринов». Журнал неорганической и ядерной химии . 32 (7): 2443. doi : 10.1016/0022-1902(70)80535-8 .
- ^ Дюпон Дж., Консорти К., Суарес П., де Соуза Р. (2004). «Приготовление ионных жидкостей комнатной температуры на основе 1-бутил-3-метилимидазолия» . Органические синтезы
{{cite journal}}: CS1 maint: multiple names: authors list (link); Сборник томов , т. 10, с. 184 . - ^ Дхара, С. (2007). «Формирование, динамика и характеристика наноструктур при ионном облучении». Критические обзоры по наукам о твердом теле и материалах . 32 (1): 1–50. Бибкод : 2007CRSSM..32....1D . дои : 10.1080/10408430601187624 . S2CID 98639891 .
Дальнейшее чтение [ править ]
- Зумдал, Стивен С. (2005). Химические принципы (5-е изд.). Нью-Йорк: Хоутон Миффлин. ISBN 0-618-37206-7 .