Гидрид калия
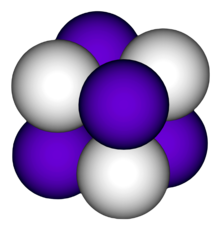 катион калия, К + анион водорода, ЧАС − | |
| Имена | |
|---|---|
| Название ИЮПАК Гидрид калия | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.028.823 |
| Номер ЕС |
|
ПабХим CID | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| КХ | |
| Молярная масса | 40.1062 g/mol |
| Появление | кристаллический порошок от белого до серого цвета |
| Плотность | 1,43 г/см 3 [1] |
| Температура плавления | разлагается при ~ 400 ° C [2] |
| реагирует | |
| Растворимость | нерастворим в бензоле , диэтиловом эфире , сероуглероде. |
| Структура | |
| кубический , cF8 | |
| Фм 3 м, №225 | |
| Термохимия | |
Теплоемкость ( С ) | 37,91 Дж/(моль⋅К) |
Стандартная энтальпия образование (Δ f H ⦵ 298 ) | -57,82 кДж/моль |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности | коррозионный, пирофорный , бурно реагирует с кислотами и водой. |
| NFPA 704 (огненный алмаз) | |
| Родственные соединения | |
Другие катионы | Гидрид лития Гидрид натрия Гидрид рубидия Гидрид цезия |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Гидрид калия , KH, представляет собой соединение калия . и водорода неорганическое Это гидрид щелочного металла . Это белое твердое вещество, хотя коммерческие образцы кажутся серыми. Это мощное супероснование , полезное в органическом синтезе . Он продается на коммерческой основе в виде суспензии (~35%) в минеральном масле или иногда в парафине для облегчения дозирования. [3]
Подготовка
[ редактировать ]Гидрид калия получают прямым соединением металла и водорода при температуре от 200 до 350 °C:
- 2 К + Ч 2 → 2 КХ
Эта реакция была открыта Хамфри Дэви вскоре после открытия калия в 1807 году, когда он заметил, что металл испаряется в токе водорода при нагревании чуть ниже точки кипения. [4] : стр. 25
Гидрид калия растворим в конденсированных гидроксидах (таких как расплавленный гидроксид натрия ) и смесях солей, но не в органических растворителях. [5]
Реакции
[ редактировать ]КН реагирует с водой по реакции:
- КН + Н 2 О → КОН + Н 2
Как супероснование гидрид калия является более основным, чем гидрид натрия . Он используется для депротонирования некоторых карбонильных соединений с образованием енолятов . Он также депротонирует амины с образованием соответствующих амидов типа KNHR и КНР 2 . [6]
Безопасность
[ редактировать ]KH может быть пирофорным на воздухе, бурно реагировать с кислотами и воспламеняться при контакте с окислителями. В виде суспензии в минеральном масле КН менее опасен.
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Роберт Э. Гоули, Сяоцзе Чжан, Цюньчжао Ван, Энциклопедия реагентов для органического синтеза «Гидрид калия», 2007 John Wiley & Sons. дои : 10.1002/047084289X.rp223.pub2
- ^ Дэвид Артур Джонсон; Открытый университет (12 августа 2002 г.). Металлы и химические изменения . Королевское химическое общество. стр. 167–. ISBN 978-0-85404-665-2 . Проверено 1 ноября 2011 г.
- ^ Дуглас Ф. Табер, Кристофер Г. Нельсон (2006). «Гидрид калия в парафине: полезная основа для органического синтеза» . Дж. Орг. Хим . 71 (23): 8973–8974. дои : 10.1021/jo061420v . ПМЦ 3248818 . ПМИД 17081034 .
- ^ Хамфри Дэви (1808), Бейкеровская лекция о некоторых новых явлениях химических изменений, вызываемых электричеством, особенно о разложении фиксированных щелочей, и обнаружении новых веществ, составляющих их основы; и об общей природе щелочных тел. Философские труды Королевского общества, том 88, страницы 1–44. В книге «Развитие химии, 1789–1914: Избранные эссе » под редакцией Д. Найта, стр. 17–47.
- ^ Прадьот Патнаик (1 июля 2007 г.). Комплексное руководство по опасным свойствам химических веществ . Джон Уайли и сыновья. стр. 631–. ISBN 978-0-470-13494-8 . Проверено 1 ноября 2011 г.
- ^ Чарльз А. Браун, Прабхакав К. Джадхав (1925). «(-)-α-пинен путем изомеризации (-)-β-пинена» . Органические синтезы . 65 :224 ; Сборник томов , т. 8, с. 553 .
