Бораны

Боран – это соединение формулы B x H y или родственный анион. Известно много таких боранов. Наиболее распространены те, которые содержат от 1 до 12 атомов бора . Хотя у них мало практического применения, бораны обладают структурой и связями, которые сильно отличаются от структур, наблюдаемых в углеводородах. Гибриды боранов и углеводородов, карбораны, также хорошо развиты. [1]
История [ править ]
Развитие химии боранов привело к инновациям в методах синтеза, а также в структуре и связях. Во-первых, потребовались новые методы синтеза для работы с дибораном и многими его производными, которые являются пирофорными и летучими. Для этой цели Альфред Сток изобрел вакуумную линию для стекла. [2]
Структура диборана была правильно предсказана в 1943 году, спустя много лет после его открытия. [3] Структуры кластеров гидрида бора были установлены начиная с 1948 г., когда были охарактеризованы декабораны . Уильям Липскомб был удостоен Нобелевской премии по химии в 1976 году За это и многие последующие кристаллографические исследования . Эти исследования выявили преобладание дельтаэдрических структур, т. е. сетей треугольных массивов центров ЧД.
Соединение кластеров положило начало теории многогранных скелетных электронных пар и правилам Уэйда, которые можно использовать для предсказания структуры боранов. [4] Было обнаружено, что эти правила описывают структуры многих кластерных соединений.
Интерес к боранам возрос во время Второй мировой войны из-за потенциала борогидрида урана для обогащения изотопов урана и в качестве источника водорода для надувания метеозондов. В США группа под руководством Шлезингера разработала основы химического состава анионных гидридов бора и родственных гидридов алюминия. Работа Шлезингера заложила основу для множества боргидридных реагентов для органического синтеза , большая часть которых была разработана его учеником Гербертом К. Брауном . Реагенты на основе борана в настоящее время широко используются в органическом синтезе. Браун был удостоен Нобелевской премии по химии в 1979 году. За эту работу [5]
и соглашения именах об Химическая формула
Кластеры борана классифицируются следующим образом, где n — количество атомов бора в одном кластере: [1] [6] [7]
| Тип кластера | Химическая формула | Пример | Примечания |
|---|---|---|---|
| гиперклозо - | Б н Ч н | Нестабильный; производные известны [8] | |
| близко - | [Б н Ч н ] 2− | Додекаборат цезия | |
| нидо - | Б н Ч н +4 | пентаборан(9) | |
| arachnoарахно- | Б н Ч н +6 | пентаборан(11) | |
| гиф - | Б н Ч н +8 | Встречается только в аддуктах |
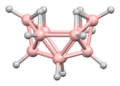
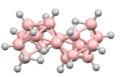
Международного союза теоретической и прикладной химии Правила систематического наименования основаны на префиксе, обозначающем класс соединения, за которым следует количество атомов бора и, наконец, количество атомов водорода в скобках. Различные детали можно опустить, если нет двусмысленности в значении, например, если возможен только один структурный тип. Некоторые примеры структур показаны ниже.
- изо- Б 18 Ч 22
- Гексаборат(6)
[Б 6 Ч 6 ] 2− - Гептаборат(7)
[Б 7 Ч 7 ] 2− - Октаборат(8)
[Б 8 Ч 8 ] 2− - Неборат(9)
[Б 9 Ч 9 ] 2− - Декаборат(10)
[Б 10 Ч 10 ] 2− - Недекаборатный(11)
[Б 11 Ч 11 ] 2−
Названия анионов иллюстрируются
- октагидридопентаборат, [Б 5 Ч 8 ] −
Сначала указывается количество водорода, а затем количество бора. Суффикс -ate применяется к анионам . Значение ионного заряда включено в химическую формулу, но не является частью систематического названия.
Связь в боранах [ править ]
Бораны представляют собой соединения с неклассической связью, то есть электронов недостаточно для образования 2-центровых 2-электронных связей между всеми парами соседних атомов в молекуле. Описание связи в более крупных боранах было сформулировано Уильямом Липскомбом . Это включало:
- 3-центровые 2-электронные водородные мостики BHB
- 3-центровые 2-электронные связи BBB
- 2-центровые 2-электронные связи (в BB, BH и ЧД 2 )
Методология Липскомба в значительной степени была заменена молекулярно-орбитальным подходом. Это позволяет расширить концепцию многоцентрового соединения. Например, в икосаэдрическом ионе [Б 12 Ч 12 ] 2− , полностью симметричная (симметрия A g ) молекулярная орбиталь равномерно распределена между всеми 12 атомами бора. Правила Уэйда представляют собой мощный метод, который можно использовать для рационализации структур с точки зрения количества атомов и связей между ними.
Мультикластерные бораны [ править ]

Хотя относительно редко, было охарактеризовано несколько мультикластерных боранов. Например, реакция боранового кластера с B 2 H 6 (как источник BH 3 ) может привести к образованию конъюнкто -борановой разновидности, в которой субъединицы боранового кластера соединены общими атомами бора. [10]
- Б 6 Ч 10 + «ВН 3 » → Б 7 Ч 11 + Ч 2
- Б 7 Ч 11 + Б 6 Ч 10 → Б 13 Ч 19 + Ч 2
Другие конъюнкто -бораны, субъединицы которых соединены связью BB, могут быть получены ультрафиолетовым облучением нидо -боранов. Некоторые BB-связанные конъюнкто -бораны можно получить с использованием PtBr 2 в качестве катализатора. [11]
Аналогично правилам Уэйда, схема подсчета электронов была разработана для предсказания или рационализации мультикластерных боранов.
| Префикс | Значение | Пример |
|---|---|---|
| клада - | разветвленные кластеры | |
| комбинированный - | соединенные кластеры | |
| мегало - | несколько объединенных кластеров |
Реакционная способность боранов [ править ]
Самый низший боран, BH 3 существует лишь временно, мгновенно димеризуясь с образованием диборана. Б 2 Ч 6 . Его аддукты BH 3 · ТГФ и BH 3 · ДМСО достаточно стабильны, чтобы их можно было использовать в реакциях гидроборирования . Напоминая поведение диборана, некоторые низшие бораны реагируют с воздухом весьма экзотермически, даже взрывчато. Напротив, многие клозо -борановые кластеры, такие как [Б 12 Ч 12 ] 2− , не вступает в реакцию с воздухом.
Кластеры гидрида бора настолько разнообразны, что обобщения об их реакциях невозможны.
-основное Кислотно поведение Льюиса
Некоторые функционируют как доноры электронов из-за относительного основного характера B-H Концевые группы . Бораны могут выступать в качестве лигандов в координационных соединениях . [13] Гаптичности η 1 до η 6 Были обнаружены донорство электронов с участием мостиковых атомов H или донорство со стороны связей BB. Например, нидо- B 6 H 10 может заменять этен в соли Цейзе с образованием транс -Pt(η 2 -B 6 H 10 )Cl 2 . [13]
Они также могут действовать как кислоты Льюиса с одновременным раскрытием кластера. Пример с триметилфосфином :
- B 5 H 9 + 2 P(CH 3 ) 3 → B 5 H 9 ·2P(CH 3 ) 3
Кислотно-основное Брёнстеду поведение по
Некоторые высшие бораны, особенно с мостиковыми атомами водорода, можно депротонировать сильным основанием. Пример:
- B 5 H 9 + NaH → Na[B 5 H 8 ] + H 2
Кислотность увеличивается с увеличением размера борана, при этом B 10 H 14, имеющий p K значение 2,7. [14] [15]
Структурные реакции [ править ]

Для химика, специализирующегося на гидриде бора, одной из наиболее важных реакций является процесс образования, при котором меньшие кластеры гидрида бора присоединяют боран, образуя более крупные кластеры. Этот подход применим и к синтезу металлоборанов .
Гидроборация [ править ]
Напоминая поведение диборана и его аддуктов, высшие бораны участвуют в гидроборировании. Когда гидриды бора добавляют алкин , углерод включается в кластер, образуя карбораны , например С 2 В 10 Ч 12 . [17]
Приложения [ править ]
Полезными реагентами являются диборан и его мономерные аддукты боран-тетрагидрофуран или боран-диметилсульфид . Их часто используют для гидроборирования в органическом синтезе . Некоторые кобальтовые производные карборанов были коммерциализированы для секвестрации. 137 Cs из радиоактивных отходов . [18]
Бораны имеют более высокую удельную энергию сгорания по сравнению с углеводородами , что делает их потенциально привлекательными в качестве топлива или воспламенителей. В 1950-х годах были проведены интенсивные исследования их использования в качестве присадок к реактивному топливу , но эти усилия не привели к практическим результатам.
Целевое использование [ править ]
Потому что 10 B имеет очень высокое сечение захвата нейтронов , производные гидрида бора часто исследовались на предмет применения в нейтронно-захватной терапии рака . [19]
- 10 Б+ 1 п → ( 11 Б*) → 4 Он + 7 Li + γ (2,4 Мэв)
См. также [ править ]
- Категория: Бораны , содержащие все конкретные изделия из соединений борана.
- Сара Риетти , химик-ядерщик из Аргентины
Ссылки [ править ]
- ^ Jump up to: Перейти обратно: а б Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 . стр. 151-195
- ^ Сток, Альфред (1933). Гидриды бора и кремния . Нью-Йорк: Издательство Корнельского университета.
- ^ Лонге-Хиггинс, ХК ; Белл, Р.П. (1943). «64. Строение гидридов бора». Журнал Химического общества (возобновленное) . 1943 : 250–255. дои : 10.1039/JR9430000250 .
- ^ Фокс, Марк А.; Уэйд, Кен (2003). «Развивающиеся закономерности в химии кластеров бора» (PDF) . Чистое приложение. хим. 75 (9): 1315–1323. дои : 10.1351/pac200375091315 . S2CID 98202127 .
- ^ Браун, HC Органический синтез через бораны John Wiley & Sons, Inc. Нью-Йорк: 1975. ISBN 0-471-11280-1 .
- ^ Коттон, Ф. Альберт ; Уилкинсон, Джеффри ; Мурильо, Карлос А.; Бохманн, Манфред (1999), Передовая неорганическая химия (6-е изд.), Нью-Йорк: Wiley-Interscience, ISBN 0-471-19957-5
- ^ Липскомб В. Н. Гидриды бора . Бенджамин, Нью-Йорк (1963).
- ^ Пейманн, Торальф; Ноблер, Кэролайн Б.; Хан, Саид И.; Хоторн, М. Фредерик (2001). «Додека(бензилокси)додекаборан, B 12 (OCH 2 Ph) 12 : стабильное производное гиперклозо - B 12 H 12 ». Энджью. хим. Межд. Эд. 40 (9): 1664–1667. doi : 10.1002/1521-3773(20010504)40:9<1664::AID-ANIE16640>3.0.CO;2-O . ПМИД 11353472 .
- ^ Лондсборо, Майкл Г.С.; Боулд, Джонатан; Баше, Томаш; Гник, Драгомир; Бакарджиев, Марио; Голуб, Йозеф; Цисаржова, Ивана; Кеннеди, Джон Д. (2010). «Экспериментальное решение вопроса о «недостающих водородах», окружающем макрополиэдрический 19-вершинный моноанион гидрида бора [B19H22]-, упрощение его синтеза и его использование в качестве промежуточного продукта в первом примере превращения син-B18H22 в анти-B18H22-изомер Конверсия». Неорганическая химия . 49 (9): 4092–4098. дои : 10.1021/ic901976y . ПМИД 20349936 .
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 . п. 162
- ^ Снеддон, LG (2009). «Переходный металл способствует реакциям полиэдрических боранов и карборанов» . Чистая и прикладная химия . 59 (7): 837–846. дои : 10.1351/pac198759070837 . S2CID 55817512 .
- ^ Боулд, Джонатан; Клегг, Уильям; Тит, Саймон Дж.; Бартон, Лоуренс; Рат, Нигам П.; Торнтон-Петт, Марк; Кеннеди, Джон Д. (1999). «Подход к мегалоборанам. Смешанные и множественные кластерные синтезы с участием кластерных соединений иридаборана и платинаборана. Определение кристаллической структуры традиционными и синхротронными методами». Неорганика Химика Акта . 289 (1–2): 95–124. дои : 10.1016/S0020-1693(99)00071-7 .
- ^ Jump up to: Перейти обратно: а б Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . п. 177, «Представление о боранах как лигандах». ISBN 978-0-08-037941-8 .
- ^ температура не указана
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 . п. 171
- ^ Канг, ХК; Ли, СС; Кноблер, CB; Хоторн, МФ (1991). «Синтез предшественников дикарболлидных лигандов с компенсацией заряда и их использование при получении новых металлакарборанов». Неорганическая химия . 30 (9): 2024–2031. дои : 10.1021/ic00009a015 .
- ^ Джеммис, ЭД (1982). «Контроль перекрытия и стабильность многогранных молекул. Клозо-карбораны». Журнал Американского химического общества . 104 (25): 7017–7020. дои : 10.1021/ja00389a021 .
- ^ Чаудхури, Санхита; Бхаттачарья, Арунасис; Госвами, Асок (2014). «Электроприводной селективный транспорт Cs + с использованием хлорированного дикарболлида кобальта в полимерной мембране включения: новый подход к удалению цезия из смоделированного раствора ядерных отходов». Экологические науки и технологии . 48 (21): 12994–13000. Бибкод : 2014EnST...4812994C . дои : 10.1021/es503667j . ПМИД 25299942 .
- ^ Зауэрвейн, Вольфганг; Виттиг, Андреа; Мосс, Раймонд; Накагава, Ёсинобу (2012). Нейтрон-захватная терапия . Берлин: Шпрингер. дои : 10.1007/978-3-642-31334-9 . ISBN 978-3-642-31333-2 .

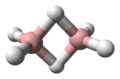



![Гексаборат(6) [B6H6]2-](http://upload.wikimedia.org/wikipedia/commons/thumb/9/9c/Hexaborate%286%29-dianion-from-xtal-3D-bs-17.png/105px-Hexaborate%286%29-dianion-from-xtal-3D-bs-17.png)
![Гептаборат(7) [B7H7]2-](http://upload.wikimedia.org/wikipedia/commons/thumb/0/01/Heptaborate%287%29-dianion-from-xtal-3D-bs-17.png/120px-Heptaborate%287%29-dianion-from-xtal-3D-bs-17.png)
![Октаборат(8) [B8H8]2-](http://upload.wikimedia.org/wikipedia/commons/thumb/3/33/Octaborate%288%29-dianion-from-xtal-3D-bs-17.png/120px-Octaborate%288%29-dianion-from-xtal-3D-bs-17.png)
![Нонаборат(9) [B9H9]2-](http://upload.wikimedia.org/wikipedia/commons/thumb/c/ca/Nonaborate%289%29-dianion-from-xtal-3D-bs-17.png/120px-Nonaborate%289%29-dianion-from-xtal-3D-bs-17.png)
![Декаборат(10) [B10H10]2-](http://upload.wikimedia.org/wikipedia/commons/thumb/e/e5/Decaborate%2810%29-dianion-from-xtal-3D-bs-17.png/95px-Decaborate%2810%29-dianion-from-xtal-3D-bs-17.png)
![Ундекаборат(11) [B11H11]2-](http://upload.wikimedia.org/wikipedia/commons/thumb/a/ab/Closo-undecaborate%2811%29-dianion-from-xtal-3D-bs-17.png/120px-Closo-undecaborate%2811%29-dianion-from-xtal-3D-bs-17.png)
![Додекаборат(12) [B12H12]2-](http://upload.wikimedia.org/wikipedia/commons/thumb/0/0e/Dodecaborate%2812%29-dianion-from-xtal-3D-bs-17.png/107px-Dodecaborate%2812%29-dianion-from-xtal-3D-bs-17.png)