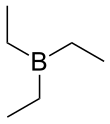
Триэтилборан
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК Триэтилборан | |||
| Другие имена Триэтилборин, триэтилбор | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.002.383 | ||
| Номер ЕС |
| ||
ПабХим CID | |||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| (СН 3 СН 2 ) 3 Б | |||
| Молярная масса | 98.00 g/mol | ||
| Появление | Бесцветная жидкость | ||
| Плотность | 0,677 г/см 3 | ||
| Температура плавления | -93 ° C (-135 ° F; 180 К) | ||
| Точка кипения | 95 ° C (203 ° F; 368 К) | ||
| Непригодный; высокореактивный | |||
| Опасности | |||
| Безопасность и гигиена труда (OHS/OSH): | |||
Основные опасности | Самовозгорается на воздухе; вызывает ожоги | ||
| СГС Маркировка : | |||
    | |||
| Опасность | |||
| Х225 , Х250 , Х301 , Х314 , Х330 , Х360 | |||
| P201 , P202 , P210 , P222 , P233 , P240 , P241 , P242 , P243 , P260 , P264 , P270 , P271 , P280 , P284 , P281 , P301+P310 , P301+P330+P331 , П302+П334 , П303+П361+ P353 , P304+P340 , P305+P351+P338 , P308+P313 , P310 , P320 , P321 , P330 , P363 , P370+P378 , P403+P233 , P403+P235 , P405 , P422 , P501 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | < -20 ° C (-4 ° F; 253 К) | ||
| -20 ° C (-4 ° F; 253 К) | |||
| Паспорт безопасности (SDS) | Внешний паспорт безопасности | ||
| Родственные соединения | |||
Родственные соединения | |||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Триэтилборан ( ТЭБ ), также называемый триэтилбором , представляет собой органоборан (соединение со связью B–C). Это бесцветная пирофорная жидкость. Его химическая формула (СН 3 СН 2 ) 3 В или (C 2 H 5 ) 3 B , сокращенно Эт 3 Б . Он растворим в органических растворителях: тетрагидрофуране и гексане .
Подготовка и структура
[ редактировать ]Триэтилборан получают реакцией триметилбората с триэтилалюминием : [1]
- Et 3 Al + (MeO) 3 B → Et 3 B + (MeO) 3 Al
Молекула мономерна, в отличие от H 3 B и Et 3 Al, склонных к димеризации. Он имеет планарное ядро BC 3 . [1]
Приложения
[ редактировать ]Турбореактивные двигатели
[ редактировать ]Триэтилборан использовался для воспламенения топлива JP-7 в двигателях Pratt & Whitney J58, турбореактивных / прямоточных установленных на Lockheed SR-71 Blackbird. [2] и его предшественник A-12 OXCART . Триэтилборан подходит, поскольку он легко воспламеняется при воздействии кислорода. Он был выбран в качестве способа воспламенения из соображений надежности, а в случае с «Блэкбердом» — потому, что топливо JP-7 имеет очень низкую летучесть и его трудно воспламенить. Обычные свечи зажигания представляли высокий риск неисправности. Триэтилборан использовался для запуска каждого двигателя и зажигания форсажных камер . [3]
Ракетная техника
[ редактировать ]Смешанный с 10–15% триэтилалюминия , он использовался перед стартом для зажигания двигателей F-1 на ракете Сатурн-5 . [4]
В двигателях Merlin, которыми оснащена ракета SpaceX Falcon 9, используется смесь триэтилалюминия и триэтилборана (TEA-TEB). в качестве воспламенителя первой и второй ступени [5]
Двигатели Reaver ракеты-носителя Firefly Aerospace Alpha также воспламеняются смесью триэтилалюминия и триэтилборана. [6]
Органическая химия
[ редактировать ]используется в качестве инициатора радикальных В промышленности триэтилборан реакций, где он эффективен даже при низких температурах. [1] В качестве инициатора он может заменить некоторые оловоорганические соединения.
Он реагирует с енолятами металлов , образуя энокситриэтилбораты, которые могут алкилироваться по α-углеродному атому кетона более селективно, чем в его отсутствие. Например, енолят от обработки циклогексанона гидридом калия дает 2-аллилциклогексанон с выходом 90% в присутствии триэтилборана. Без него смесь продуктов содержит 43% моноаллилированного продукта, 31% диаллилированных циклогексанонов и 28% непрореагировавшего исходного материала. [7] Выбор основания и температуры влияет на получение более или менее стабильного енолята, что позволяет контролировать положение заместителей. Начиная с 2- метилциклогексанона , реакция с гидридом калия и триэтилбораном в ТГФ при комнатной температуре приводит к более замещенному (и более стабильному) еноляту, тогда как реакция при -78 ° C с гексаметилдисилазидом калия , KN[Si(CH
3 )
3 ]
2 и триэтилборан образуют менее замещенный (и менее стабильный) енолят. После реакции с метилиодидом первая смесь дает 2,2-диметилциклогексанон с выходом 90%, а вторая дает 2,6-диметилциклогексанон с выходом 93%. [7] [8] Et означает этильную группу. СН 3 СН 2 - .

Он используется в реакции дезоксигенации Бартона-МакКомби для дезоксигенирования спиртов. В сочетании с три- трет -бутоксиалюмогидридом лития расщепляет простые эфиры. Например, ТГФ после гидролиза превращается в 1-бутанол . Он также способствует некоторым вариантам реакции Реформатского . [9]
Триэтилборан является предшественником восстановителей триэтилборгидрида лития (« Супергидрид ») и триэтилборгидрида натрия . [10]
- MH + Et 3 B → MBHEt 3 (M = Li, Na)
Триэтилборан реагирует с метанолом с образованием диэтил(метокси)борана, который используется в качестве хелатирующего агента при восстановлении Нарасака-Прасада для стереоселективного получения син -1,3- диолов из β-гидроксикетонов. [11] [12]
Безопасность
[ редактировать ]Триэтилборан сильно пирофорен , с температурой самовоспламенения -20 ° C (-4 ° F). [13] горит яблочно-зеленым пламенем, характерным для соединений бора. Таким образом, его обычно обрабатывают и хранят без использования воздуха . Триэтилборан также очень токсичен при проглатывании: смертельная доза 50 для подопытных крыс составляет 235 мг/кг. [14]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б с Браттон, Роберт Дж.; Вебер, К. Джозеф; Гвиберт, Кларенс Р.; Литтл, Джон Л. (15 июня 2000 г.). «Соединения бора». Энциклопедия промышленной химии Ульмана . Вайли-ВЧ. дои : 10.1002/14356007.a04_309 . ISBN 3-527-30673-0 .
- ^ «Локхид SR-71 Блэкберд» . Марч Филдский музей авиации. Архивировано из оригинала 4 марта 2000 г. Проверено 5 мая 2009 г.
- ^ «Руководство по летной эксплуатации Lockheed SR-71 Blackbird» . www.sr-71.org. Архивировано из оригинала 2 февраля 2011 г. Проверено 26 января 2011 г.
- ^ А. Янг (2008). Двигатель Saturn V F-1: вхождение Аполлона в историю . Спрингер. п. 86. ИСБН 978-0-387-09629-2 .
- ^ Центр статуса миссии, 2 июня 2010 г., 1905 г. по Гринвичу. Архивировано 30 мая 2010 г., в Wayback Machine , SpaceflightNow , по состоянию на 2 июня 2010 г., Цитата: «Фланцы соединят ракету с наземными резервуарами для хранения, содержащими жидкий кислород и керосин. топливо, гелий, газообразный азот и источник воспламенителя первой ступени, называемый триэтилалюминий-триэтилборан, более известный как TEA-TEB».
- ^ «https://twitter.com/Firefly_Space/status/1090319933534334977» . Твиттер . Проверено 5 февраля 2023 г.
{{cite web}}: Внешняя ссылка в|title= - ^ Jump up to: а б Крич, Дэвид, изд. (2008). «Энокситриэтилбораты и эноксидиэтилбораны» . Реагенты для радикальной и ион-радикальной химии . Справочник реагентов для органического синтеза. Том. 11. Джон Уайли и сыновья . ISBN 978-0-470-06536-5 . Архивировано из оригинала 19 февраля 2022 г. Проверено 27 января 2019 г.
- ^ Негиси, Эйичи ; Чаттерджи, Сугата (1983). «Высоко региоселективное получение «термодинамических» енолятов и их прямая характеристика с помощью ЯМР». Буквы тетраэдра . 24 (13): 1341–1344. дои : 10.1016/S0040-4039(00)81651-2 .
- ^ Ямамото, Ёсинори; Ёсимицу, Такэхико; Вуд, Джон Л .; Шехерер, Лаура Николь (15 марта 2007 г.). «Триэтилборан». Энциклопедия реагентов для органического синтеза . Уайли. дои : 10.1002/047084289X.rt219.pub3 . ISBN 978-0-471-93623-7 .
- ^ Бингер, П.; Кестер, Р. (1974). «Триэтилгидроборат натрия, тетраэтилборат натрия и триэтил-1-пропинилборат натрия». Неорганические синтезы . Неорганические синтезы . Том. 15. С. 136–141. дои : 10.1002/9780470132463.ch31 . ISBN 978-0-470-13246-3 .
- ^ Чен, Кау-Мин; Гундерсон, Карл Г.; Хардтманн, Гетц Э.; Прасад, Капа; Репич, Ольян; Шапиро, Майкл Дж. (1987). «Новый метод получения алкоксидиалкилборанов in situ и их использование для селективного получения 1,3- синдиолов » . Химические письма . 16 (10): 1923–1926. дои : 10.1246/кл.1987.1923 .
- ^ Ян, Джемун (2008). «Диастереоселективное син -восстановление β-гидроксикетонов» . Шестичленные переходные состояния в органическом синтезе . Джон Уайли и сыновья . стр. 151–155. ISBN 978-0-470-19904-6 . Архивировано из оригинала 19 февраля 2022 г. Проверено 27 января 2019 г.
- ^ «Топливо и химикаты – Температура самовоспламенения» . Архивировано из оригинала 4 мая 2015 г. Проверено 26 августа 2017 г.
- ^ «Архивная копия» . Архивировано из оригинала 19 февраля 2022 г. Проверено 26 сентября 2020 г.
{{cite web}}: CS1 maint: архивная копия в заголовке ( ссылка )