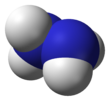
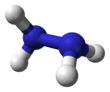
Гидразин
| |||
| |||
 Безводный гидразин | |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Гидразин [2] | |||
| Систематическое название ИЮПАК Диазан [2] | |||
| Другие имена | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| 3DMeet | |||
| 878137 | |||
| ЧЭБИ | |||
| ЧЕМБЛ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.005.560 | ||
| Номер ЕС |
| ||
| 190 | |||
| КЕГГ | |||
| МеШ | Гидразин | ||
ПабХим CID | |||
| номер РТЭКС |
| ||
| НЕКОТОРЫЙ | |||
| Число | 2029 | ||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| Н 2 Ч 4 | |||
| Молярная масса | 32.0452 g/mol | ||
| Появление | Бесцветная, дымящая, маслянистая жидкость [3] | ||
| Запах | Аммиак -подобный [3] | ||
| Плотность | 1,021 г/см 3 | ||
| Температура плавления | 2 °С; 35 °Ф; 275 К | ||
| Точка кипения | 114 °С; 237 °Ф; 387 К | ||
| смешивается [3] | |||
| войти P | 0.67 | ||
| Давление пара | 1 кПа (при 30,7 °C) | ||
| Кислотность ( pKa ) | 8.10 ( [Н 2 Ч 5 ] + ) [4] | ||
| Основность (p K b ) | 5.90 | ||
| Конъюгатная кислота | Гидразиний | ||
Показатель преломления ( n D ) | 1,46044 (при 22 °С) | ||
| Вязкость | 0,876 сП | ||
| Структура | |||
| Треугольная пирамида на N | |||
| 1,85 Д [5] | |||
| Термохимия | |||
Стандартный моляр энтропия ( S ⦵ 298 ) | 121,52 Дж/(К·моль) | ||
Стандартная энтальпия образование (Δ f H ⦵ 298 ) | 50,63 кДж/моль | ||
| Опасности | |||
| СГС Маркировка : | |||
     | |||
| Опасность | |||
| Х226 , Х301 , Х311 , Х314 , Х317 , Х331 , Х350 , Х410 | |||
| П201 , П261 , П273 , П280 , П301+П310 , П305+П351+П338 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 52 ° С (126 ° F; 325 К) | ||
| От 24 до 270 ° C (от 75 до 518 ° F; от 297 до 543 К) | |||
| Взрывоопасные пределы | 1.8–100% | ||
| Летальная доза или концентрация (LD, LC): | |||
ЛД 50 ( средняя доза ) | 59–60 мг/кг (перорально крысам, мышам) [6] | ||
ЛК 50 ( средняя концентрация ) | 260 частей на миллион (крыса, 4 часа ) 630 частей на миллион (крыса, 1 час) 570 частей на миллион (крыса, 4 ч) 252 ppm (мышь, 4 ч) [7] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
МЕХ (Допускается) | TWA 1 ppm (1,3 мг/м 3 ) [кожа] [3] | ||
РЕЛ (рекомендуется) | Ca C 0,03 ppm (0,04 мг/м 3 ) [2 часа] [3] | ||
IDLH (Непосредственная опасность) | Са [50 частей на миллион] [3] | ||
| Паспорт безопасности (SDS) | КМГС 0281 | ||
| Родственные соединения | |||
Другие анионы | Тетрафторгидразин Перекись водорода дифосфан Дифосфор тетрайодид | ||
Другие катионы | Органические гидразины | ||
Связанные бинарные азаны | Аммиак Триазан | ||
Родственные соединения | Диазен Триазен Тетразен Дифосфен | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Гидразин — неорганическое соединение с химической формулой Н 2 Ч 4 . Это простой гидрид пниктогена , бесцветная легковоспламеняющаяся жидкость с запахом аммиака . Гидразин очень опасен, если с ним не обращаться в растворе, например, с гидразингидратом ( Н 2 ЧАС 4 · Икс ЧАС 2 О ).
Гидразин в основном используется в качестве пенообразователя при приготовлении полимерных пен , но его применение также включает его использование в качестве прекурсора фармацевтических , и агрохимических препаратов а также в качестве топлива длительного хранения для движения космических кораблей. Кроме того, гидразин используется в различных ракетных топливах и для приготовления прекурсоров газа, используемых в подушках безопасности . Гидразин используется в поглотителя паровых циклах как атомных, так и обычных электростанций в качестве кислорода для контроля концентрации растворенного кислорода с целью уменьшения коррозии. [8] По состоянию на 2000 год [update]Ежегодно во всем мире производится около 120 000 тонн гидразингидрата (что соответствует 64% раствору гидразина в воде по весу). [9]
Гидразины — класс органических веществ, полученных путем замены одного или нескольких атомов водорода в гидразине органической группой. [9]
Этимология
[ редактировать ]Номенклатура представляет собой двухвалентную форму с префиксом гид-, используемым для обозначения присутствия атомов водорода , и суффиксом, начинающимся с -аз- , от azote , французского слова, обозначающего азот .
Приложения
[ редактировать ]Производители газа и топлива
[ редактировать ]Наибольшее применение гидразин имеет в качестве предшественника пенообразователей . Конкретные соединения включают азодикарбонамид и азобисизобутиронитрил , которые выделяют 100–200 мл газа на грамм прекурсора. В аналогичном применении азид натрия , газообразующий агент в воздушных подушках , получают из гидразина реакцией с нитритом натрия . [9]
длительного Гидразин также используется в качестве топлива хранения на борту космических аппаратов, таких как миссия Dawn на Церере и Весте, а также для снижения концентрации растворенного кислорода и контроля pH воды, используемой в крупных промышленных котлах. Истребитель F-16 Еврофайтер Тайфун . [10] Спейс шаттл и самолет-разведчик U-2 используют гидразин для заправки своей системы аварийного запуска в случае остановки двигателя. [11]
Прекурсор пестицидов и фармацевтических препаратов
[ редактировать ]
Гидразин является предшественником ряда фармацевтических препаратов и пестицидов. Часто эти применения включают преобразование гидразина в гетероциклические кольца, такие как пиразолы и пиридазины . Примеры коммерческих биоактивных производных гидразина включают цефазолин , ризатриптан , анастрозол , флуконазол , метазахлор, метамитрон, метрибузин , паклобутразол , диклобутразол, пропиконазол , гидразинсульфат , [12] диимид , триадимефон , [9] и дибензоилгидразин .
Соединения гидразина могут быть эффективными в качестве активных ингредиентов инсектицидов, митицидов, нематицидов , фунгицидов, противовирусных средств, аттрактантов, гербицидов или регуляторов роста растений. [13]
Мелкомасштабные, нишевые и исследовательские
[ редактировать ]Итальянский производитель катализаторов Acta (химическая компания) предложил использовать гидразин в качестве альтернативы водороду в топливных элементах . Основное преимущество использования гидразина заключается в том, что он может производить более 200 мВт / см. 2 больше, чем аналогичный водородный элемент, не требуя (дорогих) платиновых катализаторов. [14] Поскольку топливо является жидким при комнатной температуре, с ним легче обращаться и хранить, чем с водородом. При хранении гидразина в баке, наполненном карбонилом с двойной связью углерод кислород , - топливо вступает в реакцию и образует безопасное твердое вещество, называемое гидразоном . При последующей промывке резервуара теплой водой выделяется жидкий гидразингидрат. Гидразин имеет более высокую электродвижущую силу - 1,56 В по сравнению с 1,23 В у водорода. Гидразин распадается в клетке с образованием азота и водорода , которые связываются с кислородом, выделяя воду. [14] Гидразин использовался в топливных элементах, производимых Allis-Chalmers Corp. , в том числе в тех, которые обеспечивали электроэнергией космические спутники в 1960-х годах.
Смесь, состоящая из 63% гидразина, 32% нитрата гидразина и 5% воды, является стандартным порохом для экспериментальной жидкостной артиллерии с объемным заряжанием . Вышеуказанная пороховая смесь является одной из наиболее предсказуемых и стабильных, с пологим профилем давления при выстреле. Причиной пропусков зажигания обычно является неправильное зажигание. Движение оболочки после неправильного воспламенения приводит к образованию большого пузыря с большей площадью поверхности воспламенения, а большая скорость выделения газа вызывает очень высокое давление, иногда приводящее к катастрофическим отказам трубок (т. е. взрывам). [15] С января по июнь 1991 года Исследовательская лаборатория армии США провела анализ первых программ жидкостных пороховых орудий с объемной загрузкой на предмет их возможного соответствия программе электротермических химических двигателей. [15]
ВВС США (ВВС США) регулярно используют H-70, смесь 70% гидразина и 30% воды, в операциях с использованием General Dynamics F-16 «Fighting Falcon» истребителей Lockheed U-2 «Dragon Lady». и самолетов-разведчиков . Однореактивный двигатель F-16 использует гидразин для питания своей аварийной силовой установки (ЭПУ), которая обеспечивает аварийную электрическую и гидравлическую мощность в случае загорания двигателя. EPU активируется автоматически или вручную под управлением пилота в случае потери гидравлического давления или электроэнергии для обеспечения аварийного управления полетом. В однореактивном двигателе У-2 для питания системы аварийного запуска (ESS) используется гидразин, который обеспечивает высоконадежный метод перезапуска двигателя в полете в случае сваливания. [16]
Ракетное топливо
[ редактировать ]
Гидразин впервые был использован в качестве компонента ракетного топлива во время Второй мировой войны . Смесь с содержанием 30% по весу, 57% метанола (называемого M-Stoff в немецких Люфтваффе называли C-Stoff . ) и 13% воды , немцы [17] Смесь использовалась для питания истребителя Messerschmitt Me 163B с ракетным двигателем, в котором немецкий высокопрочный перекись T-Stoff в качестве окислителя использовался называли B-Stoff . Несмешанный гидразин немцы , это обозначение также использовалось позже для топлива из этанола и воды для ракет Фау-2 . [18]
Гидразин используется в качестве монотоплива малой мощности для маневрирующих (RCS/система управления реакцией) двигателей космических кораблей, а также для питания космического корабля "Шаттл вспомогательных силовых установок (ВСУ) ". Кроме того, при конечном спуске космических кораблей часто используются монотопливные ракетные двигатели на гидразиновом топливе. Такие двигатели использовались на спускаемых модулях программы «Викинг» в 1970-х годах, а также на марсианских кораблях «Феникс» (май 2008 г.), «Кьюриосити» (август 2012 г.) и «Настойчивость» (февраль 2021 г.).
Смесь гидразина и красной дымящей азотной кислоты ( HNO 3 + N 2 H 4 ) использовался в качестве жидкого ракетного топлива во время советской космической программы стал известен как « дьявольский яд ». , где из-за своей крайне опасной природы [19]
Во всех гидразиновых монотопливных двигателях гидразин пропускают через катализатор, такой как металлический иридий с большой площадью поверхности , поддерживаемый оксидом алюминия (оксид алюминия), что вызывает его разложение на аммиак ( NH 3 ), газообразный азот ( N 2 ) и водород ( H 2 ) газ по трем следующим реакциям: [20]
- Реакция 1: Н 2 Ч 4 → Н 2 + 2 Ч 2
- Реакция 2: 3 Н 2 Н 4 → 4 NH 3 + Н 2
- Реакция 3: 4 НХ 3 + Н 2 Н 4 → 3 Н 2 + 8 Н 2
Первые две реакции чрезвычайно экзотермичны (температура в камере катализатора может достигать 800 °C за считанные миллисекунды). [21] ) и производят большие объемы горячего газа из небольшого объема жидкости, [22] что делает гидразин довольно эффективным топливом для двигателей с удельным импульсом в вакууме около 220 секунд. [23] Реакция 2 является наиболее экзотермической, но дает меньшее количество молекул, чем реакция 1. Реакция 3 является эндотермической и возвращает эффект реакции 2 к тому же эффекту, что и реакция 1 (более низкая температура, большее количество молекул). Структура катализатора влияет на долю NH 3 , диссоциирующий в реакции 3; более высокая температура желательна для ракетных двигателей, в то время как большее количество молекул желательно, когда реакции предназначены для производства большего количества газа. [24]
Поскольку гидразин является твердым веществом при температуре ниже 2 ° C, он не пригоден в качестве ракетного топлива общего назначения для военного применения. Другими вариантами гидразина , которые используются в качестве ракетного топлива, являются монометилгидразин , CH 3 NHNH 2 , также известный как MMH (температура плавления -52 °C), и несимметричный диметилгидразин , (CH 3 ) 2 NNH 2 , также известный как НДМГ (температура плавления -57 °C). Эти производные используются в двухкомпонентном ракетном топливе, часто вместе с четырехокисью азота . Н 2 О 4 . Смесь гидразина и НДМГ в соотношении 50:50 по массе использовалась в двигателе служебной двигательной установки командно-служебного модуля «Аполлон» , как взлетных, так и спускаемых двигателей лунного модуля «Аполлон» и «Титан II» межконтинентальных баллистических ракет и известна как Aerozine 50. . [17] Эти реакции чрезвычайно экзотермичны, горение также гиперголическое (горение начинается без всякого внешнего воспламенения). [25]
В художественной книге «Марсианин » (также адаптированной к художественному фильму ) главный герой использует иридиевый катализатор для отделения газообразного водорода от избыточного гидразинового топлива, которое он затем сжигает, чтобы получить воду для выживания.
В аэрокосмической отрасли продолжаются попытки найти замену гидразину, учитывая его потенциальный запрет на территории Европейского Союза. [26] [27] [28] Многообещающие альтернативы включают комбинации топлива на основе закиси азота , разработку которых ведут коммерческие компании Dawn Aerospace , Impulse Space , [29] и Лаунчер . [30] Первая система на основе закиси азота, когда-либо запущенная в космос, была осуществлена компанией D-Orbit на борту их спутникового носителя ION в 2021 году с использованием шести двигателей Dawn Aerospace B20. [31] [32]
Профессиональные вредности
[ редактировать ]Влияние на здоровье
[ редактировать ]Потенциальные пути воздействия гидразина включают кожный, глазной, ингаляционный и проглатывающий пути. [33]
Воздействие гидразина может вызвать раздражение кожи/контактный дерматит и жжение, раздражение глаз/носа/горла, тошноту/рвоту, одышку, отек легких, головную боль, головокружение, угнетение центральной нервной системы, летаргию, временную слепоту, судороги и кому. Воздействие также может вызвать повреждение органов печени, почек и центральной нервной системы. [33] [34] Гидразин задокументирован как сильный сенсибилизатор кожи с возможностью перекрестной сенсибилизации к производным гидразина после первоначального воздействия. [35] Помимо рассмотренных выше профессиональных применений, воздействие гидразина в небольших количествах также возможно из-за табачного дыма. [34]
Официальные рекомендации США по поводу гидразина как канцерогена неоднозначны, но в целом признается его потенциальное канцерогенное воздействие. Национальный институт безопасности и гигиены труда (NIOSH) относит его к «потенциальным профессиональным канцерогенам». Национальная программа токсикологии (NTP) пришла к выводу, что он «вполне ожидаемо является канцерогеном для человека». Американская конференция правительственных специалистов по промышленной гигиене (ACGIH) классифицирует гидразин как «А3 — подтвержденный канцероген для животных с неизвестным воздействием на человека». Агентство по охране окружающей среды США (EPA) оценивает его как «B2 — вероятный канцероген для человека, согласно данным исследований на животных». [36]
Международное агентство по изучению рака (IARC) оценивает гидразин как «2А — вероятно, канцерогенный для человека», при этом наблюдается положительная связь между воздействием гидразина и раком легких. [37] На основании когортных и перекрестных исследований профессионального воздействия гидразина комитет Национальной академии наук , инженерии и медицины пришел к выводу, что существуют убедительные доказательства связи между воздействием гидразина и раком легких, при этом доказательств связи с раком других заболеваний недостаточно. сайты. [38] комитет Европейской комиссии Научный по пределам профессионального воздействия (SCOEL) относит гидразин к канцерогенам «группы B — генотоксичным канцерогенам». Генотоксический механизм, который привел комитет, ссылается на реакцию гидразина с эндогенным формальдегидом и образование агента, метилирующего ДНК. [39]
В случае чрезвычайной ситуации, связанной с воздействием гидразина, NIOSH рекомендует немедленно снять загрязненную одежду, промыть кожу водой с мылом, а при попадании в глаза снять контактные линзы и промыть глаза водой в течение как минимум 15 минут. NIOSH также рекомендует всем, кто потенциально подвергается воздействию гидразина, как можно скорее обратиться за медицинской помощью. [33] Конкретных рекомендаций по лабораторным или медицинским визуализациям после заражения не существует, а медицинское обследование может зависеть от типа и тяжести симптомов. Всемирная организация здравоохранения (ВОЗ) рекомендует лечить потенциальное воздействие симптоматически, уделяя особое внимание возможному повреждению легких и печени. Прошлые случаи воздействия гидразина документально подтвердили успех лечения пиридоксином ( витамином B6 ). [35]
Пределы профессионального воздействия
[ редактировать ]- Рекомендуемый NIOSH предел воздействия (REL): 0,03 ppm (0,04 мг/м). 3 ) 2-часовой потолок [36]
- Допустимый предел воздействия OSHA (PEL): 1 ppm (1,3 мг/м). 3 ) Средневзвешенное по времени 8-часовое значение [36]
- ACGIH (TLV): 0,01 ppm (0,013 мг/м). Пороговое предельное значение 3 ) Средневзвешенное по времени 8-часовое значение [36]
Порог запаха гидразина составляет 3,7 частей на миллион, поэтому, если работник чувствует запах, напоминающий запах аммиака, то, скорее всего, он превысил предел воздействия. Однако этот порог запаха сильно варьируется и не должен использоваться для определения потенциально опасного воздействия. [40]
Для аэрокосмического персонала ВВС США используют руководство по аварийному воздействию, разработанное Комитетом по токсикологии Национальной академии наук , которое используется для нестандартного облучения населения и называется «Руководство по кратковременному аварийному воздействию на население» (англ. СПЕГЛ). SPEGL, который не применяется к профессиональному воздействию, определяется как приемлемая пиковая концентрация для непредсказуемого, единичного, кратковременного аварийного воздействия на население и представляет собой редкие воздействия в течение жизни работника. Для гидразина 1-часовой SPEGL составляет 2 ppm, а 24-часовой SPEGL - 0,08 ppm. [41]
Обращение и медицинское наблюдение
[ редактировать ]Полная программа наблюдения за гидразином должна включать систематический анализ биологического мониторинга, медицинский осмотр и информацию о заболеваемости/смертности. Центры по контролю и профилактике заболеваний рекомендуют предоставлять сводные данные наблюдения и проводить обучение для руководителей и работников. Предварительное и периодическое медицинское обследование должно проводиться с особым акцентом на потенциальное воздействие гидразина на функционирование глаз, кожи, печени, почек, кроветворной, нервной и дыхательной систем. [33]
Общие средства контроля, используемые для гидразина, включают технологическое помещение, местную вытяжную вентиляцию и средства индивидуальной защиты (СИЗ). [33] Рекомендации по использованию СИЗ, содержащих гидразин, включают непроницаемые перчатки и одежду, защитные очки с непрямой вентиляцией, защиту от брызг, защитную маску и, в некоторых случаях, респиратор. [40] Использование респираторов при работе с гидразином должно быть последним средством контроля воздействия на работников. В тех случаях, когда необходимы респираторы, OSHA . следует осуществить правильный выбор респираторов и полную программу защиты органов дыхания, соответствующую рекомендациям [33]
Для персонала ВВС США стандарт 48-8 по охране труда ВВС (AFOSH), Приложение 8, рассматривает соображения, касающиеся профессионального воздействия гидразина в ракетных, авиационных и космических системах. Конкретные рекомендации по реагированию на воздействие включают обязательный аварийный душ и станции для промывания глаз, а также процесс обеззараживания защитной одежды. Руководство также определяет обязанности и требования к надлежащим СИЗ, обучению сотрудников, медицинскому наблюдению и реагированию на чрезвычайные ситуации. [41] Базы ВВС США, требующие использования гидразина, обычно имеют специальные базовые правила, регулирующие местные требования по безопасному использованию гидразина и реагированию на чрезвычайные ситуации.
Молекулярная структура
[ редактировать ]Гидразин, H 2 N−NH 2 , содержит две аминогруппы. NH 2 соединен одинарной связью между двумя атомами азота. Каждый N-NH 2 Субъединица имеет пирамидальную форму. Структура свободных молекул установлена методами газовой электронной дифракции и микроволновой спектроскопии . Длина одинарной связи N–N 1,447(2) Å (144,7(2) пм ), расстояние NH 1,015(2) Å , углы NNH 106(2)° и 112(2)°, угол HNH составляет 107°. [42] Молекула принимает конформацию гош с торсионным углом 91(2)° (двугранный угол между плоскостями, содержащими связь NN, и биссектрисами углов HNH). Барьер вращения в два раза больше, чем у этана . Эти структурные свойства напоминают свойства газообразной перекиси водорода , которая принимает «перекошенную» антиклинальную конформацию, а также испытывает сильный вращательный барьер.
Строение твердого гидразина установлено методом рентгеновской дифракции. В этой фазе связь NN имеет длину 1,46 Å , а ближайшие несвязанные расстояния составляют 3,19, 3,25 и 3,30 Å . [43]
Синтез и производство
[ редактировать ]Были разработаны разнообразные синтетические пути получения гидразина. [9] Ключевым шагом является создание одинарной связи N –N. Многие пути можно разделить на те, в которых используются окислители хлора (и образуют соль), и те, в которых этого не происходит.
Окисление аммиака оксазиридинами из перекиси
[ редактировать ]Гидразин можно синтезировать из аммиака и перекиси водорода с помощью кетонового катализатора с помощью процедуры, называемой пероксидным процессом (иногда называемым процессом Печини-Юджина-Кульмана, циклом Атофина-PCUK или кетазиновым процессом). [9] Чистая реакция: [44]
- 2 NH 3 + H 2 O 2 → N 2 H 4 + 2 H 2 O
По этому пути кетон и аммиак сначала конденсируются с образованием имина , который окисляется перекисью водорода до оксазиридина , трехчленного кольца, содержащего углерод, кислород и азот. Затем оксазиридин дает гидразон при обработке аммиаком , в результате чего образуется одинарная связь азот-азот. Этот гидразон конденсируется с еще одним эквивалентом кетона.
Полученный азин гидролизуют с образованием гидразина и регенерируют кетон, метилэтилкетон :
В отличие от большинства других процессов, этот подход не приводит к образованию соли в качестве побочного продукта. [45]
Окисления на основе хлора
[ редактировать ]Процесс Олина Рашига , впервые анонсированный в 1907 году, производит гидразин из гипохлорита натрия (активного ингредиента многих отбеливателей ) и аммиака без использования кетонового катализатора. Этот метод основан на реакции монохлорамина с аммиаком с образованием N –N, одинарной связи а также побочного продукта хлористого водорода : [12]
- NH 2 Cl + NH 3 → N 2 H 4 + HCl
Что касается процесса Рашига, то мочевина вместо аммиака может окисляться . Окислителем снова служит гипохлорит натрия. Чистая реакция показана: [46]
- (NH 2 ) 2 CO + NaOCl + 2 NaOH → N 2 H 4 + H 2 O + NaCl + Na 2 CO 3
Этот процесс генерирует значительное количество побочных продуктов и в основном практикуется в Азии. [9]
является Кетазиновый процесс Байера предшественником пероксидного процесса. В качестве окислителя вместо перекиси водорода используется гипохлорит натрия. Как и все способы, основанные на гипохлорите, этот метод дает эквивалент соли на каждый эквивалент гидразина. [9]
Реакции
[ редактировать ]Кислотно-щелочное поведение
[ редактировать ]
Гидразин образует моногидрат N 2 H 4 ·H 2 O более плотный (1,032 г/см 3 ), чем безводная форма Н 2 Н 4 (1,021 г/см 3 ). Гидразин имеет основные ( щелочные ) химические свойства, сравнимые с аммиаком : [47]
- Н 2 Ч 4 + Ч 2 О → [Н 2 Ч 5 ] + + ОН − , К б = 1,3 × 10 −6 , п К б = 5,9
(для аммиака K b = 1,78 × 10 −5 )
Дипротонировать трудно: [48]
- [Н 2 Ч 5 ] + + Ч 2 О → [Н 2 Ч 6 ] 2+ + ОН − , К б = 8,4 × 10 −16 , п К б = 15
Воздействие чрезвычайно сильных оснований или щелочных металлов приводит к образованию депротонированных гидразидных солей. Большинство из них взрываются при воздействии воздуха или влаги. [49]
Окислительно-восстановительные реакции
[ редактировать ]В идеале при горении гидразина в кислороде образуются азот и вода:
- Н 2 Н 4 + О 2 → Н 2 + 2 Н 2 О
Избыток кислорода дает оксиды азота, в том числе оксид азота и диоксид азота :
- Н 2 Н 4 + 2 О 2 → 2 НО + 2 Н 2 О
- Н 2 Н 4 + 3 О 2 → 2 НО 2 + 2 Н 2 О
Теплота сгорания гидразина в кислороде (воздухе) составляет 19,41 МДж/кг (8345 БТЕ/фунт). [50]
Гидразин является удобным восстановителем, поскольку побочными продуктами обычно являются газообразный азот и вода. Это свойство делает его полезным в качестве антиоксиданта кислорода , поглотителя и ингибитора коррозии в водогрейных котлах и системах отопления. Он также напрямую восстанавливает до элемента соли менее активных металлов (например, висмута, мышьяка, меди, ртути, серебра, свинца, платины и палладия). [51] Это свойство имеет коммерческое применение в области химического никелирования и плутония извлечения из отходов ядерных реакторов . В некоторых процессах цветной фотографии также используется слабый раствор гидразина в качестве стабилизирующей промывки, поскольку он удаляет краситель и непрореагировавшие галогениды серебра. Гидразин является наиболее распространенным и эффективным восстановителем, используемым для преобразования оксида графена (GO) в восстановленный оксид графена (rGO) посредством гидротермальной обработки. [52]
Гидразиниевые соли
[ редактировать ]Гидразин можно протонировать с образованием различных твердых солей катиона . гидразиния [Н 2 Ч 5 ] + , путем обработки минеральными кислотами. Обычная соль — гидросульфат гидразиния . [Н 2 Ч 5 ] + [HSO 4 ] − . [53] Гидросульфат гидразиния исследовался как средство лечения кахексии , вызванной раком , но оказался неэффективным. [54]
Двойное протонирование дает дикатий гидразиния или гидразиндиий. [Н 2 Ч 6 ] 2+ , из которых известны различные соли. [55]
Органическая химия
[ редактировать ]Гидразины входят в состав многих органических синтезов , часто имеющих практическое значение в фармацевтике (см. раздел «Применение»), а также в текстильных красителях и в фотографии. [9]
Гидразин используется в восстановлении Вольфа-Кишнера , реакции, которая превращает карбонильную группу кетона в метиленовый мостик (или альдегид в метильную группу ) через промежуточное соединение гидразона . Производство высокостабильного динитрога из производного гидразина помогает стимулировать реакцию.
Будучи бифункциональным, содержащим два амина, гидразин является ключевым строительным блоком для получения многих гетероциклических соединений путем конденсации с рядом бифункциональных электрофилов . С 2,4-пентандионом он конденсируется с образованием 3,5-диметилпиразола . [56] В реакции Эйнхорна-Бруннера гидразины реагируют с имидами с образованием триазолов .
Будучи хорошим нуклеофилом, N 2 H 4 может атаковать сульфонилгалогениды и ацилгалогениды. [57] Тозилгидразин также образует гидразоны при обработке карбонилами.
Гидразин используется для расщепления N -алкилированных производных фталимида. Эта реакция разрыва позволяет использовать фталимид-анион в качестве предшественника амина в синтезе Габриэля . [58]
Образование гидразона
[ редактировать ]Показательной конденсацией гидразина с простым карбонилом является его реакция с ацетоном с образованием азина ацетона . Последний далее реагирует с гидразином с образованием гидразона ацетона : [59]
- 2 (CH 3 ) 2 CO + N 2 H 4 → 2 H 2 O + ((CH 3 ) 2 C=N) 2
- ((CH 3 ) 2 C=N) 2 + N 2 H 4 → 2 (CH 3 ) 2 C=NNH 2
Пропанон азин является промежуточным продуктом процесса Atofina-PCUK . Прямое алкилирование гидразинов алкилгалогенидами в присутствии основания дает алкилзамещенные гидразины, но реакция обычно неэффективна из-за плохого контроля уровня замещения (так же, как и в обычных аминах ). Восстановление гидразонов до гидразинов представляет собой чистый способ получения 1,1-диалкилированных гидразинов.
В родственной реакции 2-цианопиридины реагируют с гидразином с образованием амидгидразидов, которые можно превратить с помощью 1,2-дикетонов в триазины .
Биохимия
[ редактировать ]Гидразин является промежуточным продуктом процесса анаэробного окисления аммиака ( анаммокс ). [60] Его производят некоторые дрожжи и бактерия анаммокс открытого океана ( Brocadia anammoxydans ). [61]
Ложный сморчок производит яд гиромитрин , который представляет собой органическое производное гидразина, который превращается в монометилгидразин в результате метаболических процессов . Даже самый популярный съедобный гриб «пуговица» Agaricus bisporus производит органические производные гидразина, включая агаритин , гидразиновое производное аминокислоты, и гиромитрин . [62] [63]
История
[ редактировать ]Название «гидразин» было придумано Эмилем Фишером в 1875 году; он пытался получить органические соединения, состоящие из монозамещенного гидразина. [64] К 1887 году Теодор Куртиус получил сульфат гидразина путем обработки органических диазидов разбавленной серной кислотой; однако, несмотря на неоднократные попытки, ему не удалось получить чистый гидразин. [65] [66] [67] Чистый безводный гидразин был впервые получен голландским химиком Лобри де Брюйном в 1895 году. [68] [69] [70]
См. также
[ редактировать ]- Топливная смесь закиси азота - Класс жидкого ракетного топлива.
- США-193 - военный спутник США (2006–2008 гг.)
Ссылки
[ редактировать ]- ^ «Руководство НИОСХ — Гидразин» . Центры по контролю заболеваний . Проверено 16 августа 2012 г.
- ^ Перейти обратно: а б «гидразин — общедоступная химическая база данных PubChem» . Проект ПабХим . США: Национальный центр биотехнологической информации.
- ^ Перейти обратно: а б с д и ж Карманный справочник NIOSH по химическим опасностям. «#0329» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Холл Х.К. и др. (1957). «Корреляция основных сил аминов1». Дж. Ам. хим. Соц. 79 (20): 5441. doi : 10.1021/ja01577a030 .
- ^ Гринвуд Н.Н. , Эрншоу А. (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
- ^ Мартел Б., Кэссиди К. и др. (2004). Анализ химического риска: Практическое руководство . Амстердам: Баттерворт – Хайнеманн. п. 361. ИСБН 978-1-903996-65-2 . OCLC 939257974 .
- ^ «Гидразин» . Непосредственно опасные для жизни и здоровья концентрации (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Цубакизаки С., Такада М., Гото Х., Маватари К., Исихара Н., Кай Р. (2009). «Альтернативы гидразину при очистке воды на теплоэлектростанциях» (PDF) . Технический обзор Mitsubishi Heavy Industries . 6 (2): 43–47.
- ^ Перейти обратно: а б с д и ж г час я Ширманн Дж. П., Бурдодук П. (2001). «Гидразины». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a13_177 . ISBN 3-527-30673-0 .
- ^ «Краткий обзор разливов и пожаров, связанных с гиперголическим топливом НАСА и ВВС США» (PDF) . Космический центр Кеннеди .
- ^ Саггс Х.Дж., Лускус Л.Дж., Килиан Х.Дж., Мокри Дж.В. (1979). «Состав выхлопных газов аварийной энергоблока Ф-16» (технический отчет). ВВС США . ЗРК-ТР-79-2. Архивировано из оригинала 4 марта 2016 года . Проверено 23 января 2019 г.
- ^ Перейти обратно: а б Адамс Р., Браун Б.К. (1922). «Гидразинсульфат». Орг. Синтез. 2 : 37. дои : 10.15227/orgsyn.002.0037 . S2CID 221547391 .
- ^ Токи Т., Коянаги Т., Ёсида К., Ямамото К., Морита М. (1994). «Гидразиновые соединения, полезные в качестве пестицидов» (патент США). Ishihara Sangyo Kaisha Ltd (первоначальный правопреемник). US5304657A.
- ^ Перейти обратно: а б «Ликвидный актив» . Инженер . Компания «Кентавр Медиа». 15 января 2008 г. Проверено 23 января 2019 г.
- ^ Перейти обратно: а б Кнаптон Дж.Д., Стоби И.С., Элмор Л. (март 1993 г.). «Обзор программы создания жидкостных пороховых пушек с большой загрузкой на предмет возможного соответствия программе электротермических химических двигателей» (PDF) . Армейская исследовательская лаборатория. АДА263143 . Архивировано (PDF) из оригинала 7 марта 2020 г.
- ^ «Наземное обслуживание самолетов и статическое заземление» (PDF) . ВВС США (техническое руководство). 13 марта 2017 г. ТО 00-25-172 . Проверено 23 ноября 2018 г.
- ^ Перейти обратно: а б Кларк Джей Ди (23 мая 2018 г.). Зажигание!: Неофициальная история жидкого ракетного топлива . Издательство Университета Рутгерса. п. 302. ИСБН 978-0-8135-9918-2 .
- ^ Т.В. Прайс, Д.Д. Эванс. Технический отчет 32-7227 Статус технологии монотопливного гидразина (PDF) (Отчет). Национальное управление по аэронавтике и исследованию космического пространства (НАСА). п. 1 . Проверено 22 февраля 2022 г.
- ^ «Катастрофа Неделина, часть 1» . 28 октября 2014 г. Архивировано из оригинала 15 февраля 2022 г. Проверено 15 февраля 2022 г.
- ^ Хос Дж.Л., Харден Д.Г. (1965). «Термодинамические свойства гидразина». Журнал космических кораблей и ракет . 2 (6): 972–974. Бибкод : 1965JSpRo...2..972H . дои : 10.2514/3.28327 .
- ^ Виейра Р., Фам-Хуу С., Келлера Н., Ледукса М.Дж. (2002). «Новый композит углеродного нановолокна и графитового войлока для использования в качестве носителя катализатора каталитического разложения гидразина». хим. Комм. 44 (9): 954–955. дои : 10.1039/b202032g . ПМИД 12123065 .
- ^ Чен X, Чжан Т, Ся Л, Ли Т, Чжэн М, У Цз, Ван Х, Вэй Цз, Синь Ц, Ли С (апрель 2002 г.). «Каталитическое разложение гидразина на нанесенных катализаторах из нитрида молибдена в монотопливном двигателе». Письма о катализе . 79 : 21–25. дои : 10.1023/А:1015343922044 . S2CID 92094908 .
- ^ «Страница выхода из BIG-IP» . www.eso-io.com . Архивировано из оригинала 23 июня 2008 года . Проверено 20 мая 2020 г.
- ^ Валера-Медина А., Сяо Х., Оуэн-Джонс М., Дэвид В.И., Боуэн П.Дж. (01.11.2018). «Аммиак для власти» . Прогресс в области энергетики и науки о горении . 69 : 63–102. дои : 10.1016/j.pecs.2018.07.001 . ISSN 0360-1285 . S2CID 106214840 .
- ^ Митчелл MC, Ракофф Р.В., Джобе Т.О., Санчес Д.Л., Уилсон Б. (2007). «Термодинамический анализ уравнений состояния монотоплива гидразина». Журнал теплофизики и теплопередачи . 21 (1): 243–246. дои : 10.2514/1.22798 .
- ^ «Запрет на гидразин может стоить европейской космической промышленности миллиарды» . Космические новости . 25 октября 2017 г. Проверено 19 августа 2022 г.
- ^ «Международные исследовательские проекты | Министерство бизнеса, инноваций и занятости» . www.mbie.govt.nz. Проверено 19 августа 2022 г.
- ^ Урбан V (15 июля 2022 г.). «Dawn Aerospace предоставила ЕС 1,4 миллиона евро на экологически чистую двигательную технологию» . SpaceWatch.Global . Проверено 19 августа 2022 г.
- ^ Бергер Э (19 июля 2022 г.). «Две компании присоединяются к SpaceX в гонке на Марс, запуск которой возможен в 2024 году» . Арс Техника . Проверено 19 августа 2022 г.
- ^ «Ракета-носитель для создания орбитального транспортного средства» . Космические новости . 15 июня 2021 г. Проверено 19 августа 2022 г.
- ^ «Dawn Aerospace проверяет двигатели B20 в космосе – Bits&Chips» . Проверено 19 августа 2022 г.
- ^ «Двигатели Dawn B20 проверены в космосе» . Дон Аэроспейс . Проверено 19 августа 2022 г.
- ^ Перейти обратно: а б с д и ж «Руководство по охране труда и технике безопасности для гидразина — потенциального канцерогена для человека» (PDF) . НИОШ . 1988 год . Проверено 23 ноября 2018 г.
- ^ Перейти обратно: а б «Гидразин 302-01-2» (PDF) . Агентство по охране окружающей среды США . Проверено 23 ноября 2018 г.
- ^ Перейти обратно: а б «Международная программа по химической безопасности – Руководство по охране труда и технике безопасности № 56 – Гидразин» . МПКС ИНХЕМ . Женева: ВОЗ . 1991 год . Проверено 24 ноября 2018 г.
- ^ Перейти обратно: а б с д «База данных по профессиональной химии — гидразин» . www.osha.gov . ОША . Проверено 24 ноября 2018 г.
- ^ «Гидразин» (PDF) . МАИР . Июнь 2018 г. Архивировано из оригинала (PDF) 26 ноября 2020 г. . Проверено 23 ноября 2018 г.
- ^ Медицинский институт (2005). «Глава 9: Гидразины и азотная кислота». Война в Персидском заливе и здоровье: топливо, продукты сгорания и топливо . Том. 3. Вашингтон, округ Колумбия: Издательство национальных академий. п. 347. дои : 10.17226/11180 . ISBN 978-0-309-09527-3 . S2CID 228274601 .
- ^ «Рекомендации Научного комитета по пределам профессионального воздействия гидразина» (PDF) . Европейская комиссия . Август 2010 года . Проверено 23 ноября 2018 г.
- ^ Перейти обратно: а б «Информационный бюллетень об опасном веществе — гидразин» (PDF) . Департамент общественного здравоохранения штата Нью-Джерси . Ноябрь 2009 г. Проверено 23 ноября 2018 г.
- ^ Перейти обратно: а б «Стандарт ВВС по безопасности и гигиене труда (AFOSH) 48-8» (PDF) . ВВС США . 1 сентября 1997 года . Проверено 23 ноября 2018 г.
- ^ Кохата К., Фукуяма Т., Кучицу К. (март 1982 г.). «Молекулярная структура гидразина, изученная методом газовой электронографии». Журнал физической химии . 86 (5): 602–606. дои : 10.1021/j100394a005 . ISSN 0022-3654 .
- ^ Коллин Р.Л., Липскомб В.Н. (1 января 1951 г.). «Кристаллическая структура гидразина» . Акта Кристаллографика . 4 (1): 10–14. Бибкод : 1951AcCry...4...10C . дои : 10.1107/s0365110x51000027 . ISSN 0365-110X .
- ^ Матар С., Хэтч Л.Ф. (2001). Химия нефтехимических процессов (2-е изд.). Берлингтон: Gulf Professional Publishing. п. 148. ИСБН 978-1-4933-0346-5 . OCLC 990470096 – через Elsevier.
- ^ Ригель Э.Р., Кент Дж.А. (2003). «Гидразин» . Справочник Ригеля по промышленной химии (10-е изд.). Нью-Йорк: Springer Science & Business Media. п. 192. ИСБН 978-0-306-47411-8 . OCLC 55023601 .
- ^ «Гидразин: Информация о химическом продукте» . chemindustry.ru . Архивировано из оригинала 22 января 2018 года . Проверено 8 января 2007 г.
- ^ Справочник по химии и физике (83-е изд.). ЦРК Пресс. 2002.
- ^ Холлеман А.Ф., Виберг Э., Виберг Н. (2001). Неорганическая химия (1-е англ. изд.). Сан-Диего: Академическая пресса. ISBN 978-0-12-352651-9 . ОСЛК 813400418 .
- ^ Юджин Ф. Ротджери (2004), «Гидразин и его производные», Энциклопедия химической технологии Кирка-Отмера , Нью-Йорк: Джон Уайли, номер документа : 10.1002/0471238961.0825041819030809.a01.pub2 , ISBN 9780471238966
- ^ «Гидразин — Таблица свойств химической опасности» (PDF) . NOAA.gov . 1999.
- ^ Одриет Л.Ф., Кляйнберг Дж. (1953). Неводные растворители . Нью-Йорк: Джон Уайли и сыновья. п. 133. LCCN 52-12057 .
- ^ Станкович С., Дикин Д.А., Пинер Р.Д., Кольхаас К.А., Кляйнхаммес А., Цзя Ю., Ву Ю., Нгуен С.Т., Руофф Р.С. (2007). «Синтез нанолистов на основе графена путем химического восстановления расслоенного оксида графита». Карбон . 45 (7): 1558–1565. Бибкод : 2007Carbo..45.1558S . doi : 10.1016/j.carbon.2007.02.034 . S2CID 14548921 .
- ^ «ГИДРАЗИНСУЛЬФАТ» . опасность.com . Проверено 22 января 2019 г.
- ^ Ганьон Б., Брюэра Э. (май 1998 г.). «Обзор медикаментозного лечения кахексии, связанной с раком». Наркотики . 55 (5): 675–88. дои : 10.2165/00003495-199855050-00005 . ПМИД 9585863 . S2CID 22180434 .
- ^ «Диазандиий» . ЧарХем . Проверено 22 января 2019 г.
- ^ Уайли Р.Х., Хекснер П.Е. (1951). «3,5-Диметилпиразол». Орг. Синтез. 31 : 43. дои : 10.15227/orgsyn.031.0043 .
- ^ Фридман Л., Литтл Р.Л., Райхле В.Р. (1960). «п-толуолсульфонилгидразид». Орг. Синтез. 40 : 93. дои : 10.15227/orgsyn.040.0093 .
- ^ Вайншенкер Н.М., Шен С.М., Вонг Дж.Ю. (1977). «Полимерный карбодиимид. Получение». Орг. Синтез. 56 : 95. дои : 10.15227/orgsyn.056.0095 .
- ^ Дэй AC, Уайтинг MC (1970). «Ацетон гидразон». Органические синтезы . 50 :3. дои : 10.15227/orgsyn.050.0003 .
- ^ Страус М., Джеттен М.С. (2004). «Анаэробное окисление метана и аммония». Анну Рев Микробиол . 58 : 99–117. дои : 10.1146/annurev.micro.58.030603.123605 . hdl : 2066/60186 . ПМИД 15487931 .
- ^ Хандверк Б (9 ноября 2005 г.). «Бактерии питаются человеческими нечистотами и производят ракетное топливо» . Нэшнл Географик . Проверено 12 ноября 2007 г. - через Wild Singapore.
- ^ Хашида С., Хаяши К., Цзе Л., Хага С., Сакураи М., Симидзу Х. (1990). «[Количество агаритина в грибах ( Agaricus bisporus ) и канцерогенность метанольных экстрактов грибов на эпителии мочевого пузыря мыши]». Ниппон Косю Эйсэй Засси (на японском языке). 37 (6): 400–5. ПМИД 2132000 .
- ^ Зигер А.А., изд. (1 января 1998 г.). «Споровые отпечатки №338» . Бюллетень микологического общества Пьюджет-Саунд . Проверено 13 октября 2008 г.
- ^ Фишер Э (1875 г.). « Об ароматических гидразиновых соединениях». Бер. Немецкий. Хим. 8 : 589–594. дои : 10.1002/cber.187500801178 .
- ^ Курций Т. (1887). « О диамиде (гидразине)». Бер. Немецкий. Хим. Гес 20 : 1632–1634. дои : 10.1002/cber.188702001368 .
- ^ Куртиус Т., Джей Р. (1889). «Диазо- и азосоединения жирового ряда. IV. Трактат о гидразине» [Диазо- и азосоединения алканов. Четвертый трактат. О гидразине. В Эрдманне О.Л. (ред.). Журнал практической химии . Том 147. Издано Иоганном Амброзиусом Бартом. На стр. 129, Курциус признает: « Свободный диамид NH 2 -NH 2 еще не анализировался » . [Свободный гидразин еще не анализировался.]
- ^ Курциус Т., Шульц Х. (1890). « О гидразингидрате и галогенсодержащих соединениях диаммония » . Журнал практической химии . Том 150. С. 521–549.
- ^ Лобри де Брюин, Калифорния (1894 г.). «Sur l’Hydrazine (diamid) libre» [О свободном гидразине (диамиде)]. Рек. Трав. Хим. Платит-Бас . 13 (8): 433–440. дои : 10.1002/recl.18940130816 .
- ^ Лобри де Брюин, Калифорния (1895 г.). «Сур л'гидрат д'гидразина» [О гидрате гидразина]. Рек. Трав. Хим. Платит-Бас . 14 (3): 85–88. дои : 10.1002/recl.18950140302 .
- ^ Лобри де Брюин, Калифорния (1896 г.). «L’Hydrazine libre I» [Свободный гидразин, Часть 1]. Рек. Трав. Хим. Платит-Бас . 15 (6): 174–184. дои : 10.1002/recl.18960150606 .