Азид хлора
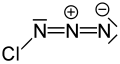 | |||
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Азид хлора | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
ПабХим CID | |||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| КлН 3 | |||
| Молярная масса | 77.4731 g/mol | ||
| Появление | Желто-оранжевая жидкость; бесцветный газ | ||
| Температура плавления | -100 ° C (-148 ° F; 173 К) | ||
| Точка кипения | −15 ° C (5 ° F; 258 К) | ||
| Растворимость | Растворимый [ нечеткий ] в бутане , пентане , бензоле , метаноле , этаноле , диэтиловом эфире , ацетоне , хлороформе , четыреххлористом углероде и сероуглероде ; мало растворим в воде | ||
| Структура | |||
| орторомбический | |||
| Кмк 2 1 , № 36 [1] | |||
| Взрывоопасные данные | |||
| Чувствительность к ударам | Экстрим | ||
| Чувствительность к трению | Экстрим | ||
| Опасности | |||
| Безопасность и гигиена труда (OHS/OSH): | |||
Основные опасности | Чрезвычайно чувствительное взрывчатое вещество | ||
| NFPA 704 (огненный алмаз) | |||
| Родственные соединения | |||
Родственные соединения | Гидрозойная кислота Азид фтора Азид брома Азид йода | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Азид хлора ( Cl N 3 ) — неорганическое соединение , открытое в 1908 году Фридрихом Рашигом . [2] Концентрированный ClN 3 крайне нестабилен и может самопроизвольно взорваться при любой температуре. [3]
Подготовка и обработка
[ редактировать ]Азид хлора получают пропусканием газообразного хлора над азидом серебра или добавлением уксусной кислоты к раствору гипохлорита натрия и азида натрия . [4]
Взрывоопасные характеристики
[ редактировать ]Азид хлора чрезвычайно чувствителен. Он может взорваться, иногда даже без видимой причины; таким образом, он слишком чувствителен, чтобы его можно было использовать в коммерческих целях, если его предварительно не разбавить в растворе. Азид хлора бурно реагирует с 1,3-бутадиеном , этаном , этином , метаном , пропаном , фосфором , азидом серебра и натрием . При контакте с кислотой азид хлора разлагается с выделением токсичного и едкого газообразного хлористого водорода . [5]
Нормативная информация
[ редактировать ]Его отгрузка подлежит строгим требованиям и правилам отчетности Министерства транспорта США .
Ссылки
[ редактировать ]- ^ Лихс, Бенджамин; Блязер, Дитер; Вёльпер, Кристоф; Шульц, Стефан; Янсен, Георг (2012). «Сравнение твердотельных структур галогеназидов XN 3 (X = Cl, Br, I)» . Международное издание «Прикладная химия» . 51 (51): 12859–12863. дои : 10.1002/anie.201206028 . ПМИД 23143850 .
- ^ Фриерсон, WJ; Браун, AW (1943). «Азид хлора. II. Взаимодействие азида хлора и азида серебра. Азинохлорид серебра, N 3 AgCl». Журнал Американского химического общества . 65 (9): 1698–1700. дои : 10.1021/ja01249a013 .
- ^ Фриерсон, WJ; Кронрад Дж.; Браун, AW (1943). «Азид хлора, ClN 3. I.». Журнал Американского химического общества . 65 (9): 1696–1698. дои : 10.1021/ja01249a012 .
- ^ Рашиг, Ф. (1908). «О хлоразиде N3Cl » . Отчеты Немецкого химического общества . 41 (3): 4194–4195. дои : 10.1002/cber.190804103130 .
- ^ CID 61708 от PubChem
Внешние ссылки
[ редактировать ] СМИ, связанные с азидом хлора, на Викискладе?
СМИ, связанные с азидом хлора, на Викискладе?


