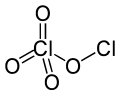
Перхлорат хлора
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Перхлорат хлора [1] | |||
| Систематическое название ИЮПАК Перхлорат хлора [1] | |||
| Другие имена Оксид хлора(I,VII) Четырехокись дихлора | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| ХимическийПаук | |||
ПабХим CID | |||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| Cl 2 О 4 | |||
| Молярная масса | 134.90 g·mol −1 | ||
| Появление | Бледно-зеленая жидкость | ||
| Плотность | 1,81 г·см −3 | ||
| Температура плавления | -117 ° C (-179 ° F; 156 К) | ||
| Точка кипения | 20 ° C (68 ° F; 293 К) (разлагается) | ||
| Реагирует | |||
| Опасности | |||
| Безопасность и гигиена труда (OHS/OSH): | |||
Основные опасности | окислитель | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Перхлорат хлора – химическое соединение формулы Cl 2 O 4 . Этот оксид хлора представляет собой асимметричный оксид, в котором один атом хлора находится в степени окисления +1 , а другой - +7, с правильной формулой ClOClO 3 . Его получают фотодимеризацией диоксида хлора ( ClO 2 ) при комнатной температуре под действием ультрафиолетового света с длиной волны 436 нм : [2] [3] [4]
- 2ClO 2 → ClOClO 3
Перхлорат хлора также можно получить по следующей реакции при -45 ° C.
- CsClO 4 + ClOSO 2 F → Cs(SO 3 )F + ClOClO 3
Характеристики
[ редактировать ]Перхлорат хлора представляет собой бледно-зеленоватую жидкость. Он менее стабилен, чем ClO 2 (диоксид хлора). [ нужна ссылка ] и разлагается при комнатной температуре с образованием O 2 ( кислорода ), Cl 2 ( хлора ) и Cl 2 O 6 ( гексоксида дихлора ):
- 2ClOClO 3 → O 2 + Cl 2 + Cl 2 O 6
Перхлорат хлора реагирует с хлоридами металлов с образованием хлора и соответствующего безводного перхлората:
- CrO 2 Cl 2 + 2ClOClO 3 → 2Cl 2 + CrO 2 (ClO 4 ) 2
- TiCl 4 + 4ClOClO 3 → 4Cl 2 + Ti(ClO 4 ) 4
- 2AgCl + 2 ClOClO 3 → 2AgClO 4 + Cl 2
Реакции
[ редактировать ]| Реагент | Условия | Продукты |
|---|---|---|
| — | Нагревать | гексоксид дихлора (80%), диоксид хлора , хлор, кислород |
| — | Ультрафиолетовый свет | гептоксид дихлора , хлор, кислород [4] |
| йодид цезия | −45 °С | Cs[I(OClO 3 ) 4 ] [примечание 1] |
| ClOSO 2 F или ClF | — | MClO 4 (M = Cs или NO 2 ) [примечание 2] |
| бром | −45 °С | перхлорат брома (BrOClO 3 ) [примечание 2] |
| йод (0,33 моль ) | −50 °С | I(OClO 3 ) 3 [примечание 3] |
Примечания
[ редактировать ]- ^ Cs[I(OClO 3 ) 4 ] представляет собой бледно-желтую соль, стабильную при комнатной температуре. Он имеет квадратный блок IO 4 .
- ^ Перейти обратно: а б MClO 4 (M = Cs или NO 2 ) реагирует с BrOSO 2 F при -20 °C с образованием перхлората брома (BrOClO 3 ). Перхлорат брома затем реагирует с бромистым водородом (HBr) при -70°C и дает элементарный бром (Br 2 ) и хлорную кислоту (HClO 4 ).
- ^ Последний [5] попытка образования моноперхлората йода (IOClO 3 ) произошла в 1972 году, [6] и даже при низких температурах вместо этого образуется триперхлорат. При нагревании последний затем разлагается на йодат .
Ссылки
[ редактировать ]- ^ Перейти обратно: а б «Перхлорат хлора - Публичная химическая база данных PubChem» . Проект ПабХим . США: Национальный центр биотехнологической информации.
- ^ А. Дж. Шелл-Сорокин; Д.С. Бетьюн; Дж. Р. Ланкард; ММТ Лой; П. П. Сорокин (1982). «Перхлорат хлора - основной продукт фотолиза диоксида хлора». Дж. Физ. Хим . 86 (24): 4653–4655. дои : 10.1021/j100221a001 .
- ^ М. И. Лопес; Дж. Э. Сикре (1988). «Ультрафиолетовый спектр перхлората хлора». Дж. Физ. Хим . 92 (2): 563–564. дои : 10.1021/j100313a062 .
- ^ Перейти обратно: а б Рао, Баладжи; Андерсон, Тодд А.; Реддер, Аарон; Джексон, В. Эндрю (15 апреля 2010 г.). «Образование перхлората путем окисления озоном водных соединений хлора/оксихлора: роль радикалов ClxOy». Экологические науки и технологии . 44 (8): 2961–2967. Бибкод : 2010EnST...44.2961R . дои : 10.1021/es903065f . ISSN 0013-936X . ПМИД 20345093 .
- ^ Зефиров Н.С.; Зеданкин В.В.; Козьмин, А.С. (1988). «Синтез и свойства ковалентных органических перхлоратов». Российское химическое обозрение . 57 (11). Турпион: 1047. doi : 10.1070/RC1988v057n11ABEH003410 . Перевод из «Успехов химии» , том 57 (1988), стр. 1815-1839.
- ^ Кристе, Карл О.; Шак, Карл Дж. (1972) [20 сентября 1971 г.]. «Трис(перхлорат) йода и тетракис(перхлорато)йодат(III) цезия». Неорганическая химия . 11 (7): 1684. doi : 10.1021/ic50113a047 .