Перхлорат серебра
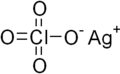 | |
| Имена | |
|---|---|
| Название ИЮПАК Перхлорат серебра(I) | |
| Систематическое название ИЮПАК Хлорат серебра(I)(VII) | |
| Другие имена Хлорная кислота, соль серебра(1+) Серебристый перхлорат | |
| Идентификаторы | |
| |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.029.123 |
| Номер ЕС |
|
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| AgClO 4 | |
| Молярная масса | 207.319 g/mol |
| Появление | Бесцветные гигроскопичные кристаллы |
| Плотность | 2,806 г/см 3 |
| Температура плавления | 486 ° C (907 ° F, 759 К) (разлагается) |
| 557 г/100 мл (25 °С) 792,8 г/100 мл (99 °С) | |
| Растворимость | растворим в органических растворителях |
| Структура | |
| кубический | |
| Опасности | |
| СГС Маркировка : | |
  | |
| Опасность | |
| Х272 , Х314 | |
| P210 , P220 , P221 , P260 , P264 , P280 , P301+P330+P331 , P303+P361+P353 , P304+P340 , P305+P351+P338 , P310 , P321 , P363 , P370+P378 , П405 , П501 | |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Перхлорат серебра – химическое соединение с формулой AgClO 4 . Это белое твердое вещество образует моногидрат и слегка расплывается . Это полезный источник Ag. + ион, хотя присутствие перхлората представляет опасность. Используется в качестве катализатора в органической химии.
Производство
[ редактировать ]Перхлорат серебра получают путем нагревания смеси хлорной кислоты с нитратом серебра .
Альтернативно его можно получить реакцией перхлората бария и сульфата серебра или реакцией хлорной кислоты с оксидом серебра .
Растворимость
[ редактировать ]Перхлорат серебра примечателен своей растворимостью в ароматических растворителях, таких как бензол (52,8 г/л) и толуол (1010 г/л). [1] В этих растворителях катион серебра связывается с ареном, как показали обширные кристаллографические исследования кристаллов, полученных из таких растворов. [2] [3] Его растворимость в воде чрезвычайно высока — до 500 г на 100 мл воды.
Сопутствующие реагенты
[ редактировать ]Подобно нитрату серебра , перхлорат серебра является эффективным реагентом для замены галогенидных лигандов перхлоратом, который представляет собой слабо или некоординирующийся анион . Использование перхлората серебра в химическом синтезе сократилось из-за опасений по поводу взрывоопасности перхлоратных солей. Другими серебряными реагентами являются тетрафторборат серебра и родственные ему трифторметансульфонат серебра и гексафторфосфат серебра .
Ссылки
[ редактировать ]- ^ Ф. Бжезин; Дж. Моллин; Р. Пинторек; З. Шинделарж (1986). Химические таблицы неорганических соединений [ Химические таблицы неорганических соединений ] (на чешском языке). Прага: СНТЛ.
- ^ Э.А. Холл Гриффит; ЭЛЬ Амма (1974). «Ионно-ароматические комплексы металлов. XVIII. Получение и молекулярная структура тетрагидрата нафталин-тетракис (перхлората серебра)». Журнал Американского химического общества . 96 (3): 743–749. дои : 10.1021/ja00810a018 .
- ^ Р.К. Макмаллан; Т.Ф. Кетцле; Си Джей Фритчи младший (1997). «Низкотемпературное нейтронографическое исследование π-комплекса перхлорат серебра – бензол». Акта Кристаллографика Б. 53 (4): 645–653. Бибкод : 1997AcCrB..53..645M . дои : 10.1107/S0108768197000712 . S2CID 97838907 .
