Серебряный гремучник
 | |
| Имена | |
|---|---|
| ИЮПАК имена | |
| Другие имена Серебряный гремучник Серебро(I) гремучее Серебристый гремучник | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| AgCNO | |
| Молярная масса | 149.885 g/mol |
| Плотность | 3,938 г/см 3 |
| Взрывоопасные данные | |
| Чувствительность к ударам | Чрезвычайно высокий |
| Чувствительность к трению | Чрезвычайно высокий |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности | Чувствительный взрывоопасный |
| NFPA 704 (огненный алмаз) | |
| 170 ° С (338 ° F; 443 К) | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Гремучее серебро (AgCNO) — взрывоопасная серебряная соль кислоты гремучей .
Гремучее серебро является основным взрывчатым веществом , но его применение как таковое ограничено из-за его чрезвычайной чувствительности к ударам, теплу, давлению и электричеству. Соединение становится все более чувствительным по мере агрегации, даже в небольших количествах; Прикосновение падающего пера , удар одной капли воды или небольшой статический разряд — все это способно привести к взрывному взрыву неограниченной груды гремучего серебра размером не больше десятицентовика и не тяжелее нескольких миллиграммов . Агрегирование больших количеств невозможно из-за склонности соединения к самодетонации под собственным весом.
Гремучее серебро было впервые получено в 1800 году Эдвардом Чарльзом Говардом в его исследовательском проекте по приготовлению большого количества гремучих веществ . Наряду с гремучей ртутью , это единственный гремучая мышь, достаточно стабильная для коммерческого использования. Детонаторы с использованием гремучего серебра использовались для инициирования пикриновой кислоты в 1885 году, но с тех пор использовались только итальянским военно-морским флотом . [3] В настоящее время коммерческое использование заключается в производстве безвредных новых шумогенераторов в качестве детских игрушек.
Структура
[ редактировать ]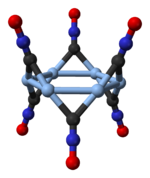
Гремучее серебро встречается в двух полиморфных формах — ромбической и тригональной с ромбоэдрической решеткой . [4] Тригональный полиморф состоит из циклических гексамеров (AgCNO) 6 . [5]

Характеристики
[ редактировать ]Гремучие вещества токсичны примерно так же, как и цианиды . [3] В чистом виде гремучее серебро химически стабильно и не разлагается после многих лет хранения. Как и многие соли серебра, он темнеет под воздействием света. Он мало растворим в холодной воде и может быть перекристаллизован из горячей воды. [3] [6] Его также можно перекристаллизовать из 20%-ного раствора ацетата аммония. [3] Он не гигроскопичен и может взорваться во влажном состоянии или под водой; Сообщалось, что он оставался взрывоопасным после 37 лет пребывания под водой. [3] Он взрывается при контакте с концентрированной серной кислотой , хлором или бромом , но не при контакте с йодом . [3] Нерастворим в азотной кислоте , но растворяется в аммиаке , хлоридах щелочных металлов , цианидах щелочных металлов , анилине , пиридине и йодиде калия , образуя комплексы. [3] Концентрированная соляная кислота разлагает его невзрывоопасно с шипением; тиосульфат также разлагает его невзрывоопасно и может быть использован для утилизации. [3]
Подготовка
[ редактировать ]Это соединение можно получить, выливая раствор нитрата серебра в азотной кислоте в этанол , при тщательном контроле условий реакции, чтобы избежать взрыва. [7] Реакцию обычно проводят при температуре 80–90 °C; при 30 °C осадок может не образовываться. [3] Сразу следует готовить только небольшое количество гремучего серебра, так как даже вес кристаллов может вызвать их самодетонацию.Другой способ получения гремучего серебра — реакция карбоната серебра с аммиака . раствором [ нужна ссылка ]
Гремучее серебро также образуется при пропускании газообразного оксида азота через раствор нитрата серебра в этаноле. [3]
кислого раствора нитрата серебра со спиртом. Гремучее серебро может быть получено непреднамеренно при контакте [7] Это представляет опасность для некоторых составов химически серебренных зеркал .
Новинка взрывчатого вещества
[ редактировать ]Гремучее серебро, часто в сочетании с хлоратом калия , используется в устройствах для создания трюков, известных как «броски», «крекеры», «луцианы», «хлысты», «поп-ит» или «бэнг-щелк». популярный вид новинок фейерверков . Они содержат около 200 миллиграммов мелкого гравия, покрытого небольшим количеством (приблизительно 80 микрограммов) [8] из гремучего серебра. При броске на твердую поверхность удара достаточно, чтобы взорвать небольшое количество взрывчатки, создавая небольшой салют от сверхзвукового взрыва. Защелки сконструированы таким образом, чтобы не вызывать повреждений (даже при взрыве на коже) из-за буферного эффекта, обеспечиваемого гораздо большей массой гравийной среды. Это также химическое вещество, которое содержится в рождественских крекерах. [9] Впервые он был использован для этой цели Томом Смитом в 1860 году. Химическое вещество нанесено на одну из двух узких полосок картона, а на вторую нанесен абразив. Когда крекер вытаскивают, абразив взрывает гремучее серебро.
Гремучая смесь с 10–20% хлората калия дешевле и более блестящая , чем сама гремучая мышь. [3]
Гремящее серебро и «гремящее серебро»
[ редактировать ]Гремучее серебро часто путают с нитридом серебра , азидом серебра или гремучим серебром . «Гремящее серебро», хотя всегда относится к взрывчатому серебросодержащему веществу, является неоднозначным термином. Хотя это может быть синонимом гремучего серебра, оно также может относиться к нитриду или азиду, продукту разложения реагента Толлена или алхимической смеси, которая не содержит гремучего аниона.
См. также
[ редактировать ]- Первичное взрывчатое вещество
- Юстус фон Либих
- Фридрих Вёлер
- Цианат серебра
- Изомерия
- Молниеносный
- Фульминовая кислота
- Калий гремучий
- гремучая ртуть(II)
Ссылки
[ редактировать ]- ^ Международный союз теоретической и прикладной химии (2005). Номенклатура неорганической химии (Рекомендации ИЮПАК 2005 г.). Кембридж (Великобритания): RSC – IUPAC . ISBN 0-85404-438-8 . п. 291. Электронная версия.
- ^ «Гремоносное серебро» . ХимБейс . Проверено 8 июня 2012 года . [ постоянная мертвая ссылка ]
- ^ Jump up to: а б с д и ж г час я дж к Матьяс, Роберт; Пахман, Иржи (12 марта 2013 г.). Первичные взрывчатые вещества . Springer Science & Business Media, 338 страниц.
- ^ Бриттон, Д.; Дуниц, доктор юридических наук (1965). «Кристаллическая структура гремучего серебра». Акта Кристаллографика . 19 (4): 662–668. Бибкод : 1965AcCry..19..662B . дои : 10.1107/S0365110X6500405X .
- ^ Бриттон, Д. (1991). «Переопределение тригональной структуры гребенчатого серебра». Акта Кристаллографика C. 47 (12): 2646–2647. Бибкод : 1991AcCrC..47.2646B . дои : 10.1107/S0108270191008855 .
- ^ 0,0075 г при 13 °C, 0,018 г при 30 °C и 0,25 г на 100 г H 2 O при 100 °C.
- ^ Jump up to: а б Коллинз, штат Пенсильвания; Холлоуэй, KJ (1978). «Переоценка гремучего серебра как детонанта». Метательные вещества, взрывчатые вещества, пиротехника . 3 (6): 159–162. дои : 10.1002/prep.19780030603 .
- ^ раскрытие упаковки компании Alexron Co. Ltd, Гонконг, Phantom Brand Bang Snaps, (c) 2013 г.
- ^ Спектр. «Комментарий №70» . Расположение старой фабрики фейерверков . Британское пиротехническое общество . Проверено 20 декабря 2011 г.
Дальнейшее чтение
[ редактировать ]- Сингх, К. (1959). «Кристаллическая структура гремучего серебра» . Акта Кристаллографика . 12 (12): 1053. Бибкод : 1959AcCry..12.1053S . дои : 10.1107/S0365110X5900295X .
