Азид серебра
 | |
| Имена | |
|---|---|
| Название ИЮПАК Азид серебра(I) | |
| Другие имена Серебристый азид | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.034.173 |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| AgNAgN3 | |
| Молярная масса | 149.888 g/mol |
| Появление | бесцветные кристаллы |
| Плотность | 4,42 г/см 3 |
| Температура плавления | 250 ° C (482 ° F; 523 К) взрывоопасный |
| Точка кипения | разлагается |
| Растворимость в других растворителях | 2.0×10 −8 г/л |
| Структура | |
| Орторомбический oI16 [1] | |
| Ибам, № 72 | |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности | Очень токсичен, взрывоопасен. |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Азид серебра – соединение формулы химическое АгН 3 . Это серебряная (I) соль азотистоводородной кислоты . Образует бесцветные кристаллы. Как и большинство азидов, это первичное взрывчатое вещество .
Структура и химия
[ редактировать ]Азид серебра можно получить обработкой водного раствора нитрата серебра азидом натрия . [2] Азид серебра выпадает в осадок в виде белого твердого вещества, оставляя нитрат натрия в растворе.
Рентгеновская кристаллография показывает, что AgN 3 — координационный полимер с плоско-квадратной структурой. В + координируется четырьмя азидными лигандами . Соответственно, каждый конец каждого азидного лиганда соединен с парой В + центры. Конструкция состоит из двумерных Слои AgN 3 наложены друг на друга, связи Ag–N между слоями более слабые. Координация В + альтернативно может быть описан как сильно искаженный октаэдр 4 + 2, причем два более удаленных атома азота являются частью слоев выше и ниже. [3]
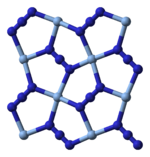 |  | 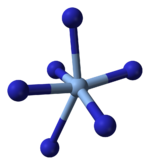 |  |
| Часть слоя | Укладка слоев | координация 4+2 В + | 2+1 координация N в Н - 3 |
В своей наиболее характерной реакции твердое вещество разлагается со взрывом с выделением газообразного азота:
- 2 AgN 3 (т) → 3 N 2 (г) + 2 Ag(т)
Первым шагом в этом разложении является образование свободных электронов и азидных радикалов; таким образом, скорость реакции увеличивается за счет добавления полупроводниковых оксидов. [4] Чистый азид серебра взрывается при 340 °C , но наличие примесей снижает температуру до 270 °C. [5] Эта реакция имеет меньшую энергию активации и начальную задержку, чем соответствующее разложение азида свинца . [6]
Безопасность
[ редактировать ]AgN 3 , как и большинство азидов тяжелых металлов , является опасным первичным взрывчатым веществом . Разложение может быть вызвано воздействием ультрафиолета или ударом. [2] Церийно-аммиачная селитра [NH 4 ] 2 [Ce(NO 3 ) 6 ] используется в качестве окислителя для разрушения AgN 3 в разливах. [5]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Марр HE III.; Стэнфорд Р.Х. младший (1962). «Размеры элементарной ячейки азида серебра». Акта Кристаллографика . 15 (12): 1313–1314. Бибкод : 1962AcCry..15.1313M . дои : 10.1107/S0365110X62003497 .
- ^ Перейти обратно: а б Роберт Матьяс, Иржи Пахман (2013). Первичные взрывчатые вещества (1-е изд.). Спрингер. п. 93. ИСБН 978-3-642-28435-9 . [1]
- ^ Шмидт, К. Л. Диннебир, Р.; Ведиг, У.; Янсен, М. (2007). «Кристаллическая структура и химическая связь высокотемпературной фазы AgN 3 ». Неорганическая химия . 46 (3): 907–916. дои : 10.1021/ic061963n . ПМИД 17257034 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Эндрю Нокс Голви; Майкл Э. Браун (1999). Термическое разложение ионных твердых веществ (т.86 Исследования по физической и теоретической химии . Elsevier. стр. 335. ISBN 978-0-444-82437-0 .
- ^ Перейти обратно: а б Маргарет-Энн Армор (2003). Руководство по утилизации опасных лабораторных химикатов, Химия окружающей среды и токсикология (3-е изд.). ЦРК Пресс. п. 452. ИСБН 978-1-56670-567-7 .
- ^ Иегуда Йинон; Шмуэль Зитрин (1996). Современные методы и приложения анализа взрывчатых веществ . Джон Уайли и сыновья. стр. 15–16. ISBN 978-0-471-96562-6 .
