Окись ниобия
 | |
| Имена | |
|---|---|
| Другие имена оксид ниобия(II) | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.031.631 |
ПабХим CID | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| НБО | |
| Молярная масса | 108.905 g/mol [1] |
| Появление | серый сплошной [1] |
| Запах | без запаха |
| Плотность | 7,30 г/см 3 [1] |
| Температура плавления | 1937 ° C (3519 ° F; 2210 К) [1] |
| Растворимость | мало растворим в HCl нерастворим в азотной кислоте |
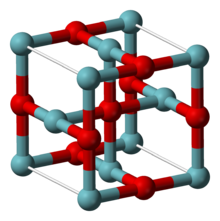
| Структура [2] | |
| Кубический, cP6 | |
| Пм 3 м, № 221 | |
а = 0,4211 нм | |
Формульные единицы ( Z ) | 3 |
| Термохимия [3] | |
Теплоемкость ( С ) | 41,3 Дж/(моль·К) |
Стандартный моляр энтропия ( S ⦵ 298 ) | 48,1 Дж/(моль·К) |
Стандартная энтальпия образование (Δ f H ⦵ 298 ) | = -405,85 кДж/моль |
Свободная энергия Гиббса (Δ f G ⦵ ) | -378,6 кДж/моль |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
ниобия — соединение формулы NbO неорганическое . Моноксид Это серое твердое вещество с металлической проводимостью. [1]
Структура и электронные свойства
[ редактировать ]NbO принимает необычную кубическую структуру, похожую на структуру каменной соли, но с некоторыми недостающими атомами по сравнению с ней, так что атомы ниобия и кислорода имеют квадратную плоскую координационную геометрию. Ниобиевые центры расположены в виде октаэдров, и имеется структурное сходство с октаэдрическими кластерами ниобия в низших галогенидах ниобия. В NbO длина связи Nb-Nb составляет 298 пм по сравнению с 285 пм в металле. [2] Одно исследование связи пришло к выводу, что между металлическими центрами существуют прочные и почти ковалентные связи. [4]
Это сверхпроводник с температурой перехода 1,38 К. [5] Он используется в конденсаторах, где слой Nb 2 O 5 формируется вокруг зерен NbO в качестве диэлектрика. [6] [7] [8]
Подготовка
[ редактировать ]NbO можно получить восстановлением Nb 2 O 5 H 2 . Чаще всего его готовят путем сопропорционирования : [9]
- Nb 2 O 5 + 3 Nb → 5 NbO
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и Хейнс, с. 4,76
- ^ Jump up to: а б Пиалу, А.; Мерри, МЛ; Сизерон, Г. (1982). «Исследование поведения ниобия в вакууме методом высокотемпературной рентгеновской дифракции». Журнал менее распространенных металлов . 87 :1–19. дои : 10.1016/0022-5088(82)90036-4 .
- ^ Хейнс, с. 5.29
- ^ Шульц, Вернер В.; Венцкович, Рената М. (1993). «Электронная зонная структура и связь в Nb 3 O 3 ». Физический обзор B . 48 (23): 16986–16991. Бибкод : 1993PhRvB..4816986S . дои : 10.1103/PhysRevB.48.16986 . ПМИД 10008298 .
- ^ Халм, Дж. К.; Джонс, СК; Хейн, РА; Гибсон, JW (1972). «Сверхпроводимость в системах TiO и NbO». Журнал физики низких температур . 7 (3–4): 291–307. Бибкод : 1972JLTP....7..291H . дои : 10.1007/BF00660068 . S2CID 122554738 .
- ^ Нико, К.; Соарес, МРН; Родригес, Дж.; Матос, М.; Монтейро, Р.; Граса, MPF; Валенте, Массачусетс; Коста, FM; Монтейро, Т. (2011). «Спеченные порошки NbO для применения в электронных устройствах». Журнал физической химии C. 115 (11): 4879–4886. дои : 10.1021/jp110672u .
- ^ Нико, Клаудио; Рино, Луис; Матос, Мариана; Монтейро, Руи; Коста, Флоринда М.; Монтейро, Тереза; Граса, Мануэль П.Ф. (2013). «NbO/Nb 2 O 5 ядро–оболочка методом термического окисления». Журнал Европейского керамического общества . 33 (15–16): 3077–3083. doi : 10.1016/j.jeurceramsoc.2013.06.020 .
- ^ Наито, Кадзуми и Кабе, Исао (2005) «Метод производства твердого электролитического конденсатора», патент США 6 882 522.
- ^ Рид, ТБ; Поллард, скорая помощь; Лонни, Луизиана; Ломан, Р.Э.; Хониг, Дж. М. (2007). «Монооксид ниобия». Неорганические синтезы . стр. 108–110. дои : 10.1002/9780470132616.ch22 . ISBN 9780470132616 .
Цитированные источники
[ редактировать ]- Хейнс, Уильям М., изд. (2016). Справочник CRC по химии и физике (97-е изд.). Бока-Ратон, Флорида: CRC Press . ISBN 9781498754293 .