Пероксинитрит
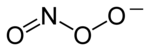 Химическая структура пероксинитрит-аниона | |
| Имена | |
|---|---|
| Название ИЮПАК оксид нитрита | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ЧЭБИ | |
| КЕГГ | |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| НЕТ 3 − | |
| Молярная масса | 62.005 g·mol −1 |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |

Пероксинитрит (иногда называемый пероксонитритом ) представляет собой ион с формулой ONOO. − . Это структурный нитрата . NO изомер −
3
Подготовка
[ редактировать ]Пероксинитрит можно получить реакцией супероксида с оксидом азота : [1] [2] [3]
- НЕТ + О - 2 → НЕТ(О 2 ) −
Его получают реакцией перекиси водорода с нитритом : [4]
- Н 2 О 2 + НЕТ −
2 → СЧАСТЛИВЫЙ − + Н 2 О
На его присутствие указывает поглощение при 302 нм (pH 12, ε 302 = 1670 М −1 см −1 ).
Реакции
[ редактировать ]Пероксинитрит является слабоосновным с p K a ~6,8.
Он реактивен по отношению к ДНК и белкам .
СЧАСТЛИВЫЙ − реагирует Нуклеофильно с углекислым газом . In vivo концентрация углекислого газа составляет около 1 мМ, а его реакция с ONOO − происходит быстро. Таким образом, в физиологических условиях реакция ONOO − с углекислым газом с образованием нитрозопероксикарбоната ( ONOOCO −
2 ) на сегодняшний день является преобладающим путем для ONOO. − . ОНООКО −
2 гомолизируется с образованием карбонатного радикала и диоксида азота, опять же в виде пары каркасных радикалов. Примерно в 66% случаев эти два радикала рекомбинируются с образованием углекислого газа и нитрата. В остальных 33% случаев эти два радикала покидают клетку растворителя и становятся свободными радикалами. Считается, что именно эти радикалы ( карбонатный радикал и диоксид азота ) вызывают повреждение клеток, связанное с пероксинитритом.
Пероксиазотистая кислота
[ редактировать ]Сопряженная с ним кислота пероксиазотистая кислота обладает высокой реакционной способностью, хотя пероксинитрит стабилен в основных растворах. [5] [6]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Боле, Д. Скотт; Саган, Элизабет С. (2004). «Тетраметиламмониевые соли супероксида и пероксинитрита». Неорганические синтезы : 36. doi : 10.1002/0471653683.ch1 .
- ^ Пэчер, П; Бекман, Дж. С.; Лиодэ, Л. (2007). «Оксид азота и пероксинитрит в здоровье и болезни» . Физиологические обзоры . 87 (1): 315–424. doi : 10.1152/physrev.00029.2006 . ПМК 2248324 . ПМИД 17237348 .
- ^ Сабо, К; Исчиропулос, Х; Ради, Р. (2007). «Пероксинитрит: биохимия, патофизиология и разработка методов лечения». Nature Reviews Открытие лекарств . 6 (8): 662–80. дои : 10.1038/nrd2222 . ПМИД 17667957 .
- ^ Бекман, Дж. С.; Коппенол, WH (1996). «Оксид азота, супероксид и пероксинитрит: хороший, плохой и уродливый». Американский журнал физиологии. Клеточная физиология . 271 (5, часть 1): C1424–37. дои : 10.1152/ajpcell.1996.271.5.C1424 . ПМИД 8944624 .
- ^ Холлеман, А.Ф.; Виберг, Э. неорганической химии : Сан-Диего, 2001. Академическое издательство ISBN 0-12-352651-5 .
- ^ Коппенол, WH (1998). «Химия пероксинитрита, биологического токсина» . Кимика Нова . 21 (3): 326–331. дои : 10.1590/S0100-40421998000300014 .