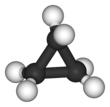
Циклопопропан
| |||
| |||
 | |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК Циклопопропан [2] | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| ЧЭБИ | |||
| ЧЕМБЛ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.000.771 | ||
| КЕГГ | |||
ПабХим CID | |||
| НЕКОТОРЫЙ | |||
| Число | 1027 | ||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| C3HC3H6 | |||
| Молярная масса | 42.08 g/mol | ||
| Появление | Бесцветный газ | ||
| Запах | Сладкий, неземной | ||
| Плотность | 1,879 г/л (1 атм, 0 °С) 680 г/л (жидкость) | ||
| Температура плавления | -128 ° C (-198 ° F; 145 К) | ||
| Точка кипения | -32,9 ° C (-27,2 ° F; 240,2 К) | ||
| 502 мг/л | |||
| Давление пара | 640 кПа (20 °С) 1350 кПа (50 °С) | ||
| Кислотность ( pKa ) | ~46 | ||
| -39.9·10 −6 см 3 /моль | |||
| Опасности | |||
| Безопасность и гигиена труда (OHS/OSH): | |||
Основные опасности | Легковоспламеняющийся удушающий | ||
| СГС Маркировка : | |||
  | |||
| Опасность | |||
| NFPA 704 (огненный алмаз) | |||
| 495 ° C (923 ° F; 768 К) | |||
| Взрывоопасные пределы | 2,4 % (ниже) 10,4 % (верхний) | ||
| Паспорт безопасности (SDS) | Эйр Ликид | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Циклоппропан — это циклоалкан с молекулярной формулой (СН 2 ) 3 , состоящий из трех метиленовых групп (СН 2 ), связанных друг с другом с образованием треугольного кольца. Небольшой размер кольца создает значительную кольцевую деформацию конструкции. Сам циклопропан представляет в основном теоретический интерес, но многие его производные — циклопропаны — имеют коммерческое или биологическое значение. [3]
Циклоппропан использовался в качестве клинического ингаляционного анестетика с 1930-х по 1980-е годы. Высокая воспламеняемость вещества создает опасность пожара и взрыва в операционных из-за его склонности к накоплению в закрытых помещениях, поскольку его плотность выше, чем у воздуха.
История [ править ]
Циклоппропан был открыт в 1881 году Августом Фройндом , который также предложил правильную структуру вещества в своей первой статье. [4] Фрейнд обработал 1,3-дибромпропан натрием ведущую , вызвав внутримолекулярную реакцию Вюрца, непосредственно к циклопропану. [5] Выход реакции был улучшен Густавсоном в 1887 году с использованием цинка вместо натрия. [6] Циклоппропан не имел коммерческого применения до тех пор, пока Хендерсон и Лукас не обнаружили его анестезирующие свойства в 1929 году; [7] промышленное производство началось к 1936 году. [8] В современной анестезиологической практике его заменили другие агенты.
Анестезия [ править ]
Циклоппропан был введен в клиническое применение американским анестезиологом Ральфом Уотерсом , который использовал закрытую систему с абсорбцией углекислого газа для сохранения этого дорогостоящего на тот момент агента.Циклоппропан — относительно сильнодействующий, не вызывающий раздражения агент со сладким запахом, минимальная альвеолярная концентрация которого составляет 17,5%. [9] и коэффициент распределения кровь/газ 0,55. Это означало, что индукция анестезии путем ингаляции циклопропана и кислорода была быстрой и не неприятной. Однако по завершении длительной анестезии у пациентов может произойти внезапное снижение артериального давления, что потенциально может привести к сердечной аритмии : реакции, известной как «циклопропановый шок». [10] По этой причине, а также из-за его высокой стоимости и взрывоопасного характера, [11] в последнее время он использовался только для индукции анестезии и не был доступен для клинического использования с середины 1980-х годов.Цилиндры и расходомеры были окрашены в оранжевый цвет.
Фармакология [ править ]
Циклоппропан неактивен в отношении рецепторов ГАМК А и глицина и вместо этого действует как антагонист рецепторов NMDA . [12] [13] Он также ингибирует рецептор AMPA и рецепторы ацетилхолина и активирует определенные K2P каналы никотиновые . [12] [13] [14]
Структура и связь [ править ]

Треугольная структура циклопропана требует, чтобы валентные углы между ковалентными связями углерод-углерод составляли 60 °. Молекула имеет D3h молекулярную симметрию . Дистанции ЦК 151 против 153-155. [15] [16]
Несмотря на свою короткость, связи CC в циклопропане ослаблены на 34 ккал/моль по сравнению с обычными связями CC. Помимо кольцевой деформации, молекула также испытывает деформацию кручения из-за затменной конформации ее атомов водорода. Связи CH в циклопропане прочнее, чем обычные связи CH, о чем свидетельствуют константы взаимодействия ЯМР.
Связь между углеродными центрами обычно описывается как изогнутые связи . [17] В этой модели связи углерод-углерод изогнуты наружу так, что межорбитальный угол составляет 104°.
Необычные структурные свойства циклопропана породили множество теоретических дискуссий. Одна из теорий использует σ- ароматичность : стабилизацию, обеспечиваемую делокализацией шести электронов трех CC σ-связей циклопропана, чтобы объяснить, почему напряжение циклопропана составляет «всего» 27,6 ккал/моль по сравнению с циклобутаном (26,2 ккал/моль) с циклогексаном как ссылка с E str =0 ккал/моль, [18] [19] [20] в отличие от обычной π-ароматичности, которая, например, оказывает сильное стабилизирующее действие на бензол . Другие исследования не подтверждают роль σ-ароматичности в циклопропане и существование индуцированного кольцевого тока; такие исследования дают альтернативное объяснение энергетической стабилизации и аномального магнитного поведения циклопропана. [21]
Синтез [ править ]
Циклоппропан был впервые получен с помощью реакции Вюрца , в которой 1,3-дибромпропан циклизовался с использованием натрия . [4] Выход этой реакции можно улучшить, используя цинк в качестве дегалогенирующего агента и йодид натрия в качестве катализатора. [22]
- BrCH 2 CH 2 CH 2 Br + 2 Na → (CH 2 ) 3 + 2 NaBr
Получение циклопропановых колец называется циклопропанированием .
Реакция [ править ]
Часто полагают, что из-за повышенного π-характера связей CC циклопропан присоединяется к брому с образованием 1,3-дибромпропана, но эта реакция протекает плохо. [23] Гидрогалогенирование галоидоводородными кислотами дает линейные 1-галогенпропаны. Замещенные циклопропаны также реагируют по правилу Марковникова . [24]
Циклопопропан и его производные могут окислительно присоединяться к переходным металлам в процессе, называемом активацией C–C .
Безопасность [ править ]
Циклоппропан легко воспламеняется. Однако, несмотря на свою энергию деформации, он не проявляет взрывного поведения, существенно отличающегося от других алканов .
См. также [ править ]
- Тетраэдр содержит четыре сросшихся циклопропановых кольца, образующих грани тетраэдра.
- Пропеллан содержит три циклопропановых кольца, которые имеют одну центральную связь углерод-углерод.
- Циклоппен
- Метиленциклопропан
Ссылки [ править ]
- ^ Индекс Merck , 11-е издание, 2755 .
- ^ «Фронт материи». Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга) . Кембридж: Королевское химическое общество . 2014. с. 137. дои : 10.1039/9781849733069-FP001 . ISBN 978-0-85404-182-4 .
- ^ Фауст, Рюдигер (2001). «Увлекательные природные и искусственные циклопропановые архитектуры». Angewandte Chemie, международное издание . 40 (12): 2251–2253. doi : 10.1002/1521-3773(20010618)40:12<2251::AID-ANIE2251>3.0.CO;2-R . ПМИД 11433485 .
- ^ Jump up to: а б Август Фройнд (1881). « О триметилене». Журнал практической химии . 26 (1): 367–377. дои : 10.1002/prac.18820260125 .
- ^ Август Фройнд (1882 г.). « О триметилене». Ежемесячные журналы по химии . 3 (1): 625–635. дои : 10.1007/BF01516828 . S2CID 197767176 .
- ^ Г. Густавсон (1887). «О новом способе получения триметилена». Журнал практической химии . 36 :300-305. дои : 10.1002/prac.18870360127 .
- ^ ГХВ Лукас; В. Е. Хендерсон (1 августа 1929 г.). «Новый анестетик: циклопропан: предварительный отчет» . Может ли Med Assoc J. 21 (2): 173–5. ПМК 1710967 . ПМИД 20317448 .
- ^ Х.Б. Хасс; ET Макби; Дж. Э. Хиндс (1936). «Синтез циклопропана». Промышленная и инженерная химия . 28 (10): 1178–81. дои : 10.1021/ie50322a013 .
- ^ Эгер, Эдмонд И.; Брандстатер, Бернард; Саидман, Лоуренс Дж.; Риган, Майкл Дж.; Северингхаус, Джон В.; Мансон, Эдвин С. (1965). «Эквипотентные альвеолярные концентрации метоксифлурана, галотана, диэтилового эфира, флуроксена, циклопропана, ксенона и закиси азота у собаки» . Анестезиология . 26 (6): 771–777. дои : 10.1097/00000542-196511000-00012 . ПМИД 4378907 .
- ^ ДЖОНСТОН, М; Альбертс, младший (июль 1950 г.). «Циклопропановая анестезия и желудочковые аритмии» . Британский кардиологический журнал . 12 (3): 239–44. дои : 10.1136/hrt.12.3.239 . ПМЦ 479392 . ПМИД 15426685 .
- ^ Макдональд, AG (июнь 1994 г.). «Краткая история пожаров и взрывов, вызванных анестетиками» . Британский журнал анестезии . 72 (6): 710–22. дои : 10.1093/бья/72.6.710 . ПМИД 8024925 .
- ^ Jump up to: а б Хью К. Хеммингс; Филип М. Хопкинс (2006). Основы анестезии: фундаментальные науки для клинической практики . Elsevier Науки о здоровье. стр. 292–. ISBN 978-0-323-03707-5 .
- ^ Jump up to: а б Хеммингс, Хью К. (2009). «Молекулярные мишени общих анестетиков в нервной системе». Подавление разума : 11–31. дои : 10.1007/978-1-60761-462-3_2 . ISBN 978-1-60761-463-0 .
- ^ Хара К., Эгер Э.И., Ластер М.Дж., Харрис Р.А. (декабрь 2002 г.). «Негалогенированные алканы циклопропан и бутан влияют на ионные каналы, управляемые нейротрансмиттерами, и рецепторы, связанные с G-белком: дифференциальное действие на ГАМКА и глициновые рецепторы» . Анестезиология . 97 (6): 1512–20. дои : 10.1097/00000542-200212000-00025 . ПМИД 12459679 . S2CID 21160239 . [ постоянная мертвая ссылка ]
- ^ Аллен, Фрэнк Х.; Кеннард, Ольга; Уотсон, Дэвид Г.; Браммер, Ли; Орпен, А. Гай; Тейлор, Робин (1987). «Таблицы длин связей, определенных методами рентгеновской и нейтронной дифракции. Часть 1. Длины связей в органических соединениях» . Журнал Химического общества, Perkin Transactions 2 (12): S1 – S19. дои : 10.1039/P298700000S1 .
- ^ Булатов Роман, изд. (2015). Механохимия полимеров . Спрингер. п. 9. ISBN 978-3-319-22824-2 .
- ^ Эрик В. Анслин и Деннис А. Догерти. Современная физико-органическая химия. 2006. страницы 850-852.
- ^ SW Бенсон, Термохимическая кинетика, S. 273, J. Wiley & Sons, Нью-Йорк, Лондон, Сидней, Торонто, 1976 г.
- ^ Дьюар, MJ (1984). «Химические последствия σ-конъюгации». Дж. Ам. хим. Соц . 106 (3): 669–682. дои : 10.1021/ja00315a036 .
- ^ Кремер, Д. (1988). «Плюсы и минусы σ-ароматичности». Тетраэдр . 44 (2): 7427–7454. дои : 10.1016/s0040-4020(01)86238-4 .
- ^ Ву, Вэй; Ма, Бен; Ву, Джуди И-Чиа; фон Раге, Шлейер; Мо, Йиронг (2009). «Действительно ли циклопропан является σ-ароматической парадигмой?» . Химия: Европейский журнал . 15 (38): 9730–9736. дои : 10.1002/chem.200900586 . ПМИД 19562784 .
- ^ Волвебер, Хартмунд (2000). «Анестетики, генерал». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a02_289 . ISBN 978-3527306732 .
- ^ Гордон, Арнольд Дж. (1967). «Галогенирование и олефиновая природа циклопропана». Журнал химического образования . 44 (8): 461. doi : 10.1021/ed044p461 .
- ^ Продвинутая органическая химия, реакции, механизмы и структура 3-е изд. Джерри Марч ISBN 0-471-85472-7