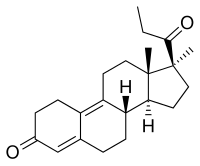
Промегестон
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Хирургический камень |
| Другие имена | ПМГ; Р-5020; РУ-5020; 17α,21-Диметил-δ 9 -19-норпрогестерон; 17α,21-Диметил-19-норпрегна-4,9-диен-3,20-дион |
| Маршруты администрация | Через рот [1] |
| Класс препарата | прогестаген ; Прогестин |
| код АТС | |
| Фармакокинетические данные | |
| Связывание с белками | К альбумину [1] |
| Метаболизм | Печень ( гидроксилирование ) [1] [3] |
| Метаболиты | • Тримегестон |
| Период полувыведения | Промегестон: ? Тримегестон: 13,8–15,6 часов. [1] [2] |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.207.681 |
| Химические и физические данные | |
| Формула | С 22 Н 30 О 2 |
| Молярная масса | 326.480 g·mol −1 |
| 3D model ( JSmol ) | |
Прогестон , продаваемый под торговой маркой Surgestone , представляет собой прогестиновый препарат, который используется в гормональной терапии в период менопаузы и при лечении гинекологических заболеваний . [4] [1] [5] [6] Его принимают внутрь . [1]
Побочные эффекты прогестона включают, среди прочего, нарушения менструального цикла . [7] Прогестон представляет собой прогестин или синтетический прогестаген и, следовательно, является агонистом рецептора прогестерона , биологической мишени прогестагенов, таких как прогестерон . [1] Он обладает слабой антиандрогенной , глюкокортикоидной и антиминералокортикоидной активностью и не имеет другой важной гормональной активности. [1] [8] [2] Препарат в основном пролекарством тримегестона . является [7] [1]
Промегестон был впервые описан в 1973 году и введен в медицинское применение во Франции в 1983 году. [9] [10] [11] Он продается только в нескольких странах, включая Францию, Португалию , Тунис и Аргентину . [6] [12] Помимо использования в качестве лекарства, прогестон широко использовался в научных исследованиях в качестве радиолиганда рецептора прогестерона. [4] [13]
Медицинское использование
[ редактировать ]Промегестон используется в менопаузальной гормональной терапии и при лечении гинекологических состояний, вызванных лютеиновой недостаточностью , включая предменопаузальные расстройства, дисменорею и другие нарушения менструального цикла , а также предменструальный синдром . [1] [5] Его также использовали для лечения доброкачественных заболеваний молочной железы, таких как масталгия (боль в груди). [14] Таблетки Прогестона обладают противозачаточным эффектом и используются в качестве противозачаточных средств, содержащих только прогестаген , хотя они не имеют специальной лицензии как таковые. [15]
Побочные эффекты
[ редактировать ]Побочные эффекты прогестона включают, среди прочего, нарушения менструального цикла . [7] Он не имеет андрогенных побочных эффектов. [4] [5]
Фармакология
[ редактировать ]Фармакодинамика
[ редактировать ]
Прогестон является прогестагеном или агонистом рецептора прогестерона . [1] [3] около 200% сродства прогестерона к Он имеет PR. [1] [3] Дозировка трансформации эндометрия прогестона для составляет 10 мг за цикл, а доза, ингибирующая овуляцию, — 0,5 мг/день. [1] [3] обладает слабой глюкокортикоидной активностью. Прогестон помимо прогестагенной активности [1] [3] И наоборот, он не обладает андрогенной , эстрогенной , минералокортикоидной или другой гормональной активностью. [1] [3] [5] По-видимому, он обладает антиандрогенной активностью. [13] Его основной метаболит тримегестон обладает слабой антиминералокортикоидной и антиандрогенной активностью. [8] [2] Кроме того, было обнаружено, что прогестон обладает некоторой нейростероидной активностью, действуя как неконкурентный антагонист никотиновых рецепторов ацетилхолина , подобно прогестерону. [16]
Фармакокинетика
[ редактировать ]После приема перорального пиковые уровни прогестона в сыворотке крови достигаются через 1–2 часа. [1] [3] Лекарство в основном связано с альбумином ; он не связывается с глобулином, связывающим половые гормоны , и лишь слабо связывается с глобулином, связывающим кортикостероиды . [1] [3] [17] Метаболизм гидроксилирования прогестона осуществляется главным образом посредством в положении С21 и в других положениях. [1] [3] Прогестерон аналогичным образом гидроксилируется в положении С21 с образованием 11-дезоксикортикостерона (21-гидроксипрогестерона). [18] C9(10) Однако двойная связь прогестона значительно ограничивает восстановление А-кольца , которому подвергается прогестерон, в результате чего 21-гидроксилирование является основным путем метаболизма прогестона. [18] Лекарство стереоселективно метаболизируется в тримегестон , 21( S )-гидрокси метаболит , который является основным соединением, обнаруживаемым в плазме ; его уровень циркулирует примерно в два раза больше, чем сам прогестон. [7] Кроме того, тригестон имеет более чем в три раза более высокое сродство к PR, чем прогестон. [1] Таким образом, прогестон в значительной степени является пролекарством тримегестона. [7] [19] Второй метаболит, 21( R )-гидроксипрогестон, циркулирует в гораздо более низких концентрациях ( AUC для ( S )- и ( R ) -изомеров около 21). [7] Период полувыведения тримегестона составляет от 13,8 до 15,6 часов. [1] [2] Промегестон, тримегестон и 21( R )-гидроксипрогестон не выводятся с мочой , тогда как 3% дозы выводится в виде глюкуронидного и/или сульфатного конъюгата тримегестона, а 1% дозы выводится в виде глюкуронида и/или сульфата. конъюгат 21( R )-гидроксипрогестона. [7]
Химия
[ редактировать ]Прогестон, также известный как 17α,21-диметил-δ. 9 -19-норпрогестерон или 17α,21-диметил-19-норпрегна-4,9-диен-3,20-дион представляет синтетический норпрегнановый стероид и производное прогестерона собой . [9] [12] [11] [1] В частности, это комбинированное производное 17α-метилпрогестерона и 19-норпрогестерона или 17α-метил-19-норпрогестерона . [9] [11] [1] Родственные производные 17α-метил-19-норпрогестерона включают дегегестон и тримегестон . [9] [12] [1]
История
[ редактировать ]Промегестон был впервые описан в литературе в 1973 году и введен для медицинского применения во Франции в 1983 году. [9] [10] [11] [5] Он был разработан Русселем Уклафом во Франции. [5]
Общество и культура
[ редактировать ]Общие имена
[ редактировать ]Промегестон — это непатентованное название препарата и его по МНН , а промегестон — это наименование в подсказке DCF . [6] [9] [12] Он также известен под кодовым названием разработки R-5020 или RU-5020 . [6] [9] [12]
Названия брендов
[ редактировать ]Промегестон продается исключительно под торговой маркой Surgestone. [6] [12]
Доступность
[ редактировать ]Промегестон продается или продавался во Франции , Португалии , Тунисе и Аргентине . [6] [12]
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж г час я дж к л м н тот п д р с т в v В Куль Х. (август 2005 г.). «Фармакология эстрогенов и прогестагенов: влияние различных путей введения» (PDF) . Климактерический . 8 (Приложение 1): 3–63. дои : 10.1080/13697130500148875 . ПМИД 16112947 . S2CID 24616324 .
- ^ Jump up to: а б с д Ситрук-Уэр Р., Боссмайер Р., Бушар П. (июнь 2007 г.). «Доклинические и клинические свойства тримегестона: мощного и селективного прогестина». Гинекологическая эндокринология . 23 (6): 310–319. дои : 10.1080/09513590701267727 . ПМИД 17616854 . S2CID 39422122 .
- ^ Jump up to: а б с д и ж г час я Куль Х (2011). «Фармакология прогестагенов» (PDF) . Журнал репродуктивной медицины и эндокринологии – Журнал репродуктивной медицины и эндокринологии . 8 (Специальный выпуск 1): 157–176.
- ^ Jump up to: а б с Рейно Дж.П., Оджасу Т. (1983). «[Промегестон, новый прогестин]». Журнал гинекологии, акушерства и репродуктивной биологии (на французском языке). 12 (7): 697–710. ПМИД 6366037 .
- ^ Jump up to: а б с д и ж Аллен Р.С. (11 сентября 1984 г.). «На рынок – 1983» . В Бейли ДМ (ред.). Годовые отчеты по медицинской химии . Том. 19. Академическая пресса. стр. 323–. ISBN 978-0-08-058363-1 .
- ^ Jump up to: а б с д и ж «Список прогестинов» .
- ^ Jump up to: а б с д и ж г Тулунай, Орм М (6 декабря 2012 г.). Европейское сотрудничество: на пути к разработке лекарств [ sic ] и рациональной лекарственной терапии: материалы шестого конгресса Европейской ассоциации клинической фармакологии и терапии Стамбул, 24–28 июня 2003 г. Springer Science & Business Media. стр. 107–. ISBN 978-3-642-55454-4 .
Исследование фармакокинетики и метаболизма прогестона у здоровых женщин-добровольцев после однократного перорального приема 1 мг прогестона I Гуалано В., 1 Женето А., И Чассар Д., И Фордэм П., 2 Шац Б. И Астер-Цефак, 3/5 , Rue Eugene Millon, 75015 Париж, Франция 2Laboratoire Aventis, 46 Quai De La Rapee, F-75601 Paris Cedex 12, Франция. 12 здоровым женщинам в пременопаузе была назначена однократная пероральная доза прогестона в дозе 1 мг (Surgestonee, 2x0,5 мг). Целью было определить концентрации прогестона и его метаболитов, а также их фармакокинетические параметры. Образцы крови и мочи контролировались в течение 96 часов после введения дозы. Чтобы избежать какого-либо вмешательства в естественные гормоны, прогестон давали между 7 и 10 днями менструального цикла. Клиническая безопасность и переносимость были хорошими. Большинство наблюдаемых незначительных нежелательных явлений были оценены как возможно связанные с исследуемым препаратом (нарушения менструального цикла), поскольку классически они связаны с терапией прогестинами. Кроме того, не наблюдалось никаких клинически значимых биологических модификаций. Наблюдался стереоселективный метаболизм прогестона в пользу 21S гидроксипрогестона, основного циркулирующего соединения в плазме (соотношение AUC 5/R около 21). Уровни 21S гидроксипрогестона примерно в два раза выше, чем уровни неизмененного прогестона. Уровни второго метаболита, т.е. 21R гидроксипрогестона, в плазме значительно ниже уровней прогестона и 21S гидроксипрогестона. Промегестон, 215 гидрокси- и 21R гидроксипрогестон не выводятся с мочой. Около 3% дозы обнаруживалось в моче в виде сульфо- и/или глюкуроконъюгата 21S гидроксипрогестона и около 1% дозы в виде сульфо- и/или глюкуроконъюгата 21R гидроксипрогестона.
- ^ Jump up to: а б Виннекер Р.К., Битран Д., Чжан З. (ноябрь 2003 г.). «Доклиническая биология нового мощного и селективного прогестина: тримегестона». Стероиды . 68 (10–13): 915–920. дои : 10.1016/s0039-128x(03)00142-9 . ПМИД 14667983 . S2CID 24893971 .
- ^ Jump up to: а б с д и ж г Элкс Дж. (14 ноября 2014 г.). Словарь лекарств: Химические данные: Химические данные, структуры и библиография . Спрингер. стр. 1026–. ISBN 978-1-4757-2085-3 .
- ^ Jump up to: а б Филибер Д., Рейно Дж. П. (июль 1973 г.). «Связывание прогестерона в незрелой матке мыши и крысы». Стероиды . 22 (1): 89–98. дои : 10.1016/0039-128x(73)90073-1 . ПМИД 4353432 .
- ^ Jump up to: а б с д Издательство Уильяма Эндрю (22 октября 2013 г.). Энциклопедия фармацевтического производства, 3-е издание . Эльзевир. стр. 2935–36. ISBN 978-0-8155-1856-3 .
- ^ Jump up to: а б с д и ж г Index Nominum 2000: Международный каталог лекарств . Тейлор и Фрэнсис. Январь 2000 г., стр. 883–. ISBN 978-3-88763-075-1 .
- ^ Jump up to: а б Рейно Дж.П., Оджасу Т., Ваше В. (1981). «Стабильные и специфические трассеры». Репродуктивные процессы и контрацепция . Биохимическая эндокринология. Спрингер. стр. 163–179. дои : 10.1007/978-1-4684-3824-6_7 . ISBN 978-1-4684-3826-0 .
- ^ Узан С, Денис С, Поми В, Варин С (февраль 1992 г.). «Двойное слепое исследование прогестона (R 5020) и линестренола при лечении доброкачественных заболеваний молочной железы» . Европейский журнал акушерства, гинекологии и репродуктивной биологии . 43 (3): 219–227. дои : 10.1016/0028-2243(92)90177-з . ПМИД 1563574 .
- ^ Гурди П., Бачело А., Катто-Жонар С., Шаббер-Бюффе Н., Кристин-Мэтр С., Конард Дж. и др. (ноябрь 2012 г.). «Гормональная контрацепция у женщин с риском сосудистых и метаболических нарушений: рекомендации Французского общества эндокринологии». Анналы эндокринологии . 73 (5): 469–487. дои : 10.1016/j.ando.2012.09.001 . ПМИД 23078975 .
- ^ Член парламента Блэнтона, Се Ю, Данготт Л.Дж., Коэн Дж.Б. (февраль 1999 г.). «Стероид промегестон является неконкурентным антагонистом никотинового ацетилхолинового рецептора Торпедо, который взаимодействует с границей раздела липид-белок». Молекулярная фармакология . 55 (2): 269–278. дои : 10.1124/моль.55.2.269 . ПМИД 9927618 . S2CID 491327 .
- ^ Чан Д.В., Слонуайт В.Р. (май 1977 г.). «Связывание синтетического прогестина R5020 с транскортином и сывороточным альбумином». Журнал клинической эндокринологии и метаболизма . 44 (5): 983–985. doi : 10.1210/jcem-44-5-983 . ПМИД 858781 .
- ^ Jump up to: а б Литвак Г. (2 декабря 2012 г.). Биохимическое действие гормонов . Эльзевир. стр. 314–. ISBN 978-0-323-15344-7 .
- ^ Карп HJ (9 апреля 2015 г.). Прогестагены в акушерстве и гинекологии . Спрингер. стр. 34–. ISBN 978-3-319-14385-9 .
Дальнейшее чтение
[ редактировать ]- Рейно Дж.П., Оджасу Т. (1983). «[Промегестон, новый прогестин]». Журнал гинекологии, акушерства и репродуктивной биологии (на французском языке). 12 (7): 697–710. ПМИД 6366037 .
- Брун Дж., Дарджент Д., Понтонье Дж., Петреску Л. (май 1984 г.). «[Клиническое использование прогестона, гестагенного агента с высокой специфичностью к рецепторам]». Французский обзор гинекологии и акушерства (на французском языке). 79 (5): 423–426. ПМИД 6396815 .