Этинодиола диацетат
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Овулен, Демулен и другие. |
| Другие имена | этинодиола диацетат; Норэтиндрола диацетат; 3β-гидроксинорэтистерона 3β,17β-диацетат; [ 1 ] 17α-этинилэстр-4-ен-3β,17β-диилдиацетат; CB-8080; СК-11800 |
| Данные лицензии | |
| Беременность категория |
|
| Маршруты администрация | Через рот |
| Класс препарата | прогестаген ; Прогестин ; Сложный эфир прогестагена |
| код АТС | |
| Юридический статус | |
| Юридический статус | |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| КЭБ | |
| ХЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.005.496 |
| Химические и физические данные | |
| Формула | С 24 Н 32 О 4 |
| Молярная масса | 384.516 g·mol −1 |
| 3D model ( JSmol ) | |
Диацетат этинодиола , или диацетат этинодиола под торговой маркой Ovulen , продаваемый , среди прочего, , представляет собой прогестиновый препарат, который используется в противозачаточных таблетках . [ 4 ] [ 5 ] [ 6 ] Препарат доступен только в сочетании с эстрогеном . [ 7 ] Его принимают внутрь . [ 8 ]
Этинодиола диацетат представляет собой прогестин или синтетический прогестаген и, следовательно, является агонистом рецептора прогестерона , биологической мишени прогестагенов, таких как прогестерон . [ 9 ] [ 10 ] Он обладает слабой андрогенной и эстрогенной активностью и не имеет другой важной гормональной активности. [ 11 ] [ 12 ] [ 13 ] Лекарство представляет собой пролекарство норэтистерона этинодиол в организме, а выступает в качестве промежуточного продукта . [ 9 ] [ 10 ] [ 14 ]
Родственное соединение этинодиол было открыто в 1954 году, а диацетат этинодиола был введен для медицинского применения в 1965 году. [ 15 ] [ 16 ] Комбинация этинодиола с местранолом (Овулен) была одобрена для медицинского применения в США в 1966 году. [ 17 ] Комбинация этинилэстрадиола с этинодиолом (демулен) была одобрена для медицинского применения в США в 1970 году. [ 18 ]
В 2021 году комбинация с этинилэстрадиолом заняла 276-е место среди наиболее часто назначаемых лекарств в США: было выписано более 800 000 рецептов. [ 19 ] [ 20 ]
Медицинское использование
[ редактировать ]Диацетат этинодиола используется в сочетании с эстрогенами, такими как этинилэстрадиол или местранол, в комбинированных пероральных контрацептивах для женщин для предотвращения беременности. [ 8 ]
Побочные эффекты
[ редактировать ]Фармакология
[ редактировать ]
этинодиола практически неактивен с точки зрения сродства к рецепторам прогестерона и андрогенов и действует как быстро превращающееся пролекарство норэтистерона Диацетат , при этом этинодиол выступает в качестве промежуточного продукта . [ 9 ] [ 10 ] [ 14 ] При пероральном приеме и во время метаболизма первого прохождения в печени диацетат этинодиола быстро превращается под действием эстераз в этинодиол. [ 14 ] за которым следует оксигенация C3 гидроксильной группы с образованием норэтистерона. [ 10 ] Помимо прогестагенной активности, этинодиола диацетат обладает слабой андрогенной активностью. [ 11 ] [ 12 ] и, в отличие от большинства прогестинов, но подобно норэтистерону и норетинодрелу , [ 21 ] также обладает некоторой эстрогенной активностью. [ 12 ] [ 13 ]
диацетата . Проведен обзор фармакокинетики этинодиола [ 22 ]
Химия
[ редактировать ]Диацетат этинодиола, также известный как 3β-гидрокси-17α-этинил-19-нортестостерона 3β,17β-диацетат, 3β-гидроксинорэтистерона 3β,17β-диацетат или 17α-этинилэстр-4-ен-3β,17β-диол 3β,17β- — синтетический эстрановый стероид , производное тестостерона . диацетат [ 1 ] [ 5 ] [ 6 ] В частности, это производное 19-нортестостерона и 17α-этинилтестостерона или норэтистерона (17α-этинил-19-нортестостерона), в котором кетоновая группа C3 дегидрирована , а к C3β C3β в гидроксильную группу ацетатные эфиры присоединены . и положения C17β. [ 5 ] [ 6 ] Диацетат этинодиола представляет собой 3β,17β- диацетатный эфир этинодиола (17α-этинилэстр-4-ен-3β,17β - диол). [ 5 ] [ 6 ]
Синтез
[ редактировать ]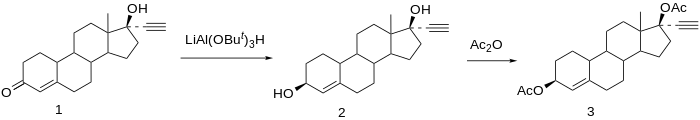
химического синтеза диацетата этинодиола. Опубликованы результаты [ 22 ]
Восстановление норэтистерона ( 1 ) дает 3,17-диол. Желаемым продуктом является 3β-гидроксисоединение; поскольку реакции при C3 не проявляют почти такой же стереоселективности , как реакции при C17, из-за относительного отсутствия стереонаправляющих ближайших заместителей, образование желаемого изомера достигается за счет использования объемистого восстановителя, три-трет-бутоксиалюмогидрида лития. . Ацетилирование 3β,17β-диола дает диацетат этинодиола ( 3 ). [ 23 ]
История
[ редактировать ]Этинодиол был впервые синтезирован в 1954 году путем восстановления норэтистерона , а диацетат этинодиола был введен для медицинского использования в 1965 году. [ 15 ] [ 16 ]
Общество и культура
[ редактировать ]Общие имена
[ редактировать ]Диацетат этинодиола — это непатентованное название препарата ( INN Tooltip его свободной спиртовой формы — этинодиол), тогда как диацетат этинодиола — это США , одобренное , и JAN . [ 5 ] [ 6 ] [ 7 ] Он также известен под своими прежними кодовыми названиями CB-8080 и SC-11800. [ 5 ] [ 6 ] [ 7 ]
Названия брендов
[ редактировать ]Диацетат этинодиола продается или продается под торговыми марками, включая Conova, Continuin, Demulen, [ 18 ] [ 25 ] Femulen, Kelnor, [ 3 ] [ 25 ] Ло-Мальморед, [ 26 ] Лютеонорм, Луто-Метродиол, Мальморед, [ 27 ] Метродиол, Овулен, [ 17 ] [ 25 ] Солуна, Зовия, [ 2 ] и другие. [ 5 ] [ 6 ] [ 7 ]
Доступность
[ редактировать ]Диацетат этинодиола продается лишь в нескольких странах, включая США, Канаду, Аргентину и Оман. [ 7 ]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б Шиндлер А.Е., Кампаньоли С., Друкманн Р., Хубер Дж., Паскуалини Дж.Р., Швеппе К.В. и др. (декабрь 2003 г.). «Классификация и фармакология прогестинов». Матуритас . 46 (Приложение 1): С7–С16. дои : 10.1016/зрелость.2003.09.014 . ПМИД 14670641 .
- ^ Перейти обратно: а б «Зовия 1/35-набор в таблетках этинодиола диацетата и этинилэстрадиола» . Архивировано из оригинала 28 сентября 2022 года . Проверено 20 января 2024 г.
- ^ Перейти обратно: а б «Келнор 1/35-набор этинодиолдиацетата и этинилэстрадиола» . Архивировано из оригинала 29 марта 2023 года . Проверено 20 января 2024 г.
- ^ Шупе Д., Хазелтин Ф.П. (6 декабря 2012 г.). Контрацепция . Springer Science & Business Media. стр. 21–. ISBN 978-1-4612-2730-4 .
- ^ Перейти обратно: а б с д и ж г Элкс Дж. (14 ноября 2014 г.). Словарь лекарств: Химические данные: Химические данные, структуры и библиография . Спрингер. стр. 522–. ISBN 978-1-4757-2085-3 .
- ^ Перейти обратно: а б с д и ж г Список названий 2000 г.: Международный каталог лекарств . Тейлор и Фрэнсис США. 2000. с. 422. ИСБН 978-3-88763-075-1 . Проверено 30 мая 2012 г.
- ^ Перейти обратно: а б с д и «Этинодиол» . Наркотики.com . Архивировано из оригинала 5 февраля 2018 года . Проверено 4 февраля 2018 г.
- ^ Перейти обратно: а б Блюм RW (22 октября 2013 г.). Здравоохранение подростков: клинические проблемы . Эльзевир Наука. стр. 216–. ISBN 978-1-4832-7738-7 .
- ^ Перейти обратно: а б с Хаммерштейн Дж. (декабрь 1990 г.). «Пролекарства: преимущество или недостаток?». Американский журнал акушерства и гинекологии . 163 (6, ч. 2): 2198–2203. дои : 10.1016/0002-9378(90)90561-К . ПМИД 2256526 .
- ^ Перейти обратно: а б с д Рабочая группа МАИР по оценке канцерогенных рисков для человека, Всемирная организация здравоохранения, Международное агентство по исследованию рака (2007). Комбинированные эстроген-прогестагенные контрацептивы и комбинированная эстроген-прогестагенная менопаузальная терапия . Всемирная организация здравоохранения. стр. 146–. ISBN 978-92-832-1291-1 .
- ^ Перейти обратно: а б Ташджян А.Х., Армстронг Э.Дж. (21 июля 2011 г.). Принципы фармакологии: патофизиологические основы лекарственной терапии . Липпинкотт Уильямс и Уилкинс. стр. 523–. ISBN 978-1-4511-1805-6 . Архивировано из оригинала 11 января 2023 года . Проверено 11 октября 2016 г.
- ^ Перейти обратно: а б с Беккер К.Л. (24 апреля 2001 г.). Принципы и практика эндокринологии и обмена веществ . Липпинкотт Уильямс и Уилкинс. п. 1004. ИСБН 978-0-7817-1750-2 . Проверено 30 мая 2012 г.
- ^ Перейти обратно: а б Горолл А.Х., Mulley AG (27 января 2009 г.). Медицина первичной медико-санитарной помощи: кабинетная оценка и ведение взрослого пациента . Липпинкотт Уильямс и Уилкинс. п. 876. ИСБН 978-0-7817-7513-7 . Проверено 30 мая 2012 г.
- ^ Перейти обратно: а б с Станчик ФЗ (сентябрь 2002 г.). «Фармакокинетика и эффективность прогестинов, используемых для заместительной гормональной терапии и контрацепции». Обзоры по эндокринным и метаболическим расстройствам . 3 (3): 211–224. дои : 10.1023/А:1020072325818 . ПМИД 12215716 . S2CID 27018468 .
- ^ Перейти обратно: а б Петров В. (1971). «Средства против бесплодия» . Прогресс медицинской химии . 8 (2): 171–229. дои : 10.1016/s0079-6468(08)70130-9 . ISBN 9780408703147 . ПМИД 4947236 .
- ^ Перейти обратно: а б Издательство Уильяма Эндрю (22 октября 2013 г.). Энциклопедия фармацевтического производства, 3-е издание . Эльзевир. стр. 1516–. ISBN 978-0-8155-1856-3 . Архивировано из оригинала 20 января 2024 года . Проверено 4 февраля 2018 г.
- ^ Перейти обратно: а б «Овулен: препараты, одобренные FDA» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . Архивировано из оригинала 8 декабря 2022 года . Проверено 20 января 2024 г.
- ^ Перейти обратно: а б «Демулен: препараты, одобренные FDA» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . Архивировано из оригинала 10 мая 2021 года . Проверено 20 января 2024 г.
- ^ «Топ-300 2021 года» . КлинКальк . Архивировано из оригинала 15 января 2024 года . Проверено 14 января 2024 г.
- ^ «Этинилэстрадиол; Этинодиол - Статистика употребления лекарств» . КлинКальк . Архивировано из оригинала 18 января 2024 года . Проверено 14 января 2024 г.
- ^ Руннебаум БК, Рабе Т, Кизель Л (6 декабря 2012 г.). Женская контрацепция: последние новости и тенденции . Springer Science & Business Media. стр. 36–. ISBN 978-3-642-73790-9 .
- ^ Перейти обратно: а б Конституция J (27 ноября 2013 г.). «Свойства прогестагенов» . Справочник по экспериментальной фармакологии . Чам: Спрингер Верлаг. стр. 14–15, 286. ISBN. 978-3-642-99941-3 .
- ^ Перейти обратно: а б Климстра П.Д., Колтон Ф.Б. (октябрь 1967 г.). «Синтез 3бета-гидроксиэстр-4-ен-17-она и 3бета-гидроксиандрост-4-ен-17-она». Стероиды . 10 (4): 411–424. дои : 10.1016/0039-128X(67)90119-5 . ПМИД 6064262 .
- ^ Сондхаймер Ф, Клибански Ю (1959). «Синтез 3β-гидроксианалогов стероидных гормонов — биологически активного класса соединений». Тетраэдр . 5 : 15–26. дои : 10.1016/0040-4020(59)80066-1 .
- ^ Перейти обратно: а б с «Эстроген и прогестин (оральные контрацептивы)» . Архивировано из оригинала 18 января 2024 года . Проверено 20 января 2024 г.
- ^ «Ло-Мальморед» . Архивировано из оригинала 24 марта 2021 года . Проверено 20 января 2024 г.
- ^ «Мальморед» . Архивировано из оригинала 1 октября 2023 года . Проверено 20 января 2024 г.