Катехин
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК (2R , 3S ) -2-(3,4-Дигидроксифенил)-3,4-дигидро- 2H- хромен-3,5,7-триол | |
| Другие имена Цианиданол Цианиданол (+)-катехин D-Катехин Катехиновая кислота Катеховая кислота Цианидол Дексианиданол (2R , 3S ) -Катехин 2,3- транс -Катехин (2R , 3S ) -Флаван-3,3',4',5,7-пентол | |
| Идентификаторы | |
| |
3D model ( JSmol ) | |
| 3DMeet | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.005.297 |
| Номер ЕС |
|
| КЕГГ | |
ПабХим CID | |
| НЕКОТОРЫЙ |
|
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 15 Н 14 О 6 | |
| Молярная масса | 290.271 g·mol −1 |
| Появление | Бесцветное твердое вещество |
| Температура плавления | От 175 до 177 ° C (от 347 до 351 ° F; от 448 до 450 К) |
| УФ-видимое излучение (λ макс .) | 276 нм |
Хиральное вращение ([α] D ) | +14.0° |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности | Мутагенен для соматических клеток млекопитающих, мутагенен для бактерий и дрожжей. |
| СГС Маркировка : | |
 | |
| Предупреждение | |
| Х315 , Х319 , Х335 | |
| P261 , P264 , P271 , P280 , P302+P352 , P304+P340 , P305+P351+P338 , P312 , P321 , P332+P313, P337+P313 P362 , P403 , P301 , P403+P233 , P405, P5013 +P233, P405, P501, P501, P501 , , P362 , P403+P233, P3 | |
| Летальная доза или концентрация (LD, LC): | |
ЛД 50 ( средняя доза ) | (+)-катехин: 10 000 мг/кг у крыс (RTECS) 10 000 мг/кг у мышей 3890 мг/кг у крыс (другой источник) |
| Паспорт безопасности (SDS) | научная лаборатория AppliChem [ постоянная мертвая ссылка ] |
| Фармакология | |
| Оральный | |
| Фармакокинетика : | |
| Моча | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
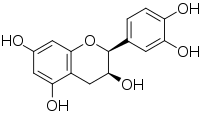
Катехин / ˈ k æ t ɪ tʃ ɪ n / представляет собой флаван-3-ол , тип вторичного метаболита, обеспечивающего антиоксидантную роль в растениях . Он принадлежит к подгруппе полифенолов, называемых флавоноидами .
Название химического семейства катехинов происходит от слова «катеху» , которое представляет собой дубильный сок или вареный экстракт мимозы катеху ( Acacia catechu Lf). [1]
Химия
[ редактировать ]
Катехин имеет два бензольных кольца (называемые кольцами A и B) и дигидропирановый гетероцикл (кольцо C) с гидроксильной группой на углероде 3. Кольцо A похоже на фрагмент резорцина , а кольцо B похоже на фрагмент катехола . имеются два хиральных В молекуле центра на атомах углерода 2 и 3. Следовательно, она имеет четыре диастереоизомера . Два изомера находятся в транс -конфигурации и называются катехинами , а два других находятся в цис- конфигурации и называются эпикатехинами .
Наиболее распространенным изомером катехина является (+)-катехин. Другой стереоизомер представляет собой (-)-катехин или энт -катехин. Наиболее распространенным изомером эпикатехина является (-)-эпикатехин (также известный под названиями L -эпикатехин, эпикатехин, (-)-эпикатехин, L -акакатехин, L -эпикатехин, эпикатехин, 2,3- цис -эпикатехин или (2 R) ,3 R )-(-)-эпикатехин).
Различные эпимеры можно разделить с помощью хиральной колоночной хроматографии . [2]
Не имея ссылки на какой-либо конкретный изомер, молекулу можно назвать просто катехином. Смеси различных энантиомеров можно назвать (±)-катехином или DL -катехином и (±)-эпикатехином или DL -эпикатехином.
Катехин и эпикатехин являются строительными блоками проантоцианидинов , разновидности конденсированных танинов.
- Галерея диастереоизомеров
- (+)-катехин ( 2R , 3S )
- (-)-катехин ( 2S , 3R )
- (-)-эпикатехин ( 2R , 3R )
- (+)-эпикатехин ( 2S , 3S )

Более того, гибкость C-кольца позволяет иметь две конформационные изомеры , помещая B-кольцо либо в псевдоэкваториальное положение (E-конформер), либо в псевдоаксиальное положение (A-конформер). Исследования подтвердили, что (+)-катехин принимает смесь А- и Е-конформеров в водном растворе, и их конформационное равновесие оценивается как 33:67. [3]
Как флавоноиды, катехины могут действовать как антиоксиданты в высоких концентрациях in vitro , но по сравнению с другими флавоноидами их антиоксидантный потенциал низок. [4] Способность тушить синглетный кислород, по-видимому, связана с химической структурой катехина, наличием катехинового фрагмента в кольце B и наличием гидроксильной группы, активирующей двойную связь в кольце C. [5]
Окисление
[ редактировать ]Электрохимические эксперименты показывают, что механизм окисления (+)-катехина протекает в последовательные стадии, связанные с катехоловыми и резорциновыми группами, и окисление зависит от pH. Окисление катехол-3',4'-дигидроксиэлектронодонорных групп происходит сначала при очень низких положительных потенциалах и является обратимой реакцией. Показано, что гидроксильные группы окисляющегося впоследствии резорцинового фрагмента вступают в необратимую реакцию окисления. [6]
Система лакказа / ABTS окисляет (+)-катехин до олигомерных продуктов. [7] которого является проантоцианидин А2 димером .
Спектральные данные
[ редактировать ]
| УФ-Вид | |
|---|---|
| Лямбда-макс : | 276 нм |
| Коэффициент затухания (log ε ) | 4.01 |
| И | |
| Основные полосы поглощения | 1600 см −1 (бензольные кольца) |
| ЯМР | |
| Протонный ЯМР
| д : 2,49 (1H, дд, J = 16,0, 8,6 Гц, H-4а), |
| ЯМР углерода-13 | |
| Другие данные ЯМР | |
| РС | |
| Массы основные фрагменты | ЭСИ-МС [М+Н] + м / з : 291,0
|
Природные явления
[ редактировать ](+)-Катехин и (-)-эпикатехин, а также их конъюгаты с галловой кислотой являются повсеместными компонентами сосудистых растений и частыми компонентами традиционных растительных лекарственных средств , таких как Uncaria rhynchophylla . Эти два изомера в основном встречаются в составе какао и чая , а также в Vitis vinifera . винограде [9] [10] [11]
В еде
[ редактировать ]Основными диетическими источниками катехинов в Европе и США являются чай и семечковые плоды. [12] [13]
Катехины и эпикатехины содержатся в какао . [14] который, согласно одной из баз данных, имеет самое высокое содержание (108 мг/100 г) катехинов среди проанализированных продуктов, за ним следует черносливовый сок (25 мг/100 мл) и стручок фасоли (16 мг/100 г). [15] Масло асаи , полученное из плодов пальмы асаи ( Euterpe oleracea ), содержит (+)-катехины (67 мг/кг). [16]
Катехины разнообразны в продуктах питания, [15] из персиков [17] зеленый чай и уксус . [15] [18] Катехины содержатся в зерне ячменя , где они являются основным фенольным соединением, ответственным за изменение цвета теста . [19] Вкус мономерного (+)-катехина или (-)-эпикатехина описывается как слегка вяжущий , но не горький. [20]
Метаболизм
[ редактировать ]Биосинтез
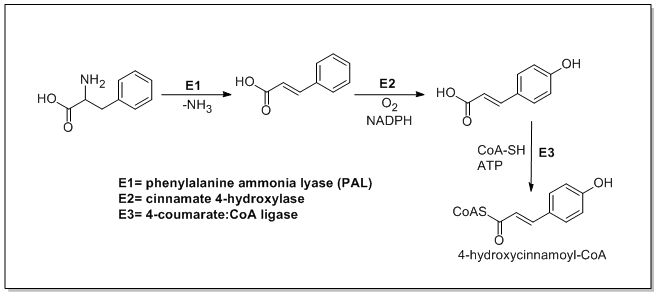
[ редактировать ]Биосинтез катехина начинается с стартовой единицы 4-гидроксициннамоил-КоА , цепь которой удлиняется за счет добавления трех малонил-КоА по пути PKSIII. 4-Гидроксициннамоил-КоА биосинтезируется из L -фенилаланина по шикиматному пути. L -фенилаланин сначала дезаминируется фенилаланин-аммиаклиазой (PAL), образуя коричную кислоту, которая затем окисляется до 4-гидроксикоричной кислоты циннамат-4-гидроксилазой. Халконсинтаза затем катализирует конденсацию 4-гидроксикоричного КоА и трех молекул малонил-КоА с образованием халкона . Затем халкон изомеризуется в нарингенин халконизомеразой, которая окисляется до эриодиктиола флавоноид-3'-гидроксилазой и далее окисляется до таксифолина флаванон-3-гидроксилазой. Затем таксифолин восстанавливается дигидрофлаванол-4-редуктазой и лейкоантоцианидинредуктазой с образованием катехина. Биосинтез катехина показан ниже. [21] [22] [23]
Лейкоцианидинредуктаза (LCR) использует 2,3- транс -3,4- цис - лейкоцианидин для производства (+)-катехина и является первым ферментом специфического пути проантоцианидина (PA). Его активность была измерена в листьях, цветах и семенах бобовых Medicago sativa , Lotus japonicus , Lotus uliginosus , Hedysarumulfurescens и Robinia pseudoacacia . [24] Фермент также присутствует в Vitis vinifera (виноград). [25]
Биодеградация
[ редактировать ]Катехиноксигеназа, ключевой фермент расщепления катехина, присутствует в грибах и бактериях. [26]
Среди бактерий деградацию (+)-катехина может осуществлять Acinetobacter Calcoaceticus . Катехин метаболизируется до протокатехиновой кислоты (PCA) и флороглюцинолкарбоновой кислоты (PGCA). [27] Он также разлагается Bradyrhizobium japonicum . Флороглюцинкарбоновая кислота далее декарбоксилируется до флороглюцинола , который дегидроксилируется до резорцина . Резорцин гидроксилируется до гидроксихинола . Протокатеховая кислота и гидроксихинол подвергаются итрадиоловому расщеплению с помощью протокатехоат-3,4-диоксигеназы и гидроксихинол-1,2-диоксигеназы с образованием β-карбоксицис , цис - муконовой кислоты. и малеилацетат . [28]
Среди грибов разложение катехина может осуществляться Chaetomium cupreum . [29]
Метаболизм у человека
[ редактировать ]

Катехины метаболизируются при поступлении из желудочно-кишечного тракта , особенно тощей кишки . [31] и в печени , что приводит к образованию так называемых структурно родственных метаболитов эпикатехина (SREM). [32] Основными путями метаболизма SREM являются глюкуронидация , сульфатирование и метилирование катехоловой , при этом в плазме группы катехол-О-метилтрансферазой обнаруживаются лишь небольшие количества. [33] [30] Однако большинство пищевых катехинов метаболизируются микробиомом толстой кишки до гамма-валеролактонов и гиппуровых кислот , которые подвергаются дальнейшей биотрансформации , глюкуронидации , сульфатированию и метилированию в печени . [33]
Стереохимическая конфигурация катехинов оказывает сильное влияние на их усвоение и метаболизм, поскольку поглощение является самым высоким для (-)-эпикатехина и самым низким для (-)-катехина. [34]
Биотрансформация
[ редактировать ]Биотрансформация (+)-катехина в таксифолин путем двухстадийного окисления может быть достигнута Burkholderia sp. [35]
(+)-Катехин и (-)-эпикатехин трансформируются эндофитным нитчатым грибом Diaporthe sp. на производные 3,4-цис-дигидроксифлавана, (+)-(2R , 3S , 4S ) -3,4,5,7,3',4'-гексагидроксифлаван (лейкоцианидин) и (-)-( 2 R ,3 R ,4 R )-3,4,5,7,3',4'-гексагидроксифлаван соответственно, тогда как (-)-катехин и (+)-эпикатехин с (2 S )-фенильной группой сопротивлялись биоокисление. [36]
Лейкоантоцианидинредуктаза (LAR) использует (2R , 3S ) -катехин, НАДФ. + и H 2 O с образованием 2,3- транс -3,4- цис - лейкоцианидина , НАДФН и H + . Экспрессия его гена изучалась при выращивании виноградных ягод и листьев виноградной лозы. [37]
Гликозиды
[ редактировать ]- (2R , 3S ) -Катехин-7 -О -β- D -глюкопиранозид можно выделить из ячменя ( Hordeum vulgare L.) и солода. [38]
- Эпигеозид (катехин-3- О -α- L -рамнопиранозил-(1–4)-β- D -глюкопиранозил-(1–6)-β- D -глюкопиранозид) можно выделить из корневищ Epigynum auritum . [39]
Исследовать
[ редактировать ]
Сосудистая функция
[ редактировать ]Лишь ограниченные данные диетических исследований указывают на то, что катехины могут влиять на эндотелий -зависимую вазодилатацию , которая может способствовать нормальной регуляции кровотока у людей. [40] [41] Катехины зеленого чая могут улучшить кровяное давление, особенно когда систолическое кровяное давление превышает 130 мм рт. ст. [42] [43]
Из-за интенсивного метаболизма в процессе пищеварения судьба и активность метаболитов катехинов, ответственных за такое воздействие на кровеносные сосуды, а также фактический механизм действия неизвестны. [33] [44]
Побочные эффекты
[ редактировать ]Катехин и его метаболиты могут прочно связываться с эритроцитами и тем самым вызывать выработку аутоантител , что приводит к гемолитической анемии и почечной недостаточности . [45] Это привело к отмене катехинсодержащего препарата Катерген, используемого для лечения вирусного гепатита . [46] с рынка в 1985 году. [47]
Катехины зеленого чая могут быть гепатотоксичными [48] а Европейское управление по безопасности пищевых продуктов рекомендовало не превышать 800 мг в день. [49]
Другой
[ редактировать ]Один ограниченный метаанализ показал, что увеличение потребления зеленого чая и содержащихся в нем катехинов до семи чашек в день привело к небольшому снижению заболеваемости раком простаты . [50] Методы наночастиц находятся на стадии предварительных исследований в качестве потенциальных систем доставки катехинов. [51]
Ботанические эффекты
[ редактировать ]Катехины, выделяемые в землю некоторыми растениями, могут препятствовать росту соседей — это форма аллелопатии . [52] Centaurea maculosa , василек пятнистый, который часто изучают на предмет такого поведения, выделяет изомеры катехина в землю через свои корни, потенциально оказывая действие антибиотика или гербицида . Одна из гипотез заключается в том, что он заставляет волну активных форм кислорода проходить через корень целевого растения, убивая клетки корня путем апоптоза . [53] Большинство растений в европейской экосистеме обладают защитой от катехина, но лишь немногие растения защищены от него в экосистеме Северной Америки, где Centaurea maculosa является инвазивным и неконтролируемым сорняком. [52]
Катехин действует как фактор, ингибирующий инфекцию, в листьях клубники. [54] Эпикатехин и катехин могут предотвратить болезнь кофейных ягод, ингибируя аппрессорную меланизацию Colletotrichum kahawae . [55]
Ссылки
[ редактировать ]- ^ «Происхождение растений катча и катеху» . Продовольственная и сельскохозяйственная организация Объединенных Наций. 5 ноября 2011 г. Архивировано из оригинала 10 февраля 2019 г. . Проверено 26 июля 2016 г.
- ^ Ринальдо Д., Батиста Х.М., Родригес Х., Бенфатти А.С., Родригес К.М., душ Сантос Л.К. и др. (август 2010 г.). «Определение диастереомеров катехина из листьев видов Byrsonima с использованием хиральной ВЭЖХ-PAD-CD». Хиральность . 22 (8): 726–733. дои : 10.1002/чир.20824 . ПМИД 20143413 .
- ^ Крис З., Коча Дж., Имберти А., Шарло А., Озели-Велти Р. (июль 2003 г.). «Исследование комплексообразования (+)-катехина с бета-циклодекстрином с помощью сочетания методов ЯМР, микрокалориметрии и методов молекулярного моделирования». Органическая и биомолекулярная химия . 1 (14): 2590–2595. дои : 10.1039/B302935M . ПМИД 12956082 .
- ^ Пиетта П.Г. (июль 2000 г.). «Флавоноиды как антиоксиданты». Журнал натуральных продуктов . 63 (7): 1035–1042. дои : 10.1021/np9904509 . ПМИД 10924197 . S2CID 23310671 .
- ^ Турнер С, Кру С., Моретт М.Т., Бек И., Хоко М., Браун А.М., Оливерос Э. (август 1993 г.). «Антиоксидантная активность флавоноидов: эффективность синглетного кислорода ( 1 Δg 10.1016 / ) тушение». Журнал фотохимии и фотобиологии. B, Biology . 19 (3): 205–215. doi : 1011-1344(93)87086-3 . PMID 8229463 .
- ^ Жанейро П., Оливейра Бретт AM (2004). «Механизмы электрохимического окисления катехинов». Аналитика Химика Акта . 518 (1–2): 109–115. дои : 10.1016/j.aca.2004.05.038 . hdl : 10316/5128 .
- ^ Осман А.М., Вонг К.К., Фернихоу А. (апрель 2007 г.). «Система лакказа/ABTS окисляет (+)-катехин до олигомерных продуктов». Ферментные и микробные технологии . 40 (5): 1272–1279. doi : 10.1016/j.enzmictec.2006.09.018 .
- ^ Линь Ю.П., Чен Т.Ю., Ценг Х.В., Ли М.Х., Чен С.Т. (июнь 2009 г.). «Защитные соединения для нервных клеток, выделенные из Phoenix hanceana var. formosana». Фитохимия . 70 (9): 1173–1181. Бибкод : 2009PChem..70.1173L . doi : 10.1016/j.phytochem.2009.06.006 . ПМИД 19628235 . S2CID 28636157 .
- ^ Айспуруа-Олайсола О, Ормазабаль М, Вальехо А, Оливарес М, Наварро П, Эчебарриа Н, Усобиага А (январь 2015 г.). «Оптимизация сверхкритической жидкостной последовательной экстракции жирных кислот и полифенолов из отходов винограда Vitis vinifera». Журнал пищевой науки . 80 (1): Е101–Е107. дои : 10.1111/1750-3841.12715 . ПМИД 25471637 .
- ^ Фрейденберг К., Кокс Р.Ф., Браун Э. (1932). «Катехин какао-бобов1». Журнал Американского химического общества . 54 (5): 1913–1917. дои : 10.1021/ja01344a026 .
- ^ «Митиё Цудзимура (1888–1969)» . Архивировано из оригинала 21 ноября 2015 года . Проверено 10 ноября 2015 г.
- ^ Чун ОК, Чунг С.Дж., Сон ВО (май 2007 г.). «Оценочное потребление флавоноидов с пищей и основные источники пищи взрослого населения США» . Журнал питания . 137 (5): 1244–1252. дои : 10.1093/jn/137.5.1244 . ПМИД 17449588 .
- ^ Вогиацоглу А., Маллиган А.А., Лентьес М.А., Любен Р.Н., Спенсер Дж.П., Шретер Х. и др. (2015). «Потребление флавоноидов взрослыми европейцами (от 18 до 64 лет)» . ПЛОС ОДИН . 10 (5): e0128132. Бибкод : 2015PLoSO..1028132V . дои : 10.1371/journal.pone.0128132 . ПМЦ 4444122 . ПМИД 26010916 .
- ^ Квик-Урибе С., Бекташ Р.М. (2008). «Флаванолы какао - измерение, биодоступность и биологическая активность» (PDF) . Азиатско-Тихоокеанский журнал клинического питания . 17 (Приложение 1): 280–283. ПМИД 18296356 .
- ^ Jump up to: а б с «Полифенолы в настое зеленого чая» . Фенол-Эксплорер, v 3.5. 2014 . Проверено 1 ноября 2014 г.
- ^ Пачеко-Паленсия Л.А., Мертенс-Талкотт С., Талкотт С.Т. (июнь 2008 г.). «Химический состав, антиоксидантные свойства и термическая стабильность фитохимически обогащенного масла из Асаи ( Euterpe oleracea Mart.)». Журнал сельскохозяйственной и пищевой химии . 56 (12): 4631–4636. дои : 10.1021/jf800161u . ПМИД 18522407 .
- ^ Ченг Г.В., Крисосто Ч. (1995). «Потенциал потемнения, фенольный состав и полифенолоксидазная активность буферных экстрактов ткани кожицы персика и нектарина» . Журнал Американского общества садоводческих наук . 120 (5): 835–838. дои : 10.21273/JASHS.120.5.835 .
- ^ Гальвес MC, Баррозу CG, Перес-Бустаманте Х.А. (1994). «Анализ полифенольных соединений разных образцов уксуса». Журнал пищевых исследований и исследований . 199 (1): 29–31. дои : 10.1007/BF01192948 . S2CID 91784893 .
- ^ Квинде-Акстелл З., Байк Б.К. (декабрь 2006 г.). «Фенольные соединения зерна ячменя и их влияние на изменение цвета пищевых продуктов». Журнал сельскохозяйственной и пищевой химии . 54 (26): 9978–9984. дои : 10.1021/jf060974w . ПМИД 17177530 .
- ^ Килхорн, С.; Торнгейт, JH III (1999). «Ощущения во рту, связанные с флаван-3-олами (+)-катехином и (-)-эпикатехином». Качество и предпочтения продуктов питания . 10 (2): 109–116. дои : 10.1016/S0950-3293(98)00049-4 .
- ^ Рани А., Сингх К., Ахуджа П.С., Кумар С. (март 2012 г.). «Молекулярная регуляция биосинтеза катехинов в чае [ Camellia sinensis (L.) О. Кунце]». Джин . 495 (2): 205–210. дои : 10.1016/j.gene.2011.12.029 . ПМИД 22226811 .
- ^ Пуньясири П.А., Абейсингхе И.С., Кумар В., Трейтер Д., Дуй Д., Гош С. и др. (ноябрь 2004 г.). «Биосинтез флавоноидов в чайном растении Camellia sinensis: свойства ферментов основных путей эпикатехина и катехина». Архив биохимии и биофизики . 431 (1): 22–30. дои : 10.1016/j.abb.2004.08.003 . ПМИД 15464723 .
- ^ Дьюик ПМ (2009). Лекарственные натуральные продукты: биосинтетический подход (3-е изд.). Великобритания: Джон Уайли и сыновья. ISBN 978-0-470-74167-2 . [ нужна страница ]
- ^ Скадхауге Б., Грубер М.Ю., Томсен К.К., Фон Веттштайн Д. (апрель 1997 г.). «Активность лейкоцианидинредуктазы и накопление проантоцианидинов в развивающихся тканях бобовых». Американский журнал ботаники . 84 (4): 494–503. дои : 10.2307/2446026 . JSTOR 2446026 .
- ^ Може С., Гранье Т., д'Эстенто Б.Л., Гаргури М., Маниганд С., Шмиттер Дж.М. и др. (апрель 2010 г.). «Кристаллическая структура и каталитический механизм лейкоантоцианидинредуктазы Vitis vinifera». Журнал молекулярной биологии . 397 (4): 1079–1091. дои : 10.1016/j.jmb.2010.02.002 . ПМИД 20138891 .
- ^ Аруначалам, М.; Мохан Радж, М.; Мохан, Н.; Махадеван, А. (2003). «Биодеградация катехина» (PDF) . Труды Индийской национальной академии наук . Б69 (4): 353–370. Архивировано из оригинала (PDF) 16 марта 2012 г.
- ^ Аруначалам М., Мохан Н., Сугадев Р., Челлаппан П., Махадеван А. (июнь 2003 г.). «Деградация (+)-катехина под действием Acinetobacter Calcoaceticus MTC 127». Biochimica et Biophysical Acta (BBA) – Общие предметы . 1621 (3): 261–265. дои : 10.1016/S0304-4165(03)00077-1 . ПМИД 12787923 .
- ^ Хоппер В., Махадеван А. (1997). «Деградация катехина Bradyrhizobium japonicum ». Биодеградация . 8 (3): 159–165. дои : 10.1023/А:1008254812074 . S2CID 41221044 .
- ^ Самбандам Т., Махадеван А. (январь 1993 г.). «Деградация катехина, очистка и частичная характеристика катехиноксигеназы Chaetomium cupreum ». Всемирный журнал микробиологии и биотехнологии . 9 (1): 37–44. дои : 10.1007/BF00656513 . ПМИД 24419836 . S2CID 1257624 .
- ^ Jump up to: а б с д Оттавиани Дж.И., Борхес Дж., Момма Тай, Спенсер Дж.П., Кин С.Л., Крозье А., Шретер Х. (июль 2016 г.). «Метаболом [2- 14 C](-)-эпикатехин у человека: значение для оценки эффективности, безопасности и механизмов действия полифенольных биоактивных веществ» . Scientific Reports . 6 : 29034. Bibcode : 2016NatSR...629034O . doi : 10.1038/srep29034 . PMC 4929566 . ПМИД 27363516 .
- ^ Актис-Горетта Л., Левек А., Рейн М., Темл А., Шефер С., Хофманн У. и др. (октябрь 2013 г.). «Кишечная абсорбция, метаболизм и выведение (-)-эпикатехина у здоровых людей, оцененные с помощью метода кишечной перфузии» . Американский журнал клинического питания . 98 (4): 924–933. дои : 10.3945/ajcn.113.065789 . ПМИД 23864538 .
- ^ Оттавиани Дж.И., Момма Т.Я., Кунле Г.К., Кин С.Л., Шретер Х. (апрель 2012 г.). «Структурно родственные (-)-эпикатехиновые метаболиты у человека: оценка с использованием химически синтезированных de novo аутентичных стандартов» . Свободно-радикальная биология и медицина . 52 (8): 1403–1412. doi : 10.1016/j.freeradbiomed.2011.12.010 . ПМИД 22240152 .
- ^ Jump up to: а б с «Флавоноиды» . Институт Лайнуса Полинга, Университет штата Орегон, Корваллис. 2016 . Проверено 24 июля 2016 г.
- ^ Оттавиани Дж.И., Момма Т.Ю., Хейсс С., Квик-Урибе С., Шретер Х., Кин С.Л. (январь 2011 г.). «Стереохимическая конфигурация флаванолов влияет на уровень и метаболизм флаванолов у человека, а также на их биологическую активность in vivo». Свободно-радикальная биология и медицина . 50 (2): 237–244. doi : 10.1016/j.freeradbiomed.2010.11.005 . ПМИД 21074608 .
- ^ Мацуда М., Оцука Ю., Джин С., Васаки Дж., Ватанабэ Дж., Ватанабэ Т., Осаки М. (февраль 2008 г.). «Биотрансформация (+)-катехина в таксифолин путем двухэтапного окисления: первичная стадия метаболизма (+)-катехина новой (+)-катехин-деградирующей бактерией, Burkholderia sp. KTC-1, выделенной из тропического торфа» . Связь с биохимическими и биофизическими исследованиями . 366 (2): 414–419. дои : 10.1016/j.bbrc.2007.11.157 . ПМИД 18068670 .
- ^ Сибуя Х., Агуста А., Охаши К., Маэхара С., Симанджунтак П. (июль 2005 г.). «Биоокисление (+)-катехина и (-)-эпикатехина в производные 3,4-дигидроксифлавана эндофитным грибом Diaporthe sp., выделенным из чайного растения» . Химический и фармацевтический вестник . 53 (7): 866–867. дои : 10.1248/cpb.53.866 . ПМИД 15997157 .
- ^ Богс Дж., Дауни М.О., Харви Дж.С., Эштон А.Р., Таннер Г.Дж., Робинсон С.П. (октябрь 2005 г.). «Синтез проантоцианидина и экспрессия генов, кодирующих лейкоантоцианидинредуктазу и антоцианидинредуктазу, в развивающихся ягодах винограда и листьях виноградной лозы» . Физиология растений . 139 (2): 652–663. дои : 10.1104/стр.105.064238 . JSTOR 4281902 . ПМК 1255985 . ПМИД 16169968 .
- ^ Фридрих В., Галенса Р. (2002). «Идентификация нового флаванол-глюкозида из ячменя ( Hordeum vulgare L.) и солода». Европейские пищевые исследования и технологии . 214 (5): 388–393. дои : 10.1007/s00217-002-0498-x . S2CID 84221785 .
- ^ Джин QD, Му QZ (1991). «[Исследование гликозидных компонентов Epigynum auritum ]». Яо Сюэ Сюэ Бао (Acta Pharmaceutica Sinica) (на китайском языке). 26 (11): 841–845. ПМИД 1823978 .
- ^ Хупер Л., Кей С., Абдельхамид А., Крун П.А., Кон Дж.С., Римм Э.Б., Кэссиди А. (март 2012 г.). «Влияние шоколада, какао и флаван-3-олов на здоровье сердечно-сосудистой системы: систематический обзор и метаанализ рандомизированных исследований» . Американский журнал клинического питания . 95 (3): 740–751. дои : 10.3945/ajcn.111.023457 . ПМИД 22301923 .
- ^ Эллингер С., Ройш А., Штеле П., Хелфрих Х.П. (июнь 2012 г.). «Эпикатехин, поступающий с какао-продуктами, снижает кровяное давление у людей: модель нелинейной регрессии с байесовским подходом» . Американский журнал клинического питания . 95 (6): 1365–1377. дои : 10.3945/ajcn.111.029330 . ПМИД 22552030 .
- ^ Халеси С., Сан Дж., Байс Н., Джамшиди А., Никбахт-Насрабади Е., Хосрави-Бороужени Х. (сентябрь 2014 г.). «Катехины зеленого чая и артериальное давление: систематический обзор и метаанализ рандомизированных контролируемых исследований». Европейский журнал питания . 53 (6): 1299–1311. дои : 10.1007/s00394-014-0720-1 . ПМИД 24861099 . S2CID 206969226 .
- ^ Aprotosoaie AC, Мирон А, Трифан А, Лука В.С., Косташ II (декабрь 2016 г.). «Сердечно-сосудистые эффекты полифенолов какао — обзор» . Болезни . 4 (4): 39. doi : 10.3390/diseases4040039 . ПМЦ 5456324 . ПМИД 28933419 .
- ^ Шретер Х., Хейсс С., Бальцер Дж., Кляйнбонгард П., Кин К.Л., Холленберг Н.К. и др. (январь 2006 г.). «(-)-Эпикатехин опосредует благотворное влияние богатого флаванолом какао на функцию сосудов у человека» . Труды Национальной академии наук Соединенных Штатов Америки . 103 (4): 1024–1029. Бибкод : 2006PNAS..103.1024S . дои : 10.1073/pnas.0510168103 . ПМЦ 1327732 . ПМИД 16418281 .
- ^ Мартинес С.Е., Дэвис Н.М., Рейнольдс Дж.К. (2013). «Токсикология и безопасность флавоноидов». Методы анализа, доклиническая и клиническая фармакокинетика, безопасность и токсикология . Джон Уайли и сын. п. 257. ИСБН 978-0-470-57871-1 .
- ^ Боде Дж. К. (1987). Околичшаньи Л., Чомош Г., Крепальди Г. (ред.). Оценка и лечение гепатобилиарных заболеваний . Берлин: Springer-Verlag. п. 371. дои : 10.1007/978-3-642-72631-6 . ISBN 978-3-642-72631-6 . S2CID 3167832 .
- ^ «Приостановление действия разрешения Catergen» (PDF) . Немецкий медицинский журнал . 82 (38): 2706.
- ^ Министерство здравоохранения Канады (15 ноября 2017 г.). «Краткий обзор безопасности. Натуральные продукты для здоровья, содержащие экстракт зеленого чая. Оценка потенциального риска повреждения печени (гепатотоксичности)» . www.canada.ca . Проверено 6 мая 2022 г.
- ^ Юнес М., Аггетт П., Агилар Ф., Кребелли Р., Дюземунд Б., Филипич М. и др. (апрель 2018 г.). «Научное мнение о безопасности катехинов зеленого чая» . Журнал EFSA . 16 (4): e05239. дои : 10.2903/j.efsa.2018.5239 . ПМК 7009618 . ПМИД 32625874 .
- ^ Го Ю, Чжи Ф, Чэнь П, Чжао К, Сян Х, Мао Ц и др. (март 2017 г.). «Зеленый чай и риск рака простаты: систематический обзор и метаанализ» . Лекарство . 96 (13): е6426. дои : 10.1097/MD.0000000000006426 . ПМК 5380255 . ПМИД 28353571 .
- ^ Йе Дж.Х., Огюстен М.А. (2018). «Нано- и микрочастицы для доставки катехинов: физические и биологические характеристики». Критические обзоры в области пищевой науки и питания . 59 (10): 1563–1579. дои : 10.1080/10408398.2017.1422110 . ПМИД 29345975 . S2CID 29522787 .
- ^ Jump up to: а б Броз А.К., Виванко Дж.М., Шульц М.Дж., Перри Л.Г., Пашке М.В. (2006). «Вторичные метаболиты и аллелопатия при инвазиях растений: пример Centaurea maculosa » . В Таиз Л., Зейгер Э., Мёллер И.М., Мерфи А. (ред.). Физиология и развитие растений (6-е изд.). Синауэр Ассошиэйтс.
- ^ Байс Х.П., Вепачеду Р., Гилрой С., Каллауэй Р.М., Виванко Дж.М. (сентябрь 2003 г.). «Аллелопатия и инвазия экзотических растений: от молекул и генов к взаимодействию видов». Наука . 301 (5638): 1377–1380. Бибкод : 2003Sci...301.1377B . дои : 10.1126/science.1083245 . ПМИД 12958360 . S2CID 26483595 .
- ^ Ямамото М., Накацука С., Отани Х., Кохмото К., Нишимура С. (июнь 2000 г.). «(+)-Катехин действует как фактор, ингибирующий инфекцию, в листьях клубники». Фитопатология . 90 (6): 595–600. дои : 10.1094/PHYTO.2000.90.6.595 . ПМИД 18944538 .
- ^ Чен З., Лян Дж., Чжан С., Родригес С.Дж. (октябрь 2006 г.). «Эпикатехин и катехин могут предотвратить болезнь кофейных ягод путем ингибирования аппрессорной меланизации Colletotrichum kahawae ». Биотехнологические письма . 28 (20): 1637–1640. дои : 10.1007/s10529-006-9135-2 . ПМИД 16955359 . S2CID 30593181 .
Внешние ссылки
[ редактировать ] СМИ, связанные с (+)-катехином, на Викискладе?
СМИ, связанные с (+)-катехином, на Викискладе?