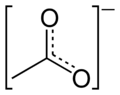
Ацетат
 | |
| Имена | |
|---|---|
| Название ИЮПАК Ацетат | |
| Систематическое название ИЮПАК Этаноат | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
ПабХим CID | |
| НЕКОТОРЫЙ | |
| Характеристики | |
| С 22Ч 33О − 2 | |
| Конъюгатная кислота | Уксусная кислота |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Ацетат образующуюся представляет собой соль, в результате соединения уксусной кислоты с основанием (например, щелочным , землистым , металлическим , неметаллическим или радикальным основанием ). «Ацетат» также описывает сопряженное основание или ион (в частности, отрицательно заряженный ион, называемый анионом ), обычно встречающийся в водном растворе и записываемый химической формулой C.
22Ч
33О −
2 . Нейтральные молекулы, образованные комбинацией ацетат-иона и положительного иона (называемого катионом ) , также обычно называются «ацетатами» (отсюда и ацетат свинца , ацетат алюминия и т. д.). Самый простой из них — ацетат водорода (называемый уксусной кислотой ) с соответствующими солями, эфирами и многоатомным анионом CH.
3 СО −
2 или СН
3 операционный директор −
.
Большая часть из примерно 5 миллионов тонн уксусной кислоты, ежегодно производимой в промышленности, используется в производстве ацетатов, которые обычно имеют форму полимеров . В природе ацетат является наиболее распространенным строительным блоком для биосинтеза .
Номенклатура и общая формула
[ редактировать ]В составе соли формула ацетат-иона записывается как CH.
3 СО −
2 , С
22Ч
33О −
2 или СН
3 операционный директор −
. Химики часто представляют ацетат как OAc. − или, реже, AcO − . Таким образом, HOAc является символом уксусной кислоты, NaOAc — ацетата натрия , а EtOAc — этилацетата. [1] (поскольку Ac является общим символом ацетильной группы CH 3 CO [2] [3] ). Символ псевдоэлемента «Ac» также иногда встречается в химических формулах как обозначающий весь ацетат-ион ( CH
3 СО −
2 ). [ нужна ссылка ] Его не следует путать с символом актиния , первого элемента ряда актинидов ; контекст помогает устранить неоднозначность. Например, формула ацетата натрия может быть сокращена как «NaOAc», а не как «NaC 2 H 3 O 2 ». Следует также соблюдать осторожность, чтобы не путать надуксусную кислоту при использовании аббревиатуры OAc; для ясности и во избежание ошибок при переводе следует избегать использования HOAc в литературе, в которой упоминаются оба соединения.
Хотя его систематическое название — этаноат ( / ɪ ˈ θ æ n oʊ . eɪ t / ), обычный ацетат остается предпочтительным названием IUPAC . [4]
Соли
[ редактировать ]
Ацетат- анион , [CH 3 COO] − ,(или [C 2 H 3 O 2 ] − ) принадлежит к семейству карбоксилатов . Это сопряженное основание кислоты уксусной . При pH выше 5,5 уксусная кислота превращается в ацетат: [1]
- СН 3 СООН ⇌ СН 3 СОО − + Ч +
Многие ацетатные соли являются ионными, о чем свидетельствует их склонность хорошо растворяться в воде. Обычно встречающийся в домашних условиях ацетат — это ацетат натрия , белое твердое вещество, которое можно получить путем объединения уксуса и бикарбоната натрия («бикарбонат соды»):
- CH 3 COOH + NaHCO 3 → CH 3 COO − Уже + + Н 2 О + СО 2
Переходные металлы могут образовывать комплексы с ацетатом. Примеры ацетатных комплексов включают ацетат хрома (II) и основной ацетат цинка.
Коммерчески важными ацетатными солями являются ацетат алюминия , используемый при окрашивании , ацетат аммония , предшественник ацетамида , и ацетат калия , используемый в качестве мочегонного средства . Все три соли бесцветны и хорошо растворимы в воде. [5]
Эфиры
[ редактировать ]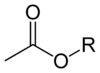
Ацетатные эфиры имеют общую формулу CH 3 CO 2 R, где R представляет собой органильную группу . Эфиры являются доминирующими формами ацетата на рынке. В отличие от ацетатных солей, ацетатные эфиры часто являются жидкостями, липофильными, а иногда и летучими. Они популярны, поскольку имеют безобидный, часто сладкий запах, недороги и обычно малотоксичны.
Почти половина производимой уксусной кислоты расходуется на производство винилацетата , предшественника поливинилового спирта , входящего в состав многих красок . Второе место по объему использования уксусной кислоты приходится на производство ацетата целлюлозы . Фактически, «ацетат» — это жаргонное обозначение ацетата целлюлозы, который используется в производстве волокон или различных продуктов, например, ацетатных дисков, используемых в производстве аудиозаписей. Ацетат целлюлозы можно найти во многих предметах домашнего обихода. Многие промышленные растворители представляют собой ацетаты, в том числе метилацетат , этилацетат, изопропилацетат , этилгексилацетат. Бутилацетат – ароматизатор, используемый в пищевых продуктах. [5]
Ацетат в биологии
[ редактировать ]Ацетат - распространенный анион в биологии. Он в основном используется организмами в форме ацетил-коэнзима А. [6]
Было обнаружено, что внутрибрюшинное введение ацетата натрия (20 или 60 мг на кг массы тела) вызывает головную боль у сенсибилизированных крыс, и было высказано предположение, что ацетат, образующийся в результате окисления этанола, является основным фактором, вызывающим похмелье . Повышенные уровни ацетата в сыворотке приводят к накоплению аденозина во многих тканях, включая мозг, а введение антагониста аденозиновых рецепторов кофеина крысам после того, как было обнаружено, что этанол снижает ноцицептивное поведение. [7] [8]
Ацетат обладает известными иммуномодулирующими свойствами и может влиять на врожденный иммунный ответ на патогенные бактерии, такие как респираторный возбудитель Haemophilus influenzae . [9]
Ферментация ацетил-КоА в ацетат
[ редактировать ]Пируват превращается в ацетил-кофермент А (ацетил-КоА) под действием фермента пируватдегидрогеназы . Этот ацетил-КоА затем превращается в ацетат в E. coli , производя при этом АТФ путем фосфорилирования на уровне субстрата . Для образования ацетата необходимы два фермента: фосфатацетилтрансфераза и ацетаткиназа. [10]

ацетил-КоА + фосфат → ацетил-фосфат + КоА
ацетилфосфат + АДФ → ацетат + АТФ
Ферментация ацетата
[ редактировать ]Уксусная кислота также может подвергаться реакции дисмутации с образованием метана и углекислого газа : [11] [12]
- CH 3 COO − + Ч + → CH 4 + CO 2 Δ G ° = −36 кДж/моль
Эту реакцию диспропорционирования катализируют метаногенные археи в их ферментативном метаболизме. Один электрон переносится от карбонильной функции ( e − донор ) карбоксильной группы к метильной группе ( e − акцептор ) уксусной кислоты для получения соответственно CO 2 и метана.
Структуры
[ редактировать ]- Модель заполнения пространства ацетат-аниона
- резонансный гибрид ацетат-аниона
- канонические формы ацетат-аниона
См. также
[ редактировать ]- Ацетилирование
- Ацетат целлюлозы
- Ацетат меди(II)
- Ферментация (биохимия)
- Ацетат натрия
- Смешанное кислое брожение
- Уксусная кислота
- Ацетилхлорид
- Ацетат цинка
Ссылки
[ редактировать ]- ^ Jump up to: а б Зумдал, СС «Химия» Хит, 1986: Лексингтон, Массачусетс. ISBN 0-669-04529-2 .
- ^ Международный союз теоретической и прикладной химии (2005). Номенклатура неорганической химии (Рекомендации ИЮПАК 2005 г.). Кембридж (Великобритания): RSC – IUPAC . ISBN 0-85404-438-8 . п. 63. Электронная версия.
- ^ Бримбл, Маргарет А.; Блэк, Дэвид Ст.К.; Хартшорн, Ричард; Раутер, Амелия П.; Ша, Чин-Кан; Сиднес, Лейв К. (10 ноября 2012 г.). «Правила сокращения защитных групп (Технический отчет ИЮПАК)» . Чистая и прикладная химия . 85 (1): 310. doi : 10.1351/PAC-REP-12-07-12 . S2CID 55102299 .
- ^ R-9.1 Тривиальные и полусистематические названия сохранены для обозначения органических соединений. Архивировано 8 февраля 2014 г. в Wayback Machine , Руководство по номенклатуре органических соединений ИЮПАК , Комиссия ИЮПАК по номенклатуре органической химии.
- ^ Jump up to: а б Осия Чунг, Робин С. Танке, Г. Пол Торренс «Уксусная кислота» в Энциклопедии промышленной химии Ульмана , Вайнхайм, Германия: Wiley-VCH, 2005. два : 10.1002/14356007.a01_045
- ^ Нельсон, DL; Кокс, М.М. «Ленингер, Принципы биохимии» 3-е изд. Стоит публикации: Нью-Йорк, 2000. ISBN 1-57259-153-6 .
- ^ Максвелл, Кристина; и др. (2010). «Ацетат вызывает головную боль при алкогольном похмелье у крыс» . ПЛОС ОДИН . 5 (12): e15963. Бибкод : 2010PLoSO...515963M . дои : 10.1371/journal.pone.0015963 . ПМК 3013144 . ПМИД 21209842 .
- ^ «Является ли кофе настоящим лекарством от похмелья?» Боб Холмс, New Scientist , 15 января 2011 г., стр. 17.
- ^ Хосмер, Дженнифер; Насрин, Маруфа; Дуиб, Рабеб; Эссильфи, Ама-Тавия; Ширра, Хорст Иоахим; Хеннингем, Анна; Фантино, Эммануэль; Хитрый, Питер; Макьюэн, Аластер Г.; Капплер, Ульрика (27 января 2022 г.). «Доступ к высокоспециализированным субстратам роста и выработке эпителиальных иммуномодулирующих метаболитов определяют выживаемость Haemophilus influenzae в эпителиальных клетках дыхательных путей человека» . ПЛОС Патогены . 18 (1): e1010209. дои : 10.1371/journal.ppat.1010209 . ISSN 1553-7374 . ПМЦ 8794153 . ПМИД 35085362 .
- ^ Кеселер, Ингрид М.; и др. (2011). «EcoCyc: обширная база данных биологии Escherichia coli» . Исследования нуклеиновых кислот . 39 (Проблема с базой данных): D583–D590. дои : 10.1093/нар/gkq1143 . ПМК 3013716 . ПМИД 21097882 .
- ^ Ферри, Дж. Г. (1992). «Метан из ацетата» . Журнал бактериологии . 174 (17): 5489–5495. дои : 10.1128/jb.174.17.5489-5495.1992 . ПМК 206491 . ПМИД 1512186 .
- ^ Фогельс, Джорджия; Келтьенс, Дж. Т.; Ван Дер Дрифт, К. (1988). «Биохимия производства метана». В Zehnder AJB (ред.). Биология анаэробных микроорганизмов . Нью-Йорк: Уайли. стр. 707–770.