Смешанное кислое брожение

В биохимии , смешаннокислое брожение — это метаболический процесс , в ходе которого образуется шестиуглеродный сахар (например глюкоза , C 6 H 12 O 6 ) превращается в сложную и изменчивую смесь кислот . Это анаэробная (не требующая кислорода) реакция ферментации , распространенная у бактерий . Это характерно для представителей Enterobacteriaceae , большого семейства грамотрицательных бактерий , включающего E. coli . [3]
Смесь конечных продуктов, получаемых смешанокислым брожением, включает лактат , ацетат , сукцинат , формиат , этанол и газы. Н 2 и СО 2 . Образование этих конечных продуктов зависит от присутствия определенных ключевых ферментов в бактерии . Пропорция, в которой они образуются, варьируется у разных видов бактерий. [4] Путь смешанного кислого брожения отличается от других путей ферментации, которые производят меньше конечных продуктов в фиксированных количествах. Конечные продукты смешаннокислого брожения могут найти множество полезных применений в биотехнологии и промышленности . Например, этанол широко используется в качестве биотоплива . [5] было метаболически сконструировано Поэтому в лаборатории несколько штаммов бактерий для увеличения индивидуального выхода определенных конечных продуктов. [2] Это исследование проводилось в основном на кишечной палочке и продолжается. Вариации смешанного кислотного брожения встречаются у ряда видов бактерий, включая бактериальные патогены, такие как Haemophilus influenzae , где в основном продуцируются ацетат и сукцинат, а лактат может служить субстратом для роста. [6]
Смешаннокислое брожение в E.coli
[ редактировать ]E. coli использует пути ферментации как последний вариант энергетического метаболизма, поскольку они производят очень мало энергии по сравнению с дыханием. [7] Смешаннокислое брожение в E. coli протекает в две стадии. Эти стадии описаны в биологической базе данных E. coli EcoCyc . [1]
Первой из этих двух стадий является реакция гликолиза . В анаэробных условиях происходит реакция гликолиза, при которой глюкоза превращается в пируват :
глюкоза → 2 пируват
приходится чистое производство 2 молекул АТФ и 2 НАДН На одну молекулу преобразованной глюкозы . АТФ образуется путем фосфорилирования на уровне субстрата . НАДН образуется в результате восстановления НАД.
На втором этапе пируват, полученный в результате гликолиза, превращается в один или несколько конечных продуктов посредством следующих реакций. В каждом случае обе молекулы НАДН, образующиеся в результате гликолиза, повторно окисляются до НАД. + . Каждый альтернативный путь требует отдельного ключевого фермента E. coli . После того как этими путями образуются различные количества различных конечных продуктов, они секретируются из клетки. [1]
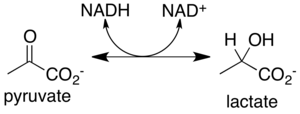
Образование лактата
[ редактировать ]Пируват, образующийся в результате гликолиза, превращается в лактат . Эту реакцию катализирует фермент лактатдегидрогеназа (ЛДГА). [1]
пируват + НАДН + Н + → молочные продукты + НАД +
Образование ацетата
[ редактировать ]Пируват превращается в ацетил-кофермент А (ацетил-КоА) под действием фермента пируватдегидрогеназы . Этот ацетил-КоА затем превращается в ацетат в E. coli , производя при этом АТФ путем фосфорилирования на уровне субстрата . Для образования ацетата необходимы два фермента: фосфатацетилтрансфераза и ацетаткиназа. [1]

ацетил-КоА + фосфат → ацетил-фосфат + КоА
ацетилфосфат + АДФ → ацетат + АТФ
Образование этанола
[ редактировать ]Этанол образуется в E. coli путем восстановления ацетилкофермента А с помощью НАДН. Для этой двухэтапной реакции требуется фермент алкогольдегидрогеназа (ADHE). [1]
ацетил-КоА + НАДН + Н + → ацетальдегид + НАД + + Сертификат подлинности
ацетальдегид + НАДН + Н + → этанол + НЕТ +
Образование формиата
[ редактировать ]Формиат образуется при расщеплении пирувата. Эту реакцию катализирует фермент пируват-формиатлиаза (ПФЛ), который играет важную роль в регуляции анаэробного брожения в E. coli . [8]
пируват + КоА → ацетил-КоА + формиат
Образование сукцината
[ редактировать ]
Сукцинат образуется в E. coli в несколько стадий.
Фосфоенолпируват продукт гликолиза (PEP), промежуточный , карбоксилируется ферментом PEP-карбоксилазой с образованием оксалоацетата . [9] За этим следует превращение оксалоацетата в малат под действием фермента малатдегидрогеназы . Фумаратгидратаза затем катализирует дегидратацию малата с образованием фумарата . [10]
фосфоенолпируват + HCO 3 → оксалоацетат + фосфат
оксалоацетат + НАДН + Н + → малат + НАД +
малат → фумарат + H 2 O
Последней реакцией образования сукцината является восстановление фумарата. Катализируется ферментом фумаратредуктазой .
фумарат + НАДН + Н + → сукцинат + НАД +
Это восстановление является анаэробной реакцией дыхания в E. coli , поскольку оно использует электроны, связанные с НАДН-дегидрогеназой и цепью переноса электронов . АТФ генерируется с помощью электрохимического градиента и АТФ-синтазы . Это единственный случай смешаннокислого брожения, когда АТФ не образуется посредством фосфорилирования на уровне субстрата. [1] [2]
Витамин К 2 , также известный как менахинон, очень важен для транспорта электронов к фумарату в E. coli . [11]
Образование водорода и углекислого газа
[ редактировать ]Формиат может быть преобразован в газообразный водород и углекислый газ в E. coli . Для этой реакции необходим фермент формиат-водородлиаза . Его можно использовать для предотвращения слишком кислой среды внутри клетки. [1]
формиат → H 2 и CO 2
Метиловый красный тест
[ редактировать ]
Тест с метиловым красным (MR) может определить, возникает ли у микробов путь смешанно-кислотного брожения при введении глюкозы. 4,4 . Используется индикатор pH, который окрашивает тестовый раствор в красный цвет, если pH падает ниже [12] Если процесс ферментации имел место, смесь кислот, которую он произвел, сделает раствор очень кислым и вызовет изменение цвета на красный.
Тест на метиловый красный принадлежит к группе, известной как тесты IMViC .
Метаболическая инженерия
[ редактировать ]Множественные бактериальные штаммы были метаболически сконструированы для увеличения индивидуального выхода конечных продуктов, образующихся в результате смешаннокислой ферментации. Например, были разработаны штаммы для увеличения продукции этанола, лактата, сукцината и ацетата из-за полезности этих продуктов в биотехнологии . [2] Основным ограничивающим фактором для этой технологии является необходимость поддержания окислительно-восстановительного баланса в смеси кислот, образующихся в результате ферментации. [13]
Для производства этанола
[ редактировать ]Этанол является наиболее часто используемым биотопливом и может производиться в больших масштабах путем ферментации. Максимальный теоретический выход производства этанола был достигнут примерно через 20 лет. [14] [15] плазмиду, содержащую гены пируватдекарбоксилазы и алкогольдегидрогеназы из бактерий Z. mobilis Ученые использовали . Его вставили в E. coli , что привело к увеличению выхода этанола. Геном этого штамма E. coli , KO11, совсем недавно был секвенирован и картирован. [16]


Для производства ацетата
[ редактировать ]Штамм E. coli W3110 был генетически спроектирован так, чтобы генерировать 2 моля ацетата на каждый 1 моль глюкозы, подвергающейся ферментации. Это известно как гомоацетатный путь. [17]
Для производства лактата
[ редактировать ]Лактат можно использовать для производства биопластика, называемого полимолочной кислотой (PLA). Свойства PLA зависят от соотношения двух оптических изомеров лактата (D-лактата и L-лактата). D-лактат производится путем смешаннокислой ферментации в E.coli . [18] Ранние эксперименты позволили штамму E. coli RR1 производить один из двух оптических изомеров лактата. [19]
Более поздние эксперименты модифицировали штамм E. coli KO11, первоначально разработанный для увеличения производства этанола. Ученым удалось увеличить выход D-лактата в результате ферментации, выполнив несколько делеций . [20]
Для производства сукцината
[ редактировать ]Увеличение выхода сукцината в результате смешанокислой ферментации было впервые достигнуто за счет сверхэкспрессии фермента PEP-карбоксилазы . [21] Это привело к выходу сукцината, который был примерно в 3 раза выше обычного. За этим последовало несколько экспериментов с использованием аналогичного подхода.
Альтернативные подходы изменили баланс окислительно-восстановительного потенциала и АТФ для оптимизации выхода сукцината. [22]
Связанные пути ферментации
[ редактировать ]Существует ряд других путей ферментации, которые происходят у микробов. [4] Все эти пути начинаются с преобразования пирувата, но их конечные продукты и ключевые ферменты, которые им необходимы, различны. Эти пути включают в себя:
- Этаноловое брожение
- Молочнокислое брожение
- пропионовой кислоты Ферментация
- Бутаноловое брожение
- Бутандиоловая ферментация
Внешние ссылки
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж г час Кеселер, Ингрид М.; и др. (2011). «EcoCyc: обширная база данных биологии Escherichia coli » . Исследования нуклеиновых кислот . 39 (Проблема с базой данных): D583–D590. дои : 10.1093/нар/gkq1143 . ПМК 3013716 . ПМИД 21097882 .
- ^ Jump up to: а б с д Фёрстер, Андреас Х. и Йоханнес Гешер (2014). «Метаболическая инженерия Escherichia coli для производства конечных продуктов смешанокислотного брожения» . Границы биоинженерии и биотехнологии . 2 : 506–508. дои : 10.3389/fbioe.2014.00016 . ПМК 4126452 . ПМИД 25152889 .
- ^ М.Магидан и Дж. Мартинко (2006). «Биология микроорганизмов Брока, Нью-Джерси, Пирсон Прентис Холл». 11 : 352.
{{cite journal}}: Для цитирования журнала требуется|journal=( помощь ) - ^ Jump up to: а б Шарма, П. Д. (2007). «Микробиология»: 104.
{{cite journal}}: Для цитирования журнала требуется|journal=( помощь ) - ^ Фаррелл, Александр Э.; и др. (2006). «Этанол может способствовать достижению энергетических и экологических целей». Наука . 311 (5760): 506–508. Бибкод : 2006Sci...311..506F . дои : 10.1126/science.1121416 . ПМИД 16439656 . S2CID 16061891 .
- ^ Хосмер, Дженнифер; Насрин, Маруфа; Дуиб, Рабеб; Эссильфи, Ама-Тавия; Ширра, Хорст Иоахим; Хеннингем, Анна; Фантино, Эммануэль; Хитрый, Питер; Макьюэн, Аластер Г.; Капплер, Ульрика (27 января 2022 г.). «Доступ к высокоспециализированным субстратам роста и выработке эпителиальных иммуномодулирующих метаболитов определяют выживаемость Haemophilus influenzae в эпителиальных клетках дыхательных путей человека» . ПЛОС Патогены . 18 (1): e1010209. дои : 10.1371/journal.ppat.1010209 . ISSN 1553-7374 . ПМЦ 8794153 . ПМИД 35085362 .
- ^ Соерс, Р. Гэри; Блокеш, Мелани ; Бек, август (2004 г.). «Анаэробный формиат и водородный обмен». ЭкоСал Плюс . 1 (1). дои : 10.1128/ecosalplus.3.5.4 . ПМИД 26443350 .
- ^ Кнаппе, Иоахим и Гэри Сойерс (1990). «Радикально-химический путь к ацетил-КоА: анаэробно индуцированная пируватформиат-лиазная система Escherichia coli » . Обзоры микробиологии FEMS . 6 (4): 383–398. дои : 10.1111/j.1574-6968.1990.tb04108.x . ПМИД 2248795 .
- ^ Кай, Ясуши, Хироёси Мацумура и Кацура Изуи (2003). «Фосфоенолпируваткарбоксилаза: трехмерная структура и молекулярные механизмы». Архив биохимии и биофизики . 414 (2): 170–179. дои : 10.1016/S0003-9861(03)00170-X . ПМИД 12781768 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Таккер, Чандреш; и др. (2012). «Продукция сукцината в Escherichia coli » . Биотехнологический журнал . 7 (2): 213–224. дои : 10.1002/biot.201100061 . ПМК 3517001 . ПМИД 21932253 .
- ^ Гость, ДЖОН Р. (1977). «Биосинтез менахинона: мутанты Escherichia coli K-12, требующие 2-сукцинилбензоата» . Журнал бактериологии . 130 (3): 1038–1046. дои : 10.1128/jb.130.3.1038-1046.1977 . ПМК 235325 . ПМИД 324971 .
- ^ Х. Т. Кларк; В. Р. Кирнер (1922). «Метиловый красный». Орг. Синтез. 2 : 47. дои : 10.15227/orgsyn.002.0047 .
- ^ ван Хук; Милан Дж. А. и Роланд М. Х. Меркс (2012). «Окислительно-восстановительный баланс является ключом к объяснению полного или частичного перехода на низкопродуктивный метаболизм» . Системная биология BMC . 6 (1): 22. дои : 10.1186/1752-0509-6-22 . ПМК 3384451 . ПМИД 22443685 .
- ^ Ингрэм, Лоу; и др. (1987). «Генная инженерия получения этанола в Escherichia coli » . Прикладная и экологическая микробиология . 53 (10): 2420–2425. Бибкод : 1987ApEnM..53.2420I . дои : 10.1128/aem.53.10.2420-2425.1987 . ПМК 204123 . ПМИД 3322191 .
- ^ Охта, Казуёси; и др. (1991). «Генетическое улучшение Escherichia coli для производства этанола: хромосомная интеграция генов Zymomonas mobilis, кодирующих пируватдекарбоксилазу и алкогольдегидрогеназу II» . Прикладная и экологическая микробиология . 57 (4): 893–900. Бибкод : 1991ApEnM..57..893O . doi : 10.1128/aem.57.4.893-900.1991 . ПМЦ 182819 . ПМИД 2059047 .
- ^ Тернер, Питер К.; и др. (2012). «Оптическое картирование и секвенирование генома Escherichia coli KO11 выявили обширные хромосомные перестройки и множественные тандемные копии генов pdc и adhB Zymomonas mobilis» . Журнал промышленной микробиологии и биотехнологии . 39 (4): 629–639. дои : 10.1007/s10295-011-1052-2 . ПМИД 22075923 . S2CID 15100287 .
- ^ Кози, туберкулез; и др. (2003). «Инженерия метаболизма Escherichia coli W3110 для превращения сахара в окислительно-нейтральные и окисленные продукты: производство гомоацетата» . Труды Национальной академии наук . 100 (3): 825–832. Бибкод : 2003PNAS..100..825C . дои : 10.1073/pnas.0337684100 . ПМК 298686 . ПМИД 12556564 .
- ^ Кларк, Дэвид П. (1989). «Пути ферментации кишечной палочки » . Обзоры микробиологии FEMS . 5 (3): 223–234. дои : 10.1111/j.1574-6968.1989.tb03398.x . ПМИД 2698228 .
- ^ Чанг, Дон Ын; и др. (1999). «Гомоферментативное производство d-орл-лактата в метаболически сконструированной Escherichia coli RR1» . Прикладная и экологическая микробиология . 65 (4): 1384–1389. Бибкод : 1999ApEnM..65.1384C . дои : 10.1128/АЕМ.65.4.1384-1389.1999 . ПМЦ 91196 . ПМИД 10103226 .
- ^ Чжоу, С.; и др. (2005). «Ферментация 10% (масс./об.) сахара до D (-)-лактата с помощью инженерной Escherichia coli B». Биотехнологические письма . 27 (23–24): 1891–1896. дои : 10.1007/s10529-005-3899-7 . ПМИД 16328986 . S2CID 43204090 .
- ^ Миллард, Синтия Санвилл; и др. (1996). «Увеличенное производство янтарной кислоты за счет сверхэкспрессии фосфоенолпируваткарбоксилазы в Escherichia coli » . Прикладная и экологическая микробиология . 62 (5): 1808–1810. Бибкод : 1996ApEnM..62.1808M . дои : 10.1128/аэм.62.5.1808-1810.1996 . ПМК 167956 . ПМИД 8633880 .
- ^ Сингх, Амарджит; и др. (2011). «Управление балансом окислительно-восстановительного потенциала и АТФ для улучшения производства сукцината в E. coli ». Метаболическая инженерия . 13 (1): 76–81. дои : 10.1016/j.ymben.2010.10.006 . ПМИД 21040799 .