Ацетил-КоА
В этой статье нечеткий стиль цитирования . Причина: несколько номеров страниц в одной ссылке, которая используется несколько раз: неясно, какой из них что поддерживает. Некоторые ISBN могут указывать на неправильное издание книги. Нужны номера страниц для ссылок на целые учебники широкого охвата. ( Август 2017 г. ) |
 | |
 | |
 | |
| Имена | |
|---|---|
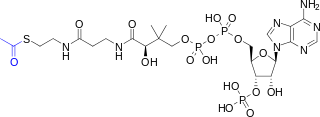
| Предпочтительное название ИЮПАК ТО 1 -{(3 R )-4-[(3-{[2-(Ацетилсульфанил)этил]амино}-3-оксопропил)амино]-3-гидрокси-2,2-диметил-4-оксобутил} O 3 -{[(2R , 3S , 4R , 5R ) -5-(6-амино-9Н- пурин -9-ил)-4-гидрокси-3-(фосфоноокси)оксолан-2-ил]метил } дигидродифосфат | |
| Идентификаторы | |
| |
3D model ( JSmol ) | |
| ЧЭБИ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.000.719 |
| КЕГГ | |
| МеШ | Ацетил+Коэнзим+А |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 23 Ч 38 Н 7 О 17 П 3 С | |
| Молярная масса | 809.57 g·mol −1 |
| УФ-видимое излучение (λ макс .) | 260 нм; 232 нм [1] |
| Поглощение | ε 260 = 16,4 мМ −1 см −1 (аденозин) [1] ε 232 = 8,7 мМ −1 см −1 (тиоэфир) [1] Δε мМ 232 при гидролизе тиоэфира = -4,5 −1 см −1 [1] |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Ацетил-КоА ( ацетил-коэнзим А ) — молекула, которая участвует во многих биохимических реакциях белкового, углеводного и липидного обмена . [2] Его основная функция — доставка ацетильной группы в цикл лимонной кислоты (цикл Кребса) для окисления для производства энергии.
Коэнзим А (CoASH или CoA) состоит из группы β-меркаптоэтиламина, связанной с пантотеновой кислотой (витамином B5) через амидную связь. [3] и 3'-фосфорилированный АДФ. Ацетильная группа (обозначена синим цветом на структурной диаграмме справа) ацетил-КоА связана с сульфгидрильным заместителем β-меркаптоэтиламинной группы. Эта тиоэфирная связь представляет собой «высокоэнергетическую» связь, которая является особенно реакционноспособной. Гидролиз тиоэфирной связи экзергонический (-31,5 кДж/моль).
КоА ацетилируется до ацетил-КоА в результате расщепления углеводов посредством гликолиза и распада жирных кислот посредством β-окисления . Затем ацетил-КоА вступает в цикл лимонной кислоты, где ацетильная группа окисляется до углекислого газа и воды, а высвободившаяся энергия улавливается в виде 11 АТФ и одного ГТФ на ацетильную группу.
Конрад Блох и Федор Линен были удостоены Нобелевской премии по физиологии и медицине 1964 года за открытия, связывающие метаболизм ацетил-КоА и жирных кислот. Фриц Липманн получил Нобелевскую премию в 1953 году за открытие кофактора А. коэнзима [4]
Роль
[ редактировать ]Ацетил-КоА представляет собой промежуточный продукт метаболизма , который участвует во многих метаболических путях в организме. Он образуется при расщеплении глюкозы , жирных кислот и аминокислот и используется в синтезе многих других биомолекул , включая холестерин , жирные кислоты и кетоновые тела . Ацетил-КоА также является ключевой молекулой в цикле лимонной кислоты , который представляет собой серию химических реакций, происходящих в митохондриях клеток и отвечающих за выработку энергии в форме АТФ . [5] [6]
Кроме того, ацетил-КоА является предшественником биосинтеза различных ацетил-химических веществ, выступая в качестве промежуточного продукта для переноса ацетильной группы во время биосинтеза этих ацетил-химических веществ. Ацетил-КоА также участвует в регуляции различных клеточных механизмов, предоставляя ацетильные группы для нацеливания на аминокислотные остатки для реакций посттрансляционного ацетилирования белков. [7]
Биосинтез
[ редактировать ]Ацетилирование КоА определяется источниками углерода. [8] [9]
Экстрамитохондриальный
[ редактировать ]- При высоких глюкозы уровнях гликолиз происходит быстро, тем самым увеличивая количество цитрата, вырабатываемого в цикле лимонной кислоты . Этот цитрат затем экспортируется в другие органеллы за пределами митохондрий, где он расщепляется на ацетил-КоА и оксалоацетат с помощью фермента АТФ-цитратлиазы (ACL). Эта основная реакция связана с гидролизом АТФ. [10] [11]
- При низком уровне глюкозы:
- КоА ацетилируется с помощью ацетата ацетил -СоА-синтетазой (ACS), что также сопровождается гидролизом АТФ . [12]
- Этанол также служит источником углерода для ацетилирования КоА с использованием фермента алкогольдегидрогеназы . [13]
- с разветвленной цепью, Происходит деградация кетогенных аминокислот таких как валин , лейцин и изолейцин . Эти аминокислоты превращаются в α-кетокислоты путем трансаминирования и, в конечном итоге, в изовалерил-КоА посредством окислительного декарбоксилирования с помощью дегидрогеназного комплекса α-кетокислот. Изовалерил-КоА подвергается дегидрированию , карбоксилированию и гидратации с образованием другого промежуточного продукта-производного КоА, прежде чем он расщепляется на ацетил-КоА и ацетоацетат . [14] [ нужна страница ]
Внутримитохондриальный
[ редактировать ]
- При высоких уровнях глюкозы ацетил-КоА вырабатывается посредством гликолиза . [15] Пируват подвергается окислительному декарбоксилированию, при котором он теряет карбоксильную группу (в виде диоксида углерода ) с образованием ацетил-КоА, выделяя 33,5 кДж/моль энергии. Окислительное превращение пирувата в ацетил-КоА называется пируватдегидрогеназной реакцией . Катализируется пируватдегидрогеназным комплексом . Возможны и другие превращения пирувата в ацетил-КоА. Например, пируватформиатлиаза диспропорционирует пируват на ацетил-КоА и муравьиную кислоту .

- При низких уровнях глюкозы выработка ацетил-КоА связана с β-окислением жирных кислот . Жирные кислоты сначала превращаются в ацил-КоА. Затем ацил-КоА разлагается в четырехэтапном цикле окисления , гидратации , окисления и тиолиза, катализируемом четырьмя соответствующими ферментами, а именно ацил-КоА-дегидрогеназой , еноил-КоА-гидратазой , 3-гидроксиацил-КоА-дегидрогеназой и тиолазой . Цикл производит новую цепь жирных кислот с на два атома углерода меньше и ацетил-КоА в качестве побочного продукта. [16]
Функции
[ редактировать ]Промежуточные соединения в различных путях
[ редактировать ]- В клеточном дыхании
- Цикл лимонной кислоты :
- В результате серии химических реакций запасенная энергия высвобождается за счет окисления ацетил-КоА, полученного из углеводов, жиров и белков, в аденозинтрифосфат (АТФ) и углекислый газ .
- Метаболизм жирных кислот
- Ацетил-КоА образуется в результате расщепления как углеводов (путем гликолиза ), так и липидов (путем β-окисления ). Затем он входит в цикл лимонной кислоты в митохондриях, соединяясь с оксалоацетатом с образованием цитрата . [17] [18]
- Две молекулы ацетил-КоА конденсируются с образованием ацетоацетил-КоА , что приводит к образованию ацетоацетата и β-гидроксибутирата . [17] Ацетоацетат, β-гидроксибутират и продукт их самопроизвольного распада ацетон. [19] их часто, но сбивает с толку, называют кетоновыми телами (поскольку они вовсе не «тела», а водорастворимые химические вещества). Кетоновые тела выбрасываются печенью в кровь. Все клетки с митохондриями могут забирать кетоновые тела из крови и превращать их в ацетил-КоА, который затем можно использовать в качестве топлива в циклах лимонной кислоты, поскольку никакая другая ткань не может направить свой оксалоацетат в глюконеогенный путь так, как это происходит с митохондриями. печень делает. В отличие от свободных жирных кислот, кетоновые тела могут преодолевать гематоэнцефалический барьер и поэтому доступны в качестве топлива для клеток центральной нервной системы , действуя в качестве заменителя глюкозы, на которой эти клетки обычно выживают. [17] Возникновение высокого уровня кетоновых тел в крови при голодании , низкоуглеводной диете , длительных тяжелых физических нагрузках и неконтролируемом сахарном диабете 1-го типа известно как кетоз , а в его крайней форме – при вышедшем из-под контроля 1-м типе. сахарный диабет, как кетоацидоз .
- С другой стороны, когда концентрация инсулина в крови высокая, а глюкагона низкая (т.е. после еды), ацетил-КоА, образующийся в результате гликолиза, конденсируется как обычно с оксалоацетатом с образованием цитрата в митохондриях. Однако вместо того, чтобы продолжать цикл лимонной кислоты для превращения в углекислый газ и воду, цитрат удаляется из митохондрии в цитоплазму . [17] Там он расщепляется АТФ-цитратлиазой на ацетил-КоА и оксалоацетат. Оксалоацетат возвращается в митохондрии в виде малата (а затем превращается обратно в оксалоацетат для выведения большего количества ацетил-КоА из митохондрии). [20] Этот цитозольный ацетил-КоА затем можно использовать для синтеза жирных кислот посредством карбоксилирования ацетил-КоА-карбоксилазой в малонил-КоА , что является первым обязательным этапом синтеза жирных кислот. [20] [21] Это преобразование происходит главным образом в печени, жировой ткани и лактирующих молочных железах , где жирные кислоты соединяются с глицерином с образованием триглицеридов , основного топливного резервуара большинства животных. Жирные кислоты также являются компонентами фосфолипидов , составляющих основную часть липидных бислоев всех клеточных мембран . [17]
- У растений синтез жирных кислот de novo происходит в пластидах . Многие семена накапливают большие запасы семенного масла, поддерживающего прорастание и ранний рост проростка, прежде чем он станет чистым фотосинтезирующим организмом.
- Цитозольный ) , ацетил-КоА также может конденсироваться с ацетоацетил-КоА с образованием 3-гидрокси-3-метилглутарил-КоА ( ГМГ-КоА что является лимитирующей стадией, контролирующей синтез холестерина . [17] Холестерин можно использовать как есть, как структурный компонент клеточных мембран, или его можно использовать для синтеза стероидных гормонов , солей желчных кислот и витамина D. [17] [21]
- Ацетил-КоА может карбоксилироваться в цитозоле под действием ацетил-КоА-карбоксилазы , образуя малонил-КоА , субстрат, необходимый для синтеза флавоноидов и родственных поликетидов , для удлинения жирных кислот с образованием воска , кутикулы и масел семян в членах семейство Brassica , а также для малонации белков и других фитохимических веществ. [22] У растений к ним относятся сесквитерпены , брассиностероиды (гормоны) и мембранные стерины .
- Синтез стероидов :
- Ацетил-КоА участвует в мевалонатном пути , участвуя в синтезе гидроксиметилглутарил-КоА.
- ацетилхолина Синтез :
- Ацетил-КоА также является важным компонентом биогенного синтеза нейромедиатора ацетилхолина . Холин в сочетании с ацетил-КоА катализируется ферментом холин-ацетилтрансферазой с образованием ацетилхолина и кофермента А в качестве побочного продукта.
- мелатонина Синтез
- Ацетилирование
- Ацетил-КоА также является источником ацетильной группы, включенной в определенные лизина остатки гистонов и негистоновых белков при посттрансляционной модификации ацетилирования . Это ацетилирование катализируется ацетилтрансферазами . Это ацетилирование влияет на рост клеток , митоз и апоптоз . [23]
- Аллостерический регулятор
- Ацетил-КоА служит аллостерическим регулятором ( киназы пируватдегидрогеназы ПДК). Он регулирует соотношение ацетил-КоА и КоА. Повышенная концентрация ацетил-КоА активирует PDK. [24]
- Ацетил-КоА также является аллостерическим активатором пируваткарбоксилазы . [25]
Интерактивная карта маршрутов
[ редактировать ]Нажмите на гены, белки и метаболиты ниже, чтобы посетить страницы Gene Wiki и соответствующие статьи Википедии. Путь можно загрузить и отредактировать на WikiPathways .
TCACycle_WP78 редактировать | пути статинов Редактирование |
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: Перейти обратно: а б с д Доусон Р.М., Эллиотт Д.К., Эллиотт У.Х., Джонс К.М. (2002). Данные для биохимических исследований (3-е изд.). Кларендон Пресс. п. 117. ИСБН 978-0-19-855299-4 .
- ^ «Перекресток ацетил-КоА» . chemistry.elmhurst.edu . Архивировано из оригинала 15 ноября 2016 г. Проверено 8 ноября 2016 г.
- ^ «Жирные кислоты - структура ацетил-КоА» . библиотека.med.utah.edu . Проверено 2 июня 2017 г.
- ^ «Все Нобелевские премии по физиологии и медицине» . Нобелевская премия .
- ^ Чжан С., Ян В., Чен Х., Лю Б., Линь Б., Тао Ю. (август 2019 г.). «Метаболическая инженерия для эффективного снабжения ацетил-КоА из различных источников углерода в Escherichia coli» . Факт о микробной клетке . 18 (1): 130. дои : 10.1186/s12934-019-1177-y . ПМК 6685171 . ПМИД 31387584 .
- ^ «5.12G: Путь ацетил-КоА» . 9 мая 2017 г.
- ^ «Центральный метаболический промежуточный продукт» . МедхимЭкспресс.com . Проверено 15 февраля 2024 г.
- ^ Хайнс М.Дж., Мюррей С.Л. (1 июля 2010 г.). «АТФ-цитрат-лиаза необходима для производства цитозольного ацетил-коэнзима А и развития Aspergillus nidulans» . Эукариотическая клетка . 9 (7): 1039–1048. дои : 10.1128/EC.00080-10 . ISSN 1535-9778 . ПМК 2901662 . ПМИД 20495057 .
- ^ Веллен К.Е., Томпсон CB (1 апреля 2012 г.). «Улица с двусторонним движением: взаимная регуляция метаболизма и передачи сигналов». Nature Reviews Молекулярно-клеточная биология . 13 (4): 270–276. дои : 10.1038/nrm3305 . ISSN 1471-0072 . ПМИД 22395772 . S2CID 244613 .
- ^ Этажное КБ (25 февраля 2005 г.). Функциональный метаболизм: регуляция и адаптация . Джон Уайли и сыновья. ISBN 9780471675570 .
- ^ «ACLY АТФ-цитрат-лиаза [Homo sapiens (человек)] - Ген - NCBI» . www.ncbi.nlm.nih.gov . Проверено 6 ноября 2016 г.
- ^ Рэгсдейл SW (2004). «Жизнь с угарным газом». Критические обзоры CRC по биохимии и молекулярной биологии . 39 (3): 165–195. дои : 10.1080/10409230490496577 . ПМИД 15596550 . S2CID 16194968 .
- ^ Чаттерджи (1 января 2004 г.). Учебник биохимии для студентов-стоматологов, сестер и фармацевтов . Издательство Jaypee Brothers. ISBN 9788180612046 . [ постоянная мертвая ссылка ]
- ^ Берг Дж. М., Тимочко Дж. Л., Страйер Л. (2002). Биохимия (5-е изд.). У. Х. Фриман. ISBN 978-0716730514 .
- ^ Блэксток Джей Си (28 июня 2014 г.). Руководство по биохимии . Баттерворт-Хайнеманн. ISBN 9781483183671 .
- ^ Хаутен С.М., Вандерс Р.Дж. (2 марта 2010 г.). «Общее введение в биохимию β-окисления митохондриальных жирных кислот» . Журнал наследственных метаболических заболеваний . 33 (5): 469–477. дои : 10.1007/s10545-010-9061-2 . ISSN 0141-8955 . ПМК 2950079 . ПМИД 20195903 .
- ^ Jump up to: Перейти обратно: а б с д и ж г Страйер Л. (1995). Биохимия (Четвертое изд.). Нью-Йорк: WH Freeman and Company. стр. 510–515, 559–565, 581–613, 614–623, 775–778. ISBN 978-0-7167-2009-6 .
- ^ «Окисление жирных кислот» . 11 октября 2013 г.
- ^ «Кетоновый обмен веществ» . Университет Ватерлоо.
- ^ Jump up to: Перейти обратно: а б Ферре П., Ф. Фуфель (2007). «Фактор транскрипции SREBP-1c и липидный гомеостаз: клиническая перспектива». Гормональные исследования . 68 (2): 72–82. doi : 10.1159/000100426 (неактивен 7 июля 2024 г.). ПМИД 17344645 .
этот процесс графически представлен на стр. 73.
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на июль 2024 г. ( ссылка ) - ^ Jump up to: Перейти обратно: а б Воэт Д., Джудит Г. Воэт, Шарлотта В. Пратт (2006). Основы биохимии, 2-е издание . John Wiley and Sons, Inc., стр. 547, 556 . ISBN 978-0-471-21495-3 .
- ^ Фатланд БЛ (2005). «Обратная генетическая характеристика генерации цитозольного ацетил-КоА с помощью АТФ-цитратлиазы у Arabidopsis» . Растительная клетка онлайн . 17 (1): 182–203. дои : 10.1105/tpc.104.026211 . ПМК 544498 . ПМИД 15608338 .
- ^ Йи Ч., Вакифахметоглу-Норберг Х., Юань Дж. (01.01.2011). «Интеграция апоптоза и метаболизма» . Симпозиумы Колд-Спринг-Харбор по количественной биологии . 76 : 375–387. дои : 10.1101/sqb.2011.76.010777 . ISSN 0091-7451 . ПМИД 22089928 .
- ^ Петтит Ф.Х., Пелли Дж.В., Рид Л.Дж. (22 июля 1975 г.). «Регуляция киназы и фосфатазы пируватдегидрогеназы с помощью соотношений ацетил-КоА/КоА и НАДН/НАД». Связь с биохимическими и биофизическими исследованиями . 65 (2): 575–582. дои : 10.1016/S0006-291X(75)80185-9 . ПМИД 167775 .
- ^ Джитрапакди С., Морис М.С., Рэймент I , Клеланд В.В., Уоллес Дж.К., Эттвуд П.В. (01 августа 2008 г.). «Структура, механизм и регуляция пируваткарбоксилазы» . Биохимический журнал . 413 (3): 369–387. дои : 10.1042/BJ20080709 . ISSN 0264-6021 . ПМЦ 2859305 . ПМИД 18613815 .
Внешние ссылки
[ редактировать ]- Ацетил + Коэнзим + А в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)





















