Триптофан
 Скелетная формула L - триптофана | |||
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Триптофан | |||
| Систематическое название ИЮПАК (2 S )-2-амино-3-(1 H -индол-3-ил)пропановая кислота | |||
| Другие имена 2-Амино-3-(1H - индол-3-ил)пропановая кислота | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| ЧЭБИ | |||
| ЧЕМБЛ | |||
| ХимическийПаук | |||
| Лекарственный Банк | |||
| Информационная карта ECHA | 100.000.723 | ||
| КЕГГ | |||
ПабХим CID | |||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| С 11 Н 12 Н 2 О 2 | |||
| Молярная масса | 204.229 g·mol −1 | ||
| Растворимый: 0,23 г/л при 0 °C, 11,4 г/л при 25 °C, | |||
| Растворимость | Растворим в горячем спирте, гидроксидах щелочных металлов; нерастворим в хлороформе . | ||
| Кислотность ( pKa ) | 2,38 (карбоксил), 9,39 (амино) [2] | ||
| -132.0·10 −6 см 3 /моль | |||
| Фармакология | |||
| N06AX02 ( ВОЗ ) | |||
| Страница дополнительных данных | |||
| Триптофан (страница данных) | |||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Триптофан (символ Trp или W ) [3] представляет собой α- , которая используется в биосинтезе белков аминокислоту . Триптофан содержит α -аминогруппу, группу α- карбоновой кислоты и индол боковой цепи , что делает его полярной молекулой с неполярным ароматическим бета-углеродным заместителем. Триптофан также является предшественником нейромедиатора серотонина , гормона мелатонина и витамина B3 . [4] Он кодируется кодоном UGG .
Как и другие аминокислоты, триптофан представляет собой цвиттер-ион при физиологическом pH , где аминогруппа протонирована (- NH +
3 ; pK a = 9,39) и карбоновая кислота депротонируется ( –COO − ; рК а = 2,38). [5]
Люди и многие животные не могут синтезировать триптофан: им необходимо получать его с пищей, что делает его незаменимой аминокислотой . В 2023 году спектр излучения триптофана был обнаружен в межзвездном газе звездного скопления IC 348 . [6]
Триптофан назван в честь пищеварительного фермента трипсина , который был использован при его первом выделении из казеиновых белков. [7] Ему был присвоен однобуквенный символ W, поскольку двойное кольцо визуально напоминало громоздкую букву. [8]
Функция [ править ]

Аминокислоты, включая триптофан, используются в качестве строительных блоков в биосинтезе белков , а белки необходимы для поддержания жизни. Триптофан относится к числу менее распространенных аминокислот, встречающихся в белках, но он играет важную структурную или функциональную роль, когда бы он ни появлялся. Например, остатки триптофана и тирозина играют особую роль в «заякоривании» мембранных белков внутри клеточной мембраны . Триптофан, наряду с другими ароматическими аминокислотами , также важен во взаимодействиях гликан-белок . Кроме того, триптофан действует как биохимический предшественник следующих соединений :
- Серотонин ( нейромедиатор ), синтезируемый триптофангидроксилазой . [9] [10]
- Мелатонин ( нейрогормон ), в свою очередь, синтезируется из серотонина с помощью ферментов N-ацетилтрансферазы и 5-гидроксииндол-О-метилтрансферазы . [11]
- Кинуренин , в который преимущественно (более 95%) метаболизируется триптофан. Два фермента, а именно индоламин-2,3-диоксигеназа (ИДО) в иммунной системе и мозге и триптофан-2,3-диоксигеназа (ТДО) в печени, ответственны за синтез кинуренина из триптофана. Кинурениновый путь катаболизма триптофана изменяется при ряде заболеваний, включая психические расстройства, такие как шизофрения , [12] большое депрессивное расстройство, [12] и биполярное расстройство . [12] [13]
- Ниацин , также известный как витамин B3 , синтезируется из триптофана посредством кинуренина и хинолиновых кислот . [14]
- Ауксины (класс фитогормонов ) синтезируются из триптофана. [15]
Нарушение мальабсорбции фруктозы вызывает неправильное всасывание триптофана в кишечнике, снижение уровня триптофана в крови, [16] и депрессия. [17]
У бактерий, синтезирующих триптофан, высокие клеточные уровни этой аминокислоты активируют белок -репрессор , который связывается с опероном trp . [18] Связывание этого репрессора с триптофановым опероном предотвращает транскрипцию последующей ДНК, которая кодирует ферменты, участвующие в биосинтезе триптофана. Столь высокий уровень триптофана предотвращает синтез триптофана посредством петли отрицательной обратной связи , и когда уровень триптофана в клетке снова падает, транскрипция оперона trp возобновляется. Это позволяет жестко регулировать и быстро реагировать на изменения внутреннего и внешнего уровня триптофана в клетке.
Метаболизм триптофана желудочно-кишечной микробиотой человека ( ) |
норма диетическая Рекомендуемая
В 2002 году Институт медицины США установил рекомендуемую диетическую норму (RDA) триптофана в размере 5 мг/кг массы тела в день для взрослых 19 лет и старше. [23]
источники Диетические
Триптофан присутствует в большинстве белковых продуктов или пищевых белков. Его особенно много в шоколаде , овсе , сушеных финиках , молоке , йогурте , твороге , красном мясе , яйцах , рыбе , птице , кунжуте , нуте , миндале , семечках подсолнечника , тыквенных семечках , конопли семенах , гречке , спирулине и арахисе . Вопреки распространенному мнению [24] [25] что приготовленная индейка содержит большое количество триптофана, содержание триптофана в индейке типично для домашней птицы. [26]
| Еда | Триптофан [г/100 г пищи] | Белок [г/100 г пищи] | Триптофан/белок [%] |
|---|---|---|---|
| Яичный белок , сушеный | 1.00 | 81.10 | 1.23 |
| Спирулина , сушеная | 0.92 | 57.47 | 1.62 |
| Треска Атлантическая , сушеная | 0.70 | 62.82 | 1.11 |
| Соевые бобы , сырые | 0.59 | 36.49 | 1.62 |
| Сыр, Пармезан | 0.56 | 37.90 | 1.47 |
| Семена чиа , сушеные | 0.44 | 16.50 | 2.64 |
| Семя кунжута | 0.37 | 17.00 | 2.17 |
| Семя конопли , очищенное | 0.37 | 31.56 | 1.17 |
| Сыр, Чеддер | 0.32 | 24.90 | 1.29 |
| Семечка подсолнечника | 0.30 | 17.20 | 1.74 |
| Свинина, отбивная | 0.25 | 19.27 | 1.27 |
| Турция | 0.24 | 21.89 | 1.11 |
| Курица | 0.24 | 20.85 | 1.14 |
| Говядина | 0.23 | 20.13 | 1.12 |
| Овес | 0.23 | 16.89 | 1.39 |
| Лосось | 0.22 | 19.84 | 1.12 |
| Баранина, отбивная | 0.21 | 18.33 | 1.17 |
| Окунь, Атлантика | 0.21 | 18.62 | 1.12 |
| Нут , сырой | 0.19 | 19.30 | 0.96 |
| Яйцо | 0.17 | 12.58 | 1.33 |
| Мука пшеничная, белая | 0.13 | 10.33 | 1.23 |
| Шоколад для выпечки , несладкий | 0.13 | 12.90 | 1.23 |
| Молоко | 0.08 | 3.22 | 2.34 |
| Рис белый среднезернистый вареный | 0.03 | 2.38 | 1.18 |
| Киноа , сырая | 0.17 | 14.12 | 1.20 |
| Киноа, приготовленная | 0.05 | 4.40 | 1.10 |
| Картофель, красновато-коричневый | 0.02 | 2.14 | 0.84 |
| Тамаринд | 0.02 | 2.80 | 0.64 |
| Банан | 0.01 | 1.03 | 0.87 |
Медицинское использование
Депрессия [ править ]
Поскольку триптофан превращается в 5-гидрокситриптофан (5-HTP), который затем превращается в нейромедиатор серотонин, было высказано предположение, что потребление триптофана или 5-HTP может улучшить симптомы депрессии за счет повышения уровня серотонина в мозге. Триптофан продается без рецепта в Соединенных Штатах (после того, как он был запрещен в той или иной степени в период с 1989 по 2005 год ) и Соединенном Королевстве в качестве пищевой добавки для использования в качестве антидепрессанта , анксиолитика и снотворного . В некоторых европейских странах он также продается как рецептурный препарат для лечения большой депрессии . Имеются данные о том, что уровень триптофана в крови вряд ли изменится при изменении диеты. [28] [29] но потребление очищенного триптофана повышает уровень серотонина в мозге, тогда как употребление продуктов, содержащих триптофан, этого не делает. [30]
В 2001 году был опубликован Кокрейновский обзор влияния 5-HTP и триптофана на депрессию. Авторы включили только исследования с высокой степенью строгости и включили в свой обзор как 5-HTP, так и триптофан из-за ограниченности данных по каждому из них. Из 108 исследований 5-HTP и триптофана при депрессии, опубликованных в период с 1966 по 2000 год, только два соответствовали стандартам качества авторов для включения, всего в исследовании приняли участие 64 участника. В двух включенных исследованиях эти вещества были более эффективными, чем плацебо , но авторы заявляют, что «доказательства были недостаточно качественными, чтобы быть убедительными», и отмечают, что «поскольку существуют альтернативные антидепрессанты, эффективность и безопасность которых доказаны, клиническая польза 5-HTP и триптофан в настоящее время ограничены». [31] Использование триптофана в качестве дополнительной терапии в дополнение к стандартному лечению расстройств настроения и тревожных расстройств не подтверждается научными данными. [31] [32]
Бессонница [ править ]
Американской академии медицины сна от 2017 года В рекомендациях по клинической практике не рекомендуется использовать триптофан при лечении бессонницы из-за низкой эффективности. [33]
Побочные эффекты [ править ]
Потенциальные побочные эффекты приема триптофана включают тошноту , диарею , сонливость , головокружение , головную боль , сухость во рту , помутнение зрения , седативный эффект , эйфорию и нистагм (непроизвольные движения глаз). [34] [35]
Взаимодействие [ править ]
Триптофан, принимаемый в виде пищевой добавки (например, в форме таблеток), может вызывать серотониновый синдром в сочетании с антидепрессантами класса ИМАО или СИОЗС или другими сильно серотонинергическими препаратами. [35] Поскольку добавка триптофана не была тщательно изучена в клинических условиях, ее взаимодействие с другими препаратами малоизвестно. [31]
Изоляция [ править ]
Впервые о выделении триптофана сообщил Фредерик Хопкинс в 1901 году. [36] Хопкинс извлек триптофан из гидролизованного казеина , извлекая 4–8 г триптофана из 600 г сырого казеина. [37]
Биосинтез и промышленное производство [ править ]
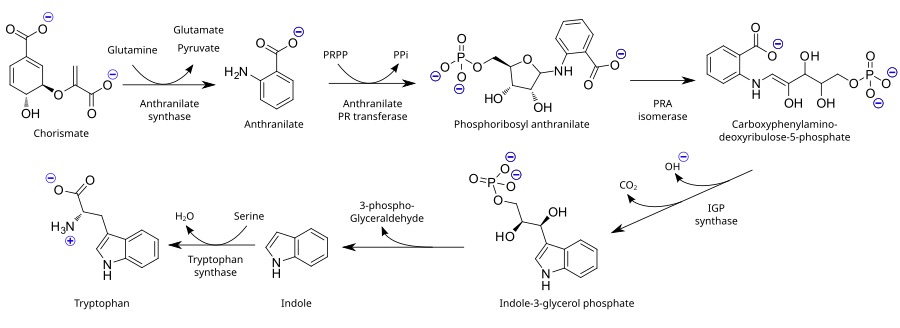
Являясь незаменимой аминокислотой, триптофан не синтезируется из более простых веществ у человека и других животных, поэтому ему необходимо присутствовать в рационе питания в виде триптофансодержащих белков. Растения и микроорганизмы обычно синтезируют триптофан из шикимовой кислоты или антранилата : [38] антранилат конденсируется с фосфорибозилпирофосфатом (PRPP), образуя пирофосфат в качестве побочного продукта. Кольцо рибозы с образованием индол- 3 раскрывается и подвергается восстановительному декарбоксилированию -глицеринфосфата; он, в свою очередь, превращается в индол . На последнем этапе триптофансинтаза катализирует образование триптофана из индола и аминокислоты серина .
Промышленное производство триптофана также является биосинтетическим и основано на ферментации серина и с использованием либо индола дикого типа, либо генетически модифицированных бактерий, таких как B. amyloliquefaciens , B. subtilis , C.lutamicum или E.coli . Эти штаммы несут мутации , которые предотвращают обратный захват ароматических аминокислот или множественные/сверхэкспрессированные опероны trp . Превращение катализируется ферментом триптофансинтазой . [39] [40] [41]
и Общество культура
Скандал с заражением Сёва Денко
В 1989 году в США произошла крупная вспышка синдрома эозинофилии-миалгии было зарегистрировано более 1500 случаев (СЭМ), при этом в CDC и по меньшей мере 37 случаев смерти. [42] После того, как предварительное расследование показало, что вспышка была связана с потреблением триптофана, Управление по контролю за продуктами и лекарствами США (FDA) отозвало добавки с триптофаном в 1989 году и запретило большую часть публичных продаж в 1990 году. [43] [44] [45] и другие страны последовали этому примеру. [46] [47]
Последующие исследования показали, что EMS был связан с определенными партиями L -триптофана, поставляемыми одним крупным японским производителем Showa Dko . [43] [48] [49] [50] В конце концов стало ясно, что недавние партии L -триптофана Сева Денко были загрязнены следами примесей, которые, как впоследствии считалось, были ответственны за вспышку скорой медицинской помощи в 1989 году. [43] [51] [52] Однако другие данные свидетельствуют о том, что триптофан сам по себе может быть потенциально основным фактором, способствующим развитию ЭМС. [53] Есть также утверждения, что прекурсор достиг концентрации, достаточной для образования токсичного димера . [54]
FDA ослабило ограничения на продажу и маркетинг триптофана в феврале 2001 года. [43] но продолжал ограничивать импорт триптофана, не предназначенного для использования без исключений, до 2005 года. [55]
Тот факт, что на предприятии в Сёва Денко использовались генно-инженерные бактерии для производства загрязненных партий L -триптофана, которые, как позже выяснилось, вызвали вспышку синдрома эозинофилии-миалгии, был приведен в качестве доказательства необходимости «тщательного мониторинга химической чистоты биотехнологических материалов». -производные продукты». [56] Те, кто призывает к контролю за чистотой, в свою очередь, подвергаются критике как активисты против ГМО , которые игнорируют возможные причины загрязнения, не связанные с ГМО, и угрожают развитию биотехнологий. [57]
и Гипотеза сонливости о мясе индейки
Распространенное утверждение в США и Великобритании [58] заключается в том, что чрезмерное потребление мяса индейки , как это наблюдается во время Дня Благодарения и Рождества , приводит к сонливости из-за высокого уровня триптофана, содержащегося в индейке. [25] Однако количество триптофана в индейке сопоставимо с количеством в других видах мяса. [24] [26] Сонливость после еды может быть вызвана другими продуктами, употребляемыми вместе с индейкой, в частности углеводами . [59] Прием пищи, богатой углеводами, вызывает выброс инсулина . [60] [61] [62] [63] Инсулин, в свою очередь, стимулирует поглощение крупных нейтральных аминокислот с разветвленной цепью (BCAA), но не триптофана, в мышцы, увеличивая соотношение триптофана и BCAA в кровотоке. В результате повышенное соотношение триптофана снижает конкуренцию на большом переносчике нейтральных аминокислот (который транспортирует как BCAA, так и ароматические аминокислоты), что приводит к большему проникновению триптофана через гематоэнцефалический барьер в спинномозговую жидкость (СМЖ). [63] [64] [65] Попадая в спинномозговую жидкость, триптофан превращается в серотонин в ядрах шва обычным ферментативным путем. [61] [66] Образующийся серотонин далее метаболизируется в гормон мелатонин , который является важным медиатором циркадного ритма. [67] — шишковидной железой . [11] Следовательно, эти данные позволяют предположить, что «сонливость, вызванная праздником» — или постпрандиальная сонливость — может быть результатом обильной еды, богатой углеводами, которая косвенно увеличивает выработку мелатонина в мозге и тем самым способствует сну. [60] [61] [62] [66]
Исследования [ править ]
В 1912 году Феликс Эрлих продемонстрировал, что дрожжи метаболизируют природные аминокислоты, главным образом, путем отщепления углекислого газа и замены аминогруппы гидроксильной группой . В результате этой реакции триптофан дает триптофол . [68]
Триптофан влияет на синтез серотонина в мозгу при пероральном приеме в очищенной форме и используется для изменения уровня серотонина в научных исследованиях. [30] Низкий уровень серотонина в мозгу индуцируется введением белка с низким содержанием триптофана в методе, называемом острым истощением триптофана . [69] Исследования с использованием этого метода оценили влияние серотонина на настроение и социальное поведение и обнаружили, что серотонин снижает агрессию и повышает доброжелательность. [70]
Флуоресценция [ править ]
Триптофан является важным внутренним флуоресцентным зондом (аминокислотой), который можно использовать для оценки природы микроокружения вокруг остатка триптофана. Большая часть собственной флуоресценции свернутого белка обусловлена возбуждением остатков триптофана.
См. также [ править ]
- 5-гидрокситриптофан (5-HTP)
- Реакция Акри-Розенгейма
- Реакция Адамкевича
- Аттенюатор (генетика)
- N , N -Диметилтриптамин
- Реакция Хопкинса-Коула
- Серотонин
- Триптамин
Ссылки [ править ]
- ↑ Перейти обратно: Перейти обратно: а б Гёрбиц CH, Торнроос К.В., Day GM (2012). «Монокристаллическое исследование L-триптофана с Z ′ = 16». Акта Кристаллогр. Б. 68 (Часть 5): 549–557. дои : 10.1107/S0108768112033484 . ПМИД 22992800 .
- ^ Доусон Р.М. и др. (1969). Данные для биохимических исследований . Оксфорд: Кларендон Пресс. ISBN 0-19-855338-2 .
- ^ «Номенклатура и символика аминокислот и пептидов» . Совместная комиссия IUPAC-IUB по биохимической номенклатуре. 1983. Архивировано из оригинала 2 декабря 2021 года . Проверено 22 октября 2022 г.
- ^ Сломински А, Семак И, Писарчик А, Свитман Т, Щесневский А, Вортсман Дж (2002). «Превращение L-триптофана в серотонин и мелатонин в клетках меланомы человека» . Письма ФЭБС . 511 (1–3): 102–6. дои : 10.1016/s0014-5793(01)03319-1 . ПМИД 11821057 . S2CID 7820568 .
- ^ «L-триптофан | C11H12N2O2 - ПабХим» . pubchem.ncbi.nlm.nih.gov . Проверено 22 декабря 2016 г.
- ^ Иглесиас-Грот С (август 2023 г.). «Поиски триптофана в газе звездного скопления IC 348 молекулярного облака Персея». Ежемесячные уведомления Королевского астрономического общества . 523 (2): 2876–2886. Бибкод : 2023MNRAS.523.2876I . дои : 10.1093/mnras/stad1535 .
- ^ Керзон Г. (31 декабря 1987 г.), Бендер Д.А., Джозеф М.Х., Кохен В., Стейнхарт Х. (ред.), «Хопкинс и открытие триптофана» , «Прогресс в исследованиях триптофана и серотонина», 1986 г. , Берлин, Бостон: Де Грюйтер, стр. XXIX – XL, doi : 10.1515/9783110854657-004 , ISBN 978-3-11-085465-7 , получено 19 февраля 2024 г.
- ^ «Комиссия IUPAC-IUB по биохимической номенклатуре. Однобуквенное обозначение аминокислотных последовательностей» . Журнал биологической химии . 243 (13): 3557–3559. 10 июля 1968 г. doi : 10.1016/S0021-9258(19)34176-6 .
- ^ Фернстрем Дж.Д. (1983). «Роль доступности предшественников в контроле биосинтеза моноаминов в мозге». Физиологические обзоры . 63 (2): 484–546. дои : 10.1152/physrev.1983.63.2.484 . ПМИД 6132421 .
- ^ Шехтер Дж. Д., Вуртман Р. Дж. (1990). «Выброс серотонина зависит от уровня триптофана в мозге» (PDF) . Исследования мозга . 532 (1–2): 203–10. дои : 10.1016/0006-8993(90)91761-5 . ПМИД 1704290 . S2CID 8451316 . Архивировано из оригинала (PDF) 9 августа 2020 года . Проверено 30 мая 2014 г.
- ↑ Перейти обратно: Перейти обратно: а б Вуртман Р.Дж., Антон-Тай Ф. (1969). «Шишковидная железа млекопитающих как нейроэндокринный преобразователь» (PDF) . Последние достижения в исследованиях гормонов . 25 : 493–522. дои : 10.1016/b978-0-12-571125-8.50014-4 . ISBN 978-0-12-571125-8 . ПМИД 4391290 . Архивировано из оригинала (PDF) 31 мая 2014 года.
- ↑ Перейти обратно: Перейти обратно: а б с Маркс В., МакГиннесс А.Дж., Рокс Т., Руусунен А., Клеминсон Дж., Уокер А.Дж., Гомес-да-Коста С., Лейн М., Санчес М., Диас А.П., Ценг П.Т. (23 ноября 2020 г.). «Кинурениновый путь при большом депрессивном расстройстве, биполярном расстройстве и шизофрении: метаанализ 101 исследования» . Молекулярная психиатрия . 26 (8): 4158–4178. дои : 10.1038/s41380-020-00951-9 . ISSN 1476-5578 . ПМИД 33230205 . S2CID 227132820 .
- ^ Бартоли Ф, Мисиак Б, Калловини Т, Кавалери Д, Чиони РМ, Крокамо С, Савитц ЖБ, Карра Дж (19 октября 2020 г.). «Кинурениновый путь при биполярном расстройстве: метаанализ уровней триптофана и родственных метаболитов в периферической крови». Молекулярная психиатрия . 26 (7): 3419–3429. дои : 10.1038/s41380-020-00913-1 . ПМИД 33077852 . S2CID 224314102 .
- ^ Икеда М., Цудзи Х., Накамура С., Итияма А., Нисидзука Ю., Хаяиси О. (1965). «Исследования по биосинтезу никотинамидадениндинуклеотида. II. Роль пиколинкарбоксилазы в биосинтезе никотинамидадениндинуклеотида из триптофана у млекопитающих» . Журнал биологической химии . 240 (3): 1395–401. дои : 10.1016/S0021-9258(18)97589-7 . ПМИД 14284754 .
- ^ Пальме К., Надь Ф (2008). «Новый ген синтеза ауксина» . Клетка . 133 (1): 31–2. дои : 10.1016/j.cell.2008.03.014 . ПМИД 18394986 . S2CID 9949830 .
- ^ Ледоховский М., Виднер Б., Мурр С., Спернер-Унтервегер Б., Фукс Д. (2001). «Нарушение всасывания фруктозы связано со снижением уровня триптофана в плазме» (PDF) . Скандинавский журнал гастроэнтерологии . 36 (4): 367–71. дои : 10.1080/003655201300051135 . ПМИД 11336160 . Архивировано из оригинала (PDF) 19 апреля 2016 года.
- ^ Ледоховский М., Спернер-Унтервегер Б., Виднер Б., Фукс Д. (июнь 1998 г.). «Нарушение всасывания фруктозы связано с ранними признаками психической депрессии». Европейский журнал медицинских исследований . 3 (6): 295–8. ПМИД 9620891 .
- ^ Голлник П., Бабицке П., Антсон А., Янофски С. (2005). «Сложность регуляции биосинтеза триптофана у Bacillus subtilis». Ежегодный обзор генетики . 39 : 47–68. дои : 10.1146/annurev.genet.39.073003.093745 . ПМИД 16285852 .
- ↑ Перейти обратно: Перейти обратно: а б с д и ж г час я Чжан Л.С., Дэвис СС (апрель 2016 г.). «Микробный метаболизм пищевых компонентов в биоактивные метаболиты: возможности для новых терапевтических вмешательств» . Геном Мед . 8 (1): 46. дои : 10.1186/s13073-016-0296-x . ПМЦ 4840492 . ПМИД 27102537 .
Лактобактерии виды. превращают триптофан в индол-3-альдегид (I3A) с помощью неидентифицированных ферментов [125]. Clostridium sporogenes превращают триптофан в IPA [6], вероятно, посредством триптофандезаминазы. ... IPA также эффективно удаляет гидроксильные радикалы.
Таблица 2. Микробные метаболиты: их синтез, механизмы действия и влияние на здоровье и болезни.
Рисунок 1: Молекулярные механизмы действия индола и его метаболитов на физиологию и заболевание хозяина. - ^ Викофф В.Р., Анфора А.Т., Лю Дж., Шульц П.Г., Лесли С.А., Питерс Э.К., Сиуздак Г. (март 2009 г.). «Метаболомический анализ показывает значительное влияние микрофлоры кишечника на метаболиты крови млекопитающих» . Учеб. Натл. акад. наук. США . 106 (10): 3698–3703. Бибкод : 2009PNAS..106.3698W . дои : 10.1073/pnas.0812874106 . ПМЦ 2656143 . ПМИД 19234110 .
Было показано, что продукция IPA полностью зависит от присутствия микрофлоры кишечника и может быть установлена путем колонизации бактерией Clostridium sporogenes .
Диаграмма метаболизма ИПА - ^ «3-Индолпропионовая кислота» . База данных метаболомов человека . Университет Альберты . Проверено 12 июня 2018 г.
- ^ Чаан Ю.Дж., Поггелер Б., Омар Р.А., Чейн Д.Г., Франджионе Б., Гисо Дж., Папполла М.А. (июль 1999 г.). «Мощные нейропротекторные свойства против бета-амилоида болезни Альцгеймера за счет эндогенной индольной структуры, связанной с мелатонином, индол-3-пропионовой кислоты» . Ж. Биол. Хим . 274 (31): 21937–21942. дои : 10.1074/jbc.274.31.21937 . ПМИД 10419516 . S2CID 6630247 .
[Индол-3-пропионовая кислота (IPA)] ранее была идентифицирована в плазме и спинномозговой жидкости человека, но ее функции неизвестны. ... В экспериментах по кинетической конкуренции с использованием агентов, улавливающих свободные радикалы, способность IPA улавливать гидроксильные радикалы превышала способность мелатонина, индоламина, который считается самым мощным природным поглотителем свободных радикалов. В отличие от других антиоксидантов, IPA не превращался в реакционноспособные интермедиаты с прооксидантной активностью.
- ^ Медицинский институт (2002). «Белки и аминокислоты» . Диетическая норма потребления энергии, углеводов, клетчатки, жиров, жирных кислот, холестерина, белков и аминокислот . Вашингтон, округ Колумбия: Издательство национальных академий. стр. 589–768. дои : 10.17226/10490 . ISBN 978-0-309-08525-0 .
- ↑ Перейти обратно: Перейти обратно: а б Баллантайн С. (21 ноября 2007 г.). «Турция вызывает сонливость?» . Научный американец . Проверено 6 июня 2013 г.
- ↑ Перейти обратно: Перейти обратно: а б МакКью К. «Chemistry.org: День Благодарения, индейка и триптофан» . Архивировано из оригинала 4 апреля 2007 года . Проверено 17 августа 2007 г.
- ↑ Перейти обратно: Перейти обратно: а б с Холден Дж. «Национальная база данных по питательным веществам Министерства сельского хозяйства США для стандартных справок, выпуск 22» . Лаборатория данных о питательных веществах, Служба сельскохозяйственных исследований, Министерство сельского хозяйства США . Проверено 29 ноября 2009 г.
- ^ Рамбали Б., Ван Андел И., Шенк Э., Вольтеринк Г., ван де Веркен Г., Стивенсон Х., Влиминг В. (2002). «[Вклад добавки какао в зависимость от курения сигарет]» (PDF) . РИВМ (отчет 650270002/2002). Национальный институт общественного здравоохранения и окружающей среды (Нидерланды). Архивировано из оригинала (PDF) 8 ноября 2005 г.
- ^ Со Н.Л., Уолтер Г.Т. (2011). «Триптофан и депрессия: может ли диета быть ответом?». Acta Neuropsychiatrica . 23 (1): 1601–5215. дои : 10.1111/j.1601-5215.2010.00508.x . S2CID 145779393 .
- ^ Фернстрем Дж.Д. (2012). «Влияния и побочные эффекты, связанные с непищевым использованием триптофана человеком» . Журнал питания . 142 (12): 2236С–2244С. дои : 10.3945/jn.111.157065 . ПМИД 23077193 .
- ↑ Перейти обратно: Перейти обратно: а б Вуртман Р.Дж., Хефти Ф., Меламед Э. (1980). «Прекурсорный контроль синтеза нейромедиаторов». Фармакологические обзоры . 32 (4): 315–35. ПМИД 6115400 .
- ↑ Перейти обратно: Перейти обратно: а б с Шоу К., Тернер Дж., Дель Мар С. (2002). Шоу К.А. (ред.). «Триптофан и 5-гидрокситриптофан при депрессии» (PDF) . Кокрановская база данных систематических обзоров . 2010 (1): CD003198. дои : 10.1002/14651858.CD003198 . ПМИД 11869656 .
- ^ Равиндран А.В., да Силва Т.Л. (сентябрь 2013 г.). «Дополнительные и альтернативные методы лечения как дополнение к фармакотерапии расстройств настроения и тревожных расстройств: систематический обзор». Журнал аффективных расстройств . 150 (3): 707–19. дои : 10.1016/j.jad.2013.05.042 . ПМИД 23769610 .
- ^ Сатея М.Дж., Буйссе Д.Д., Кристал А.Д., Нойбауэр Д.Н., Хилд Дж.Л. (февраль 2017 г.). «Руководство по клинической практике фармакологического лечения хронической бессонницы у взрослых: Руководство по клинической практике Американской академии медицины сна» . Джей Клин Сон Мед . 13 (2): 307–349. дои : 10.5664/jcsm.6470 . ПМК 5263087 . ПМИД 27998379 .
- ^ Кимура Т., Бир Д.М., Тейлор К.Л. (декабрь 2012 г.). «Резюме дискуссий на семинаре по установлению верхних пределов содержания аминокислот с особым вниманием к имеющимся данным по незаменимым аминокислотам лейцину и триптофану» . Журнал питания . 142 (12): 2245С–2248С. дои : 10.3945/jn.112.160846 . ПМИД 23077196 .
- ↑ Перейти обратно: Перейти обратно: а б Хауленд Р.Х. (июнь 2012 г.). «Бады для лечения депрессии». Журнал психосоциального ухода и служб психического здоровья . 50 (6): 13–6. дои : 10.3928/02793695-20120508-06 . ПМИД 22589230 .
- ^ Хопкинс Ф.Г., Коул С.В. (декабрь 1901 г.). «Вклад в химию белков: Часть I. Предварительное исследование до сих пор неописанного продукта триптического переваривания» . Журнал физиологии . 27 (4–5): 418–428. дои : 10.1113/jphysicalol.1901.sp000880 . ПМК 1540554 . ПМИД 16992614 .
- ^ Кокс Дж., Кинг Х. (1930). «L-Триптофан» . Орг. Синтез . 10 : 100. дои : 10.15227/orgsyn.010.0100 .
- ^ Радвански Э.Р., Последний RL (1995). «Биосинтез и метаболизм триптофана: биохимическая и молекулярная генетика» . Растительная клетка . 7 (7): 921–34. дои : 10.1105/tpc.7.7.921 . ПМК 160888 . ПМИД 7640526 .
- ^ Икеда М (2002). «Процессы производства аминокислот». Микробное производство L-аминокислот . Достижения в области биохимической инженерии/биотехнологии. Том. 79. стр. 1–35. дои : 10.1007/3-540-45989-8_1 . ISBN 978-3-540-43383-5 . ПМИД 12523387 .
- ^ Беккер Дж., Виттманн С. (2012). «Биологическое производство химикатов, материалов и топлива - Corynebacterium Glutamicum как универсальная клеточная фабрика». Современное мнение в области биотехнологии . 23 (4): 631–40. дои : 10.1016/j.copbio.2011.11.012 . ПМИД 22138494 .
- ^ Конрадо Р.Дж., Варнер Дж.Д., ДеЛиза член парламента (2008). «Инженерия пространственной организации метаболических ферментов: имитация синергии природы». Современное мнение в области биотехнологии . 19 (5): 492–9. дои : 10.1016/j.copbio.2008.07.006 . ПМИД 18725290 .
- ^ Аллен Дж., Варга Дж. (2014). «Синдром эозинофилии-миалгии». В Векслер П. (ред.). Энциклопедия токсикологии (3-е изд.). Берлингтон: Elsevier Science. ISBN 978-0-12-386455-0 .
- ↑ Перейти обратно: Перейти обратно: а б с д «Информационный документ о L-триптофане и 5-гидрокси-L-триптофане» . ФУ. S. Управление по контролю за продуктами и лекарствами, Центр безопасности пищевых продуктов и прикладного питания, Управление пищевых продуктов, маркировки и пищевых добавок. 1 февраля 2001 г. Архивировано из оригинала 25 февраля 2005 г. Проверено 8 февраля 2012 года .
- ^ «L-триптофан: использование и риски» . ВебМД . 12 мая 2017 года . Проверено 5 июня 2017 г.
- ^ Альтман Л.К. (27 апреля 1990 г.). «Исследования связывают расстройство с производителем пищевой добавки» . Нью-Йорк Таймс .
- ^ Касто А., Бидо I, Бурнериас I, Карлье П., Эфтимиу М.Л. (1991). «[Синдром «эозинофилии-миалгии», вызванный продуктами, содержащими L-триптофан. Совместная оценка французских региональных центров фармаконадзора. Анализ 24 случаев]». Терапия . 46 (5): 355–65. ПМИД 1754978 .
- ^ «Заявление COT о триптофане и синдроме эозинофилии-миалгии» (PDF) . Комитет Великобритании по токсичности химических веществ в пищевых продуктах, потребительских товарах и окружающей среде. Июнь 2004 года.
- ^ Слуцкер Л., Хоэсли ФК, Миллер Л., Уильямс Л.П., Уотсон Дж.К., Флеминг Д.В. (июль 1990 г.). «Синдром эозинофилии-миалгии, связанный с воздействием триптофана одного производителя». ДЖАМА . 264 (2): 213–7. дои : 10.1001/jama.264.2.213 . ПМИД 2355442 .
- ^ Назад Э.Э., Хеннинг К.Дж., Калленбах Л.Р., Брикс К.А., Ганн Р.А., Мелиус Дж.М. (апрель 1993 г.). «Факторы риска развития синдрома эозинофилии-миалгии среди потребителей L-триптофана в Нью-Йорке». Журнал ревматологии . 20 (4): 666–72. ПМИД 8496862 .
- ^ Килбурн Э.М., Филен Р.М., Камб М.Л., Фальк Х. (октябрь 1996 г.). «Триптофан, вырабатываемый Сева Денко, и синдром эпидемической эозинофилии-миалгии». Журнал ревматологии. Добавка . 46 : 81–8, обсуждение 89–91. ПМИД 8895184 .
- ^ Майено А.Н., Лин Ф., Фут К.С., Легеринг Д.А., Эймс М.М., Хедберг К.В., Глейх Г.Дж. (декабрь 1990 г.). «Характеристика «пика E», новой аминокислоты, связанной с синдромом эозинофилии-миалгии». Наука . 250 (4988): 1707–8. Бибкод : 1990Sci...250.1707M . дои : 10.1126/science.2270484 . ПМИД 2270484 .
- ^ Ито Дж., Хосаки Ю., Ториго Ю., Сакимото К. (январь 1992 г.). «Идентификация веществ, образующихся при разложении вещества пика Е в триптофане». Пищевая и химическая токсикология . 30 (1): 71–81. дои : 10.1016/0278-6915(92)90139-C . ПМИД 1544609 .
- ^ Смит М.Дж., Гаррет Р.Х. (ноябрь 2005 г.). «Ранее нераскрытая суть синдрома эозинофилии-миалгии: нарушение деградации гистамина». Исследование воспаления . 54 (11): 435–50. дои : 10.1007/s00011-005-1380-7 . ПМИД 16307217 . S2CID 7785345 .
- ^ Майкл Предатор Карлтон. «Молекулярная биология и генная инженерия, объясненная кем-то, кто этим занимался» . Архивировано из оригинала 24 июня 2007 года.
- ^ Аллен Дж.А., Петерсон А., Суфит Р., Хинчклифф М.Э., Махони Дж.М., Вуд Т.А., Миллер Ф.В., Уитфилд М.Л., Варга Дж. (ноябрь 2011 г.). «Постэпидемический синдром эозинофилии-миалгии, связанный с L-триптофаном» . Артрит и ревматизм . 63 (11): 3633–9. дои : 10.1002/арт.30514 . ПМЦ 3848710 . ПМИД 21702023 .
- ^ Майено А.Н., Глейх Г.Дж. (сентябрь 1994 г.). «Синдром эозинофилии-миалгии и выработка триптофана: поучительная история». Тенденции в биотехнологии . 12 (9): 346–52. дои : 10.1016/0167-7799(94)90035-3 . ПМИД 7765187 .
- ^ Рафалс П. (ноябрь 1990 г.). «Угрожает ли медицинская тайна биотехнологиям?». Наука . 250 (4981): 619. Бибкод : 1990Sci...250..619R . дои : 10.1126/science.2237411 . ПМИД 2237411 .
- ^ Хардинг Н. (21 декабря 2023 г.). «Как не дать рождественской еде испортить вам сон» . Телеграф . ISSN 0307-1235 . Проверено 25 декабря 2023 г.
- ^ «Еда и настроение. (профессор нейробиологии Ричард Вуртман) (Интервью)» . Информационный бюллетень по вопросам питания . Сентябрь 1992 года. [ мертвая ссылка ]
- ↑ Перейти обратно: Перейти обратно: а б Лайонс П.М., Трусвелл А.С. (март 1988 г.). «На предшественник серотонина влияет тип углеводной пищи у здоровых взрослых» . Американский журнал клинического питания . 47 (3): 433–9. дои : 10.1093/ajcn/47.3.433 . ПМИД 3279747 .
- ↑ Перейти обратно: Перейти обратно: а б с Вуртман Р.Дж., Вуртман Дж.Дж., Риган М.М., Макдермотт Дж.М., Цай Р.Х., Бреу Дж.Дж. (январь 2003 г.). «Влияние обычной еды, богатой углеводами или белками, на соотношение триптофана и тирозина в плазме» . Американский журнал клинического питания . 77 (1): 128–32. дои : 10.1093/ajcn/77.1.128 . ПМИД 12499331 .
- ↑ Перейти обратно: Перейти обратно: а б Афаги А., О'Коннор Х., Чоу С.М. (февраль 2007 г.). «Углеводные блюда с высоким гликемическим индексом сокращают время сна» . Американский журнал клинического питания . 85 (2): 426–30. дои : 10.1093/ajcn/85.2.426 . ПМИД 17284739 .
- ↑ Перейти обратно: Перейти обратно: а б Бэнкс В.А., Оуэн Дж.Б., Эриксон М.А. (2012). «Инсулин в мозге: туда и обратно» . Фармакология и терапия . 136 (1): 82–93. doi : 10.1016/j.pharmthera.2012.07.006 . ISSN 0163-7258 . ПМК 4134675 . ПМИД 22820012 .
- ^ Пардридж В.М., Ольдендорф В.Х. (август 1975 г.). «Кинетический анализ гематоэнцефалического барьерного транспорта аминокислот». Biochimica et Biophysical Acta (BBA) – Биомембраны . 401 (1): 128–36. дои : 10.1016/0005-2736(75)90347-8 . ПМИД 1148286 .
- ^ Махер Т.Дж., Глейзер Б.С., Вуртман Р.Дж. (май 1984 г.). «Суточные колебания концентраций основных и нейтральных аминокислот в плазме, а также концентраций аспартата и глутамата в эритроцитах: влияние потребления белка с пищей». Американский журнал клинического питания . 39 (5): 722–9. дои : 10.1093/ajcn/39.5.722 . ПМИД 6538743 .
- ↑ Перейти обратно: Перейти обратно: а б Фернстром Дж. Д., Вуртман Р. Дж. (1971). «Содержание серотонина в мозгу: увеличивается после приема углеводной диеты». Наука . 174 (4013): 1023–5. Бибкод : 1971Sci...174.1023F . дои : 10.1126/science.174.4013.1023 . ПМИД 5120086 . S2CID 14345137 .
- ^ Атул Хуллар, доктор медицинских наук (10 июля 2012 г.). «Роль мелатонина в циркадном ритме цикла сна-бодрствования» . Psychiatric Times, том 29, № 7. 29 .
{{cite journal}}: Для цитирования журнала требуется|journal=( помощь ) - ^ Джексон Р.В. (1930). «Синтез триптофола» (PDF) . Журнал биологической химии . 88 (3): 659–662. дои : 10.1016/S0021-9258(18)76755-0 .
- ^ Молодой СН (сентябрь 2013 г.). «Острое истощение триптофана у человека: обзор теоретических, практических и этических аспектов» . Журнал психиатрии и неврологии . 38 (5): 294–305. дои : 10.1503/jpn.120209 . ПМК 3756112 . ПМИД 23428157 .
- ^ Молодой СН (2013). «Влияние повышения и понижения уровня триптофана на настроение и социальное поведение человека» . Философские труды Лондонского королевского общества. Серия Б, Биологические науки . 368 (1615): 20110375. doi : 10.1098/rstb.2011.0375 . ПМЦ 3638380 . ПМИД 23440461 .
Дальнейшее чтение [ править ]
- Вуд Р.М., Риллинг Дж.К., Санфей А.Г., Бхагвагар З., Роджерс Р.Д. (май 2006 г.). «Влияние истощения триптофана на эффективность повторной игры «Дилемма заключенного» у здоровых взрослых» . Нейропсихофармакология . 31 (5): 1075–84. дои : 10.1038/sj.npp.1300932 . ПМИД 16407905 .
Внешние ссылки [ править ]
- «ПУТЬ КЕГГА: Метаболизм триптофана - Homo sapiens» . KEGG: Киотская энциклопедия генов и геномов. 23 августа 2006 года . Проверено 20 апреля 2008 г.
- ГП Мосс. «Катаболизм триптофана (ранние стадии)» . Номенклатурный комитет Международного союза биохимии и молекулярной биологии (NC-IUBMB). Архивировано из оригинала 13 сентября 2003 года . Проверено 20 апреля 2008 г.
- ГП Мосс. «Катаболизм триптофана (более поздние стадии)» . Номенклатурный комитет Международного союза биохимии и молекулярной биологии (NC-IUBMB). Архивировано из оригинала 13 сентября 2003 года . Проверено 20 апреля 2008 г.
- Б. Миккельсон, Д.П. Миккельсон (22 ноября 2007 г.). «Индейка вызывает сонливость» . Справочные страницы городских легенд . Snopes.com . Проверено 20 апреля 2008 г.