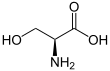
Серин
| |||
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Серин | |||
| Другие имена 2-амино-3-гидроксипропановая кислота | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| ЧЭБИ |
| ||
| ЧЕМБЛ |
| ||
| ХимическийПаук | |||
| Лекарственный Банк |
| ||
| Информационная карта ECHA | 100.000.250 | ||
| Номер ЕС |
| ||
| |||
| КЕГГ | |||
ПабХим CID | |||
| НЕКОТОРЫЙ |
| ||
Панель управления CompTox ( EPA ) | |||
| Характеристики [2] | |||
| C3H7NOC3H7NO3 | |||
| Молярная масса | 105.093 g·mol −1 | ||
| Появление | белые кристаллы или порошок | ||
| Плотность | 1,603 г/см 3 (22 °С) | ||
| Температура плавления | 246 ° C (475 ° F; 519 К) разлагается. | ||
| растворимый | |||
| Кислотность ( pKa ) | 2,21 (карбоксил), 9,15 (амино) [1] | ||
| Страница дополнительных данных | |||
| Серин (страница данных) | |||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Серин (символ Ser или S ) [3] [4] представляет собой α- аминокислоту , которая используется в биосинтезе белков. Он содержит α- аминогруппу (которая находится в протонированном состоянии – NH +
3 в биологических условиях), карбоксильная группа (находящаяся в депротонированном состоянии – COO −
образуются в биологических условиях), а боковая цепь состоит из гидроксиметильной группы, что классифицирует ее как полярную аминокислоту. Она может синтезироваться в организме человека при нормальных физиологических условиях, что делает ее заменимой аминокислотой. Он кодируется кодонами UCU , UCC, UCA, UCG, AGU и AGC.
Происшествие [ править ]
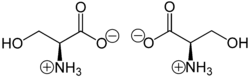
Это соединение является одной из протеиногенных аминокислот . В природе в белках встречается только L - стереоизомер . Он не имеет существенного значения для рациона человека, поскольку синтезируется в организме из других метаболитов , в том числе глицина . Серин был впервые получен из протеина шелка , особенно богатого источника, в 1865 году Эмилем Крамером. [5] Его название происходит от латинского , обозначающего шелк слова sericum . Структура Серина была основана в 1902 году. [6] [7]
Биосинтез [ править ]
Биосинтез серина начинается с окисления ( 3-фосфоглицерата промежуточного продукта гликолиза ) до 3-фосфогидроксипирувата и НАДН под действием фосфоглицератдегидрогеназы ( EC 1.1.1.95 ). Восстановительное аминирование (трансаминирование) этого кетона фосфосеринтрансаминазой ( EC 2.6.1.52 ) дает 3-фосфорсерин ( O -фосфосерин), который гидролизуется до серина фосфосеринфосфатазой ( EC 3.1.3.3 ). [8] [9]
У бактерий, таких как E. coli, эти ферменты кодируются генами serA (EC 1.1.1.95), serC (EC 2.6.1.52) и serB (EC 3.1.3.3). [10]

Биосинтез глицина : Серингидроксиметилтрансфераза (SHMT = серинтрансгидроксиметилаза) также катализирует обратимое превращение L -серина в глицин (ретро-альдольное расщепление) и 5,6,7,8-тетрагидрофолата в 5,10-метилентетрагидрофолат (мТГФ) (гидролиз). . [11] SHMT представляет собой фермент, зависимый от пиридоксальфосфата (PLP). Глицин также может образовываться из CO 2 , NH. +
4 , и mTHF в реакции, катализируемой глицинсинтазой . [8]
Синтез и реакции [ править ]
В промышленности L -серин производят из глицина и метанола, катализируемого гидроксиметилтрансферазой . [12]
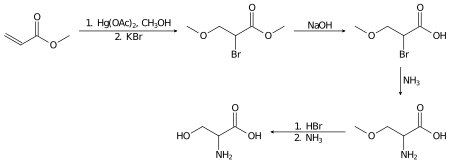
Рацемический серин можно получить в лаборатории из метилакрилата в несколько стадий: [13]
Гидрирование серина дает диол серинол :
- HOCH 2 CH(NH 2 )CO 2 H + 2 H 2 → HOCH 2 CH(NH 2 )CH 2 OH + 2 H 2 O
Биологическая функция [ править ]
Метаболический [ править ]

Серин важен в обмене веществ поскольку участвует в биосинтезе пуринов , и пиримидинов . Он является предшественником нескольких аминокислот, включая глицин и цистеин , а также триптофана в бактериях. Он также является предшественником множества других метаболитов, включая сфинголипиды и фолат , который является основным донором одноуглеродных фрагментов в биосинтезе. [ нужна ссылка ]
Сигнализация [ править ]
D -серин, синтезируемый в нейронах серинрацемазой из L -серина (его энантиомера ), служит нейромодулятором, коактивируя NMDA-рецепторы , делая их способными открываться, если они затем также связывают глутамат . D -серин является мощным агонистом глицинового участка (NR1) канонических дигетеромерных NMDA-рецепторов . Чтобы рецептор открылся, глутамат и либо глицин, либо D с ним должны связаться -серин; кроме того, блокатор пор не должен быть связан (например, Mg 2+ или Zn 2+ ). [14] Фактически, D -серин является более сильным агонистом глицина в NMDAR, чем сам глицин. [15] [16] Однако было показано, что D-серин действует как антагонист/обратный коагонист t -NMDA-рецепторов через сайт связывания глицина на субъединице GluN3. [17] [18]
Лиганды [ править ]
D До недавнего времени считалось, что -серин существует только у бактерий; это была вторая D- аминокислота, которая, как было обнаружено, естественным образом существует в организме человека и присутствует в качестве сигнальной молекулы в мозге вскоре после открытия D -аспартата . Если бы D -аминокислоты были обнаружены у людей раньше, сайт глицина на рецепторе NMDA мог бы вместо этого называться сайтом D -серина. [19] Помимо центральной нервной системы, D -серин играет сигнальную роль в периферических тканях и органах, таких как хрящи, [20] почка, [21] и кавернозное тело [22]
Вкусовые ощущения [ править ]
Чистый D -серин представляет собой беловатый кристаллический порошок с очень слабым затхлым ароматом. D -серин сладкий с небольшим кисловатым вкусом при средних и высоких концентрациях. [23]
Клиническое значение
Нарушения дефицита серина представляют собой редкие нарушения биосинтеза аминокислоты L -серина. В настоящее время зарегистрировано три расстройства:
- Дефицит 3-фосфоглицератдегидрогеназы
- Дефицит 3-фосфорсеринфосфатазы
- Дефицит фосфосеринаминотрансферазы
Эти ферментные дефекты приводят к тяжелым неврологическим симптомам, таким как врожденная микроцефалия и тяжелая психомоторная заторможенность, а также, у пациентов с дефицитом 3-фосфоглицератдегидрогеназы, к трудноизлечимым судорогам. Эти симптомы в разной степени реагируют на лечение L -серином, иногда в сочетании с глицином. [24] [25] Ответ на лечение варьируется, а долгосрочный и функциональный результат неизвестен. Чтобы обеспечить основу для улучшения понимания эпидемиологии, корреляции генотипа/фенотипа и исхода этих заболеваний, их влияния на качество жизни пациентов, а также для оценки диагностических и терапевтических стратегий, некоммерческой Международной рабочей организацией был создан реестр пациентов. Группа по расстройствам, связанным с нейротрансмиттерами (iNTD). [26]
Помимо нарушения биосинтеза серина может нарушаться и его транспорт. Одним из примеров является спастическая тетраплегия, истончение мозолистого тела и прогрессирующая микроцефалия — заболевание, вызванное мутациями, влияющими на функцию переносчика нейтральных аминокислот А.
для терапевтического использования Исследования
Классификация L -серина как незаменимой аминокислоты стала считаться условной, поскольку позвоночные, такие как человек, не всегда могут синтезировать оптимальные количества в течение всей жизни. [27] Безопасность L -серина была продемонстрирована в одобренном FDA клиническом исследовании фазы I на людях с боковым амиотрофическим склерозом, БАС , у пациентов (идентификатор ClinicalTrials.gov: NCT01835782), [28] [29] но лечение симптомов БАС еще не показано. Метаанализ 2011 года показал, что дополнительный саркозин оказывает средний эффект на негативные и общие симптомы шизофрении. [30] Также есть доказательства того, что L -серин может играть терапевтическую роль при диабете. [31]
D -серин изучается на грызунах как потенциальное средство лечения шизофрении. [32] D -серин также был описан как потенциальный биомаркер для ранней диагностики болезни Альцгеймера (БА) из-за относительно высокой его концентрации в спинномозговой жидкости вероятных пациентов с БА. [33] Было показано, что D-серин, который вырабатывается в головном мозге, действует как антагонист/обратный коагонист t -NMDA-рецепторов, смягчая потерю нейронов на животной модели височной эпилепсии . [34]
Предполагается, что D -серин является потенциальным средством лечения нейросенсорных нарушений слуха, таких как потеря слуха и шум в ушах . [35]
См. также [ править ]
- изосерин
- Гомосерин (изотреонин)
- Сериновый октамерный кластер
Ссылки [ править ]
- ^ Доусон, RMC и др., Данные для биохимических исследований , Оксфорд, Clarendon Press, 1959.
- ^ Западный RC, изд. (1981). Справочник CRC по химии и физике (62-е изд.). Бока-Ратон, Флорида: CRC Press. п. С-512. ISBN 0-8493-0462-8 .
- ^ «Номенклатура и символика аминокислот и пептидов» . Совместная комиссия IUPAC-IUB по биохимической номенклатуре. 1983. Архивировано из оригинала 9 октября 2008 года . Проверено 5 марта 2018 г.
- ^ «Номенклатура и символика аминокислот и пептидов (Рекомендации IUPAC-IUB, 1983 г.)», Pure Appl. хим. , 56 (5): 595–624, 1984, doi : 10.1351/pac198456050595 .
- ^ Крамер Э. (1865). «О составляющих шелка» . Журнал практической химии (на немецком языке). 96 :76–98. Серин назван на с. 93: «Я опишу тело, о котором идет речь, по имени Серин». (Я буду описывать рассматриваемое тело [т. е. вещество] именем «серин».)
- ^ Фишер Э., Лейхс Х. (1902). «Синтез серина, -глюкозаминовой и других оксиаминокислот » l кислоты . Отчеты Немецкого химического общества (на немецком языке). 35 (3): 3787–3805. дои : 10.1002/cber.190203503213 .
- ^ «Серин» . Колумбийская энциклопедия, 6-е изд . энциклопедия.com . Проверено 22 октября 2012 г.
- ^ Jump up to: Перейти обратно: а б Страйер Л. (1988). Биохимия (3-е изд.). Нью-Йорк: WH Freeman. п. 580 . ISBN 978-0-7167-1843-7 .
- ^ КЕГГ EC 3.1.3.3 и т. д.
- ^ Юнипрот: serB
- ^ Ленинджер А.Л., Нельсон Д.Л., Кокс М.М. (2000). Принципы биохимии (3-е изд.). Нью-Йорк: WH Freeman. ISBN 1-57259-153-6 .
- ^ Карлхайнц Драуц, Ян Грейсон, Аксель Климанн, Ханс-Петер Криммер, Вольфганг Лейхтенбергер, Кристоф Векбекер (2006). Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a02_057.pub2 . ISBN 978-3527306732 .
{{cite encyclopedia}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Картер Х.Э. , Вест HD (1940). « Дл -Серин» . Орг. Синтез. 20:81 . дои : 10.15227/orgsyn.020.0081 .
- ^ Лю Ю, Хилл Р.Х., Архем П., фон Эйлер Г. (2001). «NMDA и глицин регулируют сродство сайта блокировки Mg2+ в каналах рецептора NMDA NR1-1a/NR2A, экспрессируемых в ооцитах Xenopus». Науки о жизни . 68 (16): 1817–1826. дои : 10.1016/S0024-3205(01)00975-4 . ПМИД 11292060 .
- ^ Маккей М.А., Кравценюк М., Томас Р., Митчелл Н.Д., Дурсун С.М., Бейкер ГБ (6 февраля 2019 г.). «D-серин: потенциальный терапевтический агент и/или биомаркер при шизофрении и депрессии?» . Границы в психиатрии . 10:25 . дои : 10.3389/fpsyt.2019.00025 . ISSN 1664-0640 . ПМК 6372501 . ПМИД 30787885 .
D-серин более эффективен, чем глицин, в качестве коагониста рецептора NMDA, имеет региональное распределение в мозге, аналогичное распределению рецепторов NMDA, и, по-видимому, более тесно связан с синаптическими рецепторами NMDA, чем глицин (который более тесно связан с с несинаптическими NMDA-рецепторами).
- ^ Волоскер Х., Балу Д.Т. (9 июня 2020 г.). «D-серин как хранитель активности рецепторов NMDA: значение для фармакологического лечения тревожных расстройств» . Трансляционная психиатрия . 10 (1): 184. дои : 10.1038/s41398-020-00870-x . ISSN 2158-3188 . ПМЦ 7283225 . ПМИД 32518273 .
D-серин функционально является более мощным активатором синаптических NMDAR, чем глицин, и все больше данных свидетельствуют о том, что он служит основным коагонистом NMDAR в лимбических областях мозга, вовлеченных в нервно-психические расстройства.
- ^ Пилли Дж., Кумар С.С. (11 октября 2012 г.). «Тригетеромерные N-метил-D-аспартатные рецепторы дифференцируют синаптические входы на пирамидальные нейроны соматосенсорной коры: участие субъединицы GluN3A» . Нейронаука . 222 : 75–88. doi : 10.1016/j.neuroscience.2012.07.020 . ISSN 1873-7544 . ПМИД 22814002 . S2CID 23158971 .
- ^ Бисли С., Кумар С.С. (01 ноября 2023 г.). «Рецептор tN-метил-d-аспартата: доводы в пользу того, что d-серин следует считать его обратным коагонистом» . Нейрофармакология . 238 : 109654. doi : 10.1016/j.neuropharm.2023.109654 . ISSN 1873-7064 . ПМИД 37437688 .
- ^ Мотет Дж.П., Пэрент А.Т., Волоскер Х., Брейди Р.О., Линден DJ, Феррис КД, Рогавски М.А., Снайдер Ш. (апрель 2000 г.). «D-серин является эндогенным лигандом глицинового участка рецептора N -метил-D-аспартата» . Труды Национальной академии наук Соединенных Штатов Америки . 97 (9): 4926–4931. Бибкод : 2000PNAS...97.4926M . дои : 10.1073/pnas.97.9.4926 . ЧВК 18334 . ПМИД 10781100 .
- ^ Такарада Т., Хиной Э., Такахата Ю., Йонеда Ю. (май 2008 г.). «Серинрацемаза подавляет хондрогенную дифференцировку хряща Sox9-зависимым образом». Журнал клеточной физиологии . 215 (2): 320–328. дои : 10.1002/jcp.21310 . ПМИД 17929246 . S2CID 45669104 .
- ^ Ма MC, Хуан Х.С., Чен Ю.С., Ли Ш. (ноябрь 2008 г.). «Механочувствительные N -метил-D-аспартатные рецепторы способствуют сенсорной активации в почечной лоханке крысы» . Гипертония . 52 (5): 938–944. doi : 10.1161/ГИПЕРТОНИАХА.108.114116 . ПМИД 18809793 .
- ^ Гасеми М., Резания Ф., Левин Дж., Мур К.П., Мани А.Р. (июнь 2010 г.). «D-серин модулирует нейрогенное расслабление в кавернозных телах крыс». Биохимическая фармакология . 79 (12): 1791–1796. дои : 10.1016/j.bcp.2010.02.007 . ПМИД 20170643 .
- ^ Каваи М., Секинэ-Хаякава Ю., Окияма А., Ниномия Ю. (декабрь 2012 г.). «Вкусовые ощущения L- и D-аминокислот у человека». Аминокислоты . 43 (6): 2349–2358. дои : 10.1007/s00726-012-1315-x . ПМИД 22588481 . S2CID 17671611 .
- ^ де Конинг Т.Дж. (апрель 2006 г.). «Лечение аминокислотами при нарушениях серина». Журнал наследственных метаболических заболеваний . 29 (2): 347–351. дои : 10.1007/s10545-006-0269-0 . ПМИД 16763900 . S2CID 25013468 .
- ^ Табатабаи Л., Кломп Л.В., Бергер Р., де Конинг Т.Дж. (март 2010 г.). «Синтез L-серина в центральной нервной системе: обзор нарушений, вызванных дефицитом серина». Мол Генет Метаб . 99 (3): 256–262. дои : 10.1016/j.ymgme.2009.10.012 . ПМИД 19963421 .
- ^ «Реестр пациентов» .
- ^ Меткалф Дж.С., Данлоп Р.А., Пауэлл Дж.Т., Банак С.А., Кокс Пенсильвания (2017). «L-серин: природная аминокислота с терапевтическим потенциалом». Исследования нейротоксичности . 33 (1): 213–221. дои : 10.1007/s12640-017-9814-x . ISSN 1029-8428 . ПМИД 28929385 . S2CID 20271849 .
- ^ Данлоп Р.А., Кокс П.А., Банак С.А., Роджерс К.Дж. (2013). «Небелковая аминокислота BMAA неправильно включается в белки человека вместо L-серина, вызывая неправильное сворачивание и агрегацию белков» . ПЛОС ОДИН . 8 (9): e75376. Бибкод : 2013PLoSO...875376D . дои : 10.1371/journal.pone.0075376 . ПМЦ 3783393 . ПМИД 24086518 .
- ^ Левин Т.Д., Миллер Р.Г., Брэдли В.Г., Мур Д.Х., Саперштейн Д.С., Флинн Л.Е., Кац Дж.С., Форшью Д.А., Меткалф Дж.С., Банак С.А., Кокс Пенсильвания (2017-01-02). «Клиническое исследование I фазы безопасности L-серина для пациентов с БАС» . Боковой амиотрофический склероз и лобно-височная дегенерация . 18 (1–2): 107–111. дои : 10.1080/21678421.2016.1221971 . ISSN 2167-8421 . ПМИД 27589995 . S2CID 4584977 .
- ^ Сингх С.П., Сингх В. (октябрь 2011 г.). «Метаанализ эффективности дополнительных модуляторов рецепторов NMDA при хронической шизофрении». Препараты ЦНС . 25 (10): 859–885. дои : 10.2165/11586650-000000000-00000 . ПМИД 21936588 . S2CID 207299820 .
- ^ Холм Л.Дж., Бушард К. (2019). «L-серин: забытая аминокислота с потенциальной терапевтической ролью при диабете» . АПМИС . 127 (10): 655–659. дои : 10.1111/ап.12987 . ISSN 0903-4641 . ПМК 6851881 . ПМИД 31344283 .
- ^ Балу Д.Т., Ли Ю., Пуль М.Д., Бенниворт М.А., Басу А.С., Такаги С., Большаков В.Ю., Койл Дж.Т. (июнь 2013 г.). «Множественные пути риска шизофрении сходятся у мышей с нокаутом серинрацемазы, мышиной модели гипофункции рецептора NMDA» . Труды Национальной академии наук Соединенных Штатов Америки . 110 (26): Е2400–Е2409. Бибкод : 2013PNAS..110E2400B . дои : 10.1073/pnas.1304308110 . ПМЦ 3696825 . ПМИД 23729812 .
- ^ Мадейра К, Лоуренсу М.В., Варгас-Лопес К., Суэмото К.К., Брандао К.О., Рейс Т., Лейте Р.Е., Лакс Дж., Жакоб-Фильо В., Паскуалуччи К.А., Гринберг Л.Т., Феррейра С.Т., Паниццутти Р. (5 мая 2015 г.). «Уровни D-серина при болезни Альцгеймера: значение для разработки новых биомаркеров» . Трансляционная психиатрия . 5 (5): е561. дои : 10.1038/tp.2015.52 . ПМЦ 4471283 . ПМИД 25942042 .
- ^ Бисли С., Салленбергер Т., Кротти К., Айлани Р., Д'Орио К., Эванс К., Огунканле Э.О., Ропер М.Г., Кумар С.С. (2020-10-02). «D-серин смягчает потерю клеток, связанную с височной эпилепсией» . Природные коммуникации . 11 (1): 4966. Бибкод : 2020NatCo..11.4966B . дои : 10.1038/s41467-020-18757-2 . ISSN 2041-1723 . ПМЦ 7532172 . ПМИД 33009404 .
- ^ Ван Дж., Серратрис Н., Ли СиДжей, Франсуа Ф., Свидлер Дж.В., Пуэль Дж.Л., Мотет Дж.П., Руэль Дж. (17 декабря 2021 г.). «Физиопатологическое значение D-серина в улитке млекопитающих» . Границы клеточной нейронауки . 15 . Frontiers Media SA: 733004. doi : 10.3389/fncel.2021.733004 . ISSN 1662-5102 . ПМЦ 8718999 . ПМИД 34975405 .