Гистамин
 | |
 | |
| Имена | |
|---|---|
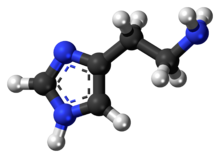
| Название ИЮПАК 2-(1H - имидазол-4-ил)этанамин | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| ХимическийПаук | |
| Лекарственный Банк | |
| Информационная карта ECHA | 100.000.092 |
| КЕГГ | |
| МеШ | Гистамин |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 5 Ч 9 Н 3 | |
| Молярная масса | 111.148 g·mol −1 |
| Температура плавления | 83,5 ° С (182,3 ° F; 356,6 К) |
| Точка кипения | 209,5 ° С (409,1 ° F; 482,6 К) |
| Легко растворим в холодной воде, горячей воде [1] | |
| Растворимость в других растворителях | Легко растворим в метаноле. Очень мало растворим в диэтиловом эфире. [1] Легко растворим в этаноле. |
| войти P | −0.7 [2] |
| Кислотность ( pKa ) | Имидазол : 6,04 Терминал NH 2 : 9,75 [2] |
| Фармакология | |
| L03AX14 ( ВОЗ ) V04CG03 ( ВОЗ ) (фосфат) | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Гистамин органическое представляет собой азотистое соединение, участвующее в передаче местных иммунных реакций , а также регулирующее функции кишечника физиологические и действующее как нейромедиатор для головного , спинного мозга и матки . [3] [4] Открытый в 1910 году гистамин считался местным гормоном ( аутокоидом ), поскольку он вырабатывается без участия классических эндокринных желез ; однако в последние годы гистамин был признан центральным нейромедиатором . [5] Гистамин участвует в воспалительной реакции и играет центральную роль медиатора зуда . [6] В рамках иммунного ответа на чужеродные патогены гистамин вырабатывается базофилами и тучными клетками, обнаруженными в близлежащих соединительных тканях . Гистамин увеличивает проницаемость капилляров патогены для лейкоцитов и некоторых белков , позволяя им воздействовать на в инфицированных тканях . [7] Он состоит из имидазольного кольца, присоединенного к этиламиновой цепи; в условиях аминогруппа физиологических боковой цепи протонируется .
Характеристики
[ редактировать ]минерального масла Гистаминовая основа, полученная в виде суспензии , плавится при 83–84 °С. [8] гидрохлорид [9] и фосфор [10] соли образуют белые гигроскопичные кристаллы и легко растворяются в воде или этаноле , но не в эфире . В водном растворе имидазольное кольцо гистамина существует в двух таутомерных формах, определяемых по тому, какой из двух атомов азота протонирован. Азот, находящийся дальше от боковой цепи, является «теле» азотом и обозначается знаком тау в нижнем регистре, а азот, расположенный ближе к боковой цепи, является «плюс» азотом и обозначается знаком «пи». Телетаутомер, N т -H -гистамин предпочтителен в растворе по сравнению с простаутомером N п -H -гистамин.

Гистамин имеет два основных центра, а именно алифатическую аминогруппу и тот атом азота имидазольного кольца, который еще не имеет протона . В физиологических условиях алифатическая аминогруппа (имеющая около pKa 9,4 ) будет протонирована , тогда как второй азот имидазольного кольца (pKa ≈ 5,8 ) не будет протонирован. [11] Таким образом, гистамин обычно протонируется до однозарядного катиона . Поскольку человеческая кровь является слабоосновной (с нормальным диапазоном pH от 7,35 до 7,45), преобладающая форма гистамина, присутствующая в крови человека, является монопротонной по алифатическому азоту. Гистамин — моноаминовый нейромедиатор .
Синтез и метаболизм
[ редактировать ]Гистамин образуется в результате декарбоксилирования аминокислоты , гистидина , реакции катализируемой ферментом - L гистидиндекарбоксилазой . Это гидрофильный вазоактивный амин .

После образования гистамин либо сохраняется, либо быстро инактивируется его первичными ферментами деградации , гистамин- N -метилтрансферазой или диаминоксидазой . В центральной нервной системе гистамин, высвобождаемый в синапсы, в первую очередь расщепляется гистамин- N -метилтрансферазой, тогда как в других тканях могут играть роль оба фермента. Некоторые другие ферменты, включая МАО-В и АЛДГ2 , дополнительно перерабатывают непосредственные метаболиты гистамина для выведения или переработки.
Бактерии также способны производить гистамин с помощью ферментов гистидиндекарбоксилазы, не связанных с теми, которые обнаружены у животных. Неинфекционная форма заболевания пищевого происхождения, отравление скомброидом , возникает из-за выработки гистамина бактериями в испорченных продуктах, особенно в рыбе. Ферментированные продукты и напитки естественным образом содержат небольшое количество гистамина из-за аналогичного преобразования, осуществляемого ферментирующими бактериями или дрожжами. Саке содержит гистамин в диапазоне 20–40 мг/л; вина содержат его в диапазоне 2–10 мг/л. [12]
Хранение и выпуск
[ редактировать ]
Большая часть гистамина в организме вырабатывается в гранулах тучных клеток и лейкоцитах (лейкоцитах), называемых базофилами . Тучных клеток особенно много в местах потенциального повреждения – носу, рту и ступнях, внутренних поверхностях тела и кровеносных сосудах. Гистамин, не являющийся тучноклеточным, обнаруживается в нескольких тканях, включая область гипоталамуса головного мозга , где он действует как нейромедиатор. местом хранения и высвобождения гистамина являются энтерохромаффиноподобные (ECL) клетки желудка Другим важным .
Наиболее важным патофизиологическим механизмом высвобождения гистамина тучными клетками и базофилами является иммунологический . Эти клетки, если они сенсибилизированы IgE -антителами, прикрепленными к их мембранам , дегранулируют при воздействии соответствующего антигена . Некоторые амины и алкалоиды , в том числе такие препараты, как морфин и алкалоиды кураре , могут вытеснять гистамин в гранулах и вызывать его высвобождение. Также обнаружено, что антибиотики, такие как полимиксин, стимулируют высвобождение гистамина.
Высвобождение гистамина происходит, когда аллергены связываются с антителами IgE, связанными с тучными клетками. Снижение перепроизводства IgE может снизить вероятность того, что аллергены найдут достаточное количество свободного IgE, чтобы вызвать выброс гистамина тучными клетками.
Деградация
[ редактировать ]Гистамин высвобождается тучными клетками в результате иммунного ответа и позже разлагается в основном двумя ферментами: диаминоксидазой (DAO), кодируемой генами AOC1, и гистамин-N-метилтрансферазой (HNMT), кодируемой геном HNMT. Наличие однонуклеотидных полиморфизмов (SNP) в этих генах связано с широким спектром заболеваний, от язвенного колита до расстройств аутистического спектра (РАС). [13] Деградация гистамина имеет решающее значение для предотвращения аллергических реакций на безвредные в остальном вещества.
ДАО обычно экспрессируется в эпителиальных клетках на кончике ворсинок слизистой оболочки тонкой кишки. [14] Снижение активности ДАО связано с желудочно-кишечными расстройствами и широко распространенной пищевой непереносимостью. Это связано с увеличением всасывания гистамина через энтероциты , что увеличивает концентрацию гистамина в кровотоке. [15] Одно исследование показало, что мигренью у пациентов с и чувствительностью к глютену положительно коррелирует более низкий уровень ДАО в сыворотке. [16] Низкая активность DAO может иметь более серьезные последствия, поскольку мутации в аллелях ABP1 гена AOC1 связаны с язвенным колитом. [17] Гетерозиготные или гомозиготные rs2052129, rs2268999, rs10156191 и rs1049742 рецессивные генотипы по аллелям повышали риск снижения активности ДАО. [18] Люди с генотипами пониженной активности ДАО могут избегать продуктов с высоким содержанием гистамина, таких как алкоголь, ферментированные продукты и выдержанные продукты, чтобы ослабить любые аллергические реакции. Кроме того, им следует знать, содержат ли пробиотики, которые они принимают, какие-либо штаммы, продуцирующие гистамин, и проконсультироваться со своим врачом, чтобы получить надлежащую поддержку. [ нужна ссылка ] .
HNMT экспрессируется в центральной нервной системе , дефицит которой приводит к агрессивному поведению и аномальным циклам сна и бодрствования у мышей. [19] Поскольку гистамин головного мозга как нейромедиатор регулирует ряд нейрофизиологических функций, упор был сделан на разработку препаратов, направленных на регуляцию гистамина. Ёсикава и др. исследует, как полиморфизмы C314T, A939G, G179A и T632C влияют на ферментативную активность HNMT и патогенез различных неврологических расстройств. [15] Эти мутации могут иметь как положительное, так и отрицательное влияние. некоторых пациентов с СДВГ Было показано, что у симптомы обостряются в ответ на пищевые добавки и консерванты, отчасти из-за выброса гистамина. В двойном слепом плацебо-контролируемом перекрестном исследовании дети с СДВГ, которые ответили ухудшением симптомов после употребления пробного напитка, с большей вероятностью имели полиморфизмы HNMT в T939C и Thr105Ile. [20] Роль гистамина в нейровоспалении и когнитивных процессах сделала его объектом изучения многих неврологических расстройств, включая расстройство аутистического спектра (РАС). Делеции de novo в гене HNMT также связаны с РАС. [13]
Тучные клетки выполняют важную иммунологическую роль, защищая организм от антигенов и поддерживая гомеостаз микробиома кишечника . Они действуют как сигнал тревоги, вызывая воспалительные реакции иммунной системы. Их присутствие в пищеварительной системе позволяет им служить ранним барьером для патогенов, проникающих в организм. Люди, которые страдают от широко распространенной чувствительности и аллергических реакций, могут страдать синдромом активации тучных клеток высвобождается чрезмерное количество гистамина (MCAS), при котором из тучных клеток , который не может быть должным образом расщеплен. Аномальное высвобождение гистамина может быть вызвано либо дисфункциональными внутренними сигналами от дефектных тучных клеток, либо развитием клональных популяций тучных клеток в результате мутаций, происходящих в тирозинкиназном наборе . [21] В таких случаях организм может оказаться не в состоянии вырабатывать достаточное количество деградирующих ферментов для правильного устранения избытка гистамина. Поскольку MCAS симптоматически характеризуется как такое обширное заболевание, его трудно диагностировать, и его можно ошибочно отнести к различным заболеваниям, включая синдром раздраженного кишечника и фибромиалгию . [21]
Гистамин часто рассматривается как потенциальная причина заболеваний, связанных с гиперреактивностью иммунной системы. У пациентов с астмой аномальная активация гистаминовых рецепторов в легких связана с бронхоспазмом , обструкцией дыхательных путей и выработкой избыточной слизи. Мутации деградации гистамина чаще встречаются у пациентов с сочетанием астмы и гиперчувствительности к аллергенам, чем у пациентов только с астмой. HNMT-464 TT и HNMT-1639 TT Полиморфизмы значительно чаще встречаются среди детей с аллергической астмой, последний из которых преобладает у афроамериканских детей. [22]
Механизм действия
[ редактировать ]У людей гистамин оказывает свое действие главным образом путем связывания с , связанными с G-белком рецепторами гистамина , обозначенными от H1 до H4 . [23] По состоянию на 2015 год [update]Считается, что гистамин активирует лиганд-управляемые хлоридные каналы в эпителии головного мозга и кишечника. [23] [24]
| Рецептор, связанный с G-белком | Расположение | Функция | Источники |
|---|---|---|---|
| гистамина H 1 Рецептор | • ЦНС : экспрессируется на дендритах выходных нейронов гистаминергического туберомаммиллярного ядра , которое проецируется на дорсальный шов , голубое пятно и дополнительные структуры. | • ЦНС : цикл сна-бодрствования (способствует бодрствованию), температура тела , ноцицепция , эндокринный гомеостаз , регулирует аппетит , участвует в когнитивной деятельности. | [23] [24] [25] [26] [27] |
| Гистаминовый H 2 рецептор | • ЦНС : Дорсальное полосатое тело ( хвостатое ядро и скорлупа ), кора головного мозга (наружные слои), гиппокампальная формация , зубчатое ядро мозжечка . | • ЦНС : Не установлено (примечание: большинство известных лигандов рецепторов H 2 не способны проникать через гематоэнцефалический барьер в концентрациях, достаточных для проведения нейропсихологических и поведенческих тестов) | [23] [24] [28] [27] |
| гистамина H 3 Рецептор | Расположен в центральной нервной системе и в меньшей степени периферической нервной системы. в тканях | Ауторецепторные и гетерорецепторные функции: снижение высвобождения нейромедиаторов гистамина, ацетилхолина , норадреналина , серотонина . Модулирует ноцицепцию, секрецию желудочной кислоты и прием пищи. | [23] |
| Гистаминовый H 4 рецептор | Расположен преимущественно на базофилах и в костном мозге . Он также экспрессируется в тимусе , тонком кишечнике , селезенке и толстой кишке . | Играет роль в хемотаксисе тучных клеток , восприятии зуда, выработке и секреции цитокинов, а также висцеральной гиперчувствительности. Другие предполагаемые функции (например, воспаление, аллергия, когнитивные функции и т. д.) полностью не охарактеризованы. | [23] |
| Лиганд-управляемый ионный канал | Расположение | Функция | Источники |
| Гистамин-управляемый хлоридный канал | Предположительно: ЦНС (гипоталамус, таламус) и эпителий кишечника. | Мозг: производит быстрые тормозные постсинаптические потенциалы. Кишечный эпителий: секреция хлоридов (связанная с секреторной диареей ) | [23] [24] |
Роли в теле
[ редактировать ]Хотя гистамин мал по сравнению с другими биологическими молекулами (содержит всего 17 атомов), он играет важную роль в организме. Известно, что он участвует в 23 различных физиологических функциях. Известно, что гистамин участвует во многих физиологических функциях благодаря своим химическим свойствам, которые позволяют ему быть универсальным в связывании. Он кулоновский (способный нести заряд), конформационный и гибкий. Это позволяет ему легче взаимодействовать и связываться. [29]
Расширение сосудов и падение артериального давления
[ редактировать ]Уже более ста лет известно, что внутривенное введение гистамина вызывает падение артериального давления. [30] Основной механизм касается как сосудистой гиперпроницаемости, так и вазодилатации. Связывание гистамина с эндотелиальными клетками заставляет их сокращаться, тем самым увеличивая утечку из сосудов. Он также стимулирует синтез и высвобождение различных релаксантов гладкомышечных клеток сосудов, таких как оксид азота , эндотелиальные гиперполяризующие факторы и другие соединения, что приводит к расширению кровеносных сосудов. [31] Эти два механизма играют ключевую роль в патофизиологии анафилаксии .
Воздействие на слизистую оболочку носа
[ редактировать ]Повышенная проницаемость сосудов приводит к выходу жидкости из капилляров в ткани, что приводит к классическим симптомам аллергической реакции: насморку и слезотечению. Аллергены могут связываться с IgE -нагруженными тучными клетками носовой полости оболочек слизистых . Это может привести к трем клиническим реакциям: [32]
- чихание из-за сенсорной нейронной стимуляции, связанной с гистамином
- гиперсекреция тканью железистой
- заложенность носа из-за нагрубания сосудов, связанного с расширением сосудов и повышенной капилляров проницаемостью
Регулирование сна и бодрствования
[ редактировать ]Гистамин — это нейромедиатор , который высвобождается гистаминэргическими нейронами , выступающими из млекопитающих гипоталамуса . Тела клеток этих нейронов расположены в части заднего гипоталамуса, известной как туберомаммилярное ядро (TMN). Гистаминовые нейроны в этой области составляют гистаминовую систему мозга , которая широко проецируется по всему мозгу и включает аксональные проекции в кору , медиальный пучок переднего мозга , другие ядра гипоталамуса, медиальную перегородку, ядро диагональной полосы, вентральную область покрышки, миндалевидное тело, полосатое тело, черная субстанция, гиппокамп, таламус и др. [33] Гистаминовые нейроны в TMN участвуют в регуляции цикла сна-бодрствования и при активации способствуют пробуждению. [34] Частота возбуждения гистаминовых нейронов в TMN сильно положительно коррелирует с состоянием возбуждения человека. Эти нейроны активируются быстро в периоды бодрствования, активируются медленнее в периоды расслабления/усталости и вообще перестают активироваться во время быстрого и медленного (небыстрого) сна. [ нужна ссылка ] .
первого поколения H1 - антигистамины (т.е. антагонисты гистаминовых рецепторов H1 ) способны преодолевать гематоэнцефалический барьер и вызывать сонливость путем антагонизма гистаминовых H1 - рецепторов в туберомаммилярном ядре. Новый класс второго поколения H1 антигистаминных препаратов с трудом проникает через гематоэнцефалический барьер и, следовательно, с меньшей вероятностью вызывает седативный эффект, хотя индивидуальные реакции, сопутствующие препараты и дозировка могут увеличить вероятность седативного эффекта. Напротив, гистаминовых H3 - антагонисты рецепторов увеличивают продолжительность бодрствования. Подобно седативному эффекту H1-антигистаминов первого поколения , неспособность сохранять бдительность может возникнуть из-за ингибирования биосинтеза гистамина или потери (т.е. дегенерации или разрушения) гистамин-высвобождающих нейронов в TMN.
Выделение желудочной кислоты
[ редактировать ]Энтерохромаффиноподобные клетки желудка выделяют гистамин, стимулируя париетальные клетки через H2 - рецепторы. Это вызывает поглощение углекислого газа и воды из крови, которые под действием карбоангидразы преобразуются в угольную кислоту. Кислота диссоциирует на ионы водорода и бикарбоната внутри париетальной клетки. Бикарбонат возвращается в кровоток, а водород закачивается в просвет желудка. Высвобождение гистамина прекращается по мере снижения pH желудка. [ нужна медицинская ссылка ] Молекулы -антагонисты , такие как ранитидин или фамотидин , блокируют рецептор H2 и предотвращают связывание гистамина, вызывая снижение секреции ионов водорода. [ нужна медицинская ссылка ]
Защитные эффекты
[ редактировать ]Хотя гистамин оказывает стимулирующее воздействие на нейроны, он также оказывает супрессивное действие, защищающее от предрасположенности к судорогам , лекарственной сенсибилизации, денервационной сверхчувствительности , ишемическим поражениям и стрессу. [35] Также было высказано предположение, что гистамин контролирует механизмы забывания воспоминаний и обучения. [36]
Эрекция и сексуальная функция
[ редактировать ]В этом разделе отсутствует информация о сексуальной дисфункции у женщин . ( октябрь 2023 г. ) |
Потеря либидо и эректильная дисфункция могут возникнуть во время лечения антагонистами гистаминовых H2 - рецепторов, такими как циметидин , ранитидин и рисперидон . [37] Введение гистамина в пещеристые тела мужчин с психогенной импотенцией вызывает полную или частичную эрекцию у 74% из них. [38] Было высказано предположение, что антагонисты H2 могут вызывать сексуальную дисфункцию за счет снижения функционального связывания тестостерона с его андрогенными рецепторами. [37]
Шизофрения
[ редактировать ]Метаболиты гистамина увеличиваются в спинномозговой жидкости у людей, страдающих шизофренией , тогда как эффективность мест связывания рецепторов H 1 снижается. Многие атипичные антипсихотические препараты увеличивают выработку гистамина, поскольку уровни гистамина у людей с этим расстройством, по-видимому, несбалансированы. [39]
Рассеянный склероз
[ редактировать ]Гистаминовая терапия для лечения рассеянного склероза в настоящее время изучается. Известно, что разные H-рецепторы по-разному влияют на лечение этого заболевания. рецепторы H1 контрпродуктивны и H4 В одном исследовании было показано, что при лечении рассеянного склероза. Считается, что рецепторы H 1 и H 4 увеличивают проницаемость гематоэнцефалического барьера, тем самым увеличивая проникновение нежелательных клеток в центральную нервную систему. Это может вызвать воспаление и ухудшение симптомов рассеянного склероза. Считается, что рецепторы H 2 и H 3 полезны при лечении пациентов с рассеянным склерозом. Было показано, что гистамин помогает дифференцировке Т-клеток. Это важно, поскольку при рассеянном склерозе иммунная система организма атакует собственные миелиновые оболочки нервных клеток (что приводит к потере сигнальной функции и возможной дегенерации нервов). Помогая Т-клеткам дифференцироваться, Т-клетки с меньшей вероятностью будут атаковать собственные клетки организма и вместо этого будут атаковать захватчиков. [40]
расстройства
[ редактировать ]Будучи неотъемлемой частью иммунной системы, гистамин может участвовать в нарушениях иммунной системы. [41] и аллергия . Мастоцитоз – редкое заболевание, при котором наблюдается пролиферация тучных клеток, вырабатывающих избыток гистамина. [42]
Непереносимость гистамина – это предполагаемый набор побочных реакций (таких как приливы крови, зуд, ринит и т. д.) на прием гистамина с пищей. Основная теория признает, что могут существовать побочные реакции на прием гистамина, но не признает непереносимость гистамина как отдельное состояние, которое можно диагностировать. [43]
Роль гистамина в здоровье и болезнях является областью продолжающихся исследований. Например, гистамин исследуется на предмет его потенциальной связи с эпизодами мигрени, когда наблюдается заметное повышение концентрации в плазме как гистамина, так и пептида, связанного с геном кальцитонина (CGRP). Эти два вещества являются мощными сосудорасширяющими средствами, и было продемонстрировано, что они взаимно стимулируют высвобождение друг друга в тригеминоваскулярной системе - механизм, который потенциально может спровоцировать возникновение мигрени. У пациентов с дефицитом деградации гистамина из-за вариантов гена AOC1, который кодирует фермент диаминоксидазы , диета с высоким содержанием гистамина вызывает мигрень, что предполагает потенциальную функциональную связь между экзогенным гистамином и CGRP, что может сыграть важную роль в понимание происхождения мигрени, вызванной диетой, так что роль гистамина, особенно в отношении CGRP, является многообещающей областью исследований для выяснения механизмов, лежащих в основе развития и обострения мигрени, особенно актуальной в контексте диетических триггеров и генетической предрасположенности, связанной с на метаболизм гистамина. [44]
История
[ редактировать ]Свойства гистамина, названного тогда β-имидазолилэтиламином, были впервые описаны в 1910 году британскими учёными Генри Х. Дейлом и П. П. Лейдлоу . [45] название гистамин» К 1913 году уже использовалось : сочетание форм гисто- « + амина давало «тканевой амин».
«Вещество Н» или «вещество Н» иногда используются в медицинской литературе для обозначения гистамина или гипотетического гистаминоподобного диффундирующего вещества, высвобождаемого при аллергических реакциях кожи и при реакциях тканей на воспаление.
См. также
[ редактировать ]- Анафилаксия
- Диаминоксидаза
- Гистамин N-метилтрансфераза
- Сенная лихорадка (аллергический ринит)
- Непереносимость гистамина
- Антагонист гистаминовых рецепторов
- Скомброидное пищевое отравление
- Световой чихательный рефлекс
Ссылки
[ редактировать ]- ^ Перейти обратно: а б Паспорт безопасности гистамина (технический отчет). sciencelab.com. 21 мая 2013 г. Архивировано из оригинала 24 марта 2012 г.
- ^ Перейти обратно: а б Вукович Д., Павлишин Ю. (март 2011 г.). «Систематическая оценка твердофазных микроэкстракционных покрытий для нецелевого метаболомного профилирования биологических жидкостей методами жидкостной хроматографии-масс-спектрометрии». Аналитическая химия . 83 (6): 1944–54. дои : 10.1021/ac102614v . ПМИД 21332182 .
- ^ Мариб Э (2001). Анатомия и физиология человека . Сан-Франциско: Бенджамин Каммингс. стр. 414 . ISBN 0-8053-4989-8 .
- ^ Ньето-Аламилья Г., Маркес-Гомес Р., Гарсиа-Гальвес А.М., Моралес-Фигероа Г.Е., Ариас-Монтаньо Х.А. (ноябрь 2016 г.). «Рецептор гистамина H3: структура, фармакология и функция» . Молекулярная фармакология . 90 (5): 649–673. дои : 10.1124/моль.116.104752 . ПМИД 27563055 .
- ^ Кеппель Хесселинк Дж. М. (декабрь 2015 г.). «Термины «аутакоид», «гормон» и «халон» и как они изменились со временем». Автономная и аутакоидная фармакология . 35 (4): 51–8. дои : 10.1111/aap.12037 . ПМИД 27028114 .
- ^ Андерсен Х.Х., Эльберлинг Дж., Арендт-Нильсен Л. (сентябрь 2015 г.). «Человеческие суррогатные модели гистаминергического и негистаминэргического зуда» (PDF) . Acta Dermato-Venereologica . 95 (7): 771–7. дои : 10.2340/00015555-2146 . ПМИД 26015312 . Архивировано (PDF) из оригинала 30 марта 2019 г. Проверено 20 февраля 2024 г.
- ^ Ди Джузеппе М., Фрейзер Д. (2003). Нельсон Биология 12 . Торонто: Томсон Канада. п. 473 . ISBN 0-17-625987-2 .
- ^ «Гистамин» . webbook.nist.gov . Архивировано из оригинала 27 апреля 2018 г. Проверено 4 января 2015 г.
- ^ «Гистамина дигидрохлорид Н7250» . Сигма-Олдрич . Архивировано из оригинала 9 августа 2015 г.
- ^ «Гистаминфосфат» (PDF) . Европейская фармакопея (5-е изд.). ISBN 9287152810 . Архивировано из оригинала (PDF) 4 января 2015 г. Проверено 4 января 2015 г.
- ^ Пайва ТБ, Томинага М, Пайва AC (июль 1970 г.). «Ионизация гистамина, N-ацетилгистамина и их йодсодержащих производных». Журнал медицинской химии . 13 (4): 689–92. дои : 10.1021/jm00298a025 . ПМИД 5452432 .
- ^ Джаяраджа К.Н., Скелли А.М., Фортнер А.Д., Мэтис Р.А. (ноябрь 2007 г.). «Анализ нейроактивных аминов в ферментированных напитках с использованием портативной системы капиллярного электрофореза с микрочипом» (PDF) . Аналитическая химия . 79 (21): 8162–9. дои : 10.1021/ac071306s . ПМИД 17892274 . Архивировано из оригинала (PDF) 19 июля 2011 года.
- ^ Перейти обратно: а б Райт С., Шин Дж.Х., Раджпурохит А., Дип-Собослай А., Колладо-Торрес Л., Брэндон Н.Дж. и др. (май 2017 г.). «Измененная экспрессия генов, передающих сигнал гистамина, при расстройствах аутистического спектра» . Трансляционная психиатрия . 7 (5): e1126. дои : 10.1038/tp.2017.87 . ПМЦ 5534955 . ПМИД 28485729 .
- ^ Томпсон Дж.С. (1990). «Значение кишечного градиента активности диаминоксидазы». Пищеварительные заболевания . 8 (3): 163–8. дои : 10.1159/000171249 . ПМИД 2110876 .
- ^ Перейти обратно: а б Ёсикава Т., Накамура Т., Янаи К. (февраль 2019 г.). «Гистамин -N -метилтрансфераза в мозге» . Международный журнал молекулярных наук . 20 (3): 737. doi : 10.3390/ijms20030737 . ПМК 6386932 . ПМИД 30744146 .
- ^ Гриауздате К., Маселис К., Жвирблиене А., Вайткус А., Янчяускас Д., Банайтите-Балейшене И. и др. (сентябрь 2020 г.). «Связь между мигренью, целиакией, нецелиакийной чувствительностью к глютену и активностью диаминоксидазы». Медицинские гипотезы . 142 : 109738. doi : 10.1016/j.mehy.2020.109738 . ПМИД 32416409 . S2CID 216303896 .
- ^ Гарсиа-Мартин Э., Мендоса Х.Л., Мартинес С., Таксонера С., Урселай Э., Ладеро Х.М. и др. (январь 2006 г.). «Тяжесть язвенного колита связана с полиморфизмом гена диаминоксидазы, но не гена гистамин-N-метилтрансферазы» . Всемирный журнал гастроэнтерологии . 12 (4): 615–20. дои : 10.3748/wjg.v12.i4.615 . ПМК 4066097 . ПМИД 16489678 .
- ^ Майнц Л., Ю. К. Ф., Родригес Э., Баурехт Х., Бибер Т., Иллиг Т. и др. (июль 2011 г.). «Ассоциация однонуклеотидных полиморфизмов в гене диаминоксидазы с активностью диаминоксидазы в сыворотке» (PDF) . Аллергия . 66 (7): 893–902. дои : 10.1111/j.1398-9995.2011.02548.x . ПМИД 21488903 . S2CID 205405463 . [ постоянная мертвая ссылка ]
- ^ Бранко АС, Ёсикава Ф.С., Пьетробон А.Дж., Сато М.Н. (27 августа 2018 г.). «Роль гистамина в модуляции иммунного ответа и воспаления» . Медиаторы воспаления . 2018 : 9524075. doi : 10.1155/2018/9524075 . ПМК 6129797 . ПМИД 30224900 .
- ^ Стивенсон Дж., Сонуга-Барк Э., Макканн Д., Гримшоу К., Паркер К.М., Роуз-Зерилли М.Дж. и др. (сентябрь 2010 г.). «Роль полиморфизмов генов деградации гистамина в смягчении воздействия пищевых добавок на симптомы СДВГ у детей». Американский журнал психиатрии . 167 (9): 1108–15. дои : 10.1176/appi.ajp.2010.09101529 . ПМИД 20551163 .
- ^ Перейти обратно: а б Хениш Б., Нётен М.М., Молдерингс Г.Дж. (ноябрь 2012 г.). «Системная болезнь активации тучных клеток: роль молекулярно-генетических изменений в патогенезе, наследственности и диагностике» . Иммунология . 137 (3): 197–205. дои : 10.1111/j.1365-2567.2012.03627.x . ПМЦ 3482677 . ПМИД 22957768 .
- ^ Анвари С., Вилидал К.А., Дай Х., Джонс Б.Л. (декабрь 2015 г.). «Генетические вариации гистаминового пути у детей с аллергической и неаллергической астмой» . Американский журнал респираторной клеточной и молекулярной биологии . 53 (6): 802–9. дои : 10.1165/rcmb.2014-0493OC . ПМЦ 4742940 . ПМИД 25909280 .
- ^ Перейти обратно: а б с д и ж г Панула П., Чазо П.Л., Коварт М., Гутцмер Р., Леурс Р., Лю В.Л. и др. (июль 2015 г.). «Международный союз фундаментальной и клинической фармакологии. XCVIII. Гистаминовые рецепторы» . Фармакологические обзоры . 67 (3): 601–55. дои : 10.1124/пр.114.010249 . ПМК 4485016 . ПМИД 26084539 .
- ^ Перейти обратно: а б с д Воутерс М.М., Викарио М., Сантос Дж. (январь 2016 г.). «Роль тучных клеток в функциональных расстройствах ЖКТ» . Гут . 65 (1): 155–68. дои : 10.1136/gutjnl-2015-309151 . ПМИД 26194403 .
- ^ Бландина П., Мунари Л., Провенси Г., Пассани М.Б. (2012). «Гистаминовые нейроны туберомиллярного ядра: целый центр или отдельные субпопуляции?» . Границы системной нейронауки . 6 : 33. дои : 10.3389/fnsys.2012.00033 . ПМЦ 3343474 . ПМИД 22586376 .
- ^ Стромберга З., Чесс-Вильямс Р., Моро К. (март 2019 г.). «Гистаминовая модуляция уротелия мочевого пузыря, собственной пластинки и сократительной активности детрузора через рецепторы H1 и H2» . Научные отчеты . 9 (1): 3899. Бибкод : 2019НатСР...9.3899С . дои : 10.1038/s41598-019-40384-1 . ПМК 6405771 . ПМИД 30846750 .
- ^ Перейти обратно: а б Пал С., Гашева О.Ю., Завея Д.С., Майнингер С.М., Гашев А.А.J (январь 2020 г.). «Гистамин-опосредованная аутокринная передача сигналов в мезентериальных перилимфатических тучных клетках» . Am J Physiol Regul Integr Comp Physiol . 318 (3): 590–604. дои : 10.1152/ajpregu.00255.2019 . ПМК 7099465 . ПМИД 31913658 . S2CID 210119438 .
- ^ Магуайр Джей Джей, Davenport AP (29 ноября 2016 г.). «Н2 - рецептор» . Руководство IUPHAR/BPS по фармакологии . Международный союз фундаментальной и клинической фармакологии. Архивировано из оригинала 21 марта 2017 года . Проверено 20 марта 2017 г.
- ^ Носзал Б., Крашни М., Рач А. (2004). «Гистамин: основы биологической химии». В Фалусе А., Гросмане Н., Дарвасе З. (ред.). Гистамин: биология и медицинские аспекты . Будапешт: SpringMed. стр. 15–28. ISBN 380557715X .
- ^ Дейл Х.Х., Лэйдлоу П.П. (декабрь 1910 г.). «Физиологическое действие бета-иминазолилэтиламина» . Журнал физиологии . 41 (5): 318–44. дои : 10.1113/jphysicalol.1910.sp001406 . ПМК 1512903 . ПМИД 16993030 .
- ^ Аббас А (2018). Клеточная и молекулярная иммунология . Эльзевир. п. 447. ИСБН 978-0-323-47978-3 .
- ^ Монро Э.В., Дейли А.Ф., Шалхуб Р.Ф. (февраль 1997 г.). «Оценка достоверности волдырей и воспалений, вызванных гистамином, для прогнозирования клинической эффективности антигистаминных препаратов» . Журнал аллергии и клинической иммунологии . 99 (2): S798-806. дои : 10.1016/s0091-6749(97)70128-3 . ПМИД 9042073 .
- ^ Брэди С. (2012). Основная нейрохимия — принципы молекулярной, клеточной и медицинской нейробиологии . Уолтем, США: Эльзевир. п. 337. ИСБН 978-0-12-374947-5 .
- ^ Браун Р.Э., Стивенс Д.Р., Хаас Х.Л. (апрель 2001 г.). «Физиология гистамина мозга». Прогресс нейробиологии . 63 (6): 637–72. дои : 10.1016/s0301-0082(00)00039-3 . ПМИД 11164999 . S2CID 10170830 .
- ^ Янаи К., Таширо М. (январь 2007 г.). «Физиологическая и патофизиологическая роль нейронального гистамина: выводы исследований позитронно-эмиссионной томографии человека». Фармакология и терапия . 113 (1): 1–15. doi : 10.1016/j.pharmthera.2006.06.008 . ПМИД 16890992 .
- ^ Альварес Э.О. (май 2009 г.). «Роль гистамина в познании». Поведенческие исследования мозга . 199 (2): 183–9. дои : 10.1016/j.bbr.2008.12.010 . hdl : 11336/80375 . ПМИД 19126417 . S2CID 205879131 .
- ^ Перейти обратно: а б Уайт Дж. М., Рамболд Г. Р. (1988). «Поведенческие эффекты гистамина и его антагонистов: обзор». Психофармакология . 95 (1): 1–14. дои : 10.1007/bf00212757 . ПМИД 3133686 . S2CID 23148946 .
- ^ Кара А.М., Лопес-Мартинс Р.А., Антунес Э., Нахум Ч.Р., Де Нуччи Дж. (февраль 1995 г.). «Роль гистамина в эрекции полового члена человека». Британский журнал урологии . 75 (2): 220–4. дои : 10.1111/j.1464-410X.1995.tb07315.x . ПМИД 7850330 .
- ^ Ито С (2004). «Роль центральной гистаминергической системы при шизофрении». Новости и перспективы наркотиков . 17 (6): 383–7. дои : 10.1358/dnp.2004.17.6.829029 . ПМИД 15334189 .
Многие атипичные антипсихотики также увеличивают оборот гистамина.
- ^ Джадиди-Ниара Ф, Миршафи А (сентябрь 2010 г.). «Гистамин и гистаминовые рецепторы в патогенезе и лечении рассеянного склероза». Нейрофармакология . 59 (3): 180–9. doi : 10.1016/j.neuropharm.2010.05.005 . ПМИД 20493888 . S2CID 7852375 .
- ^ Зампели Э, Тилигада Э (май 2009 г.). «Роль рецептора гистамина H4 в иммунных и воспалительных нарушениях» . Британский журнал фармакологии . 157 (1): 24–33. дои : 10.1111/j.1476-5381.2009.00151.x . ПМЦ 2697784 . ПМИД 19309354 .
- ^ Валент П., Хорни Х.П., Эскрибано Л., Лонгли Б.Дж., Ли С.И., Шварц Л.Б. и др. (июль 2001 г.). «Диагностические критерии и классификация мастоцитоза: консенсусное предложение». Исследования лейкемии . 25 (7): 603–25. дои : 10.1016/S0145-2126(01)00038-8 . ПМИД 11377686 .
- ^ Риз И, Баллмер-Вебер Б, Бейер К, Дёлле-Бирке С, Кляйне-Теббе Дж, Климек Л, Лэммель С, Лепп У, Салога Дж, Шефер С, Шепфалуси З, Трейдлер Р, Верфель Т, Цубербье Т, Ворм М (2021). «Руководство по ведению подозреваемых побочных реакций на пероральный гистамин: Руководство Немецкого общества аллергологии и клинической иммунологии (DGAKI), Общества детской аллергологии и экологической медицины (GPA), Медицинской ассоциации немецких аллергологов (AeDA), а также Швейцарское общество аллергологии и иммунологии (SGAI) и Австрийское общество аллергологии и иммунологии (ÖGAI)» . Аллергол Селект . 5 : 305–314. дои : 10.5414/ALX02269E . ПМЦ 8511827 . ПМИД 34651098 .
 В эту статью включен текст из этого источника, доступного по лицензии CC BY 4.0 .
В эту статью включен текст из этого источника, доступного по лицензии CC BY 4.0 . - ^ Де Мора Ф, Месслингер К (2024). «Является ли пептид, связанный с геном кальцитонина (CGRP), недостающим звеном в мигрени, вызванной пищевым гистамином? Обзор функциональных связей кишечника с тригеминоваскулярной системой» . Открытие наркотиков сегодня . 29 (4). дои : 10.1016/j.drudis.2024.103941 . ПМИД 38447930 .
- ^ Дейл Х.Х., Лэйдлоу П.П. (декабрь 1910 г.). «Физиологическое действие бета-иминазолилэтиламина» . Журнал физиологии . 41 (5): 318–44. дои : 10.1113/jphysicalol.1910.sp001406 . ПМК 1512903 . ПМИД 16993030 . [ постоянная мертвая ссылка ]