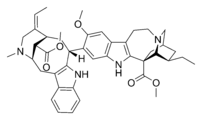
Алкалоид

Алкалоиды — это класс основных природных , органических соединений содержащих хотя бы один азота атом . В эту группу также входят некоторые родственные соединения с нейтральными [2] и даже слабокислотные свойства . [3] Некоторые синтетические соединения аналогичной структуры также можно назвать алкалоидами. [4] Помимо углерода , водорода и азота , алкалоиды могут также содержать кислород или серу . Еще реже они могут содержать такие элементы, как фосфор , хлор и бром . [5]
Алкалоиды производятся большим разнообразием организмов, включая бактерии , грибы , растения и животные . [6] Их можно очистить из сырых экстрактов этих организмов путем кислотно-щелочной экстракции с силикагелем или экстракции растворителем с последующей хроматографией на колонке . [7] Алкалоиды обладают широким спектром фармакологической активности, включая противомалярийное (например, хинин ), противоастматическое (например, эфедрин ), противораковое (например, гомохаррингтонин ), [8] холиномиметики (например, галантамин ), [9] сосудорасширяющее (например, винкамин ), антиаритмическое (например, хинидин ), анальгетическое (например, морфин ), [10] антибактериальные (например, хелеритрин ), [11] и антигипергликемическая активность (например, берберин ). [12] [13] Многие из них нашли применение в традиционной или современной медицине или в качестве отправной точки для открытия новых лекарств . Другие алкалоиды обладают психотропным (например, псилоцин ) и стимулирующим действием (например, кокаин , кофеин , никотин , теобромин ), [14] и использовались в энтеогенных ритуалах или в качестве рекреационных наркотиков . Алкалоиды могут быть токсичными также (например, атропин , тубокурарин ). [15] Хотя алкалоиды действуют на различные метаболические системы человека и других животных, они почти всегда вызывают горький вкус . [16]
Граница между алкалоидами и другими азотсодержащими природными соединениями нечеткая. [17] Такие соединения, как аминокислотные пептиды , белки , нуклеотиды , нуклеиновые кислоты , амины и антибиотики , обычно не называют алкалоидами. [2] Природные соединения, содержащие азот в экзоциклическом положении ( мескалин , серотонин , дофамин и др.), обычно относят к аминам, а не к алкалоидам. [18] Однако некоторые авторы считают алкалоиды частным случаем аминов. [19] [20] [21]
Именование [ править ]

Название «алкалоиды» (нем. Alkaloide ) было введено в 1819 году немецким химиком Карлом Фридрихом Вильгельмом Мейсснером и происходит от позднелатинского корня щелочь и греческого суффикса -οειδής - («подобный»). [номер 1] Однако широкое употребление этот термин получил только после публикации обзорной статьи Оскара Якобсена в химическом словаре Альберта Ладенбурга в 1880-х годах. [22] [23]
Единого метода названия алкалоидов не существует. [24] Многие отдельные названия образуются путем добавления суффикса «ine» к названию вида или рода. [25] Например, атропин выделен из растения Atropa belladonna ; Стрихнин получают из семян стрихнинового дерева ( Strychnos nux-vomica L.). [5] Если из одного растения извлекают несколько алкалоидов, их названия часто различаются вариациями суффикса: «идин», «анин», «алин», «инин» и т. д. Существует также по крайней мере 86 алкалоидов, названия которых содержат корень «вин». «потому что они извлечены из растений барвинка , таких как барвинок розовый ( Charanthus roseus ); [26] их называют барвинка алкалоидами . [27] [28] [29]
История [ править ]

Алкалоидсодержащие растения издревле использовались человеком в лечебных и рекреационных целях. Например, лекарственные растения были известны в Месопотамии примерно с 2000 г. до н.э. [30] В « Одиссее Гомера» говорится о подарке египетской царицы Елене — о лекарстве, приносящем забвение. Предполагается, что подарком был опиумсодержащий наркотик. [31] В китайской книге о комнатных растениях, написанной в I–III веках до нашей эры, упоминается медицинское использование эфедры и опийного мака . [32] Кроме того, листья коки использовались коренными жителями Южной Америки с древних времен. [33]
Экстракты растений, содержащих токсичные алкалоиды, такие как аконитин и тубокурарин , с древности использовались для отравления стрел. [30]
Исследования алкалоидов начались в 19 веке. В 1804 году немецкий химик Фридрих Сертюрнер выделил из опиума «снотворное начало» (лат. principium somniferum ), которое он назвал «морфием», имея в виду Морфея , греческого бога сновидений; в немецком и некоторых других центральноевропейских языках это до сих пор название препарата. Термин «морфий», используемый в английском и французском языках, был предложен французским физиком Жозефом Луи Гей-Люссаком .
Значительный вклад в химию алкалоидов в первые годы ее развития внесли французские исследователи Пьер Жозеф Пеллетье и Жозеф Бьенеме Каванту , открывшие хинин (1820) и стрихнин (1818). Примерно в это же время было открыто несколько других алкалоидов, в том числе ксантин (1817 г.), атропин (1819 г.), кофеин (1820 г.), кониин (1827 г.), никотин (1828 г.), колхицин (1833 г.), спартеин (1851 г.) и кокаин (1860 г.). . [34] Развитие химии алкалоидов ускорилось с появлением в ХХ веке спектроскопических и хроматографических методов, так что к 2008 году было идентифицировано более 12 000 алкалоидов. [35]
Первый полный синтез алкалоида был достигнут в 1886 году немецким химиком Альбертом Ладенбургом . Он получил кониин путем взаимодействия 2-метилпиридина с ацетальдегидом и восстановления полученного 2-пропенилпиридина натрием. [36] [37]

Классификации [ править ]

По сравнению с большинством других классов природных соединений алкалоиды характеризуются большим структурным разнообразием. Единой классификации не существует. [38] Первоначально, когда знания о химической структуре отсутствовали, полагались на ботаническую классификацию исходных растений. В настоящее время эта классификация считается устаревшей. [5] [39]
Более поздние классификации основаны на сходстве углеродного скелета ( например , индол- , изохинолин- и пиридин -подобного) или биохимического предшественника ( орнитина , лизина , тирозина , триптофана и др.). [5] Однако в пограничных случаях они требуют компромиссов; [38] например, никотин содержит пиридиновый фрагмент никотинамида и пирролидиновую часть орнитина. [40] и поэтому могут быть отнесены к обоим классам. [41]
Алкалоиды часто делят на следующие основные группы: [42]
- «Истинные алкалоиды» содержат азот в гетероцикле и происходят из аминокислот . [43] Их характерные примеры — атропин , никотин и морфин . В эту группу входят также некоторые алкалоиды, которые помимо азотистого гетероцикла содержат терпен ( например , эвонин [44] ) или пептидные фрагменты ( например, эрготамин [45] ). Пиперидиновые алкалоиды кониин и коницеин можно рассматривать как истинные алкалоиды (а не псевдоалкалоиды: см. ниже). [46] хотя они не происходят из аминокислот. [47]
- «Протоалкалоиды», которые содержат азот (но не азотистый гетероцикл) и также происходят из аминокислот. [43] Примеры включают мескалин , адреналин и эфедрин .
- Полиаминные алкалоиды – производные путресцина , спермидина и спермина .
- Пептидные и циклопептидные алкалоиды. [48]
- Псевдоалкалоиды – алкалоидные соединения, не происходящие от аминокислот. [49] В эту группу входят терпеноподобные и стероидоподобные алкалоиды. [50] а также пуриноподобные алкалоиды, такие как кофеин , теобромин , теакрин и теофиллин . [51] Некоторые авторы относят эфедрин и катинон к псевдоалкалоидам. Они происходят от аминокислоты фенилаланина , но получают атом азота не от аминокислоты, а путем переаминирования . [51] [52]
Некоторые алкалоиды не имеют характерного для их группы углеродного скелета. Так, галантамин и гомоапорфины не содержат изохинолинового фрагмента, а в основном относятся к изохинолиновым алкалоидам. [53]
Основные классы мономерных алкалоидов перечислены в таблице ниже:
| Сорт | Основные группы | Основные этапы синтеза | Примеры |
|---|---|---|---|
| Алкалоиды с азотистыми гетероциклами (истинные алкалоиды) | |||
пирролидина Производные [54] 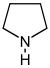 | Орнитин или аргинин → путресцин → N-метилпутресцин → N-метил-Δ 1 -пирролин [55] | Кускогигрин , гигрин , гигролин, стахидрин [54] [56] | |
тропана Производные [57]  | Группа атропина Замена в позициях 3, 6 или 7 | Орнитин или аргинин → путресцин → N-метилпутресцин → N-метил-Δ 1 -пирролин [55] | Атропин , скополамин , гиосциамин. [54] [57] [58] |
| Кокаиновая группа Замена в позициях 2 и 3 | Кокаин , экгонин [57] [59] | ||
пирролизидина Производные [60] 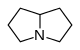 | Неэфиры | У растений: орнитин или аргинин → путресцин → гомоспермидин → ретронецин. [55] | Ретронецин , гелиотридин, лабурнин [60] [61] |
| Сложные эфиры монокарбоновых кислот | Индицин, линделофин, саррацин [60] | ||
| Макроциклические диэфиры | Платифиллин , триходесмин [60] | ||
| 1-аминопирролизидины ( лолины ) | У грибов : L -пролин + L -гомосерин → N- (3-амино-3-карбоксипропил)пролин → норлолин. [62] [63] | Лолин, N -формиллолин, N -ацетиллолин [64] | |
пиперидина Производные [65]  | Лизин → кадаверин → Δ 1 -пиперидеин [66] | Седамин , лобелин, анаферин, пиперин [46] [67] | |
| Октановая кислота → коницеин → кониин [47] | Кониин , кониин [47] | ||
| хинолизидина Производные [68] [69] | люпинина Группа | Лизин → кадаверин → Δ 1 -пиперидеин [70] | Люпинин , нуфаридин [68] |
| цитизина Группа | Цитизин [68] | ||
| Спартайнская группа | Спартеин , лупанин , анагигрин. [68] | ||
| Группа Матрин . | Матрин, оксиматрин, алломатридин [68] [71] [72] | ||
| ормосанина Группа | Ормосанин, пиптантин [68] [73] | ||
индолизидина Производные [74] 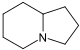 | Лизин → δ-полуальдегид α-аминоадипиновой кислоты → пипеколиновая кислота → 1 индолизидинон [75] | Свайнсонин , кастаноспермин [76] | |
пиридина Производные [77] [78] 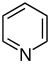 | Простые производные пиридина | Никотиновая кислота → дигидроникотиновая кислота → 1,2-дигидропиридин [79] | Тригонеллин , рицинин , ареколин. [77] [80] |
| Полициклические неконденсирующиеся производные пиридина | Никотин , норникотин , анабазин , анатабин [77] [80] | ||
| Полициклические конденсированные производные пиридина | Актинидин , генцианин , педикулинин [81] | ||
| сесквитерпена Производные пиридина | Никотиновая кислота , изолейцин [21] | Эвонин, гиппократин, триптонин. [78] [79] | |
Производные изохинолина и родственные алкалоиды [82] 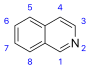 | Простые производные изохинолина [83] | Тирозин или фенилаланин → дофамин или тирамин (для алкалоидов амариллиса) [84] [85] | Сальсолин , лофоцерин [82] [83] |
| Производные 1- и 3-изохинолинов [86] | N-метилкоридалдин, нороксигидрастинин [86] | ||
| Производные 1- и 4-фенилтетрагидроизохинолинов [83] | Криптостилин [83] [87] | ||
| Производные 5-нафтил-изохинолина [88] | Анцистрокладин [88] | ||
| Производные 1- и 2-бензилизохинолинов [89] | Папаверин , лауданозин , сандаверин | ||
| Кулинарная группа [90] | Куларин, ягонин [90] | ||
| Павины и изопавины [91] | Аргемонин, амуренсин [91] | ||
| Бензопирроколины [92] | Криптаустолин [83] | ||
| Протоберберины [83] | Берберин , канадин , офиокарпин, мекамбридин, коридалин. [93] | ||
| Фталидизохинолины [83] | Гидрастин , наркотин (Носкапин) [94] | ||
| Спиробензилизохинолины [83] | Фумарицины [91] | ||
| ипекакуаны Алкалоиды [95] | Эметин, протоэметин, ипекозид [95] | ||
| Бензофенантридины [83] | Сангвинарин, оксинитидин, коринолоксин [96] | ||
| Апорфины [83] | Глауцин , коридин, лириоденин [97] | ||
| Проапорфины [83] | Пронуциферины, глазиовины [83] [92] | ||
| Гомоапорфины [98] | Крейсигинин, мультифлорамин [98] | ||
| Гомопроапорфины [98] | Бульбокодин [90] | ||
| Морфины [99] | Морфин , кодеин , тебаин , синоменин [100] | ||
| Гомоморфины [101] | Крейсигинин, андроцимбин [99] | ||
| Трополоизохинолины [83] | Гимерубрины [83] | ||
| Азофлуорантены [83] | Руфесцин, имелутеин [102] | ||
| амариллиса Алкалоиды [103] | Ликорин , амбеллин, тазеттин, галантамин , монтанин. [104] | ||
| Алкалоиды эритрины [87] | Эризодин, эритроидин [87] | ||
| фенантрена Производные [83] | Атеросперминин [83] [93] | ||
| Протопины [83] | Протопин , оксомурамин, корикавидин [96] | ||
| Аристолакт [83] | Дорифлавин [83] | ||
оксазола Производные [105] 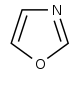 | Тирозин → тирамин [106] | Аннулолин, халординол, тексалин, тексамин [107] | |
изоксазола Производные 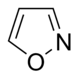 | Иботеновая кислота → Мусцимол | Иботеновая кислота, Мусцимол | |
тиазола Производные [108] 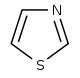 | 1-дезокси-D-ксилулозо-5-фосфат (DOXP), тирозин , цистеин [109] | Ностоцикламид, тиострептон [108] [110] | |
хиназолина Производные [111] 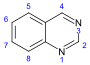 | Производные 3,4-дигидро-4-хиназолона | Антраниловая кислота или фенилаланин или орнитин [112] | жаропонижающее [113] |
| Производные 1,4-дигидро-4-хиназолона | Гликорин, арборин, гликосминин [113] | ||
| Производные пирролидина и пиперидина хиназолина | Вазицин (пеганин) [105] | ||
| акридина Производные [105] | Антраниловая кислота [114] | Рутакридон, акроницин [115] [116] | |
хинолина Производные [117] [118] 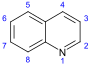 | Простые производные хинолиновых производных 2-хинолонов и 4-хинолонов | Антраниловая кислота → 3-карбоксихинолин [119] | Куспарин, эхинопсин , эвокарпин [118] [120] [121] |
| Трициклические терпеноиды | Флиндерсин [118] [122] | ||
| Производные фуранохинолина | Диктамнин , фагарин, скиммианин [118] [123] [124] | ||
| Хинин | Триптофан → триптамин → стриктозидин (с секологанином ) → коринантал → цинхонинон [85] [119] | Хинин , хинидин , цинхонин , цинхонидин [122] | |
индола Производные [100]  | Неизопреновые индольные алкалоиды | ||
| Простые производные индола [125] | Триптофан → триптамин или 5-гидрокситриптофан [126] | Серотонин , псилоцибин , диметилтриптамин (ДМТ), буфотенин. [127] [128] | |
| Простые производные β-карболина [129] | Харман, гармин , гармалин , элегнин [125] | ||
| Пирролиндольные алкалоиды [130] | Физостигмин (эзерин), эфирамин, физовенин, эптастигмин [130] | ||
| Семитерпеноидные индольные алкалоиды | |||
| Алкалоиды спорыньи [100] | Триптофан → ханоклавин → агроклавин → элимоклавин → паспаловая кислота → лизергиновая кислота. [130] | Эрготамин , эргобазин, эргозин [131] | |
| Монотерпеноидные индольные алкалоиды | |||
| Коринанта Алкалоиды типа [126] | Триптофан → триптамин → стриктозидин (с секологанином ) [126] | Аймалицин, сарпагин, вобазин, аймалин , йохимбин , резерпин , митрагинин , [132] [133] группы стрихнина и ( Стрихнин бруцин , аквамицин , вомицин [134] ) | |
| ибога Алкалоиды типа [126] | Ибогамин , ибогаин , воакангин [126] | ||
| Aspidosperma Алкалоиды типа [126] | Винкамин , барвинка алкалоиды , [27] [135] винкотин, аспидоспермин [136] [137] | ||
имидазола Производные [105] 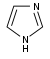 | Непосредственно из гистидина [138] | Гистамин , пилокарпин , пилозин, Стивенсин [105] [138] | |
пурина Производные [139] 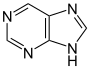 | Ксантозин (образуется при биосинтезе пуринов) → 7-метилксантозин → 7-метилксантин → теобромин → кофеин [85] | Кофеин , теобромин , теофиллин , сакситоксин. [140] [141] | |
| Алкалоиды с азотом в боковой цепи (протоалкалоиды) | |||
β- фенилэтиламина Производные [92] 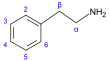 | Тирозин или фенилаланин → диоксифенилаланин → дофамин → адреналин и мескалин тирозин → тирамин фенилаланин → 1-фенилпропан-1,2-дион → катинон → эфедрин и псевдоэфедрин. [21] [52] [142] | Тирамин , эфедрин , псевдоэфедрин , мескалин , катинон , катехоламины ( адреналин , норадреналин , дофамин ). [21] [143] | |
Колхициновые алкалоиды [144]  | Тирозин или фенилаланин → дофамин → осенний → колхицин. [145] | Колхицин , колхамин [144] | |
Мускарин [146]  | Глутаминовая кислота → 3-кетоглутаминовая кислота → мускарин (с пировиноградной кислотой ) [147] | Мускарин , алломускарин, эпимускарин, эпиалломускарин [146] | |
бензиламин [148] 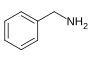 | Фенилаланин с валином , лейцином или изолейцином [149] | Капсаицин , дигидрокапсаицин , нордигидрокапсаицин, ванилиламин. [148] [150] | |
| Полиамины алкалоиды | |||
| путресцина Производные [151] | орнитин → путресцин → спермидин → спермин [152] | Пауцин [151] | |
| спермидина Производные [151] | Лунарин, кодонокарпин [151] | ||
| спермина Производные [151] | Вербасценин, афеландрин [151] | ||
| Пептидные (циклопептидные) алкалоиды | |||
| Пептидные алкалоиды с 13-членным циклом. [48] [153] | Нумулярин типа С | Из разных аминокислот [48] | Нумулярин С, Нумулярин S [48] |
| зизифина Тип | Зизифин А, сативанин H [48] | ||
| Пептидные алкалоиды с 14-членным циклом. [48] [153] | Франгуланин типа | Франгуланин, скутианин J [153] | |
| Скуцианин А тип | Скуцианин А [48] | ||
| Целочисленный тип | Интегреррин, дискарин D [153] | ||
| Амфибия типа F | Амфибин F, спинанин А [48] | ||
| Амфибин типа Б | Амфибия Б, лотозин С [48] | ||
| Пептидные алкалоиды с 15-членным циклом. [153] | Мукронин типа А | Мукронин А [45] [153] | |
| Псевдоалкалоиды ( терпены и стероиды ) | |||
Дитерпены [45]  | Тип ликоктонина | Мевалоновая кислота → Изопентенилпирофосфат → геранилпирофосфат [154] [155] | Аконитин , дельфинин [45] [156] |
Стероидные алкалоиды [157] 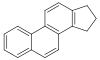 | Холестерин , аргинин [158] | Соланидин , циклопамин , батрахотоксин. [159] | |
Свойства [ править ]
Большинство алкалоидов содержат в своей молекулярной структуре кислород; эти соединения обычно представляют собой бесцветные кристаллы в условиях окружающей среды. Бескислородные алкалоиды, такие как никотин. [160] или кониин , [36] обычно представляют собой летучие, бесцветные, маслянистые жидкости. [161] Некоторые алкалоиды окрашены, например берберин (желтый) и сангвинарин (оранжевый). [161]
Большинство алкалоидов являются слабыми основаниями, но некоторые, например теобромин и теофиллин , амфотерны . [162] Многие алкалоиды плохо растворяются в воде, но легко растворяются в органических растворителях , таких как диэтиловый эфир , хлороформ или 1,2-дихлорэтан . Кофеин , [163] кокаин , [164] кодеин [165] и никотин [166] мало растворимы в воде (растворимость ≥1 г/л), тогда как другие, включая морфин [167] и йохимбин [168] очень мало растворимы в воде (0,1–1 г/л). Алкалоиды и кислоты образуют соли различной силы. Эти соли обычно хорошо растворимы в воде и этаноле и плохо растворимы в большинстве органических растворителей. Исключения включают гидробромид скополамина , растворимый в органических растворителях, и водорастворимый сульфат хинина. [161]
Большинство алкалоидов имеют горький вкус или ядовиты при приеме внутрь. Производство алкалоидов в растениях, по-видимому, возникло в ответ на питание травоядными животными; однако у некоторых животных развилась способность детоксикации алкалоидов. [169] Некоторые алкалоиды могут вызывать дефекты развития у потомства животных, которые потребляют алкалоиды, но не могут их детоксицировать. Одним из примеров является алкалоид циклопамин , вырабатываемый листьями кукурузной лилии . В 1950-е годы до 25% ягнят, рожденных от овец, пасшихся на кукурузной лилии, имели серьезные деформации лица. Они варьировались от деформированных челюстей до циклопии (см. Рисунок). После десятилетий исследований, в 1980-х годах, соединение, ответственное за эти деформации, было идентифицировано как алкалоид 11-дезоксижервин, позже переименованный в циклопамин. [170]
Распространение в природе [ править ]

Алкалоиды вырабатываются различными живыми организмами, особенно высшими растениями — около 10–25% из них содержат алкалоиды. [171] [172] Поэтому в прошлом термин «алкалоид» ассоциировался с растениями. [173]
Содержание алкалоидов в растениях обычно находится в пределах нескольких процентов и неоднородно по тканям растения. В зависимости от вида растений максимальная концентрация наблюдается в листьях (например, белена черная ), плодах или семенах ( стрихниновое дерево ), корне ( Rauvolfia serpentina ) или коре ( хинное дерево ). [174] Кроме того, разные ткани одного и того же растения могут содержать разные алкалоиды. [175]
Помимо растений, алкалоиды обнаружены в некоторых видах грибов , например псилоцибин в плодовых телах рода Psilocybe , и у животных, например буфотенин в коже некоторых жаб. [24] и ряд насекомых, особенно муравьев. [176] Многие морские организмы также содержат алкалоиды. [177] Некоторые амины , например адреналин и серотонин , играющие важную роль у высших животных, по своей структуре и биосинтезу сходны с алкалоидами и иногда называются алкалоидами. [178]
Извлечение [ править ]

Из-за структурного разнообразия алкалоидов не существует единого метода их извлечения из природного сырья. [179] В большинстве методов используется свойство большинства алкалоидов растворяться в органических растворителях. [7] но не в воде, а в противоположной тенденции их солей.
Большинство растений содержат несколько алкалоидов. Сначала экстрагируют их смесь, а затем отделяют отдельные алкалоиды. [180] Перед экстракцией растения тщательно измельчают. [179] [181] Большинство алкалоидов присутствует в сырье растений в виде солей органических кислот. [179] Экстрагированные алкалоиды могут оставаться в виде солей или превращаться в основания. [180] Экстрагирование оснований достигается путем обработки сырья щелочными растворами и экстрагирования алкалоидных оснований органическими растворителями, такими как 1,2-дихлорэтан, хлороформ, диэтиловый эфир или бензол. Затем примеси растворяют слабыми кислотами; при этом основания алкалоидов превращаются в соли, которые смываются водой. При необходимости водный раствор солей алкалоидов снова подщелачивают и обрабатывают органическим растворителем. Процесс повторяется до достижения желаемой чистоты.
При кислой экстракции растительное сырье обрабатывается слабым кислым раствором ( например , уксусной кислотой в воде, этаноле или метаноле). Затем добавляют основание для перевода алкалоидов в основные формы, которые экстрагируют органическим растворителем (если экстрагирование проводилось спиртом, то сначала удаляют его, а остаток растворяют в воде). Раствор очищают, как описано выше. [179] [182]
Алкалоиды выделяют из их смеси, используя разную их растворимость в определенных растворителях и разную реакционную способность с определенными реагентами или путем перегонки . [183]
выявлен ряд алкалоидов У насекомых , среди которых огненных муравьев алкалоиды яда , известные как соленопсины . большее внимание исследователей получили [184] Эти алкалоиды насекомых можно эффективно экстрагировать путем погружения живых огненных муравьев в растворитель. [7] или центрифугированием живых муравьев [185] с последующей хроматографической очисткой на силикагеле. [186] Было описано, что отслеживание и дозирование экстрагированных муравьиных алкалоидов соленопсина возможно на основе их пика поглощения около 232 нанометров. [187]
Биосинтез [ править ]
Биологическими предшественниками большинства алкалоидов являются аминокислоты , такие как орнитин , лизин , фенилаланин , тирозин , триптофан , гистидин , аспарагиновая и антраниловая кислоты . [188] Никотиновую кислоту можно синтезировать из триптофана или аспарагиновой кислоты. Пути биосинтеза алкалоидов слишком многочисленны и их нелегко классифицировать. [85] Однако существует несколько типичных реакций, участвующих в биосинтезе различных классов алкалоидов, включая синтез оснований Шиффа и реакцию Манниха . [188]
Синтез оснований Шиффа [ править ]
Основания Шиффа можно получить путем взаимодействия аминов с кетонами или альдегидами. [189] Эти реакции являются распространенным методом получения связей C=N. [190]
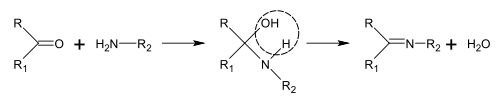
При биосинтезе алкалоидов такие реакции могут протекать внутри молекулы. [188] например, при синтезе пиперидина: [41]

Множество реакций [ править ]
Неотъемлемым компонентом реакции Манниха, помимо амина и карбонильного соединения, является карбанион , играющий роль нуклеофила при нуклеофильном присоединении к иону, образующемуся в результате реакции амина и карбонила. [190]

Реакция Манниха может протекать как межмолекулярно, так и внутримолекулярно: [191] [192]

Димерные алкалоиды [ править ]
Кроме описанных выше мономерных алкалоидов, существуют также димерные и даже тримерные и тетрамерные алкалоиды, образующиеся при конденсации двух, трех и четырех мономерных алкалоидов. Димерные алкалоиды обычно образуются из мономеров одного типа по следующим механизмам: [193]
- Реакция Манниха , в результате которой образуется, например , воакамин.
- Реакция Майкла (виллалстонин)
- Конденсация альдегидов с аминами (токсиферином)
- Окислительное присоединение фенолов (даурицина, тубокурарина)
- Лактонизация (карпаин).
Существуют также димерные алкалоиды, образованные из двух различных мономеров, такие как барвинка алкалоиды винбластин и винкристин. [27] [135] которые образуются в результате сочетания катарантина и виндолина . [194] [195] Новейший полусинтетический химиотерапевтический препарат винорелбин применяется при лечении немелкоклеточного рака легких . [135] [196] Это еще одно производное димера виндолина и катарантина, синтезируемое из ангидровинбластина . [197] начиная либо с лейрозина [198] [199] или сами мономеры. [135] [195]

роль Биологическая
Алкалоиды относятся к числу наиболее важных и наиболее известных вторичных метаболитов , т. е. биогенных веществ, не участвующих непосредственно в нормальном росте , развитии или размножении организма. Вместо этого они обычно опосредуют экологические взаимодействия , которые могут дать организму селективное преимущество за счет повышения его выживаемости или плодовитости . В некоторых случаях их функция, если таковая имеется, остается неясной. [200] Ранняя гипотеза о том, что алкалоиды являются конечными продуктами азотистого обмена у растений, как мочевина и мочевая кислота у млекопитающих, была опровергнута открытием, что их концентрация колеблется, а не постоянно увеличивается. [17]
Большинство известных функций алкалоидов связаны с защитой. Например, апорфиновый алкалоид лириоденин, вырабатываемый тюльпанным деревом, защищает его от паразитических грибов. Кроме того, наличие алкалоидов в растении препятствует насекомыми и хордовыми его поеданию животными. Однако некоторые животные адаптированы к алкалоидам и даже используют их в собственном метаболизме. [201] Такие родственные алкалоидам вещества, как серотонин , дофамин и гистамин, являются важными нейромедиаторами у животных. Известно также, что алкалоиды регулируют рост растений. [202] Одним из примеров организма, который использует алкалоиды для защиты, является Utetheisa ornatrix , более известная как декоративная моль. Пирролизидиновые алкалоиды делают этих личинок и взрослых бабочек неприятными для многих их естественных врагов, таких как жуки-кокцинелиды, зеленые златоглазки, насекомоядные полужесткокрылые и насекомоядные летучие мыши. [203] Другой пример использования алкалоидов – ядовитая моль болиголова ( Agonopterix alstroemeriana). Эта моль питается высокотоксичным и богатым алкалоидами ядовитым растением-хозяином болиголовом ( Conium maculatum ) на личиночной стадии. A. alstroemeriana может получить двойную выгоду от токсичности встречающихся в природе алкалоидов: как за счет неприятия этого вида хищниками, так и за счет способности A. alstroemeriana распознавать Conium maculatum как правильное место для откладки яиц. [204] Было продемонстрировано, что алкалоид огненных муравьев яда , известный как соленопсин, защищает королев инвазивных огненных муравьев во время основания новых гнезд, тем самым играя центральную роль в распространении этого вида муравьев-вредителей по всему миру. [205]
Приложения [ править ]
В медицине [ править ]
Медицинское использование алкалоидсодержащих растений имеет давнюю историю, поэтому, когда в XIX веке были выделены первые алкалоиды, они сразу же нашли применение в клинической практике. [206] Многие алкалоиды до сих пор используются в медицине, обычно в виде широко используемых солей, включая следующие: [17] [207]
Многие синтетические и полусинтетические препараты представляют собой структурные модификации алкалоидов, призванные усилить или изменить основной эффект препарата и уменьшить нежелательные побочные эффекты. [208] Например, налоксон , опиоидных рецепторов антагонист , является производным тебаина , который присутствует в опии . [209]
В сельском хозяйстве [ править ]
До разработки широкого спектра относительно малотоксичных синтетических пестицидов некоторые алкалоиды, такие как соли никотина и анабазин использовались в качестве инсектицидов . Их использование ограничивалось высокой токсичностью для человека. [210]
Использование в качестве психоактивных веществ [ править ]
издавна применяют препараты растений и грибов, содержащие алкалоиды и их экстракты, а позднее и чистые алкалоиды В качестве психоактивных веществ . Кокаин , кофеин и катинон являются стимуляторами центральной нервной системы . [211] [212] Мескалин и многие индольные алкалоиды (такие как псилоцибин , диметилтриптамин и ибогаин ) обладают галлюциногенным действием. [213] [214] Морфин и кодеин — сильные наркотические обезболивающие. [215]
Существуют алкалоиды, которые сами по себе не обладают сильным психоактивным действием, но являются предшественниками полусинтетических психоактивных веществ. Например, эфедрин и псевдоэфедрин используются для производства меткатинона и метамфетамина . [216] Тебаин используется в синтезе многих обезболивающих, таких как оксикодон .
См. также [ править ]
Пояснительные примечания [ править ]
- ^ Мейснер, В. (1819). «О растительных щелочах: II. О новой растительной щелочи (алкалоиде). » Журнал химии и физики . 25 :379-381. Архивировано из оригинала 18 мая 2023 года.
В предпоследнем предложении своей статьи Мейснер писал: «В целом мне кажется уместным называть известные на сегодняшний день растительные вещества не щелочами, а скорее алкалоидами, так как в них действительно есть некоторые свойства сильно отличаются от щелочей, поэтому они найдут свое место в разделе химии растений раньше, чем растительные кислоты». ["Вообще мне кажется уместным дать известным ныне растительным веществам название не "щелочи", а "алкалоиды", так как они по некоторым свойствам сильно отличаются от щелочей; среди разделов химии растений они бы поэтому находят свое место перед растительными кислотами (поскольку «Алкалоид» предшествует «Кислоте», но следует за «Щелочи»)».]
Цитаты [ править ]
- ^ Луч, Андреас (2009). Молекулярная, клиническая и экологическая токсикология, Том 1: Молекулярная токсикология . Том. 1. Спрингер. п. 20. ISBN 9783764383367 . OCLC 1056390214 .
- ^ Перейти обратно: а б ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Интернет-исправленная версия: (2006–) « алкалоиды ». doi : 10.1351/goldbook.A00220
- ^ Манске, РФФ (12 мая 2014 г.). Алкалоиды: химия и физиология, том 8 . Том. 8. Сент-Луис: Эльзевир. стр. 683–695. ISBN 9781483222004 . OCLC 1090491824 .
- ^ Льюис, Роберт Алан (23 марта 1998 г.). Токсикологический словарь Льюиса . ЦРК Пресс. п. 51. ИСБН 9781566702232 . OCLC 1026521889 .
- ^ Перейти обратно: а б с д "АЛКАЛОИДЫ - Химическая энциклопедия" [Alkaloids - Chemical Encyclopedia]. www.xumuk.ru (in Russian) . Retrieved 18 May 2023 .
- ^ Робертс, М.Ф. (Маргарет Ф.); Подмигните, Майкл (1998). Алкалоиды: биохимия, экология и медицинское применение . Бостон: Springer США. ISBN 9781475729054 . ОСЛК 851770197 .
- ^ Перейти обратно: а б с Гонсалвес Патерсон Фокс, Эдуардо; Расс Солис, Дэниел; Делазари душ Сантос, Люсилин; Апаресидо душ Сантос Пинту, Хосе Роберто; Рибейру да Силва Менегассо, анально; Кардосо Масиэль Коста Силва, Рафаэль; Серджио Пальма, Марио; Корреа Буэно, Одаир; Алькантара Мачадо, Эднильдо (апрель 2013 г.). «Простой и быстрый метод извлечения целого яда огненных муравьев (Insecta: Formicidae: Solenopsis)» . Токсикон . 65 :5–8. Бибкод : 2013Txcn...65....5G . дои : 10.1016/j.токсикон.2012.12.009 . hdl : 11449/74946 . ПМИД 23333648 .
- ^ Киттакуп П., Махидол С., Ручирават С. (2014). «Алкалоиды как важные основы в терапевтических препаратах для лечения рака, туберкулеза и прекращения курения» . Curr Top Med Chem . 14 (2): 239–252. дои : 10.2174/1568026613666131216105049 . ПМИД 24359196 .
- ^ Руссо П., Фрустачи А., Дель Буфало А., Фини М., Сезарио А. (2013). «Многоцелевые препараты растительного происхождения, действующие при болезни Альцгеймера». Curr Med Chem . 20 (13): 1686–93. дои : 10.2174/0929867311320130008 . ПМИД 23410167 .
- ^ Раймонд С. Синатра; Джонатан С. Яр; Дж. Майкл Уоткинс-Питчфорд (2010). Сущность анальгезии и анальгетиков . Издательство Кембриджского университета. стр. 82–90. ISBN 978-1139491983 .
- ^ Кушни Т.П., Кушни Б., Лэмб Эй.Дж. (2014). «Алкалоиды: обзор их антибактериальной, усиливающей действие антибиотиков и противовирусной активности» . Противомикробные агенты Int J. 44 (5): 377–386. дои : 10.1016/j.ijantimicag.2014.06.001 . ПМИД 25130096 . S2CID 205171789 .
- ^ Сингх, Сукхпал; Бансал, Абхишек; Сингх, Викрамджит; Чопра, Таня; Поддар, Джит (июнь 2022 г.). «Флавоноиды, алкалоиды и терпеноиды: новая надежда на лечение сахарного диабета» . Журнал диабета и метаболических нарушений . 21 (1): 941–950. дои : 10.1007/s40200-021-00943-8 . ISSN 2251-6581 . ПМЦ 9167359 . ПМИД 35673446 .
- ^ Перейти обратно: а б Бел, Тапан; Гупта, Амит; Альбратти, Мохаммед; Наджми, Асим; Мерайя, Абдулкарим М.; Альхазми, Хасан А.; Анвер, доктор Халид; Бхатия, Саураб; Бунгау, Симона Габриэла (9 сентября 2022 г.). «Алкалоидные фитокомпоненты для лечения диабета: исследование нераскрытого потенциала» . Молекулы . 27 (18): 5851. doi : 10,3390/molecules27185851 . ISSN 1420-3049 . ПМК 9501853 . ПМИД 36144587 .
- ^ «Алкалоид» . 18 декабря 2007 г.
- ^ Грабители Дж. Э., Спиди МК, Тайлер В. Е. (1996). «Глава 9: Алкалоиды». Фармакогнозия и фармакобиотехнология . Филадельфия: Липпинкотт, Уильямс и Уилкинс. стр. 143–185. ISBN 978-0683085006 .
- ^ Роудс, Дэвид Ф. (1979). «Эволюция химической защиты растений от травоядных». В Розентале, Джеральд А.; Янзен, Дэниел Х (ред.). Травоядные животные: их взаимодействие со вторичными метаболитами растений . Нью-Йорк: Академическая пресса. п. 41. ИСБН 978-0-12-597180-5 .
- ^ Перейти обратно: а б с Роберта А. Мейерса Энциклопедия физических наук и технологий - Алкалоиды, 3-е издание. ISBN 0-12-227411-3
- ^ Чеке, Леланд Дж.; Киракосян, Ара; Кауфман, Питер Б.; Уорбер, Сара; Дюк, Джеймс А.; Брильманн, Гарри Л. (19 апреля 2016 г.). Натуральные продукты из растений . ЦРК Пресс. п. 30. ISBN 978-1-4200-0447-2 .
- ^ Джонсон, Алин Уильям (1999). Приглашение на органическую химию . Джонс и Бартлетт Обучение. п. 433. ИСБН 978-0-7637-0432-2 .
- ^ Бансал, Радж К. (2003). Учебник органической химии . Нью Эйдж Интернэшнл Лимитед. п. 644. ИСБН 978-81-224-1459-2 .
- ^ Перейти обратно: а б с д Анишевский , с. 110
- ^ Гессен , стр. 1–3.
- ^ Ладенбург, Альберт (1882). Краткий химический словарь (на немецком языке). Э. Трюендт. стр. 213–422.
- ^ Перейти обратно: а б Гессен , с. 5
- ^ Суффикс «ine» — греческий женский суффикс-отчество, означающий «дочь»; отсюда, например, «атропин» означает «дочь Атропы» (белладонна): «Разработка систематических названий простых алканов» . Йель.edu . Архивировано из оригинала 16 марта 2012 года.
- ^ Гессен , с. 7
- ^ Перейти обратно: а б с ван дер Хейден, Роберт; Джейкобс, Дениз И.; Снойер, Вим; Халлард, Дидье; Верпорте, Роберт (2004). « Алкалоиды катаранта : фармакогнозия и биотехнология». Современная медицинская химия . 11 (5): 607–628. дои : 10.2174/0929867043455846 . ПМИД 15032608 .
- ^ Купер, Раймонд; Дикин, Джеффри Джон (2016). «Подарок Африки миру» . Ботанические чудеса: химия растений, изменивших мир . ЦРК Пресс . стр. 46–51. ISBN 9781498704304 .
- ^ Равинья, Энрике (2011). «Алкалоиды барвинка» . Эволюция открытия лекарств: от традиционных лекарств к современным лекарствам . Джон Уайли и сыновья . стр. 157–159. ISBN 9783527326693 .
- ^ Перейти обратно: а б Анишевский , с. 182
- ^ Гессен , с. 338
- ^ Гессен , с. 304
- ^ Гессен , с. 350
- ^ Гессен , стр. 313–316.
- ^ Бегли , Натуральные продукты в растениях .
- ^ Перейти обратно: а б Кониин в Большой Советской Энциклопедии , 1969–1978 (на русском языке)
- ^ Гессен , с. 204
- ^ Перейти обратно: а б Гессен , с. 11
- ^ Orekhov , p. 6
- ^ Анишевский , с. 109
- ^ Перейти обратно: а б Дьюик , с. 307
- ^ Гессен , с. 12
- ^ Перейти обратно: а б Племенков , г. 223
- ^ Анишевский , с. 108
- ^ Перейти обратно: а б с д Гессен , с. 84
- ^ Перейти обратно: а б Гессен , с. 31
- ^ Перейти обратно: а б с Дьюик , с. 381
- ^ Перейти обратно: а б с д и ж г час я Димитрис К. Гурнелиф; Грегори Г. Ласкарисb; Роберт Верпоорте (1997). «Циклопептидные алкалоиды». Нат. Прод. Представитель . 14 (1): 75–82. дои : 10.1039/NP9971400075 . ПМИД 9121730 .
- ^ Анишевский , с. 11
- ^ Племенков , с. 246
- ^ Перейти обратно: а б Анишевский , с. 12
- ^ Перейти обратно: а б Дьюик , с. 382
- ^ Гессен , стр. 44, 53.
- ^ Перейти обратно: а б с Племенков , г. 224
- ^ Перейти обратно: а б с Анишевский , с. 75
- ^ Orekhov , p. 33
- ^ Перейти обратно: а б с «Химическая энциклопедия: Тропановые алкалоиды» . xumuk.ru .
- ^ Гессен , с. 34
- ^ Анишевский , с. 27
- ^ Перейти обратно: а б с д «Химическая энциклопедия: Пирролизидиновые алкалоиды» . xumuk.ru .
- ^ Племенков , с. 229
- ^ Бланкеншип Дж.Д., Хауснехт Дж.Б., Пал С., Буш Л.П., Гроссман Р.Б., Шардл К.Л. (2005). «Биосинтетические предшественники грибных пирролизидинов, лолиновых алкалоидов». ХимБиоХим . 6 (6): 1016–1022. дои : 10.1002/cbic.200400327 . ПМИД 15861432 . S2CID 13461396 .
- ^ Фолкнер-младший, Хуссаини С.Р., Бланкеншип Дж.Д., Пал С., Бранан Б.М., Гроссман Р.Б., Шардл К.Л. (2006). «О последовательности образования связей в биосинтезе лолиновых алкалоидов». ХимБиоХим . 7 (7): 1078–1088. дои : 10.1002/cbic.200600066 . ПМИД 16755627 . S2CID 34409048 .
- ^ Шардл К.Л., Гроссман Р.Б., Нагабхиру П., Фолкнер-младший, Маллик У.П. (2007). «Лолиновые алкалоиды: валюты мутуализма». Фитохимия . 68 (7): 980–996. Бибкод : 2007PChem..68..980S . doi : 10.1016/j.phytochem.2007.01.010 . ПМИД 17346759 .
- ^ Племенков , с. 225
- ^ Анишевский , с. 95
- ^ Orekhov , p. 80
- ^ Перейти обратно: а б с д и ж «Химическая энциклопедия: Хинолизидиновые алкалоиды» . xumuk.ru .
- ^ Сакстон , Том. 1, с. 93
- ^ Анишевский , с. 98
- ^ Сакстон , Том. 1, с. 91
- ^ Джозеф П. Майкл (2002). «Индолизидиновые и хинолизидиновые алкалоиды». Нат. Прод. Представитель . 19 (5): 458–475. дои : 10.1039/b208137g . ПМИД 14620842 .
- ^ Сакстон , Том. 1, с. 92
- ^ Дьюик , с. 310
- ^ Анишевский , с. 96
- ^ Анишевский , с. 97
- ^ Перейти обратно: а б с Племенков , г. 227
- ^ Перейти обратно: а б «Химическая энциклопедия: пиридиновые алкалоиды» . xumuk.ru .
- ^ Перейти обратно: а б Анишевский , с. 107
- ^ Перейти обратно: а б Анишевский , с. 85
- ^ Племенков , с. 228
- ^ Перейти обратно: а б Гессен , с. 36
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с т «Химическая энциклопедия: изохинолиновые алкалоиды» . xumuk.ru .
- ^ Анишевский , стр. 77–78.
- ^ Перейти обратно: а б с д Бегли , Биосинтез алкалоидов.
- ^ Перейти обратно: а б Сакстон , Том. 3, с. 122
- ^ Перейти обратно: а б с Гессен , с. 54
- ^ Перейти обратно: а б Гессен , с. 37
- ^ Гессен , с. 38
- ^ Перейти обратно: а б с Гессен , с. 46
- ^ Перейти обратно: а б с Гессен , с. 50
- ^ Перейти обратно: а б с Кеннет В. Бентли (1997). «β-фенилэтиламины и изохинолиновые алкалоиды» (PDF) . Нат. Прод. Представитель . 14 (4): 387–411. дои : 10.1039/NP9971400387 . ПМИД 9281839 . Архивировано (PDF) из оригинала 9 октября 2022 года.
- ^ Перейти обратно: а б Гессен , с. 47
- ^ Гессен , с. 39
- ^ Перейти обратно: а б Гессен , с. 41
- ^ Перейти обратно: а б Гессен , с. 49
- ^ Гессен , с. 44
- ^ Перейти обратно: а б с Сакстон , Том. 3, с. 164
- ^ Перейти обратно: а б Гессен , с. 51
- ^ Перейти обратно: а б с Племенков , г. 236
- ^ Сакстон , Том. 3, с. 163
- ^ Сакстон , Том. 3, с. 168
- ^ Гессен , с. 52
- ^ Гессен , с. 53
- ^ Перейти обратно: а б с д и Племенков , г. 241
- ^ Бросси , Том. 35, с. 261
- ^ Бросси , Том. 35, с. 260–263
- ^ Перейти обратно: а б Племенков , г. 242
- ^ Бегли , Биосинтез кофактора
- ^ Джон Р. Льюис (2000). «Амариллидовые, мускарин, имидазол, оксазол, тиазол и пептидные алкалоиды и другие разные алкалоиды». Нат. Прод. Представитель . 17 (1): 57–84. дои : 10.1039/a809403i . ПМИД 10714899 .
- ^ «Химическая энциклопедия: Хиназолиновые алкалоиды» . xumuk.ru .
- ^ Анишевский , с. 106
- ^ Перейти обратно: а б Анишевский , с. 105
- ^ Ричард Б. Герберт; Герберт, Ричард Б.; Герберт, Ричард Б. (1999). «Биосинтез растительных алкалоидов и азотистых микробных метаболитов». Нат. Прод. Представитель . 16 (2): 199–208. дои : 10.1039/a705734b .
- ^ Племенков , с. 231, 246
- ^ Гессен , с. 58
- ^ Племенков , с. 231
- ^ Перейти обратно: а б с д «Химическая энциклопедия: Хинолиновые алкалоиды» . xumuk.ru .
- ^ Перейти обратно: а б Анишевский , с. 114
- ^ Orekhov , p. 205
- ^ Гессен , с. 55
- ^ Перейти обратно: а б Племенков , г. 232
- ^ Orekhov , p. 212
- ^ Анишевский , с. 118
- ^ Перейти обратно: а б Анишевский , с. 112
- ^ Перейти обратно: а б с д и ж Анишевский , с. 113
- ^ Гессен , с. 15
- ^ Сакстон , Том. 1, с. 467
- ^ Дьюик , стр. 349–350.
- ^ Перейти обратно: а б с Анишевский , с. 119
- ^ Гессен , с. 29
- ^ Гессен , стр. 23–26.
- ^ Сакстон , Том. 1, с. 169
- ^ Сакстон , Том. 5, с. 210
- ^ Перейти обратно: а б с д Кеглевич, Петр; Хазай, Ласло; Калаус, Джордж; Сантай, Чаба (2012). «Модификации основных скелетов винбластина и винкристина» . Молекулы . 17 (5): 5893–5914. дои : 10.3390/molecules17055893 . ПМК 6268133 . ПМИД 22609781 .
- ^ Гессен , стр. 17–18.
- ^ Дьюик , с. 357
- ^ Перейти обратно: а б Анишевский , с. 104
- ^ Гессен , с. 72
- ^ Гессен , с. 73
- ^ Дьюик , с. 396
- ^ «Путь PlantCyc: биосинтез эфедрина» . Архивировано из оригинала 10 декабря 2011 года.
- ^ Гессен , с. 76
- ^ Перейти обратно: а б «Химическая энциклопедия: алкалоиды колхицина» . xumuk.ru .
- ^ Анишевский , с. 77
- ^ Перейти обратно: а б Гессен , с. 81
- ^ Бросси , Том. 23, с. 376
- ^ Перейти обратно: а б Гессен , с. 77
- ^ Бросси , Том. 23, с. 268
- ^ Бросси , Том. 23, с. 231
- ^ Перейти обратно: а б с д и ж Гессен , с. 82
- ^ «Биосинтез спермина» . www.qmul.ac.uk. Архивировано из оригинала 13 ноября 2003 года.
- ^ Перейти обратно: а б с д и ж Племенков , г. 243
- ^ «Химическая энциклопедия: Терпены» . xumuk.ru .
- ^ Бегли , Натуральные продукты: обзор
- ^ Атта-ур-Рахман и М. Икбал Чоудхари (1997). «Дитерпеноиды и стероидные алкалоиды». Нат. Прод. Представитель . 14 (2): 191–203. дои : 10.1039/np9971400191 . ПМИД 9149410 .
- ^ Гессен , с. 88
- ^ Дьюик , с. 388
- ^ Племенков , с. 247
- ↑ Никотин в Большой советской энциклопедии , 1969–1978 (на русском языке)
- ^ Перейти обратно: а б с Гринкевич , с. 131
- ^ Спиллер, Джин А. (23 апреля 2019 г.). Кофеин . ЦРК Пресс. п. 140. ИСБН 978-1-4200-5013-4 .
- ^ «Кофеин» . Наркобанк . Проверено 12 февраля 2013 г.
- ^ «Кокаин» . Наркобанк . Проверено 12 февраля 2013 г.
- ^ «Кодеин» . Наркобанк . Проверено 12 февраля 2013 г.
- ^ «Никотин» . Наркобанк . Проверено 12 февраля 2013 г.
- ^ «Морфий» . Наркобанк . Проверено 12 февраля 2013 г.
- ^ «Йохимбин» . Наркобанк . Архивировано из оригинала 30 января 2013 года . Проверено 12 февраля 2013 г.
- ^ Фатторуссо , с. 53
- ^ Томас Акамович; Колин С. Стюарт; Т.В. Пенникотт (2004). Ядовитые растения и родственные им токсины, Том 2001 . КАБИ. п. 362. ИСБН 978-0-85199-614-1 .
- ^ Анишевский , с. 13
- ^ Orekhov , p. 11
- ^ Гессен , стр.4
- ^ Гринкевич , стр. 122–123.
- ^ Orekhov , p. 12
- ^ Тушар, Аксель; Айли, Самира; Фокс, Эдуардо; Эскубас, Пьер; Оривел, Жером; Николсон, Грэм; Дежан, Ален (20 января 2016 г.). «Арсенал биохимических токсинов муравьиных ядов» . Токсины . 8 (1): 30. doi : 10.3390/toxins8010030 . ISSN 2072-6651 . ПМЦ 4728552 . ПМИД 26805882 .
- ^ Фатторуссо , с. XVII
- ^ Анишевский , стр. 110–111.
- ^ Перейти обратно: а б с д Гессен , с. 116
- ^ Перейти обратно: а б Гринкевич , с. 132
- ^ Гринкевич , с. 5
- ^ Гринкевич , стр. 132–134.
- ^ Гринкевич , стр. 134–136.
- ^ Фокс, Эдуардо Гонсалвес Патерсон (2016). «Ядовитые токсины огненных муравьев». Ин Гопалакришнаконе, П.; Кальвете, Хуан Дж. (ред.). Геномика и протеомика яда . Спрингер Нидерланды. стр. 149–167. дои : 10.1007/978-94-007-6416-3_38 . ISBN 978-94-007-6415-6 .
- ^ Фокс, Эдуардо GP; Сюй, Мэн; Ван, Лей; Чен, Ли; Лу, Юн-Юэ (1 мая 2018 г.). «Быстрое доение свежего яда из остроконечных перепончатокрылых». Токсикон . 146 : 120–123. Бибкод : 2018Txcn..146..120F . дои : 10.1016/j.токсикон.2018.02.050 . ISSN 0041-0101 . ПМИД 29510162 .
- ^ Чен, Цзянь; Кантрелл, Чарльз Л.; Шан, Хань-у; Рохас, Мария Г. (22 апреля 2009 г.). «Пиперидеиновые алкалоиды из ядовитой железы красного импортированного огненного муравья (Hymenoptera: Formicidae)». Журнал сельскохозяйственной и пищевой химии . 57 (8): 3128–3133. дои : 10.1021/jf803561y . ISSN 0021-8561 . ПМИД 19326861 .
- ^ Фокс, Эдуардо GP; Сюй, Мэн; Ван, Лей; Чен, Ли; Лу, Юн-Юэ (1 июня 2018 г.). «Газовая хроматография и УФ-спектроскопия ядов перепончатокрылых, полученных тривиальным центрифугированием» . Данные вкратце . 18 : 992–998. Бибкод : 2018DIB....18..992F . дои : 10.1016/j.dib.2018.03.101 . ISSN 2352-3409 . ПМК 5996826 . ПМИД 29900266 .
- ^ Перейти обратно: а б с Племенков , г. 253
- ^ Племенков , с. 254
- ^ Перейти обратно: а б Дьюик , с. 19
- ^ Племенков , с. 255
- ^ Дьюик , с. 305
- ^ Гессен , стр. 91–105.
- ^ Хирата, К.; Миямото, К.; Миура, Ю. (1994). « Catharanthus roseus L. (Барвинок): производство виндолина и катарантина в многопобеговых культурах» . В Баджадже, YPS (ред.). Биотехнология в сельском и лесном хозяйстве 26 . Лекарственные и ароматические растения. Том. VI. Спрингер-Верлаг . стр. 46–55 . ISBN 9783540563914 .
- ^ Перейти обратно: а б Ганзойер, Андреас; Юстисия, Хосе; Фан, Чун-Ан; Воргалл, Деннис; Пистерт, Фредерик (2007). «Образование восстановительной связи C—C после раскрытия эпоксида посредством переноса электрона» . В Крише, Майкл Дж. (ред.). Образование восстановительной связи C—C, катализируемое металлом: отличие от предварительно полученных металлоорганических реагентов . Темы современной химии. Том. 279. Springer Science & Business Media . стр. 25–52. дои : 10.1007/128_2007_130 . ISBN 9783540728795 .
- ^ Фаллер, Брайан А.; Панди, Трайлокья Н. (2011). «Безопасность и эффективность винорелбина при лечении немелкоклеточного рака легких» . Клиническая медицина: онкология . 5 : 131–144. дои : 10.4137/CMO.S5074 . ПМК 3117629 . ПМИД 21695100 .
- ^ Нго, Куок Ань; Русси, Фанни; Кормье, Энтони; Торет, Сильвиана; Кноссов, Марсель; Генар, Даниэль; Геритт, Франсуаза (2009). «Синтез и биологическая оценка алкалоидов барвинка и гибридов фомопсина». Журнал медицинской химии . 52 (1): 134–142. дои : 10.1021/jm801064y . ПМИД 19072542 .
- ^ Ардуэн, Кристоф; Дорис, Эрик; Руссо, Бернар; Миосковски, Чарльз (2002). «Краткий синтез ангидровинбластина из лейрозина». Органические письма . 4 (7): 1151–1153. дои : 10.1021/ol025560c . ПМИД 11922805 .
- ^ Морсильо, Сара П.; Мигель, Делия; Кампания, Арасели Г.; Сьенфуэгос, Луис Альварес де; Джастис, Джозеф; Куэрва, Хуан М. (2014). «Недавние применения Cp 2 TiCl в синтезе природных продуктов» . Границы органической химии . 1 (1): 15–33. дои : 10.1039/c3qo00024a . hdl : 10481/47295 .
- ^ Анишевский , с. 142
- ^ Гессен , стр. 283–291.
- ^ Анишевский , стр. 142–143.
- ^ МЫ Коннер (2009). Тигровые мотыльки и шерстистые медведи — поведение, экология и эволюция Arctiidae . Нью-Йорк: Издательство Оксфордского университета. стр. 1–10. ISBN 0195327373 .
- ^ Кастельс, Ева; Беренбаум, Мэй Р. (июнь 2006 г.). «Лабораторное выращивание Agonopterix alstroemeriana, моли болиголова-дефолиатора (Conium maculatum L.) и влияние пиперидиновых алкалоидов на предпочтения и продуктивность» . Экологическая энтомология . 35 (3): 607–615. дои : 10.1603/0046-225x-35.3.607 . S2CID 45478867 – через ResearchGate.
- ^ Фокс, Эдуардо GP; У, Сяоцин; Ван, Лей; Чен, Ли; Лу, Юн-Юэ; Сюй, Ицзюань (1 февраля 2019 г.). «Изосоленопсин А из яда королевы обеспечивает быстрое выведение из строя конкурентов огненных муравьев». Токсикон . 158 : 77–83. Бибкод : 2019Txcn..158...77F . дои : 10.1016/j.токсикон.2018.11.428 . ISSN 0041-0101 . ПМИД 30529381 . S2CID 54481057 .
- ^ Гессен , с. 303
- ^ Гессен , стр. 303–309.
- ^ Гессен , с. 309
- ^ Дьюик , с. 335
- ^ Матолчи, Г.; Надаси, М.; Андриска, В. (1 января 1989 г.). Химия пестицидов . Эльзевир. стр. 21–22. ISBN 978-0-08-087491-3 .
- ^ Veselovskaya , p. 75
- ^ Гессен , с. 79
- ^ Veselovskaya , p. 136
- ^ Ибогаин: материалы Первой международной конференции (Книга 56 «Алкалоиды») . Эльзевир Наука. 1950. с. 8. ISBN 978-0-12-469556-6 .
- ^ Veselovskaya , p. 6
- ^ Veselovskaya , pp. 51–52
Общие и цитируемые ссылки [ править ]
- Анишевский, Тадеуш (2007). Алкалоиды: тайны жизни . Амстердам: Эльзевир . ISBN 978-0-444-52736-3 .
- Бегли, Тадг П. (2009). Энциклопедия химической биологии . Том. 10. Уайли. стр. 1569–1570. дои : 10.1002/cbic.200900262 . ISBN 978-0-471-75477-0 .
- Бросси, Арнольд (1989). Алкалоиды: химия и фармакология . Академическая пресса.
- Дьюик, Пол М. (2002). Лекарственные натуральные продукты: биосинтетический подход (второе изд.). Уайли. ISBN 978-0-471-49640-3 .
- Фатторуссо, Э.; Тальялатела-Скафати, О. (2008). Современные алкалоиды: структура, выделение, синтез и биология . Вайли-ВЧ. ISBN 978-3-527-31521-5 .
- Гринкевич Н.И.; Сафронич Л.Н., ред. (1983). Химический анализ лекарственных растений . Москва: Высшая школа.
- Гессен, Манфред (2002). Алкалоиды: проклятие природы или благословение? . Вайли-ВЧ. ISBN 978-3-906390-24-6 .
- Кнунянц, Иллинойс (1988). Химическая энциклопедия . Советская энциклопедия.
- Орехов, А.П. (1955). Химия алкалоидов (акад. 2-е изд.). Москва.
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ) - Племенков, В.В. (2001). Введение в химию природных соединений . Казань.
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ) - Сакстон, Дж. Э. (1971). Алкалоиды: специальный периодический отчет . Лондон: Химическое общество.
- Veselovskaya, N. B.; Kovalenko, A. E. (2000). Drugs . Moscow: Triada-X.
- Винк, М. (2009). «Способ действия и токсикология растительных токсинов и ядовитых растений». Митт. Юлиус Кюн-Инст . 421 : 93–112x.
Внешние ссылки [ править ]
 СМИ, связанные с алкалоидами, на Викискладе?
СМИ, связанные с алкалоидами, на Викискладе?  Цитаты, связанные с алкалоидами , в Wikiquote
Цитаты, связанные с алкалоидами , в Wikiquote