Дельфинин
 | |
 | |
| Имена | |
|---|---|
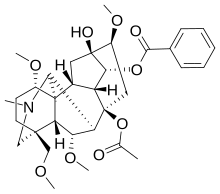
| Другие имена 8-(Ацетилокси)-13-гидрокси-1,6,16-триметокси-4-(метоксиметил)-20-метилаконитан-14-илбензоат | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.008.377 |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 33 Ч 45 НЕТ 9 | |
| Молярная масса | 599.712 |
| Появление | бесцветное твердое вещество |
| Температура плавления | От 197 до 199 ° C (от 387 до 390 ° F; от 470 до 472 К) |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности | Токсичный |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Дельфинин — токсичный дитерпеноидный алкалоид , обнаруженный в растениях родов Delphinium (живокость) и Atragene (клематис), оба семейства Ranunculaceae . [1] Дельфинин — основной алкалоид, обнаруженный в семенах Delphinium staphisagria — когда-то под названием ставэсакр, очень известном травяном средстве от платяных вшей. [2] Он близок по структуре и оказывает сходное с аконитином действие , действуя как аллостерический модулятор потенциалзависимых натриевых каналов . [3] и вызывает низкое кровяное давление , замедление сердечного ритма и аномальные сердечные ритмы . Эти эффекты делают его очень ядовитым ( LD 50 1,5–3,0 мг/кг для кроликов и собак; лягушки примерно в 10 раз более восприимчивы). [4] Хотя он использовался в некоторых альтернативных лекарствах (например, в фитотерапии). [5] [6] ), большая часть медицинского сообщества не рекомендует его использовать из-за его крайней токсичности.
Изоляция
[ редактировать ]Одно из самых ранних сообщений об выделении дельфинина из D. staphisagria было сделано французскими химиками Лассеном и Фенелем в 1819 году. [7] Менее старинный и более доступный отчет принадлежит химику Министерства сельского хозяйства США Л. Н. Марквуду, который также кратко рассмотрел более ранние работы по изоляции. [8] Примечательно, что эти ранние выделения были проведены без помощи хроматографии , поскольку дельфинин легко кристаллизуется из экстракта петролейного эфира после типичного кислотно-щелочного цикла, используемого в традиционных методах экстракции растительных алкалоидов. [9]
Химия
[ редактировать ]Несмотря на относительную легкость выделения и раннее открытие дельфинина, его молекулярная структура не была установлена в принятой в настоящее время форме до начала 1970-х годов. В то время исследовательская группа Визнера скорректировала стереохимию метоксигруппы при С-1 из β- в α- конфигурацию . [10] [11] Таким образом, любой рисунок молекулы дельфинина, появившийся до 1971–1972 годов, скорее всего, покажет неправильную стереохимию по C-1.
Фармакология
[ редактировать ]В результате раннего открытия и выделения в кристаллической форме (которая тогда считалась критерием чистоты) фармакологические свойства дельфинина были широко исследованы в 19 веке, несмотря на то, что его молекулярная структура была неизвестна. Вполне вероятно, что некоторые из этих исследований проводились с использованием нечистого препарата, и их следует интерпретировать с осторожностью. Ссылки и комментарии к этим ранним исследованиям можно найти в обзоре Бенна и Ясино. [4] Более поздние исследования были сосредоточены на сердечно-сосудистой токсичности дельфинина. [12] [13]
В целом фармакология дельфинина похожа на фармакологию аконитина , хотя острая токсичность дельфинина оказывается ниже, чем у аконитина у подопытных животных. [4]
Ссылки
[ редактировать ]- ^ Харборн Дж.Б., Бакстер Х., ред. (1993). Фитохимический словарь . Лондон: Тейлор и Фрэнсис. п. 148.
- ^ «Современный травяной сбор | Ставакр» .
- ^ Турабекова М.А., Расулев Б.Ф., Левкович М.Г., Абдуллаев Н.Д., Лещинский Ю. (апрель 2008 г.). «Алкалоиды Aconitum и Delphinium sp. как антагонистические модуляторы потенциалзависимых Na+-каналов. Исследования электронной структуры AM1/DFT и исследования QSAR» . Вычислительная биология и химия . 32 (2): 88–101. doi : 10.1016/j.compbiolchem.2007.10.003 . ПМК 5001567 . ПМИД 18201930 .
- ^ Jump up to: а б с Бенн М.Х., Ясино Дж.М. (1983). Пеллетье SW (ред.). «Глава 4». Алкалоиды: химические и биологические перспективы . 1 . Нью-Йорк: Уайли: 153–210.
- ^ Десаи Х.К., Харт Б.П., Колдуэлл Р.В., Цзяньчжун-Хуан Дж.Х., Пеллетье С.В. (июнь 1998 г.). «Некоторые нордитерпеноидные алкалоиды и их сердечно-сосудистое действие». Журнал натуральных продуктов . 61 (6): 743–8. дои : 10.1021/np970499j . ПМИД 9644057 .
- ^ Диас Х.Г., Руис Х.Г., де Ла Фуэнте Дж. (август 2000 г.). «Алкалоиды Delphinium staphisagria». Журнал натуральных продуктов . 63 (8): 1136–9. дои : 10.1021/np990453l . ПМИД 10978212 .
- ^ Лассень Ж.Л., Фенёль Х. (1819). «Анализ стафизайгара». Энн. хим. Физ . Серия 2. 12 : 358–71.
- ^ Марквуд Л.Н. (октябрь 1927 г.). «Выделение масла и алкалоидов из семян ставэсакра (Delphinium staphisagria)». Журнал Американской фармацевтической ассоциации . 16 (10): 928–32. дои : 10.1002/jps.3080161006 .
- ^ Джейкобс В.А., Крейг Л.К. (февраль 1939 г.). «ДЕЛЬФИНИН» . Журнал биологической химии . 127 (2): 361–6. дои : 10.1016/S0021-9258(18)73787-3 .
- ^ Анеха Р., Локк Д.М., Пеллетье С.В. (январь 1973 г.). «Дитерпеновые алкалоиды: строение и стереохимия гетератизина». Тетраэдр . 29 (21): 3297–308. дои : 10.1016/S0040-4020(01)93482-9 .
- ^ Пеллетье С.В., Райт Л.Х. (январь 1972 г.). «Последние разработки в химии дитерпеноидных алкалоидов». Алкалоиды . Том. 2. Лондон: Химическое общество. стр. 247–258 (254–255). дои : 10.1039/9781847555588-00247 . ISBN 978-0-85186-267-5 .
- ^ Шерф Д., Блюменфельд С., Тандер Д., Йилдиз М. (декабрь 1960 г.). «Влияние дифенилгидантоина (дилантина) натрия на трепетание и фибрилляцию предсердий, спровоцированные очаговым применением конитина или дельфинина». Американский кардиологический журнал . 60 (6): 936–47. дои : 10.1016/0002-8703(60)90125-3 . ПМИД 13747515 .
- ^ Шерф Д., Шотт А. (1973). Экстрасистолы и родственные аритмии (2-е изд.). Лондон: Хайнеманн.