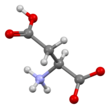
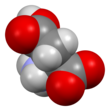
Аспарагиновая кислота
 Скелетная формула кислоты L -аспарагиновой | |||
| |||
| Имена | |||
|---|---|---|---|
Название ИЮПАК
| |||
Другие имена
| |||
| Идентификаторы | |||
3D model ( JSmol ) |
| ||
| ЧЭБИ |
| ||
| ЧЕМБЛ |
| ||
| ХимическийПаук | |||
| Лекарственный Банк |
| ||
| Информационная карта ECHA | 100.000.265 | ||
| Номер ЕС |
| ||
| КЕГГ |
| ||
ПабХим CID | |||
| НЕКОТОРЫЙ |
| ||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| С 4 Н 7 Н О 4 | |||
| Молярная масса | 133.103 g·mol −1 | ||
| Появление | бесцветные кристаллы | ||
| Плотность | 1,7 г/см 3 | ||
| Температура плавления | 270 ° С (518 ° F; 543 К) | ||
| Точка кипения | 324 ° C (615 ° F, 597 К) (разлагается) | ||
| 4,5 г/л [2] | |||
| Кислотность ( pKa ) |
| ||
| Сопряженная база | Аспартат | ||
| -64.2·10 −6 см 3 /моль | |||
| Опасности | |||
| NFPA 704 (огненный алмаз) | |||
| Страница дополнительных данных | |||
| Аспарагиновая кислота (страница данных) | |||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Аспарагиновая кислота (символ Asp или D ; [4] ионная форма известна как аспартат ) — α- аминокислота , которая используется в биосинтезе белков. [5] L - изомер аспарагиновой кислоты — одна из 22 протеиногенных аминокислот , т. е. строительных блоков белков . D -аспарагиновая кислота — одна из двух D -аминокислот, обычно встречающихся у млекопитающих. [6] [7] За редким исключением, D -аспарагиновая кислота не используется для синтеза белков, но входит в состав некоторых пептидов и играет роль нейромедиатора / нейромодулятора . [6]
Как и все другие аминокислоты, аспарагиновая кислота содержит аминогруппу и карбоновую кислоту. Его α-аминогруппа находится в протонированной –NH +
3 образуется в физиологических условиях, при этом его группа α-карбоновой кислоты депротонирована −COO − в физиологических условиях. Аспарагиновая кислота имеет кислую боковую цепь (CH 2 COOH), которая реагирует с другими аминокислотами, ферментами и белками в организме. [5] В физиологических условиях (pH 7,4) в белках боковая цепь обычно встречается в виде отрицательно заряженной формы аспартата -COO. − . [5] Для человека это незаменимая аминокислота , то есть организм может синтезировать ее по мере необходимости. Он кодируется кодонами GAU и GAC.
В белках боковые цепи аспартата часто связаны водородными связями с образованием поворотов asx или мотивов asx , которые часто встречаются на N-концах альфа-спиралей .
Аспарагиновая кислота, как и глутаминовая кислота , классифицируется как кислая аминокислота с pK a 3,9; однако в пептиде это значение сильно зависит от локальной среды и может достигать 14.
Однобуквенный код D аспартату был присвоен произвольно. [8] с предложенной мемноновой аспаровой Dic кислотой. [9]
Открытие
[ редактировать ]Аспарагиновая кислота была впервые открыта в 1827 году Огюстом-Артуром Плиссоном и Этьеном Оссианом Анри. [10] [11] гидролизом в аспарагина , выделенного из сока спаржи 1806 году. [12] В их первоначальном методе использовался гидроксид свинца , но теперь вместо него чаще используются различные другие кислоты или основания. [ нужна ссылка ]
Формы и номенклатура
[ редактировать ]Существуют две формы или энантиомеры аспарагиновой кислоты. Название «аспарагиновая кислота» может относиться как к энантиомеру, так и к смеси двух. [13] Из этих двух форм только одна, « L -аспарагиновая кислота», непосредственно включается в белки. Биологическая роль ее аналога « D -аспарагиновой кислоты» более ограничена. В то время как ферментативный синтез приводит к образованию того или другого, большинство химических синтезов производят обе формы, « DL -аспарагиновую кислоту», известную как рацемическая смесь . [ нужна ссылка ]
Синтез
[ редактировать ]Биосинтез
[ редактировать ]чаще всего синтезируется путем переаминирования оксалоацетата В организме человека аспартат . Биосинтез аспартата облегчается ферментом аминотрансферазой : перенос аминогруппы из другой молекулы, такой как аланин или глутамин, приводит к образованию аспартата и альфа-кетокислоты. [5]
Химический синтез
[ редактировать ]В промышленности аспартат получают путем аминирования фумарата, катализируемого L- аспартат-аммиаклиазой . [14]
Рацемическую аспарагиновую кислоту можно синтезировать из диэтилфталимидомалоната натрия.(C 6 H 4 (CO) 2 NC(CO 2 Et) 2 ). [15]
Метаболизм
[ редактировать ]В растениях и микроорганизмах аспартат является предшественником нескольких аминокислот, в том числе четырех незаменимых для человека: метионина , треонина , изолейцина и лизина . Превращение аспартата в эти другие аминокислоты начинается с восстановления аспартата до его «полуальдегида» O 2 CCH(NH 2 )CH 2 CHO. [16] Аспарагин получают из аспартата путем трансамидирования:
- − О 2 CCH(NH 2 )CH 2 CO 2 − + Г С(О)NH 3 + → O 2 CCH(NH 2 )CH 2 CONH 3 + + Г С(О)О
(где GC (O)NH 2 и GC (O)OH — глутамин и глутаминовая кислота соответственно)
Другие биохимические роли
[ редактировать ]Аспартат выполняет множество других биохимических ролей. Это метаболит в цикле мочевины. [17] и участвует в глюконеогенезе . Он несет восстанавливающие эквиваленты в малатно-аспартатном челноке , в котором используется взаимопревращение аспартата и оксалоацетата , который является окисленным (дегидрированным) производным яблочной кислоты . Аспартат жертвует один атом азота в биосинтезе инозина , предшественника пуриновых оснований. Кроме того, аспарагиновая кислота действует как акцептор водорода в цепи АТФ-синтазы. что пищевая L-аспарагиновая кислота действует как ингибитор бета-глюкуронидазы , которая регулирует энтерогепатическую циркуляцию билирубина Было показано , и желчных кислот. [18]
Интерактивная карта маршрутов
[ редактировать ]Нажмите на гены, белки и метаболиты ниже, чтобы перейти к соответствующим статьям. [§ 1]
- ^ Интерактивную карту маршрутов можно редактировать на WikiPathways: «Гликолиз-Глюконеогенез_WP534» .
Нейромедиатор
[ редактировать ]Аспартат ( сопряженное основание аспарагиновой кислоты) стимулирует NMDA-рецепторы , хотя и не так сильно, как аминокислотный нейротрансмиттер L-глутамат . [19]
Приложения и рынок
[ редактировать ]В 2014 году мировой рынок аспарагиновой кислоты составил 39,3 тыс. коротких тонн (35,7 тыс. тонн ). [20] или около $117 миллионов в год [21] с потенциальными областями роста, составляющими адресный рынок [ нужны разъяснения ] в размере $8,78 млрд (млрд). [22] Три крупнейших сегмента рынка включают США, Западную Европу и Китай. Текущие области применения включают биоразлагаемые полимеры ( полиаспарагиновая кислота ), низкокалорийные подсластители ( аспартам ), ингибиторы накипи и коррозии, а также смолы. [ нужна ссылка ]
Суперабсорбирующие полимеры
[ редактировать ]Одной из областей роста рынка аспарагиновой кислоты являются биоразлагаемые суперабсорбирующие полимеры (SAP) и гидрогели. [23] Ожидается, что рынок суперабсорбирующих полимеров будет расти со среднегодовыми темпами роста 5,5% в период с 2014 по 2019 год и достигнет мировой стоимости в 8,78 млрд долларов США. [22] Около 75% супервпитывающих полимеров используется в одноразовых подгузниках , а еще 20% — в страдающих недержанием продуктах женской гигиены и средствах женской гигиены, у взрослых . Полиаспарагиновая кислота , продукт полимеризации аспарагиновой кислоты, является биоразлагаемым заменителем полиакрилата . [23] [24] [25] Рынок полиаспартатов составляет небольшую долю (около 1%) от общего рынка SAP. [ нужна ссылка ]
Дополнительное использование
[ редактировать ]Помимо SAP, аспарагиновая кислота находит применение в промышленности удобрений стоимостью 19 миллиардов долларов , где полиаспартат улучшает удержание воды и поглощение азота; [26] рынок покрытий для бетонных полов стоимостью 1,1 млрд долларов (2020 г.), где полиаспарагиновая кислота представляет собой низкоэнергетическую альтернативу традиционным эпоксидным смолам с низким содержанием летучих органических соединений; [27] и, наконец, рынок ингибиторов накипи и коррозии стоимостью более 5 миллиардов долларов. [28]
Источники
[ редактировать ]Этот раздел нуждается в дополнительных цитатах для проверки . ( январь 2021 г. ) |
Диетические источники
[ редактировать ]Аспарагиновая кислота не является незаменимой аминокислотой , а это означает, что она может синтезироваться из промежуточных продуктов центрального метаболического пути человека и не обязательно должна присутствовать в рационе. В эукариотических клетках примерно 1 из 20 аминокислот, включенных в белок, представляет собой аспарагиновую кислоту. [29] и, соответственно, почти любой источник пищевого белка будет включать аспарагиновую кислоту. Кроме того, аспарагиновая кислота содержится в:
- Диетические добавки в виде самой аспарагиновой кислоты или ее солей (таких как аспартат магния ).
- Подсластитель аспартам , изготовленный из аспарагиновой кислоты и фенилаланина.
См. также
[ редактировать ]- Аспартаттрансаминаза
- Полиаспарагиновая кислота
- Полиаспартат натрия — синтетический полиамид.
Ссылки
[ редактировать ]- ^ Будавари, Сьюзен; Ко, Мерк (1989). «862. Аспарагиновая кислота» . Индекс Merck (11-е изд.). Мерк. п. 132 . ISBN 978-0-911910-28-5 .
- ^ «ICSC 1439 – L-АСПАРТИНОВАЯ КИСЛОТА» . inchem.org .
- ^ Хейнс, Уильям М., изд. (2016). Справочник CRC по химии и физике (97-е изд.). ЦРК Пресс . стр. 5–89. ISBN 978-1498754286 .
- ^ «Номенклатура и символика аминокислот и пептидов» . Совместная комиссия IUPAC-IUB по биохимической номенклатуре. 1983. Архивировано из оригинала 9 октября 2008 года . Проверено 5 марта 2018 г.
- ^ Перейти обратно: а б с д Г., Воэт, Юдит; В., Пратт, Шарлотта (29 февраля 2016 г.). Основы биохимии: жизнь на молекулярном уровне . Джон Уайли и сыновья. ISBN 9781118918401 . OCLC 910538334 .
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Перейти обратно: а б Д'Аньелло, Антимо (1 февраля 2007 г.). «D-аспарагиновая кислота: эндогенная аминокислота, играющая важную нейроэндокринную роль». Обзоры исследований мозга . 53 (2): 215–234. дои : 10.1016/j.brainresrev.2006.08.005 . ПМИД 17118457 . S2CID 12709991 .
- ^ Хуанг А.С., Бенье А., Вейль З.М., Ким П.М., Молливер М.Е., Блэкшоу С., Нельсон Р.Дж., Янг С.Г., Снайдер Ш.Х. (март 2006 г.). «D-аспартат регулирует образование и функцию меланокортина: поведенческие изменения у мышей с дефицитом D-аспартатоксидазы» . Журнал неврологии . 26 (10): 2814–9. doi : 10.1523/JNEUROSCI.5060-05.2006 . ПМК 6675153 . ПМИД 16525061 .
- ^ «Комиссия IUPAC-IUB по биохимической номенклатуре. Однобуквенное обозначение аминокислотных последовательностей» . Журнал биологической химии . 243 (13): 3557–3559. 10 июля 1968 г. doi : 10.1016/S0021-9258(19)34176-6 .
- ^ Адога, Годвин I; Николсон, Б.Х. (январь 1988 г.). «Письма в редакцию» . Биохимическое образование . 16 (1): 49. дои : 10.1016/0307-4412(88)90026-X .
- ^ Плиссон, А. (октябрь 1827 г.). «О идентичности малата алтеиновой кислоты с аспарагином (1); и о новой кислоте» [О идентичности малата алтеиновой кислоты с аспарагином (1); и у нас есть новая кислота]. Аптечный журнал (на французском языке). 13 (10): 477–492.
- ^ Берцелиус Дж. Я. , Онгрен О. Г. (1839). Трактат по химии (на французском языке). Том. 3. Брюссель: А. Вален и др. стр. 81 . Проверено 25 августа 2015 г.
- ^ Плиммер Р. (1912) [1908]. Пламмер Р., Хопкинс Ф. (ред.). Химический состав белков . Монографии по биохимии. Том. Часть I. Анализ (2-е изд.). Лондон: Longmans, Green and Co. p. 112 . Проверено 18 января 2010 г.
- ^ «Номенклатура и символика аминокислот и пептидов (Рекомендации IUPAC-IUB, 1983 г.)», Pure Appl. хим. , 56 (5): 595–624, 1984, doi : 10.1351/pac198456050595 .
- ^ Карлхайнц Драуц, Ян Грейсон, Аксель Климанн, Ханс-Петер Криммер, Вольфганг Лейхтенбергер, Кристоф Векбекер (2006). Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a02_057.pub2 . ISBN 978-3527306732 .
{{cite encyclopedia}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Данн М.С., Smart BW (1950). «DL-аспарагиновая кислота» . Органические синтезы . 30 :7 ; Сборник томов , т. 4, с. 55 ..
- ^ Ленинджер А.Л., Нельсон Д.Л., Кокс М.М. (2000). Принципы биохимии (3-е изд.). Нью-Йорк: WH Freeman. ISBN 1-57259-153-6 .
- ^ «Биохимия – Биохимия» . www.varsitytutors.com . Проверено 18 февраля 2022 г.
- ^ Кример, Сигел и Горли (октябрь 2001 г.). «Новый ингибитор бета-глюкуронидазы: L-аспарагиновая кислота» . Педиатрические исследования . 50 (4): 460–466. дои : 10.1203/00006450-200110000-00007 . ПМИД 11568288 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Чен П.Е., Гебалле М.Т., Стэнсфельд П.Дж., Джонстон А.Р., Юань Х., Джейкоб А.Л., Снайдер Дж.П., Трейнелис С.Ф., Уилли DJ (май 2005 г.). «Структурные особенности сайта связывания глутамата в рекомбинантных рецепторах N-метил-D-аспартата NR1 / NR2A, определенные с помощью сайт-направленного мутагенеза и молекулярного моделирования». Молекулярная фармакология . 67 (5): 1470–84. дои : 10.1124/моль.104.008185 . ПМИД 15703381 . S2CID 13505187 .
- ^ «Мировой рынок аспарагиновой кислоты по приложениям» . Исследование Гранд Вью . Проверено 30 ноября 2019 г.
- ^ Эванс Дж (2014). Коммерческие аминокислоты . Исследование БЦК. стр. 101–103.
- ^ Перейти обратно: а б Исследование рынка прозрачности. Рынок суперабсорбирующих полимеров – мировой отраслевой анализ, размер, доля, рост, тенденции и прогноз, 2014-2020 гг. (2014).
- ^ Перейти обратно: а б Адельния, Оссейн; Блейки, Идрисс; Литтл, Питер Дж.; Та, Ханг Т. (2019). «Гидрогели на основе полиаспарагиновой кислоты: синтез и применение» . Границы в химии . 7 : 755. Бибкод : 2019FrCh....7..755A . дои : 10.3389/fchem.2019.00755 . ISSN 2296-2646 . ПМК 6861526 . ПМИД 31799235 .
- ^ Адельния, Оссейн; Тран, Хуонг Д.Н.; Литтл, Питер Дж.; Блейки, Идрисс; Та, Ханг Т. (14 июня 2021 г.). «Поли(аспарагиновая кислота) в биомедицинских применениях: от полимеризации, модификации, свойств, деградации и биосовместимости к применениям» . ACS Биоматериалы, наука и инженерия . 7 (6): 2083–2105. doi : 10.1021/acsbimaterials.1c00150 . hdl : 10072/404497 . ПМИД 33797239 . S2CID 232761877 .
- ^ Алфорд Д.Д., Уиллер А.П., Петтигрю, Калифорния (1994). «Биодеградация термически синтезированного полиаспартата». J Environ Polym Degr . 2 (4): 225–236. Бибкод : 1994JEPD....2..225A . дои : 10.1007/BF02071970 .
- ^ Келлинг К. (2001). Реакция сельскохозяйственных культур на Амисорб в Северо-Центральном регионе . Университет Висконсин-Мэдисон.
- ^ К 2020 году мировой рынок покрытий для бетонных полов будет стоить 1,1 миллиарда долларов США. Исследование рынка прозрачности (2015).
- ^ Анализ рынка ингибиторов коррозии по продуктам, по приложениям, по отраслям конечного использования и прогнозы по сегментам до 2020 года. Grand View Research (2014).
- ^ Козловский Л.П. (январь 2017 г.). «Протеом-pI: база данных изоэлектрических точек протеома» . Исследования нуклеиновых кислот . 45 (Д1): Д1112–Д1116. дои : 10.1093/nar/gkw978 . ПМК 5210655 . ПМИД 27789699 .
Внешние ссылки
[ редактировать ]- ГМД МС Спектр
- Американское химическое общество (21 апреля 2010 г.). Кристалл «Евы предков» может объяснить происхождение леворукости жизни . ScienceDaily . Архивировано из оригинала 23 апреля 2010 года . Проверено 21 апреля 2010 г.