Глицин
| |||
| |||
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Глицин | |||
| Систематическое название ИЮПАК Аминоуксусная кислота [2] | |||
Другие имена
| |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| Сокращения | Гли , Г | ||
| ЧЭБИ | |||
| ЧЕМБЛ | |||
| ХимическийПаук | |||
| Лекарственный Банк | |||
| Информационная карта ECHA | 100.000.248 | ||
| Номер ЕС |
| ||
| номер Е | Е640 (усилитель вкуса) | ||
| КЕГГ | |||
ПабХим CID | |||
| НЕКОТОРЫЙ |
| ||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| С 2 Н 5 Н О 2 | |||
| Молярная масса | 75.067 g·mol −1 | ||
| Появление | Белый твердый | ||
| Плотность | 1,1607 г/см 3 [3] | ||
| Температура плавления | 233 ° C (451 ° F, 506 К) (разложение) | ||
| 249,9 г/л (25 °С) [4] | |||
| Растворимость | растворим в пиридине умеренно растворим в этаноле нерастворим в эфире | ||
| Кислотность ( pKa ) | 2,34 (карбоксил), 9,6 (амино) [5] | ||
| -40.3·10 −6 см 3 /моль | |||
| Фармакология | |||
| B05CX03 ( ВОЗ ) | |||
| Опасности | |||
| Летальная доза или концентрация (LD, LC): | |||
ЛД 50 ( средняя доза ) | 2600 мг/кг (мыши, перорально) | ||
| Страница дополнительных данных | |||
| Глицин (страница данных) | |||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
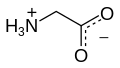
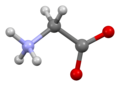
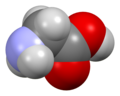
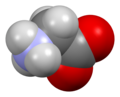
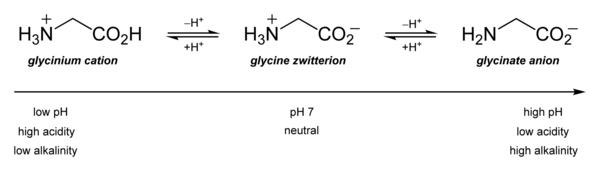
Глицин (символ Gly или G ; [6] / ˈ ɡ l aɪ s iː n / ) [7] Это аминокислота один водорода атом , имеющая в качестве боковой цепи . Это простейшая стабильная аминокислота ( карбаминовая кислота нестабильна). В газовой фазе это молекула с химической формулой NH 2 ‐ CH 2 ‐ COOH . В растворе или в твердом состоянии глицин существует в виде цвиттер-иона . Глицин – одна из протеиногенных аминокислот . Он кодируется всеми кодонами, начинающимися с GG (GGU, GGC, GGA, GGG). Глицин является неотъемлемой частью формирования альфа-спиралей во вторичной структуре белка из-за «гибкости», обусловленной такой маленькой группой R. Глицин также является тормозным нейротрансмиттером : вмешательство в его высвобождение в спинном мозге (например, во время инфекции Clostridium tetani ) может вызвать спастический паралич из-за незаторможенного сокращения мышц.
Это единственная ахиральная протеиногенная аминокислота . Он может вписываться в гидрофильную или гидрофобную среду благодаря минимальной боковой цепи, состоящей всего из одного атома водорода.
История и этимология [ править ]
Глицин был открыт в 1820 году французским химиком Анри Браконно, когда он гидролизовал желатин путем кипячения его с серной кислотой . [8] Первоначально он назвал его «желатиновым сахаром». [9] [10] но французский химик Жан-Батист Буссенго в 1838 году показал, что он содержит азот. [11] В 1847 году американский учёный Эбен Нортон Хорсфорд , тогда ученик немецкого химика Юстуса фон Либиха , предложил название «гликоколл»; [12] [13] однако шведский химик Берцелиус предложил более простое нынешнее название. год спустя [14] [15] Название происходит от греческого слова γλυκύς «сладкий вкус». [16] (что также связано с приставками глико- и глюко- , как в гликопротеине и глюкозе ). В 1858 году французский химик Огюст Каур определил, что глицин представляет собой амин уксусной кислоты . [17]
Производство [ править ]
Хотя глицин можно выделить из гидролизованного белка , этот путь не используется для промышленного производства, поскольку его удобнее производить химическим синтезом. [18] Два основных процесса — аминирование хлоруксусной кислоты с аммиаком образованием глицина и хлорида аммония . [19] и синтез аминокислот Стрекера , [20] который является основным синтетическим методом в США и Японии. [21] около 15 тысяч тонн . Ежегодно таким способом добывается [22]
Глицин также образуется в виде примеси при синтезе ЭДТА в результате реакций побочного продукта аммиака. [23]
Химические реакции [ править ]
Наиболее важны его кислотно-основные свойства. В водном растворе глицин амфотерен : при pH ниже 2,4 он превращается в катион аммония, называемый глицинием. При значении выше 9,6 он превращается в глицинат.
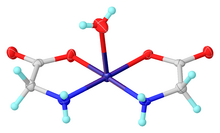
Глицин действует как бидентатный лиганд для многих ионов металлов, образуя аминокислотные комплексы . Типичным комплексом является Cu(глицинат) 2 , т.е. Cu(H 2 NCH 2 CO 2 ) 2 , который существует как в цис-, так и в транс-изомерах.
С хлорангидридами глицин превращается в амидокарбоновую кислоту, например гиппуровую кислоту. [24] и ацетилглицин . [25] С азотистой кислотой получают гликолевую кислоту ( определение Ван Слайка ). С метилйодидом амин кватернизируется с образованием триметилглицина , природного продукта:
- ЧАС
3 Н +
СН
2 операционный директор −
+ 3 СН 3 I → (СН
3 )
3 Н +
СН
2 операционный директор −
+ 3 ПРИВЕТ
Глицин конденсируется сам с собой с образованием пептидов, начиная с образования глицилглицина :
- 2 часа
3 Н +
СН
2 операционный директор −
→ Ч
3 Н +
СН
2 КОНХЧ
2 операционный директор −
+ Н 2 О
Пиролиз глицина или глицилглицина дает 2,5-дикетопиперазин , циклический диамид.
Со спиртами образует сложные эфиры. Их часто выделяют в виде гидрохлорида , например гидрохлорида метилового эфира глицина . В противном случае свободный эфир имеет тенденцию превращаться в дикетопиперазин .
Как бифункциональная молекула, глицин реагирует со многими реагентами. Их можно разделить на реакции с N-центром и карбоксилат-центром.
Метаболизм [ править ]
Биосинтез [ править ]
Глицин не является незаменимым в рационе человека , поскольку он биосинтезируется в организме из аминокислоты серина , которая, в свою очередь, образуется из 3-фосфоглицерата . У большинства организмов фермент серингидроксиметилтрансфераза катализирует это преобразование через кофактор пиридоксальфосфат : [26]
- серин + тетрагидрофолат → глицин + N 5 , Н 10 -метилентетрагидрофолат + H 2 O
В E. coli глицин чувствителен к антибиотикам, нацеленным на фолат. [27]
В печени позвоночных синтез глицина катализируется глицинсинтазой (также называемой ферментом расщепления глицина). Это преобразование легко обратимо : [26]
Помимо синтеза из серина, глицин также может быть получен из треонина , холина или гидроксипролина посредством межорганного метаболизма в печени и почках. [28]
Деградация [ править ]
Глицин разлагается тремя путями. Преобладающий путь у животных и растений является обратным пути глицинсинтазы, упомянутому выше. В этом контексте задействованную ферментативную систему обычно называют системой расщепления глицина : [26]
- Глицин + тетрагидрофолат + НАД + ⇌ СО 2 + NH +
4 + Н 5 , Н 10 -метилентетрагидрофолат + НАДН + Н +
По второму пути глицин разлагается в два этапа. Первым шагом является реверс биосинтеза глицина из серина с помощью серингидроксиметилтрансферазы. Затем серин превращается в пируват под действием сериндегидратазы . [26]
На третьем пути деградации глицин превращается в глиоксилат под действием оксидазы D-аминокислот . Затем глиоксилат окисляется лактатдегидрогеназой печени до оксалата в НАД. + -зависимая реакция. [26]
Период полувыведения глицина и его выведение из организма значительно варьируются в зависимости от дозы. [29] В одном исследовании период полувыведения варьировал от 0,5 до 4,0 часов. [29]
Физиологическая функция [ править ]
Основная функция глицина заключается в том, что он действует как предшественник белков . Большинство белков включают лишь небольшие количества глицина, заметным исключением является коллаген , который содержит около 35% глицина из-за его периодически повторяющейся роли в формировании спиральной структуры коллагена в сочетании с гидроксипролином . [26] [30] В генетическом коде глицин кодируется всеми кодонами, начинающимися с GG, а именно GGU, GGC, GGA и GGG.
В качестве промежуточного продукта биосинтеза [ править ]
У высших δ эукариот -аминолевулиновая кислота , ключевой предшественник порфиринов , биосинтезируется из глицина и сукцинил-КоА с помощью фермента АЛК-синтазы . Глицин обеспечивает центральную субъединицу C 2 N всех пуринов . [26]
Как нейромедиатор [ править ]
Глицин является тормозным нейромедиатором в центральной нервной системе , особенно в спинном мозге , стволе мозга и сетчатке . Когда глициновые рецепторы активируются, хлорид поступает в нейрон через ионотропные рецепторы, вызывая тормозной постсинаптический потенциал (ТПСП). Стрихнин является сильным антагонистом ионотропных глициновых рецепторов, тогда как бикукулин — слабым. Глицин является необходимым коагонистом наряду с глутаматом для рецепторов NMDA . В отличие от тормозной роли глицина в спинном мозге, такое поведение облегчается рецепторами ( NMDA ), глутаматергическими которые являются возбуждающими. [31] ЛД глицина 50 составляет 7930 мг/кг для крыс (перорально). [32] и это обычно приводит к смерти от гипервозбудимости.
В качестве агента конъюгации токсинов [ править ]
глицина Путь конъюгации до конца не изучен. [33] Считается, что глицин является детоксикатором печени ряда эндогенных и ксенобиотических органических кислот. [34] Желчные кислоты обычно конъюгируют с глицином, чтобы повысить их растворимость в воде. [35]
Человеческий организм быстро выводит бензоат натрия , соединяя его с глицином с образованием гиппуровой кислоты , которая затем выводится из организма. [36] Метаболический путь этого начинается с превращения бензоата бутират-КоА-лигазой в промежуточный продукт бензоил-КоА . [37] который затем метаболизируется глицин -N -ацилтрансферазой в гиппуровую кислоту. [38]
Использует [ править ]
В США глицин обычно продается в двух сортах: Фармакопея США («USP») и технический сорт. Продажи глицина согласно Фармакопее США составляют примерно 80–85 процентов рынка глицина в США. Если необходима чистота, превышающая стандарт USP, например, для внутривенных инъекций, можно использовать более дорогой глицин фармацевтического качества. Глицин технического качества, который может соответствовать или не соответствовать стандартам качества USP, продается по более низкой цене для использования в промышленных целях, например, в качестве агента при комплексообразовании и отделке металлов. [39]
Продукты животного и человеческого происхождения [ править ]
Глицин не широко используется в пищевых продуктах из-за его пищевой ценности, за исключением настоев. Вместо этого роль глицина в пищевой химии заключается в качестве ароматизатора. Он слегка сладкий и компенсирует послевкусие сахарина . Он также обладает консервирующими свойствами, возможно, из-за образования комплекса с ионами металлов. Глицинатные комплексы металлов, например глицинат меди(II), используются в качестве добавок к кормам для животных. [22]
«Управление по контролю за продуктами и лекарствами США считает глицин и его соли общепризнанными безопасными для использования в пищу человека». [41]
Химическое сырье [ править ]
Глицин является промежуточным продуктом в синтезе различных химических продуктов. Используется при производстве гербицидов глифосат . [42] ипродион , глифосин, имипротрин и эглиназин. [22] Он используется в качестве промежуточного соединения антибиотиков, таких как тиамфеникол . [ нужна ссылка ]
Лабораторные исследования [ править ]
Глицин является важным компонентом некоторых растворов, используемых в SDS-PAGE методе анализа белков . Он служит буферным агентом, поддерживая pH и предотвращая повреждение образца во время электрофореза. Глицин также используется для удаления антител, мечущих белки, с мембран вестерн-блоттинга , чтобы обеспечить зондирование многочисленных представляющих интерес белков из геля SDS-PAGE. Это позволяет получить больше данных из одного и того же образца, повышая надежность данных, уменьшая объем обработки образцов и количество необходимых образцов. Этот процесс известен как стриппинг.
Присутствие в космосе [ править ]
Присутствие глицина за пределами Земли было подтверждено в 2009 году на основе анализа проб, взятых в 2004 году НАСА космическим кораблем Stardust с кометы Уайлд-2 и впоследствии возвращенных на Землю. Глицин ранее был обнаружен в метеорите Мерчисон в 1970 году. [43] Открытие глицина в космическом пространстве укрепило гипотезу так называемой мягкой панспермии , которая утверждает, что «строительные блоки» жизни широко распространены по всей Вселенной. [44] В 2016 году было объявлено об обнаружении глицина внутри кометы 67P/Чурюмова–Герасименко кораблем Розетта космическим . [45]
Обнаружение глицина за пределами Солнечной системы в межзвездной среде обсуждается. [46]
Эволюция [ править ]
Предполагается, что глицин определяется ранними генетическими кодами. [47] [48] [49] [50] Например, области низкой сложности (в белках), которые могут напоминать протопептиды раннего генетического кода, сильно обогащены глицином. [50]
Присутствие в продуктах питания [ править ]
| Еда | Процент содержание по весу (г/100г) |
|---|---|
| Снеки, свиные шкурки | 11.04 |
| Мука кунжутная (обезжиренная) | 3.43 |
| Напитки, протеиновый порошок ( на соевой основе) | 2.37 |
| Семена, шрот семян сафлора частично обезжиренный | 2.22 |
| Мясо, бизон, говядина и др. (разные части) | 1.5–2.0 |
| Желатиновые десерты | 1.96 |
| Семена, тыквы и тыквы ядра семян | 1.82 |
| Индейка, все сорта, спинка, мясо и кожа | 1.79 |
| Курица, бройлеры или цыплята, мясо и кожа | 1.74 |
| Свинина, фарш, 96% постного мяса / 4% жира, приготовленная, крошка | 1.71 |
| Бекон и говяжьи палочки | 1.64 |
| Арахис | 1.63 |
| Ракообразные , лангусты | 1.59 |
| Специи, семена горчицы , молотые | 1.59 |
| Салями | 1.55 |
| Орехи, орехи , сушеные | 1.51 |
| Рыба, лосось, розовая, консервированная, с сушеными сухими веществами | 1.42 |
| Миндаль | 1.42 |
| Рыба, скумбрия | 0.93 |
| Крупы готовые, гранола, домашние | 0.81 |
| Лук -порей (луковица и нижняя часть листьев), сублимированный | 0.7 |
| Сыр, пармезан (и другие), тертый | 0.56 |
| Соевые бобы , зеленые, приготовленные, отварные, сушеные, без соли | 0.51 |
| Хлеб, белок (включая глютен) | 0.47 |
| Яйцо, целое, приготовленное, жареное | 0.47 |
| Фасоль белая, со зрелыми семенами, вареная, с солью | 0.38 |
| Чечевица, зрелые семена, приготовленная, отварная, с солью | 0.37 |
См. также [ править ]
Ссылки [ править ]
- ^ Индекс Merck: Энциклопедия химических веществ, лекарств и биологических препаратов (11-е изд.), Merck, 1989, ISBN. 091191028X , 4386
- ^ pubchem.ncbi.nlm.nih.gov/compound/750#section=IUPAC-Name&fullscreen=true
- ^ Справочник по химии и физике , CRC Press, 59-е издание, 1978 г.
- ^ «Растворимость и плотность» . Prowl.rockefeller.edu. Архивировано из оригинала 12 сентября 2017 года . Проверено 13 ноября 2013 г.
- ^ Доусон, RMC и др., Данные для биохимических исследований , Оксфорд, Clarendon Press, 1959.
- ^ «Номенклатура и символика аминокислот и пептидов» . Совместная комиссия IUPAC-IUB по биохимической номенклатуре. 1983. Архивировано из оригинала 9 октября 2008 года . Проверено 5 марта 2018 г.
- ^ «Глицин | Определение глицина на английском языке в Оксфордских словарях» . Архивировано из оригинала 29 января 2018 года.
- ^ Плиммер, RHA (1912) [1908]. Плиммер, RHA; Хопкинс, Ф.Г. (ред.). Химический состав белков . Монографии по биохимии. Том. Часть I. Анализ (2-е изд.). Лондон: Longmans, Green and Co. p. 82 . Проверено 18 января 2010 г.
- ^ Браконно, Анри (1820). «О превращении животного сырья в новые вещества посредством серной кислоты» . Анналы химии и физики . 2-я серия (на французском языке). 13 :113–125. ; см. стр. 114.
- ^ Маккензи, Колин (1822). Тысяча химических экспериментов: с иллюстрациями природных явлений; и практические наблюдения над производственными и химическими процессами, которые в настоящее время используются в успешном развитии полезных искусств… . Сэр Р. Филлипс и компания. п. 557 .
- ^ Буссенго (1838). «О составе сахара желатина и нитроглюкаровой кислоты Браконно» . Comptes Rendus (на французском языке). 7 : 493–495.
- ^ Хорсфорд, EN (1847 г.). «Гликоколл (желатиновый сахар) и некоторые продукты его разложения» . Американский журнал науки и искусства . 2-я серия. 3 : 369–381.
- ^ Иде, Аарон Дж. (1970). Развитие современной химии . Курьерская компания. ISBN 9780486642352 .
- ^ Берцелиус, Якоб (1848). Jahres-Bericht über die Fortschritte der Chemie und Mineralogie (Ежегодный отчет о прогрессе химии и минералогии) . Том. 47. Тюбиген, (Германия): Лаупп. п. 654. Со с. 654: «Er Hat dem Leimzucker als Basis den Namen Glycocoll gegeben.… Глицин genannt werden, und diesen Namen werde ich anwenden». (Он [т. е. американский учёный Эбен Нортон Хорсфорд , тогда ученик немецкого химика Юстуса фон Либиха ] дал название «гликоколл» Леймцукеру [сахар из желатина], основанию. Это название неблагозвучно и имеет к тому же недостаток что оно противоречит названиям остальных основ. Оно составлено из γλυχυς (сладкий) и χολλα (животный клей). Поскольку эта органическая основа — единственная, имеющая сладкий вкус, то ее можно назвать гораздо короче. «глицин», и я буду использовать это имя.)
- ^ Най, Мэри Джо (1999). До большой науки: стремление к современной химии и физике, 1800–1940 гг . Издательство Гарвардского университета. ISBN 9780674063822 .
- ^ «глицин» . Оксфордские словари . Архивировано из оригинала 13 ноября 2014 года . Проверено 6 декабря 2015 г.
- ^ Каур, А. (1858). «Исследования аминированных кислот». Comptes Rendus (на французском языке). 46 : 1044–1047.
- ^ Окафор, Ндука (9 марта 2016 г.). Современная промышленная микробиология и биотехнология . ЦРК Пресс. ISBN 9781439843239 .
- ^ Ингерсолл, AW; Бэбкок, С.Х. (1932). «Гиппуровая кислота» . Органические синтезы . 12:40 ; Сборник томов , т. 2, с. 328 .
- ^ Уайли (14 декабря 2007 г.). Kirk-Othmer Food and Feed Technology, набор из 2 томов . Джон Уайли и сыновья. ISBN 9780470174487 .
- ^ «Глициновая конференция (предварительная)» . USITC. Архивировано из оригинала 22 февраля 2012 года . Проверено 13 июня 2014 г.
{{cite web}}: CS1 maint: bot: исходный статус URL неизвестен ( ссылка ) - ^ Jump up to: а б с Драуз, Карлхайнц; Грейсон, Ян; Климанн, Аксель; Криммер, Ганс Петер; Лейхтенбергер, Вольфганг и Векбекер, Кристоф (2007). «Аминокислоты». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. ISBN 978-3527306732 .
- ^ Харт, Дж. Роджер (2005). «Этилендиаминтетрауксусная кислота и родственные хелатирующие агенты». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a10_095 . ISBN 978-3527306732 .
- ^ Ингерсолл, AW; Бэбкок, С.Х. (1932). «Гиппуровая кислота». Орг. Синтез . 12:40 . дои : 10.15227/orgsyn.012.0040 .
- ^ Хербст, РМ; Шемин, Д. (1939). «Ацетилглицин». Орг. Синтез . 19 :4. дои : 10.15227/orgsyn.019.0004 .
- ^ Jump up to: а б с д и ж г Нельсон, Дэвид Л.; Кокс, Майкл М. (2005). Принципы биохимии (4-е изд.). Нью-Йорк: WH Freeman. стр. 127, 675–77, 844, 854. ISBN. 0-7167-4339-6 .
- ^ Квон, Юн Гён; Хиггинс, Мейтал Б.; Рабиновиц, Джошуа Д. (2010). «Вызванное антифолатом истощение внутриклеточного глицина и пуринов подавляет бестиминовую гибель E. Coli » . АКС Химическая биология . 5 (8): 787–795. дои : 10.1021/cb100096f . ПМЦ 2945287 . ПМИД 20553049 .
- ^ Ван, В.; Ву, З.; Дай, З.; Ян, Ю.; Ван, Дж.; Ву, Г. (2013). «Метаболизм глицина у животных и человека: значение для питания и здоровья». Аминокислоты . 45 (3): 463–77. дои : 10.1007/s00726-013-1493-1 . ПМИД 23615880 . S2CID 7577607 .
- ^ Jump up to: а б Хан Р.Г. (1993). «Дозозависимый период полувыведения глицина». Урологические исследования . 21 (4): 289–291. дои : 10.1007/BF00307714 . ПМИД 8212419 . S2CID 25138444 .
- ^ Шпак, Пол (2011). «Химия и ультраструктура рыбьих костей: значение для тафономии и анализа стабильных изотопов» . Журнал археологической науки . 38 (12): 3358–3372. дои : 10.1016/j.jas.2011.07.022 .
- ^ «Недавние разработки рецепторов NMDA» . Китайский медицинский журнал. 2000.
- ^ «Данные по безопасности (MSDS) глицина» . Лаборатория физической и теоретической химии Оксфордского университета. 2005. Архивировано из оригинала 20 октября 2007 года . Проверено 1 ноября 2006 г.
- ^ ван дер Слюис, Ренсия; Баденхорст, Кристоффель П.С.; Эразм, Элард; ван Дайк, Этрезия; ван дер Вестхуизен, Франсуа Х.; ван Дейк, Альбердина А. (15 октября 2015 г.). «Консервативность кодирующих областей гена глицин-N-ацилтрансферазы также позволяет предположить, что конъюгация глицина является важным путем детоксикации» . Джин . 571 (1): 126–134. дои : 10.1016/j.gene.2015.06.081 . ISSN 1879-0038 . ПМИД 26149650 .
- ^ Баденхорст, Кристоффель Петрус Стефанус; Эразм, Элард; ван дер Слюис, Ренсия; Нортье, Карла; ван Дейк, Альбердина Айке (август 2014 г.). «Новый взгляд на важность конъюгации глицина в метаболизме ароматических кислот» . Обзоры метаболизма лекарств . 46 (3): 343–361. дои : 10.3109/03602532.2014.908903 . ISSN 1097-9883 . ПМИД 24754494 .
- ^ Ди Чаула, Агостино; Гаррути, Габриэлла; Лунарди Баччетто, Ракель; Молина-Молина, Эмилио; Бонфрате, Леонильда; Ван, Дэвид К.-Х.; Портинкаса, Пьеро (ноябрь 2017 г.). «Физиология желчных кислот» . Анналы гепатологии . 16 (Приложение 1: с3-105.): с4–с14. дои : 10.5604/01.3001.0010.5493 . hdl : 11586/203563 . ISSN 1665-2681 . ПМИД 29080336 .
- ^ «Окончательный отчет об оценке безопасности бензилового спирта, бензойной кислоты и бензоата натрия» . Международный журнал токсикологии . 20 (3_приложение): 23–50. Январь 2001 г. doi : 10.1080/10915810152630729 . ISSN 1091-5818 .
- ^ «бутират-КоА-лигаза» . БРЕНДА . Технический университет Брауншвейга . Проверено 7 мая 2014 г. Субстраты/Продукт
- ^ «глицин-N-ацилтрансфераза» . БРЕНДА . Технический университет Брауншвейга . Проверено 7 мая 2014 г. Субстраты/Продукт
- ^ «Глицин из Японии и Кореи» (PDF) . Комиссия по международной торговле США. Январь 2008 г. Архивировано (PDF) из оригинала 6 июня 2010 г. Проверено 13 июня 2014 г.
- ^ Казари, Б.М.; Махмудхани, Ах; Лангер, В. (2004). «Переопределение цис -Аквабис (глицинато-κ 2 N,O )медь(II)". Acta Crystallogr. E. 60 ( 12): m1949–m1951. doi : 10.1107/S1600536804030041 .
- ^ «eCFR :: 21 CFR 170.50 — Глицин (аминоуксусная кислота) в продуктах питания, предназначенных для потребления человеком» . ecfr.gov . Проверено 24 октября 2022 г.
- ^ Шталь, Шеннон С.; Альстерс, Пол Л. (13 июля 2016 г.). Жидкофазный катализ аэробного окисления: промышленное применение и академические перспективы . Джон Уайли и сыновья. ISBN 9783527690152 .
- ^ Квенволден, Кейт А.; Лоулесс, Джеймс; Перинг, Кэтрин; Петерсон, Этта; Флорес, Хосе; Поннамперума, Кирилл; Каплан, Исаак Р.; Мур, Карлтон (1970). «Доказательства наличия внеземных аминокислот и углеводородов в метеорите Мерчисон». Природа . 228 (5275): 923–926. Бибкод : 1970Natur.228..923K . дои : 10.1038/228923a0 . ПМИД 5482102 . S2CID 4147981 .
- ^ «Строительный блок жизни обнаружен на комете – Thomson Reuters, 2009» . Рейтер . 18 августа 2009 года . Проверено 18 августа 2009 г.
- ^ Европейское космическое агентство (27 мая 2016 г.). «Комета Розетты содержит ингредиенты для жизни» . Проверено 5 июня 2016 г.
- ^ Снайдер Л.Е., Ловас Ф.Дж., Холлис Дж.М. и др. (2005). «Тщательная попытка проверить межзвездный глицин». Астрофиз Дж . 619 (2): 914–930. arXiv : astro-ph/0410335 . Бибкод : 2005ApJ...619..914S . дои : 10.1086/426677 . S2CID 16286204 .
- ^ Трифонов Е.Н. (декабрь 2000 г.). «Консенсусный временной порядок аминокислот и эволюция триплетного кода» . Джин . 261 (1): 139–151. дои : 10.1016/S0378-1119(00)00476-5 . ПМИД 11164045 .
- ^ Хиггс, Пол Г.; Пудриц, Ральф Э. (июнь 2009 г.). «Термодинамическая основа синтеза пребиотических аминокислот и природа первого генетического кода». Астробиология . 9 (5): 483–490. arXiv : 0904.0402 . Бибкод : 2009AsBio...9..483H . дои : 10.1089/ast.2008.0280 . ISSN 1531-1074 . ПМИД 19566427 . S2CID 9039622 .
- ^ Халиотис, Анаргирос; Властаридис, Панайотис; Моссиалос, Димитрис; Ибба, Майкл; Беккер, Хьюберт Д.; Статопулос, Константинос; Амуциас, Григориос Д. (17 февраля 2017 г.). «Сложная эволюционная история аминоацил-тРНК-синтетаз» . Исследования нуклеиновых кислот . 45 (3): 1059–1068. дои : 10.1093/nar/gkw1182 . ISSN 0305-1048 . ПМК 5388404 . ПМИД 28180287 .
- ^ Jump up to: а б Нтунтуми, Криса; Властаридис, Панайотис; Моссиалос, Димитрис; Статопулос, Константинос; Илиопулос, Иоаннис; Промпонас, Василиос; Оливер, Стивен Дж; Амуциас, Григорис Д. (4 ноября 2019 г.). «Области низкой сложности в белках прокариот выполняют важные функциональные роли и высоко консервативны» . Исследования нуклеиновых кислот . 47 (19): 9998–10009. дои : 10.1093/nar/gkz730 . ISSN 0305-1048 . ПМК 6821194 . ПМИД 31504783 .
- ^ «Результаты поиска FoodData Central по запросу «Глицин (г)» » . fdc.nal.usda.gov . Проверено 26 мая 2024 г.
Дальнейшее чтение [ править ]
- Куан Ю.Дж., Чарнли С.Б., Хуанг Х.К. и др. (2003). «Межзвездный глицин» . Астрофиз Дж . 593 (2): 848–867. Бибкод : 2003ApJ...593..848K . дои : 10.1086/375637 .
- Новак, Рэйчел. «Аминокислота найдена в глубоком космосе – 18 июля 2002 г. – New Scientist » . Проверено 1 июля 2007 г.
Внешние ссылки [ править ]
- Глицин МС Спектр
- Глицин
- Система расщепления глицина
- Глициновая терапия – новое направление лечения шизофрении?
- «Органическая молекула, подобная аминокислоте, обнаруженная в созвездии Стрельца» . ScienceDaily . 27 марта 2008 г.
- Цай, Гочуань Э. (1 декабря 2008 г.). «Новый класс антипсихотических препаратов: усиление нейротрансмиссии, опосредованной рецепторами NMDA» . Психиатрические времена . 25 (14). Архивировано из оригинала 3 октября 2012 года . Проверено 23 января 2009 г.
- ChemSub Online (глицин) .
- Ученые НАСА обнаружили глицин, фундаментальный строительный блок жизни, в образцах кометы Уайлд-2, доставленных космическим кораблем НАСА «Звездная пыль».