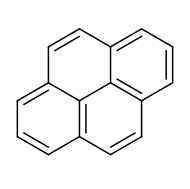
Пирен
 | |
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК Пирен [1] | |
| Другие имена Бензо[ деф ]фенантрен | |
| Идентификаторы | |
3D model ( JSmol ) | |
| 1307225 | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.004.481 |
| 84203 | |
| КЕГГ | |
ПабХим CID | |
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 16:10 H | |
| Молярная масса | 202.256 g·mol −1 |
| Появление | бесцветное твердое вещество (желтые примеси часто обнаруживаются в следовых количествах во многих образцах). |
| Плотность | 1,271 г/см 3 [2] |
| Температура плавления | 150,62 ° С (303,12 ° F; 423,77 К) [2] |
| Точка кипения | 394 ° С (741 ° F, 667 К) [2] |
| 0,049 мг/л (0 °С) 0,139 мг/л (25 °С) 2,31 мг/л (75 °С) [3] | |
| войти P | 5.08 [4] |
| Запрещенная зона | 2,02 эВ [5] |
| -147·10 −6 см 3 /моль [6] | |
| Структура [7] | |
| Моноклиника | |
| Р2 1 /а | |
а = 13,64 Å, b = 9,25 Å, c = 8,47 Å α = 90°, β = 100,28°, γ = 90° | |
Формульные единицы ( Z ) | 4 |
| Термохимия [8] | |
Теплоемкость ( С ) | 229,7 Дж/(К·моль) |
Стандартный моляр энтропия ( S ⦵ 298 ) | 224,9 Дж·моль −1 ·К −1 |
Стандартная энтальпия образование (Δ f H ⦵ 298 ) | 125,5 кДж·моль −1 |
Энтальпия плавления (Δ f H ⦵ фу ) | 17,36 кДж·моль −1 |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности | раздражитель |
| СГС Маркировка : [9] | |
  | |
| Предупреждение | |
| Х315 , Х319 , Х335 , Х410 | |
| P261 , P264 , P271 , P273 , P280 , P302+P352 , P304+P340 , P305+P351+P338 , P312 , P321 , P332+P313 , P337+P313 , P362 , P391 , P403+P233 , П405 , П501 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | негорючий |
| Родственные соединения | |
Родственные ПАУ | бензопирен |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Пирен представляет собой полициклический ароматический углеводород (ПАУ), состоящий из четырех конденсированных бензольных колец, в результате чего образуется плоская ароматическая система. Химическая формула С 16 Ч 10 . Это желто-зеленое твердое вещество представляет собой наименьший периферийно-слитый ПАУ (когда кольца слиты более чем через одну поверхность). Пирен образуется при неполном сгорании органических соединений. [10]
Возникновение и свойства
[ редактировать ]Пирен впервые был выделен из каменноугольной смолы , где его содержание составляет до 2% по массе. Как периконденсированный ПАУ, пирен гораздо более резонансно стабилизирован, чем его пятичленное кольцо, содержащее изомер флуорантен . Поэтому его производят в широком диапазоне условий горения. Например, автомобили производят около 1 мкг/км. [11]
Реакции
[ редактировать ]Окисление хроматом дает перинафтенон, а затем нафталин-1,4,5,8-тетракарбоновую кислоту. Пирен подвергается ряду реакций гидрирования и подвержен галогенированию, добавкам Дильса-Альдера и нитрованию, причем все с разной степенью селективности. [11] Бромирование происходит по одному из трех положений. [12]
Восстановление натрием дает анион-радикал. Из этого аниона можно получить разнообразные пиареновые комплексы. [13]
Фотофизика
[ редактировать ]Пирен и его производные используются в коммерческих целях для производства красителей и предшественников красителей, например пиранин и нафталин-1,4,5,8-тетракарбоновая кислота. Он имеет сильное поглощение в УФ-видимом диапазоне в трех резких полосах при 330 нм в DCM. Излучение близко к поглощению, но движется на длине волны 375 нм. [14] Морфология сигналов меняется в зависимости от растворителя. Его производные также являются ценными молекулярными зондами для флуоресцентной спектроскопии, обладая высокими квантовым выходом и временем жизни (0,65 и 410 наносекунд соответственно в этаноле при 293 К). Пирен был первой молекулой, для которой эксимерное поведение. было обнаружено [15] Такой эксимер появляется около 450 нм. Теодор Фёрстер сообщил об этом в 1954 году. [16]
Приложения
[ редактировать ]пирена Спектр флуоресценции очень чувствителен к полярности растворителя, поэтому пирен использовался в качестве зонда для определения среды растворителя. Это связано с тем, что его возбужденное состояние имеет другую неплоскую структуру, чем основное состояние. Некоторые полосы излучения не изменяются, но интенсивность других меняется из-за силы взаимодействия с растворителем.

Пирены являются сильными донорами электронов, и их можно комбинировать с несколькими материалами для создания донорно-акцепторных систем, которые можно использовать в приложениях преобразования энергии и сбора света. [14]
Факторы безопасности и окружающей среды
[ редактировать ]Хотя он не так опасен, как бензопирен , исследования на животных показали, что пирен токсичен для почек и печени . Сейчас известно, что пирен влияет на несколько жизненных функций рыб и водорослей. [18] [19] [20] [21]
Его биоразложение было тщательно изучено. Процесс начинается с дигидроксилирования по каждому из двух типов связей CH=CH. [22] Эксперименты на свиньях показывают, что 1-гидроксипирен в моче является метаболитом пирена при пероральном приеме. [23]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Международный союз теоретической и прикладной химии (2014). Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 . Королевское химическое общество . п. 206. дои : 10.1039/9781849733069 . ISBN 978-0-85404-182-4 .
- ^ Jump up to: а б с Хейнс, с. 3,472
- ^ Хейнс, с. 5.162
- ^ Хейнс, с. 5.176
- ^ Хейнс, с. 12.96
- ^ Хейнс, с. 3,579
- ^ Камераман, А.; Троттер, Дж. (1965). «Кристаллическая и молекулярная структура пирена» . Акта Кристаллографика . 18 (4): 636–643. дои : 10.1107/S0365110X65001494 .
- ^ Хейнс, стр. 5.34, 6.161.
- ^ СГС: PubChem
- ^ Фигейра-Дуарте, Тереза М.; Мюллен, Клаус (2011). «Материалы на основе пирена для органической электроники». Химические обзоры . 111 (11): 7260–7314. дои : 10.1021/cr100428a . ПМИД 21740071 .
- ^ Jump up to: а б Сенкан, Селим и Кастальди, Марко (2003) «Горение» в Энциклопедии промышленной химии Ульмана , Wiley-VCH, Вайнхайм.
- ^ Гумпрехт, WH (1968). «3-Бромпирен». Орг. Синтез . 48:30 . дои : 10.15227/orgsyn.048.0030 .
- ^ Кучера, Бенджамин Э.; Джилек, Роберт Э.; Бреннессел, Уильям В.; Эллис, Джон Э. (2014). «Бис(пирен)металлокомплексы ванадия, ниобия и титана: изолируемые гомолептические пиреновые комплексы переходных металлов». Acta Crystallographica Раздел C: Структурная химия . 70 (8): 749–753. дои : 10.1107/S2053229614015290 . ПМИД 25093352 .
- ^ Jump up to: а б Тагматарчис, Никос; Юэлс, Кристофер П.; Биттенкорт, Карла; Ареналь, Рауль; Пелаес-Фернандес, Марио; Сайед-Ахмад-Бараза, Юман; Кантон-Витория, Рубен (05.06.2017). «Функционализация MoS 2 с 1,2-дитиоланами: к донорно-акцепторным наногибридам для преобразования энергии» . npj 2D-материалы и приложения . 1 (1): 13. дои : 10.1038/s41699-017-0012-8 . ISSN 2397-7132 .
- ^ Ван Дайк, Дэвид А.; Прайор, Брайан А.; Смит, Филип Г.; Топп, Майкл Р. (май 1998 г.). «Наносекундная флуоресцентная спектроскопия с временным разрешением в лаборатории физической химии: образование эксимера пирена в растворе». Журнал химического образования . 75 (5):615. Бибкод : 1998ЖЧЭд..75..615В . дои : 10.1021/ed075p615 .
- ^ Фёрстер, Т.; Каспер, К. (июнь 1954 г.). «Концентрационная оболочка флуоресценции». Журнал физической химии . 1 (5_6): 275–277. дои : 10.1524/зпч.1954.1.5_6.275 .
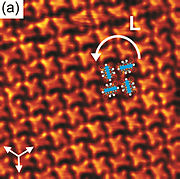
- ^ Фам, Туан Ань; Сун, Фей; Нгуен, Мань-Туонг; Штёр, Майке (2014). «Самосборка производных пирена на Au (111): влияние заместителей на межмолекулярные взаимодействия» . хим. Коммун . 50 (91): 14089–92. дои : 10.1039/C4CC02753A . ПМИД 24905327 .
- ^ Оливейра, М.; Рибейро, А.; Хайланд, К.; Гильермино, Л. (2013). «Одиночное и сочетанное воздействие микропластика и пирена на молодь (группа 0+) бычка обыкновенного Pomatoschistus microps (Teleostei, Gobiidae)». Экологические показатели . 34 : 641–647. дои : 10.1016/j.ecolind.2013.06.019 .
- ^ Оливейра, М.; Гравато, К.; Гильермино, Л. (2012). «Острое токсическое воздействие пирена на Pomatoschistus microps (Teleostei, Gobiidae): смертность, биомаркеры и плавательные способности». Экологические показатели . 19 : 206–214. дои : 10.1016/j.ecolind.2011.08.006 .
- ^ Оливейра, М.; Рибейро, А.; Гильермино, Л. (2012). «Влияние микропластика и ПАУ на микроводоросли Rhodomonas baltica и Tetraselmis chuii». Сравнительная биохимия и физиология. Часть A: Молекулярная и интегративная физиология . 163 : С19–С20. дои : 10.1016/j.cbpa.2012.05.062 .
- ^ Оливейра, М.; Рибейро, А.; Гильермино, Л. (2012). «Влияние кратковременного воздействия микропластика и пирена на микропсы Pomatoschistus (Teleostei, Gobiidae)». Сравнительная биохимия и физиология. Часть A: Молекулярная и интегративная физиология . 163 : С20. дои : 10.1016/j.cbpa.2012.05.063 .
- ^ Со, Чон Су; Кым, Ён Су; Ли, Цин (2009). «Бактериальная деградация ароматических соединений» . Международный журнал экологических исследований и общественного здравоохранения . 6 (1): 278–309. дои : 10.3390/ijerph6010278 . ПМЦ 2672333 . ПМИД 19440284 .
- ^ Кеймиг, SD; Кирби, КВ; Морган, ДП; Кейзер, Дж. Э.; Хьюберт, Т.Д. (1983). «Идентификация 1-гидроксипирена как основного метаболита пирена в моче свиней». Ксенобиотика . 13 (7): 415–20. дои : 10.3109/00498258309052279 . ПМИД 6659544 .
Цитируемые источники
[ редактировать ]- Хейнс, Уильям М., изд. (2016). Справочник CRC по химии и физике (97-е изд.). ЦРК Пресс . ISBN 9781498754293 .
Дальнейшее чтение
[ редактировать ]- Биркс, Дж. Б. (1969). Фотофизика ароматических молекул . Лондон: Уайли.
- Валер, Б. (2002). Молекулярная флуоресценция: принципы и применение . Нью-Йорк: Wiley-VCH.
- Биркс, Дж. Б. (1975). «Эксимеры». Отчеты о прогрессе в физике . 38 (8): 903–974. Бибкод : 1975РПФ...38..903Б . дои : 10.1088/0034-4885/38/8/001 . ISSN 0034-4885 . S2CID 240065177 .
- Фетцер, Дж. К. (2000). Химия и анализ крупных полициклических ароматических углеводородов . Нью-Йорк: Уайли.