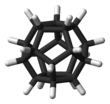
Додекаэдр
 | |||
| |||
| Имена | |||
|---|---|---|---|
| ИЮПАК имена (C 20 - I h )[5]фуллеран гексадекагидро-1,6,5,2,4,3-(эпибутан[1,1,2,3,4,4]гексаил)дипенталено[2,1,6- gha :2',1',6'- cde ]пентален | |||
| Систематическое название ИЮПАК ундекацикло [9.9.0.0 2,9 .0 3,7 .0 4,20 .0 5,18 .0 6,16 .0 8,15 .0 10,14 .0 12,19 .0 13,17 ]икозан | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| 1880116 | |||
| ЧЭБИ | |||
| ХимическийПаук | |||
| 1326921 | |||
ПабХим CID | |||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| С 20 Ч 20 | |||
| Молярная масса | 260.380 g·mol −1 | ||
| Температура плавления | 430±10°С [1] | ||
| Родственные соединения | |||
Родственные углеводороды | Кубинский Тетраэдр Пагодан (изомер додекаэдрана) Призмейн | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Додекаэдран — химическое соединение , углеводород формулы C 20 H 20 , атомы углерода которого расположены в виде вершин (углов) правильного додекаэдра . Каждый углерод связан с тремя соседними атомами углерода и с атомом водорода . Это соединение является одним из трёх возможных платоновых углеводородов , два других — кубан и тетраэдран .
Додекаэдран не встречается в природе и не имеет существенного применения. Он был синтезирован Лео Пакеттом в 1982 году, прежде всего из-за «эстетичной симметрии додекаэдрического каркаса». [2]
В течение многих лет додекаэдр был простейшей реальной молекулой на основе углерода с полной икосаэдрической симметрией . Бакминстерфуллерен ( C 60 ), открытый в 1985 году, также имеет такую же симметрию, но содержит в три раза больше атомов углерода и на 50% больше атомов. Синтез C 20 фуллерена C 20 в 2000 г., из бромированного додекаэдрана, [3] возможно, понизили в должности C 20 H 20 на втором месте.
Структура [ править ]
Угол между связями CC в каждом атоме углерода составляет 108°, что соответствует углу между соседними сторонами правильного пятиугольника . Это значение весьма близко к центральному углу правильного тетраэдра 109,5° — идеальному углу между связями атома, имеющего sp 3 гибридизация . В результате угловая деформация минимальна . Однако молекула имеет значительные уровни деформации кручения в результате затменной конформации вдоль каждого края структуры. [4]
Молекула обладает идеальной икосаэдрической (Ih ) симметрией , о чем свидетельствует ее протонный ЯМР- спектр, в котором все атомы водорода появляются при одном химическом сдвиге 3,38 м.д. В отличие от бакминстерфуллерена, додекаэдр не имеет делокализованных электронов и, следовательно, не обладает ароматичностью .
История [ править ]
На протяжении более 30 лет несколько исследовательских групп активно занимались полным синтезом додекаэдрана. В обзорной статье, опубликованной в 1978 году, описывались различные стратегии, существовавшие до того времени. [5] Первая попытка была предпринята в 1964 году Р.Б. Вудвордом с синтеза соединения трихинацена, которое, как считалось, способно просто димеризоваться до додекаэдрана. В гонке участвовали и другие группы, например, Филип Итон и Пол фон Раге Шлейер .
Группа Лео Пакетта из Университета штата Огайо первой добилась успеха, пройдя сложный 29-шаговый маршрут, который в основном строит додекаэдрический скелет по одному кольцу за раз и, наконец, закрывает последнюю дыру. [2]
нашла более универсальный альтернативный путь синтеза В 1987 году группа Хорста Принцбаха . [6] [7] Их подход был основан на изомеризации пагодана , полученного из изодрина (изомера альдрина ) в качестве исходного материала, в частности, посредством [6+6] фотоциклоприсоединения . Шлейер использовал аналогичный подход в своем синтезе адамантана .
Следуя этой идее, совместные усилия команды Принцбаха и группы Шлейера увенчались успехом, но в лучшем случае получили только 8% доходности от конверсии. В следующее десятилетие группа значительно оптимизировала этот путь, так что додекаэдран можно было получать в количествах в несколько граммов. Новый маршрут также облегчил получение производных с выбранными заменами и ненасыщенными углерод-углеродными связями . Двумя важными событиями стало открытие σ-бишомоароматичности. [8] и образование C 20 фуллерена из высокобромированных разновидностей додекаэдрана. [3] [9]
Синтез [ править ]
Исходный маршрут [ править ]
Пакетта в 1982 году Органический синтез включает около 29 этапов с использованием в качестве сырья циклопентадиена (2 эквивалента, 10 атомов углерода), диметилацетилендикарбоксилата (4 атома углерода) и аллилтриметилсилана (2 эквивалента, 6 атомов углерода).
На первом этапе процедуры [10] две молекулы циклопентадиена 1 соединяются образованием вместе реакцией с элементарным натрием (образуя циклопентадиенильный комплекс ) и йодом с дигидрофульвалена 2 . Далее идет тандемная реакция Дильса-Альдера с диметилацетилендикарбоксилатом 3 с желаемой последовательностью пентадиен-ацетилен-пентадиен, как в симметричном аддукте 4 . равное количество асимметричного пентадиен-пентадиен-ацетиленового соединения ( 4b Образуется и отбрасывается ).
На следующем этапе последовательности [11] йод временно вводится посредством йодолактонизации двухосновной кислоты 4 до дилактона 5 . Эфирная группы группа затем расщепляется метанолом до галогенгидрина 6 , спиртовые группы превращаются в кетоновые в 7 окислением Джонса , а йодные группы восстанавливаются парой цинк-медь в 8 .
Последние 6 атомов углерода встраиваются в результате нуклеофильного присоединения к кетоновым группам карбаниона 10 , образующегося из аллилтриметилсилана 9 и н -бутиллития . На следующем этапе винилсилан 11 реагирует с надуксусной кислотой в уксусной кислоте путем радикального замещения на дилактон 12 с последующим внутримолекулярным алкилированием по Фриделю-Крафтсу пентоксидом фосфора до дикетона 13 . Эта молекула содержит все необходимые 20 атомов углерода, а также является симметричной, что облегчает построение остальных 5 углерод-углеродных связей .
Восстановление двойных связей в 13-14 натрия , осуществляется гидрированием палладием на углероде а кетоновых групп до спиртовых групп в 15 - боргидридом . Замена гидроксила на хлор в 17 путем нуклеофильного алифатического замещения происходит через дилактон 16 ( тозилхлорид ). Первая реакция образования связи C–C представляет собой своего рода алкилирование по Берчу ( литий , аммиак ) с непосредственным продуктом реакции, улавливаемым хлорметилфениловым эфиром , [12] другой атом хлора в 17 просто восстанавливается. Это временное приложение на более позднем этапе предотвратит нежелательную енолизацию . Вновь образованная кетоновая группа затем образует еще одну связь C–C посредством фотохимической реакции Норриша с 19 , спиртовая группа которой индуцируется отщеплением с помощью TsOH до алкена 20 .
Двойная связь восстанавливается гидразином и последовательным восстановлением диизобутилалюминийгидрида и хлорхромата пиридиния окислением 21 образуется альдегид 22 . Вторая реакция Норриша затем добавляет еще одну связь C–C к спирту 23 , и, выполнив свою задачу, фенокси-хвост удаляется в несколько стадий: восстановление Берча до диола 24 , окисление хлорхроматом пиридиния до кетоальдегида 25 и обратная конденсация Кляйзена до кетона 26. . Третья реакция Норриша дает спирт 27 , вторая дегидратация 28 и еще одно восстановление 29 , после чего синтез остается полностью без функциональных групп . Недостающая связь CC восстанавливается путем дегидрирования под давлением водорода с палладием на углероде при 250 °C до додекаэдрана 30 .
Пагоданский маршрут [ править ]
В оптимизированном пути Принцбаха от пагодана к додекаэдрану первоначальная изомеризация исходного пагодана в додекаэдран с низким выходом заменяется более длинной, но более высокопродуктивной последовательностью, которая, тем не менее, по-прежнему в значительной степени зависит от производных пагодана. На схеме ниже отличие от оригинала происходит после соединения 16.
Производные [ править ]
В литературе синтезированы различные производные додекаэдрана.
Замещение водорода [ править ]
Замещение всех 20 атомов водорода атомами фтора приводит к относительно нестабильному перфтордодекаэдрану C 20 F 20 , который получается в миллиграммовых количествах. Следовые количества аналогичного перхлорододекаэдрана C 20 Cl 20 были получены среди других частично хлорированных производных путем реакции C 20 H 20 растворяют в жидком хлоре под давлением около 140°С и под интенсивным светом в течение пяти дней. Полная замена более тяжелыми галогенами кажется все более сложной из-за их большего размера. Половина или более атомов водорода могут быть заменены гидроксильными группами с образованием полиолов крайнее соединение C 20 (OH) 20 оставалось неуловимым. , но по состоянию на 2006 год [13] аминододекаэдраны, сравнимые с амантадином , но более токсичные и обладающие более слабым противовирусным действием. Были получены [14]
кольцеобразные структуры додекаэдрана. Были предложены [15] [16]
Инкапсуляция [ править ]
Молекулы, каркас которых образует закрытую клетку, такие как додекаэдр и бакминстерфуллерен, могут инкапсулировать атомы и небольшие молекулы в пустом пространстве внутри. Эти вставки не связаны химически с каркасным соединением, а просто механически задерживаются в нем.
Кроссу, Сондерсу и Принцбаху удалось инкапсулировать атомы гелия в додекаэдр, стреляя в He. + ионы на пленке соединения. Они получили микрограммовые количества He@. C 20 H 20 («@» — стандартное обозначение инкапсуляции), которое они описали как вполне стабильное вещество. [17] Молекула была описана как «самый маленький в мире гелиевый шарик ». [18]
Ссылки [ править ]
- ^ Линдберг, Томас (2 декабря 2012 г.). Стратегия и тактика органического синтеза . ISBN 9780323152938 .
- ↑ Перейти обратно: Перейти обратно: а б Тернански, Роберт Дж.; Балог, Дуглас В.; Пакетт, Лео А. (1982). «Додекаэдр». Дж. Ам. хим. Соц. 104 (16): 4503–4504. дои : 10.1021/ja00380a040 .
- ↑ Перейти обратно: Перейти обратно: а б Принцбах, Хорст; Вейлер, Андреас; Ланденбергер, Питер; Валь, Фабиан; Вёрт, Юрген; Скотт, Лоуренс Т.; Гельмонт, Марк; Олевано, Даниэла; Иссендорф, Бернд фон (7 сентября 2000 г.). «Газофазное получение и фотоэлектронная спектроскопия мельчайшего фуллерена С 20 ». Природа . 407 (6800): 60–63. Нагрудный код : 2000Nature.407...60P . дои : 10.1038/35024037 . ПМИД 10993070 . S2CID 4355045 .
- ^ Пакетт, Лео (1982). «Додекаэдр. Химическая транслитерация вселенной Платона (Обзор)» . Proc Natl Acad Sci США . 79 (14): 4495–4500. Бибкод : 1982PNAS...79.4495P . дои : 10.1073/pnas.79.14.4495 . ПМК 346698 .
- ^ Итон, Филип Э. (1979). «К додекаэдрану». Тетраэдр . 35 (19): 2189–2223. дои : 10.1016/0040-4020(79)80114-3 .
- ^ Фесснер, Вольф-Дитер; Мурти, АРК Булусу; Принцбах, Хорст (1987). «Путь пагодана к додекаэдранам - термические, восстановительные и окислительные превращения пагоданов». Энджью. хим. Межд. Эд. англ. 26 (5): 451–452. дои : 10.1002/anie.198704511 .
- ^ Фесснер, Вольф-Дитер; Мурти, АРК Булусу; Вёрт, Юрген; Ханклер, Дитер; Фриц, Ганс; Принцбах, Хорст; Рот, Вольфганг Д.; Шлейер, Поль фон Раге; МакИвен, Алан Б.; Майер, Вильгельм Ф. (1987). «Додекаэдраны из [1.1.1.1]Пагоданы». Энджью. хим. Эд. англ. 26 (5): 452–454. дои : 10.1002/anie.198704521 .
- ^ Пракаш, ГКС; Кришнамурти, В.В.; Эргес, Р.; Бау, Р.; Юань, Х.; Ола, Джорджия; Фесснер, В.-Д.; Принцбах, Х. (1988). «[1.1.1.1]- и [2.2.1.1] Дикатионы Пагодана: модели замороженного двухэлектронного переходного состояния Вудворда – Хоффмана». Дж. Ам. хим. Соц. 110 (23): 7764–7772. дои : 10.1021/ja00231a029 .
- ^ Принцбах, Х.; Выбор, Ф.; Вейлер, А.; Ланденбергер, П.; Стоит, Дж.; Скотт, LT; Гельмонт, М.; Олевано, Д.; Лето, Ф.; Иссендорф, Б. фон (2006). «Кластеры углерода C 20 : генерация фуллерена-лодочки-листа, массовый отбор, характеристика полиэтилена». Хим. J. 12 (24): 6268–6280. дои : 10.1002/chem.200501611 . ПМИД 16823785 .
- ^ Пакетт, Лео А.; Вивратт, Мэтью Дж. (1974). «Реакции Домино Дильса – Альдера. I. Применение к быстрому построению полифузионных циклопентаноидных систем». Дж. Ам. хим. Соц. 96 (14): 4671–4673. дои : 10.1021/ja00821a052 .
- ^ Пакетт, Лео А.; Вивратт, Мэтью Дж.; Шаллнер, Отто; Мутард, Жан Л.; Бегли, Уильям Дж.; Бланкеншип, Роберт М.; Балог, Дуглас (1979). «Топологически сферические молекулы. Синтез пары C 2 -симметричных гексахинандилактонов и понимание их химической реакционной способности. Эффективное π-опосредованное восстановление 1,6-дикарбонила». Дж. Орг. хим. 44 (21): 3616–3630. дои : 10.1021/jo01335a003 .
- ^ Пакетт, Лео А.; Тернански, Роберт Дж.; Балог, Дуглас В.; Кентген, Гэри (1983). «Полный синтез додекаэдрана». Дж. Ам. хим. Соц. 105 (16): 5446–5450. дои : 10.1021/ja00354a043 .
- ^ Валь, Фабиан; Вейлер, Андреас; Ланденбергер, Питер; Сакерс, Эммерих; Восс, Торстен; Хаас, Алоис; Дорогой, Макс; Ханклер, Дитер; Вёрт, Юрген; Нот, Лотар; Принцбах, Хорст (2006). «На пути к перфункциональным додекаэдранам — на пути к фуллерену C 20 ». . Евр 12 (24): 6255–6267. дои : 10.1002/chem.200501618 . ПМИД 16807931 .
- ^ Вебер Дж.К., Пакетт Л.А. Синтез аминозамещенных додекаэдранов, секододекаэдранов и гомододекаэдранов и их противовирусная связь с 1-аминоадамантаном. Дж. Орг. Хим . 1988 год; 53(22): 5315-5320. два : 10.1021/jo00257a021
- ^ Банфалвия, Гаспар (2014). «Полимеры мини-шариков додекаэдрана». РСК Адв . 4 (6): 3003–3008. Бибкод : 2014RSCAd...4.3003B . дои : 10.1039/C3RA43628D .
- ^ Лю, Фэн-Лин (26 июля 2004 г.). «Исследование методом DFT молекулы C 25 H 20 с додекаэдровой клеткой и пентапризманской клеткой, разделяющими один и тот же пятиугольник». Дж. Мол. Структур.: Теохим . 681 (1–3): 51–55. doi : 10.1016/j.theochem.2004.04.051 .
- ^ Кросс, Р. Джеймс; Сондерс, Мартин; Принцбах, Хорст (1999). «Помещение гелия внутрь додекаэдрана». Орг. Летт. 1 (9): 1479–1481. дои : 10.1021/ol991037v .
- ^ Путц, Михай В.; Мирица, Мариус Константин (2016). «4». Разработка, свойства и применение устойчивых наносистем . IGI Global. п. 124. ИСБН 978-1-5225-0493-1 .