галогидрин


В органической химии галоидидрин (также галогенспирт или β-галогенспирт ) представляет собой функциональную группу , в которой галоген и гидроксил связаны с соседними атомами углерода , которые в противном случае несут только водородные или гидрокарбильные группы (например, 2-хлорэтанол , 3-хлорпропан). -1,2-диол ). [1] Этот термин применяется только к насыщенным мотивам, поскольку такие соединения, как 2-хлорфенол, обычно не считаются галогенгидринами. Мегатонны некоторых хлоргидринов, например пропиленхлоргидрина , производятся ежегодно в качестве предшественников полимеров.
Галогенгидрины можно разделить на хлоргидрины, бромгидрины, фторгидрины или йодгидрины в зависимости от присутствующего галогена.
Синтез
[ редактировать ]Из алкенов
[ редактировать ]Галогенгидрины обычно получают обработкой алкена галогеном в присутствии воды. Реакция представляет собой форму электрофильного присоединения , где галоген действует как электрофил. [2] В этом отношении она напоминает реакцию присоединения галогена и протекает по принципу антиприсоединения , оставляя вновь добавленные группы X и OH в транс-конфигурации . Химическое уравнение превращения этилена в этиленхлоргидрин:
- H 2 C=CH 2 + Cl 2 + H 2 O → H 2 (OH)C-CH 2 Cl + HCl
Когда желательно бромирование, N -бромсукцинимид (NBS) может быть предпочтительнее брома, поскольку образуется меньше побочных продуктов.

Из эпоксидов
[ редактировать ]Галогенгидрины также могут быть получены реакцией эпоксида с галоидоводородной кислотой . [3] или галогенид металла. [4]
Эта реакция производится в промышленном масштабе для производства предшественников хлоргидрина двух важных эпоксидов, эпихлоргидрина и оксида пропилена. [ нужна ссылка ] . Когда-то 2-хлорэтанол производился в больших масштабах как предшественник оксида этилена , но сейчас последний получают путем прямого окисления этилена. [5]
Из 2-хлоркислот
[ редактировать ]2-Хлоркарбоновые кислоты можно восстановить алюмогидридом лития до 2-хлорспиртов. Необходимые 2-хлоркарбоновые кислоты получают различными способами, в том числе галогенированием Хелла-Фольхарда-Зелинского . 2-Хлорпропионовую кислоту получают хлорированием пропионилхлорида с последующим гидролизом 2-хлорпропионилхлорида. Энантиомерно чистая ( S )-2-хлорпропионовая кислота и некоторые родственные соединения могут быть получены из аминокислот путем диазотирования . [6]
Реакции
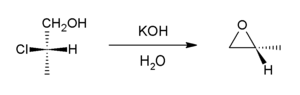
[ редактировать ]В присутствии основания галогенгидрины вступают в внутреннюю реакцию S N 2 с образованием эпоксидов . В промышленности основанием является гидроксид кальция , тогда как в лаборатории часто используют гидроксид калия.
Эта реакция является обратной реакции образования из эпоксида и может рассматриваться как вариант синтеза эфира Вильямсона . По этому маршруту осуществляется большая часть мировых поставок оксида пропилена . [7]
Такие реакции могут лечь в основу более сложных процессов, например образование эпоксида является одним из ключевых этапов реакции Дарценса .
Галогенированный галогенгидрин
[ редактировать ]
Такие соединения, как 2,2,2-трихлорэтанол , которые содержат несколько геминальных галогенов, примыкающих к гидроксильной группе, можно считать галогенгидринами (хотя, строго говоря, они не соответствуют определению ИЮПАК ), поскольку они обладают схожим химическим составом. В частности, они также подвергаются внутримолекулярной циклизации с образованием дигалоэпоксидных групп. Эти виды обладают высокой реакционной способностью и полезны в синтетическом отношении, что составляет основу реакции Джочича-Рива , реакции Барджеллини и реакции Кори-Линка . [8]
Безопасность
[ редактировать ]Как и в случае с любой функциональной группой, опасность галогидринов трудно обобщить, поскольку они могут составлять часть почти безграничного ряда соединений, каждая структура которых имеет различную фармакологию. В общем, более простые низкомолекулярные соединения часто токсичны и канцерогенны (например, 2-хлорэтанол , 3-МХПД ), поскольку являются алкилирующими агентами . Эту реактивность можно найти с пользой, например, в противораковом препарате митобронитоле . Существует ряд синтетических кортикостероидов , имеющих мотив фторгидрина ( триамцинолон , дексаметазон ).
Неправильные термины
[ редактировать ]Несмотря на свои довольно многозначительные названия, эпихлоргидрин и серный хлоргидрин не являются галогенгидринами, хотя первый чаще всего получают с использованием промежуточного соединения хлоргидрина.
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Интернет-исправленная версия: (2006–) « Галогидрины ». дои : 10.1351/goldbook.H02727
- ^ Уильям Ройш. «Реакции присоединения алкенов» . Виртуальный учебник органической химии . Архивировано из оригинала 14 декабря 2012 г.
- ^ Трэвис В.Шоу, Джулия А.Калоу, Эбигейл Дж.Дойл (2012). «Кинетическое разрешение концевых эпоксидов по раскрытию фторидного кольца: получение (S)-2-фтор-1-фенилэтанола» . Органические синтезы . 89 :9. дои : 10.15227/orgsyn.089.0009 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Бонини, Карло; Риги, Джулиана (1994). «Регио- и хемоселективный синтез галогенгидринов путем расщепления оксиранов галогенидами металлов». Синтез . 1994 (3): 225–238. дои : 10.1055/s-1994-25445 .
- ^ Лю, Гордон Ю.Т.; Ричи, В. Франк; Бетсо, Джоан Э.; Хьюз, Брайан; Клапач, Джоанна; Линднер, Йорг (2014). «Хлорогидрины». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a06_565.pub2 . ISBN 978-3527306732 .
- ^ Коппенхёфер, Бернхардт; Шуриг, Волкер (1988). «(S)-2-хлоралкановые кислоты высокой энантиомерной чистоты из (S)-2-аминокислот: (S)-2-хлорпропановая кислота». Органические синтезы . 66 : 151. дои : 10.15227/orgsyn.066.0151 .
- ^ Дитмар Калих, Уве Вихерн, Йорг Линднер «Оксид пропилена» в Энциклопедии промышленной химии Ульмана, 2002, Wiley-VCH, Вайнхайм. doi : 10.1002/14356007.a22_239 Дата размещения статьи в Интернете: 15 июня 2000 г.
- ^ Сноуден, ТС (28 февраля 2012 г.). «Недавние применения промежуточных продуктов гем-дихлорэпоксида в синтезе» . Аркивок . 2012 (2): 24–40. дои : 10.3998/ark.5550190.0013.204 . hdl : 2027/spo.5550190.0013.204 .