Алкилирование

Алкилирование – это химическая реакция , которая влечет за собой перенос алкильной группы. Алкильная группа может быть перенесена как алкилкарбокатион , свободный радикал , карбанион или карбен (или их эквиваленты). [1] Алкилирующие агенты представляют собой реагенты для осуществления алкилирования. Алкильные группы также можно удалить в процессе, известном как деалкилирование . Алкилирующие агенты часто классифицируют в зависимости от их нуклеофильного или электрофильного характера. В контексте нефтепереработки алкилирование конкретному алкилированию изобутана олефинами относится к . Для облагораживания нефти путем алкилирования получают смесь премиум-класса для бензина. [2] В медицине алкилирование ДНК используется в химиотерапии для повреждения ДНК раковых клеток. Алкилирование осуществляется с помощью класса препаратов, называемых алкилирующими противоопухолевыми агентами .
Нуклеофильные алкилирующие агенты
[ редактировать ]Нуклеофильные алкилирующие агенты доставляют эквивалент алкил- аниона ( карбаниона ). Формальный «алкиланион» атакует электрофил , образуя новую ковалентную связь между алкильной группой и электрофилом. Противоион, который представляет собой катион, такой как литий, можно удалить и смыть при обработке . Примеры включают использование металлоорганических соединений, таких как реактивы Гриньяра (магнийорганические) , литийорганические , медноорганические и натрийорганические реагенты. Эти соединения обычно могут присоединяться к атому углерода с дефицитом электронов, например, к карбонильной группе . Нуклеофильные алкилирующие агенты могут замещать галогенидные заместители у атома углерода по механизму SN2 . С помощью катализатора они также алкилируют алкил- и арилгалогениды , на примере реакций Сузуки .

Механизм SN2 недоступен для арильных заместителей, где траектория атаки атома углерода будет находиться внутри кольца. Таким образом, возможны только реакции, катализируемые металлоорганическими катализаторами.
Алкилирование углеродными электрофилами
[ редактировать ]C-алкилирование
[ редактировать ]С-алкилирование – это процесс образования углерод-углеродных связей. Самый крупный пример этого имеет место на установках алкилирования нефтехимических заводов, которые преобразуют низкомолекулярные алкены в высокооктановые компоненты бензина . Богатые электронами соединения, такие как фенолы, также обычно алкилируются с получением различных продуктов; примеры включают линейные алкилбензолы, используемые в производстве поверхностно-активных веществ, таких как LAS , или бутилированные фенолы, такие как BHT , которые используются в качестве антиоксидантов . Этого можно достичь, используя либо кислотные катализаторы, такие как Amberlyst , либо кислоты Льюиса, такие как алюминий. [3] В лабораторном масштабе в реакции Фриделя-Крафтса используются алкилгалогениды , поскольку с ними часто легче обращаться, чем с соответствующими алкенами, которые обычно представляют собой газы. Реакцию катализирует трихлорид алюминия . Этот подход редко используется в промышленности, поскольку алкилгалогениды дороже алкенов.
N-,P-, S-алкилирование
[ редактировать ]N-, P- и S-алкилирование являются важными процессами образования связей углерод-азот, углерод-фосфор и углерод-сера.
Амины легко алкилируются. Скорость алкилирования соответствует порядку третичный амин < вторичный амин < первичный амин. Типичными алкилирующими агентами являются алкилгалогениды. Промышленность часто полагается на методы зеленой химии, включающие алкилирование аминов спиртами, побочным продуктом которых является вода. Гидроаминирование — еще один экологически чистый метод N-алкилирования.
В реакции Меншуткина третичный амин превращается в четвертичную аммониевую соль при взаимодействии с алкилгалогенидом . Аналогичные реакции происходят при обработке третичных фосфинов алкилгалогенидами, продуктами которых являются фосфониевые соли.

Тиолы легко алкилируются с образованием тиоэфиров посредством тиол-еновой реакции . [4] Реакцию обычно проводят в присутствии основания или с использованием сопряженного основания с тиолом. Тиоэфиры подвергаются алкилированию с образованием ионов сульфония .
О-алкилирование
[ редактировать ]Спирты алкилируются с образованием простых эфиров :
Когда алкилирующим агентом является алкилгалогенид, такое превращение называется синтезом эфира Вильямсона .Спирты также являются хорошими алкилирующими агентами в присутствии подходящих кислотных катализаторов. Например, большинство метиламинов получают алкилированием аммиака метанолом. Алкилирование фенолов особенно просто, поскольку оно протекает с меньшим количеством конкурирующих реакций. [5]
- (с Уже + в качестве зрителя )
Более сложное алкилирование спиртов и фенолов включает этоксилирование . Оксид этилена является алкилирующей группой в этой реакции.
Окислительное присоединение к металлам
[ редактировать ]В процессе, называемом окислительным присоединением , низковалентные металлы часто реагируют с алкилирующими агентами с образованием алкилов металлов. Эта реакция является одним из этапов процесса Cativa синтеза уксусной кислоты из йодистого метила . Многие реакции кросс-сочетания также протекают посредством окислительного присоединения.
Электрофильные алкилирующие агенты
[ редактировать ]
Электрофильные алкилирующие агенты доставляют эквивалент алкильного катиона . Алкилгалогениды являются типичными алкилирующими агентами. Тетрафторборат триметилоксония и тетрафторборат триэтилоксония являются особенно сильными электрофилами из-за их явного положительного заряда и инертной уходящей группы (диметилового или диэтилового эфира). Диметилсульфат занимает промежуточное положение по электрофильности.
Метилирование диазометаном
[ редактировать ]Диазометан — популярный в лабораторных условиях метилирующий агент , но он слишком опасен (взрывоопасный газ с высокой острой токсичностью), чтобы его можно было использовать в промышленных масштабах без специальных мер предосторожности. [7] Использование диазометана было значительно сокращено за счет внедрения более безопасного и эквивалентного реагента триметилсилилдиазометана . [8]
Опасности
[ редактировать ]Электрофильные растворимые алкилирующие агенты часто токсичны и канцерогенны из-за их склонности алкилировать ДНК. Этот механизм токсичности имеет отношение к функции противораковых препаратов в форме алкилирующих противоопухолевых агентов . Некоторые виды химического оружия , такие как горчичный газ (сульфид дихлорэтила), действуют как алкилирующие агенты. Алкилированная ДНК либо не скручивается, либо не разворачивается должным образом, либо не может обрабатываться ферментами, декодирующими информацию.
Катализаторы
[ редактировать ]
При электрофильном алкилировании используются кислоты Льюиса и кислоты Бренстеда , а иногда и те и другие. Классически кислоты Льюиса, например трихлорид алюминия при использовании алкилгалогенида используются . Кислоты Бренстеда используются при алкилировании олефинами. Типичными катализаторами являются цеолиты, т.е. твердые кислотные катализаторы, и серная кислота. Кремневольфрамовая кислота используется для производства путем алкилирования уксусной кислоты этиленом этилацетата : [9]
В биологии
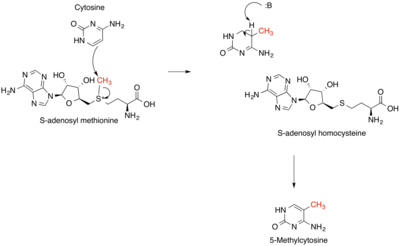
[ редактировать ]Алкилирование в биологии вызывает повреждение ДНК . Это перенос алкильных групп к азотистым основаниям . Это вызвано алкилирующими агентами, такими как EMS (этилметилсульфонат). Бифункциональные алкильные группы, содержащие две алкильные группы, вызывают поперечные сшивки в ДНК. Азотистые основания кольца, поврежденные алкилированием, восстанавливаются с помощью пути эксцизионного восстановления оснований (BER). [10]
Товарная химия
[ редактировать ]Некоторые химические вещества производятся путем алкилирования. Включено несколько основных видов сырья на основе бензола, таких как этилбензол (прекурсор стирола ), кумол (предшественник фенола и ацетона ), линейные алкилбензолсульфонаты (для моющих средств). [11]

Производство бензина
[ редактировать ]
На традиционном нефтеперерабатывающем заводе изобутан алкилируют низкомолекулярными алкенами (в первую очередь смесью пропена и бутена ) в присутствии катализатора на основе кислоты Бренстеда, который может включать твердые кислоты (цеолиты). Катализатор протонирует алкены (пропен, бутен) с образованием карбокатионов , которые алкилируют изобутан. Продукт, называемый «алкилатом», состоит из смеси высокооктановых парафиновых разветвленной цепью углеводородов с (в основном изогептана и изооктана ). Алкилат — это смесь бензинов премиум-класса , поскольку он обладает исключительными антидетонационными свойствами и обеспечивает чистое горение. Алкилат также является ключевым компонентом авиационных бензинов . Комбинируя флюид-каталитический крекинг , полимеризацию и алкилирование, нефтеперерабатывающие заводы могут получить выход бензина 70 процентов. Широкое использование серной и плавиковой кислот на нефтеперерабатывающих заводах создает значительные экологические риски. [12] Ионные жидкости используются вместо сильных кислот Бренстеда предыдущего поколения. [13] [14]
Деалкилирование
[ редактировать ]Дополняющими реакциями алкилирования являются обратные реакции деалкилирования. Преобладающими являются деметилирования , которые распространены в биологии, органическом синтезе и других областях, особенно для метиловых эфиров и метиламинов .
См. также
[ редактировать ]- Гидродеалкилирование
- Трансалкилирование
- Алкинилирование
- Реакция Фриделя – Крафтса
- Категория:Алкилирующие агенты
Ссылки
[ редактировать ]- ^ Марч Джерри; (1985). Реакции, механизмы и структура продвинутой органической химии (3-е изд.). Нью-Йорк: John Wiley & Sons, Inc. ISBN 0-471-85472-7
- ^ Стефанидакис, Г.; Гвин, Дж. Э. (1993). «Алкилирование». В Джоне Дж. МакКетте (ред.). Справочник по химической обработке . ЦРК Пресс. стр. 80–138. ISBN 0-8247-8701-3 .
- ^ Ма, Цишэн; Чакраборти, Деб; Фальони, Франческо; Мюллер, Рик П.; Годдард, Уильям. А.; Харрис, Томас; Кэмпбелл, Курт; Тан, Юнчунь (1 февраля 2006 г.). «Алкилирование фенола: механистический взгляд». Журнал физической химии А. 110 (6): 2246–2252. Бибкод : 2006JPCA..110.2246M . дои : 10.1021/jp0560213 . ПМИД 16466262 .
- ^ Д. Ландини; Ф. Ролла (1978). «Синтез сульфидов при получении диалкил- и алкиларилсульфидов: неопентилфенилсульфид». Орг. Синтез . 58 : 143. дои : 10.15227/orgsyn.058.0143 .
- ^ Г.С. Хиерс и Ф.Д. Хагер (1941). «Анизол» . Органические синтезы ; Сборник томов , т. 1, с. 58 .
- ^ Х. Перст; Д.Г. Сипи (2008). «Тетрафторборат триэтилоксония». Энциклопедия реагентов для органического синтеза . дои : 10.1002/047084289X.rt223.pub2 . ISBN 978-0471936237 .
- ^ Проктор, Ли Д.; Уорр, Энтони Дж. (ноябрь 2002 г.). «Разработка непрерывного процесса промышленного получения диазометана». Исследования и разработки органических процессов . 6 (6): 884–892. дои : 10.1021/op020049k .
- ^ Сиоири, Такаюки; Аояма, Тоёхико; Сноуден, Тимоти (2001). «Триметилсилилдиазометан». Энциклопедия реагентов для органического синтеза . Электронная энциклопедия реагентов для органического синтеза EROS . дои : 10.1002/047084289X.rt298.pub2 . ISBN 0471936235 .
- ^ Мисоно, Макото (2009). «Последний прогресс в практическом применении катализаторов на основе гетерополикислот и перовскитов: каталитические технологии для устойчивого общества». Катализ сегодня . 144 (3–4): 285–291. дои : 10.1016/j.cattod.2008.10.054 .
- ^ Бузиан, М.; Мяо, Ф.; Йе, Н.; Холмквист, Г.; Чизак, Г.; О'Коннор, TR (1998). «Репарация повреждений алкилирования ДНК» . Акта Биохимика Полоника . 45 (1): 191–202. ISSN 0001-527X . ПМИД 9701511 .
- ^ Бипин В. Вора; Джозеф А. Кокал; Пол Т. Баргер; Роберт Дж. Шмидт; Джеймс А. Джонсон (2003). «Алкилирование». Энциклопедия химической технологии Кирка-Отмера . дои : 10.1002/0471238961.0112112508011313.a01.pub2 . ISBN 0471238961 .
- ^ Михаэль Репер, Ойген Герер, Томас Нарбешубер, Вольфганг Сигель «Ацилирование и алкилирование» в Энциклопедии промышленной химии Ульмана, Wiley-VCH, Вайнхайм, 2000. два : 10.1002/14356007.a01_185
- ^ Коре, Раджкумар; Скурто, Аарон М.; Шифлетт, Марк Б. (2020). «Обзор технологии алкилирования изобутана с использованием катализаторов на основе ионных жидкостей - где мы находимся?». Исследования в области промышленной и инженерной химии . 59 (36): 15811–15838. doi : 10.1021/acs.iecr.0c03418 . S2CID 225512999 .
- ^ «Нефтегазовое машиностроение | Технология ионного жидкостного алкилирования получила награду» . 2 января 2018 г.
Внешние ссылки
[ редактировать ]- Страница макрогалереи о производстве поликарбоната
- Алкилирующие агенты Национальной медицинской библиотеки США по медицинским предметным рубрикам (MeSH)


