Деметилирование
Деметилирование – это химический процесс, приводящий к удалению метильной группы (СН 3 ) из молекулы. [1] [2] Распространенным способом деметилирования является замена метильной группы атомом водорода, что приводит к чистой потере одного атома углерода и двух атомов водорода.
Аналогом деметилирования является метилирование .
В биохимии
[ редактировать ]
Дикамба, широко используемый гербицид, биоразлагается путем деметилирования с образованием 3,6- дихлорсалициловой кислоты , катализируемого диоксигеназой ферментом . [3]
Деметилирование имеет отношение к эпигенетике . ДНК катализируется деметилазами Деметилирование . Эти ферменты окисляют N-метильные группы, которые встречаются в гистонах , производных лизина и некоторых формах ДНК. [4]
- Р 2 Н-СН 3 + О → Р 2 Н-Н + СН 2 О
Одним из семейств таких окислительных ферментов является цитохром P450 . [5] Альфа-кетоглутарат-зависимые гидроксилазы также активны в отношении деметилирования ДНК, действуя по аналогичной стехиометрии. [6] Эти реакции, протекающие посредством гидроксилирования , используют слегка ослабленные связи CH метиламинов эфиров и метиловых .
Деметилирование некоторых стеринов является этапом биосинтеза тестостерона и холестерина . Метильные группы теряются в виде формиата . [7]
Переработка биомассы
[ редактировать ]Метоксигруппы сильно декорируют биополимер лигнина . Большой интерес был проявлен к преобразованию этой обильной формы биомассы в полезные химические вещества (помимо топлива). Одним из этапов такой обработки является деметилирование. [8] [9] Для деметилирования ванилина , производного лигнина, требуется 250 °C (482 °F) и сильное основание. [10] Целлюлозно-бумажная промышленность]] переваривает лигнин с использованием водного раствора сульфида натрия , который частично деполимеризует лигнин. Делигнификация сопровождается обширным O-деметилированием с образованием метантиола , который выбрасывается в атмосферу бумажными фабриками . [11]
В органической химии
[ редактировать ]Деметилирование часто относится к расщеплению простых эфиров , особенно ариловых эфиров. [12]
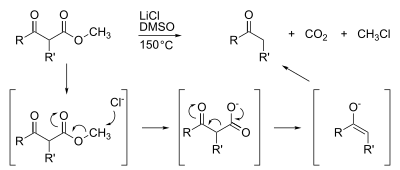
Исторически арилметиловые эфиры, включая природные продукты, такие как кодеин ( O -метилморфин), деметилировались путем нагревания вещества в расплавленном гидрохлориде пиридина (температура плавления 144 °C (291 °F)) при температуре от 180 до 220 °C (от 356 до 428 °F), иногда с избытком хлористого водорода , в процессе, известном как расщепление эфира Цейзеля-Прея . [13] [14] Количественный анализ ароматических метиловых эфиров можно провести аргентометрическим определением образовавшегося хлорида N -метилпиридиния . [15] Механизм этой реакции начинается с переноса протона от иона пиридиния к арилметиловому эфиру, что является крайне неблагоприятной стадией ( К < 10 −11 ), что объясняет необходимость суровых условий, учитывая гораздо более слабую кислотность пиридиния ( p K a = 5,2) по сравнению с протонированным арилметиловым эфиром (ион арилметилоксония, p K a = –6,7 для арил = Ph [16] ). За этим следует S N 2 атака иона арилметилоксония по метильной группе ионом пиридина или хлорида (в зависимости от субстрата) с образованием свободного фенола и, в конечном итоге, хлорида N -метилпиридиния либо непосредственно, либо путем последующего переноса метила от метилхлорид в пиридин. [15]

Другой классический (но, опять же, жесткий) метод удаления метильной группы арилметилового эфира — нагревание эфира в растворе бромистого или йодистого водорода, иногда еще и с уксусной кислотой . [17] Расщепление эфиров бромистоводородной или иодистоводородной кислотой протекает путем протонирования эфира с последующим замещением бромидом или иодидом . В несколько более мягких условиях используется циклогексилиодид (CyI, 10,0 экв.) в N , N -диметилформамиде для образования небольшого количества йодистого водорода in situ . [18]
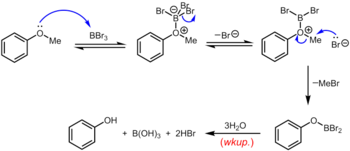
Трибромид бора , который можно использовать при комнатной температуре или ниже, является более специализированным реагентом для деметилирования арилметиловых эфиров. Механизм деалкилирования эфира протекает через первоначальное обратимое образование кислотно-основного аддукта Льюиса между сильнокислотным Льюисом BBr 3 и основным эфиром Льюиса. Этот аддукт Льюиса может обратимо диссоциировать с образованием катиона дибромборил оксония и Br. – . Разрыв эфирной связи происходит в результате последующей нуклеофильной атаки оксониевых частиц со стороны Br. – с получением арилоксидибромборана и бромистого метила. По завершении реакции фенол высвобождается вместе с борной кислотой (H 3 BO 3 ) и бромистоводородной кислотой (водн. HBr) при гидролизе производного дибромборана при водной обработке . [19]
Более сильные нуклеофилы, такие как диорганофосфиды (LiPPh 2 ), также расщепляют ариловые эфиры, иногда в мягких условиях. [20] Другие сильные нуклеофилы, которые использовались, включают тиолатные соли , такие как EtSNa. [21]
Ароматические метиловые эфиры, особенно с соседней карбонильной группой, можно региоселективно деметилировать с использованием эфирата йодида магния . [22] Примером этого является синтез природного продукта Кальфостина А. [23] как показано ниже.

Метиловые эфиры также подвержены деметилированию, которое обычно достигается путем омыления . Широко распространены узкоспециализированные деметилирования, такие как декарбоксилирование Крапчо :
Смесь анетола , КОН и спирта нагревали в автоклаве. Хотя продуктом этой реакции был ожидаемый анол в маточных растворах высокореактивный продукт димеризации, называемый дианолом также обнаружил , Чарльз Доддс .
N -деметилирование
[ редактировать ]N -деметилирование 3°-аминов осуществляется по реакции фон Брауна , в которой используется BrCN в качестве реагента с образованием соответствующих нор- производных. Был разработан современный вариант реакции фон Брауна, в котором BrCN был заменен этилхлорформиатом . Применением этой реакции является получение Паксила из ареколина , как и синтез GSK-372,475 , например.
деметилирование N имипрамина - дает дезипрамин .
См. также
[ редактировать ]- Метилирование – присоединение метильной группы к субстрату.
Ссылки
[ редактировать ]- ^ Клейден, Дж.; Гривз, Н.; Уоррен, С.; Уотерс, П. (2001). Органическая химия . Оксфорд, Оксфордшир: Издательство Оксфордского университета . ISBN 978-0-19-850346-0 .
- ^ Смит, Майкл Б.; Марч, Джерри (2007), Продвинутая органическая химия: реакции, механизмы и структура (6-е изд.), Нью-Йорк: Wiley-Interscience, ISBN 978-0-471-72091-1
- ^ Думитру, Разван; Цзян, Вэнь Чжи; Уикс, Дональд П.; Уилсон, Марк А. (2009). «Кристаллическая структура дикамба-монооксигеназы: негемовая оксигеназа Риске, которая катализирует окислительное деметилирование» . Журнал молекулярной биологии . 392 (2): 498–510. дои : 10.1016/j.jmb.2009.07.021 . ПМК 3109874 . ПМИД 19616011 .
- ^ Педерсен М.Т., Хелин К. (ноябрь 2010 г.). «Гистоновые деметилазы в развитии и заболеваниях». Тенденции в клеточной биологии . 20 (11): 662–71. дои : 10.1016/j.tcb.2010.08.011 . ПМИД 20863703 .
- ^ Роланд Сигел; Сигел, Астрид; Сигель, Хельмут (2007). Повсеместная роль белков цитохрома P450: ионы металлов в науках о жизни . Нью-Йорк: Уайли. ISBN 978-0-470-01672-5 .
- ^ Кохли Р.М., Чжан Ю (октябрь 2013 г.). «Ферменты ТЕТ, ТДГ и динамика деметилирования ДНК» . Природа . 502 (7472): 472–9. Бибкод : 2013Natur.502..472K . дои : 10.1038/nature12750 . ПМК 4046508 . ПМИД 24153300 .
- ^ Пицке, Матиас; Мейзер, Йоханнес; Васкес, Алексей (2020). «Метаболизм формиатов в здоровье и болезнях» . Молекулярный метаболизм . 33 : 23–37. doi : 10.1016/j.molmet.2019.05.012 . ПМК 7056922 . ПМИД 31402327 .
- ^ Шмидт, Сэнди (2022). «Расширение репертуара оксигеназ Риске для O-деметилирования». Химический катализ . 2 (8): 1843–1845. дои : 10.1016/j.checat.2022.07.005 .
- ^ В. Буржан; Дж. Ральф; М. Баушер (июнь 2003 г.). «Биосинтез лигнина» . Анну. Преподобный Плант Биол. 54 (1): 519–549. doi : 10.1146/annurev.arplant.54.031902.134938 . ПМИД 14503002 .
- ^ Ирвин А. Перл (1949). «Протокатехуловая кислота» . Органические синтезы . 29:85 ; Сборник томов , т. 3, с. 745 .
- ^ Хансен, Джорджия (1962). « запаха и Контроль осадков на заводе по производству крафт-целлюлозы ». Журнал Ассоциации по контролю за загрязнением воздуха . 12 (9): 409–436. дои : 10.1080/00022470.1962.10468107 . ПМИД 13904415 .
- ^ Вайсман, Стивен А.; Зевге, Дэниел (2005). «Последние достижения в деалкилировании эфира». Тетраэдр . 61 (33): 7833–7863. дои : 10.1016/j.tet.2005.05.041 .
- ^ Лоусон, Дж.А.; ДеГроу, Дж.И. (1977). «Улучшенный метод O-деметилирования кодеина». Журнал медицинской химии . 20 (1): 165–166. дои : 10.1021/jm00211a037 . ISSN 0022-2623 . ПМИД 833817 .
- ^ Хасснер, Альфред; Стумер, К. (2002). Органические синтезы на основе названных реакций (2-е изд.). Амстердам: Пергамон . ISBN 9780080513348 . OCLC 190810761 .
- ^ Перейти обратно: а б Беруэлл, Роберт Л. (1 августа 1954 г.). «Расщепление эфиров». Химические обзоры . 54 (4): 615–685. дои : 10.1021/cr60170a003 . ISSN 0009-2665 .
- ^ Воллхардт, Питер; Шор, Нил (1 января 2014 г.). Органическая химия: строение и функции (Седьмое изд.). Нью-Йорк, штат Нью-Йорк. ISBN 9781464120275 . OCLC 866584251 .
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ) - ^ Стрейтвизер, Эндрю; Хиткок, Клейтон Х.; Косауэр, Эдвард М. (1992). Введение в органическую химию (4-е изд.). Река Аппер-Сэддл, Нью-Джерси: Прентис-Холл . ISBN 978-0139738500 . OCLC 52836313 .
- ^ Цзо, Ли; Яо, Шаньян; Ван, Вэй; Дуань, Вэньху (июнь 2008 г.). «Эффективный метод деметилирования арилметиловых эфиров». Буквы тетраэдра . 49 (25): 4054–4056. дои : 10.1016/j.tetlet.2008.04.070 .
- ^ JFW МакОми, DE West (1969). «3,3'-Дигидроксибифенил» . Органические синтезы . 49:13 ; Сборник томов , т. 5, с. 412 .
- ^ Роберт Э. Ирландия; Дэвид М. Вальба (1977). Органические синтезы . Том. 56. с. 44. дои : 10.1002/0471264180.os056.11 . ISBN 978-0471264224 .
- ^ Миррингтон, Р.Н.; Фейтрилл, Дж.И. (1973). «Монометиловый эфир орцинола». Органические синтезы . 53 : 90. дои : 10.15227/orgsyn.053.0090 .
- ^ Ямагучи, Сейджи; Недачи, Масахиро; Ёкояма, Хадзиме; Хираи, Ёсиро (октябрь 1999 г.). «Региоселективное деметилирование 2,6-диметоксибензальдегидов эфиратом йодида магния». Буквы тетраэдра . 40 (41): 7363–7365. дои : 10.1016/S0040-4039(99)01411-2 .
- ^ Мерлик, Крейг А.; Олдрич, Кортни К.; Альбанез-Уокер, Дженнифер; Сагателян, Алан (1 апреля 2000 г.). «Карбеновые комплексы в синтезе сложных натуральных продуктов: полный синтез кальфостинов» . Журнал Американского химического общества . 122 (13): 3224–3225. дои : 10.1021/ja994313+ . ПМЦ 3548573 . ПМИД 23335811 .