электрофил
В химии электрофил , — это химическая разновидность , которая образует связи с нуклеофилами принимая электронную пару . [1] Поскольку электрофилы принимают электроны, они являются кислотами Льюиса . [2] положительно Большинство электрофилов заряжены , имеют атом, несущий частичный положительный заряд, или атом, не имеющий октета электронов.
Электрофилы взаимодействуют с нуклеофилами преимущественно посредством реакций присоединения и замещения . Часто встречающиеся электрофилы в органическом синтезе включают катионы, такие как H + и НЕТ + , поляризованные нейтральные молекулы, такие как HCl , алкилгалогениды , ацилгалогениды и карбонильные соединения , поляризуемые нейтральные молекулы, такие как Cl 2 и Br 2 , окислители, такие как органические перкислоты , химические соединения, которые не удовлетворяют правилу октетов, такие как карбены и радикалы. и некоторые кислоты Льюиса, такие как BH 3 и DIBAL .
Органическая химия
[ редактировать ]Добавление галогенов
[ редактировать ]Они происходят между алкенами и электрофилами, часто галогенами, как в реакциях присоединения галогенов . Общие реакции включают использование бромной воды для титрования образца, чтобы определить количество присутствующих двойных связей. Например, этен + бром → 1,2-дибромэтан :
- C 2 H 4 + Br 2 → BrCH 2 CH 2 Br
Это происходит в форме трех основных шагов, показанных ниже; [3]
- Образование π-комплекса
- Электрофильная молекула Br-Br взаимодействует с богатой электронами молекулой алкена с образованием π-комплекса 1 .
- Образование трехчленного иона бромония
- Алкен действует как донор электронов, а бром как электрофил. Трехчленный ион брома 2 состоит из двух атомов углерода и образует атом брома с выделением Br − .
- Атака бромид-иона
- Ион бромония открывается атакой Br. − с обратной стороны. В результате образуется вицинальный дибромид с антиперипланарной конфигурацией. Когда существуют другие нуклеофилы, такие как вода или спирт, они могут атаковать 2 с образованием спирта или эфира.
Этот процесс называется механизмом Ad E 2 («присоединение электрофильное второго порядка»). Йод (I 2 ), хлор (Cl 2 ), сульфенил- ион (RS + ), катион ртути (Hg 2+ ) и дихлоркарбен (:CCl 2 ) также реагируют по сходным путям. Прямое преобразование от 1 до 3 появится, когда Br − - большой избыток в реакционной среде. β-бромкарбения Промежуточный ион может быть преобладающим вместо 3 , если алкен имеет катион-стабилизирующий заместитель, такой как фенильная группа. Имеется пример выделения иона бромония 2 . [4]
Добавление галогеноводородов
[ редактировать ]Галогениды водорода, такие как хлористый водород (HCl), присоединяются к алкенам с образованием алкилгалогенидов при гидрогалогенировании . Например, реакция HCl с этиленом дает хлорэтан. Реакция протекает с промежуточным катионом, отличным от вышеуказанного присоединения галогена. Пример показан ниже:
- Протон (H + ) присоединяется (работая как электрофил) к одному из атомов углерода алкена, образуя катион 1 .
- Хлорид-ион (Cl − ) соединяется с катионом 1 с образованием аддуктов 2 и 3 .
Таким образом, определяется стереоселективность продукта, то есть то, с какой стороны Cl − Атака зависит от типов применяемых алкенов и условий реакции. По крайней мере, какой из двух атомов углерода будет атакован H + обычно определяется по правилу Марковникова . Таким образом, Х + атакует атом углерода, который несет меньше заместителей, в результате чего образуется более стабилизированный карбокатион (с более стабилизирующими заместителями).
Это еще один пример механизма Ad E 2 . [5] фтороводород Аналогично реагируют с алкенами (HF) и иодоводород (HI), при этом образуются продукты марковниковского типа. Бромистый водород (HBr) также идет по этому пути, но иногда радикальный процесс конкурирует и может образоваться смесь изомеров. Хотя во вводных учебниках эта альтернатива редко упоминается, [6] механизм Ad E 2 обычно конкурирует с механизмом Ad E 3 (более подробно описанным для алкинов ниже), при котором перенос протона и нуклеофильное присоединение происходят согласованным образом. Степень вклада каждого пути зависит от нескольких факторов, таких как природа растворителя (например, полярность), нуклеофильность галогенид-иона, стабильность карбокатиона и стерические эффекты. В качестве кратких примеров: образование стерически свободного, стабилизированного карбокатиона благоприятствует пути Ad E 2, тогда как более нуклеофильный бромид-ион Ad E 3 по сравнению с реакциями с участием хлорид-иона. в большей степени благоприятствует пути [7]
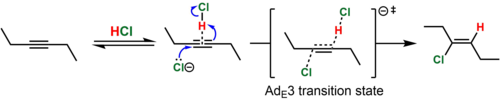
В случае диалкилзамещенных алкинов (например, 3-гексина) промежуточный винильный катион, образующийся в результате этого процесса, очень нестабильен. В таких случаях возможно одновременное протонирование (HCl) и атака алкина нуклеофилом (Cl − ), как полагают, имеет место. Этот механистический путь известен под меткой Ингольда Ad E 3 («присоединение электрофильное третьего порядка»). Поскольку одновременное столкновение трех химических частиц в реакционной ориентации маловероятно, считается, что термомолекулярное переходное состояние достигается, когда нуклеофил атакует обратимо образовавшуюся слабую ассоциацию алкина и HCl. Такой механизм согласуется с преимущественно антиприсоединением (>15:1 анти : син для показанного примера) продукта гидрохлорирования и законом термомолекулярной скорости Скорость = k [алкин][HCl] 2 . [8] [9] В подтверждение предложенной ассоциации алкин-HCl кристаллографически охарактеризован Т-образный комплекс алкина и HCl. [10]
Напротив, фенилпропин реагирует по механизму Ad E 2 ip («присоединение, электрофильная, ионная пара второго порядка»), давая преимущественно син- продукт (~10:1 син : анти ). В этом случае промежуточный винильный катион образуется при добавлении HCl, поскольку он резонансно стабилизирован фенильной группой. Тем не менее, время жизни этих высокоэнергетических частиц коротко, и образующаяся в результате ионная пара винил-катион-хлорид-анион немедленно разрушается, прежде чем ион хлорида получает возможность покинуть оболочку растворителя и дать винилхлорид. Близость аниона к той стороне винилового катиона, куда был добавлен протон, используется для объяснения наблюдаемого преобладания син- присоединения. [7]

Увлажнение
[ редактировать ]В одной из наиболее сложных реакций гидратации используется серная кислота в качестве катализатора . Эта реакция протекает аналогично реакции присоединения, но имеет дополнительную стадию, на которой группа OSO 3 H заменяется группой OH, образуя спирт:
- С 2 Н 4 + Н 2 О → С 2 Н 5 ОН
Как можно видеть, H 2 SO 4 принимает участие в общей реакции, однако остается неизменным, поэтому его классифицируют как катализатор.
Более подробно реакция:
- Молекула H–OSO 3 H имеет заряд δ+ на исходном атоме H. Он притягивается к двойной связи и реагирует с ней так же, как и раньше.
- Оставшийся (отрицательно заряженный) − Ион OSO 3 H затем присоединяется к карбокатиону , образуя этилгидросульфат (верхний путь на приведенной схеме).
- При добавлении воды (H 2 O) и нагревании смеси этанол (C 2 H 5 образуется OH). «Запасной» атом водорода из воды идет на «замещение» «потерянного» водорода и, таким образом, воспроизводит серную кислоту. Возможен и другой путь, по которому молекула воды напрямую соединяется с промежуточным карбокатионом (низший путь). Этот путь становится преобладающим при использовании водного раствора серной кислоты.
В целом, этот процесс добавляет молекулу воды к молекуле этена.
Это важная реакция в промышленности, поскольку она производит этанол , который используется в качестве топлива и исходного материала для других химических веществ.
Хиральные производные
[ редактировать ]Многие электрофилы хиральны и оптически стабильны . Обычно хиральные электрофилы также оптически чисты.
Одним из таких реагентов является органокатализатор на основе фруктозы , используемый при эпоксидировании Ши . [11] Катализатор может осуществлять высокоэнантиоселективное эпоксидирование транс -дизамещенных и тризамещенных алкенов . Катализатор Ши, кетон , окисляется стехиометрическим оксоном до активной формы диоксирана перед тем, как перейти в каталитический цикл.

Оксазиридины, такие как хиральные N-сульфонилоксазиридины, оказывают энантиоселективное альфа-окисление кетонов на пути к сегментам AB-кольца различных натуральных продуктов , включая γ-родомиционон и α-цитромицинон. [12]
связанные с полимером, Хиральные электрофилы селена, вызывают асимметричные реакции селененилирования. [13] Реагенты представляют собой арилселененилбромиды, и они сначала были разработаны для химии растворенной фазы, а затем модифицированы для твердофазного прикрепления шариков через арилоксигруппу. Твердофазные реагенты применялись для селененилирования различных алкенов с хорошей энантиоселективностью. Продукты можно отщеплять от твердого носителя с помощью оловоорганических восстановителей на основе гидрида. Реагенты на твердом носителе имеют преимущества перед химией в растворенной фазе благодаря простоте обработки и очистки.
Шкала электрофильности
[ редактировать ]| Фтор | 3.86 |
| хлор | 3.67 |
| Бром | 3.40 |
| Йод | 3.09 |
| Гипохлорит | 2.52 |
| Диоксид серы | 2.01 |
| Сероуглерод | 1.64 |
| Бензол | 1.45 |
| Натрий | 0.88 |
| Некоторые выбранные значения [14] (без размеров) | |
Существует несколько методов ранжирования электрофилов по реакционной способности. [15] и один из них изобретен Робертом Парром [14] с индексом электрофильности ω, определяемым как:
с электроотрицательность и химическая твердость . Это уравнение связано с классическим уравнением для электрической мощности :
где сопротивление Ом ( и или Ом) это напряжение . В этом смысле индекс электрофильности представляет собой разновидность электрофильной энергии. Обнаружены корреляции между электрофильностью различных химических соединений и скоростью реакций в биохимических системах и таким явлением, как аллергический контактный дермитит.
Индекс электрофильности существует и для свободных радикалов . [16] Сильно электрофильные радикалы, такие как галогены, реагируют с богатыми электронами реакционными центрами, а сильно нуклеофильные радикалы, такие как 2-гидроксипропил-2-ил и трет-бутильный радикал, реагируют с предпочтением реакционных центров с низким содержанием электронов.
Суперэлектрофилы
[ редактировать ]Суперэлектрофилы определяются как катионные электрофильные реагенты со значительно повышенной реакционной способностью в присутствии суперкислот . Эти соединения были впервые описаны Джорджем А. Олахом . [17] Суперэлектрофилы образуются как суперэлектрофилы с двойным дефицитом электронов в результате протосольватации катионного электрофила. Как заметил Ола, смесь уксусной кислоты и трифторида бора способна удалять гидрид-ион из изобутана при соединении с плавиковой кислотой посредством образования суперкислоты из BF 3 и HF. Ответственным реактивным промежуточным продуктом является [CH 3 CO 2 H 3 ] 2+ дикция. Аналогичным образом метан можно нитровать до нитрометана NO тетрафторборатом нитрония . +
22БФ −
4 только в присутствии сильной кислоты, такой как фторсерная кислота, через протонированный дикатион нитрония.
В гитонных ( гитоновых ) суперэлектрофилах заряженные центры разделены не более чем одним атомом, например, ион протонитрония O=N + =О + —H (протонированный ион нитрония ). А у дистонных суперэлектрофилов они разделены 2 и более атомами, например, в реагенте фторирования F-TEDA-BF 4 . [18]
См. также
[ редактировать ]- нуклеофил
- ТРПА1 , [19] [20] сенсорная нейронная мишень для электрофильных раздражителей у млекопитающих.
Ссылки
[ редактировать ]- ^ «Нуклеофилы и электрофилы» . бутан.chem.uiuc.edu . Архивировано из оригинала 01 августа 2020 г. Проверено 21 сентября 2020 г.
- ^ «Электрофил | химия» . Британская энциклопедия . Проверено 21 сентября 2020 г.
- ^ Ленуар, Д.; Кьяппе, К. (2003). «Какова природа первых промежуточных продуктов электрофильного галогенирования алкенов, алкинов и алленов?». хим. Евро. Дж. 9 (5): 1036–1044. дои : 10.1002/chem.200390097 . ПМИД 12596140 .
- ^ Браун, Р.С. (1997). «Исследование ранних этапов электрофильного бромирования путем изучения реакции со стерически обремененными олефинами». Акк. хим. Рез. 30 (3): 131–137. дои : 10.1021/ar960088e .
- ^ По аналогии с ароматическим замещением этот процесс также получил название механизма AS E 2 .
- ^ Воллхардт, К. Питер К.; Шор, Нил Эрик (январь 2014 г.). Органическая химия: строение и функции (7-е изд.). Нью-Йорк, штат Нью-Йорк. ISBN 978-1-4641-2027-5 . OCLC 866584251 .
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ) - ^ Перейти обратно: а б Х., Лоури, Томас (1987). Механизм и теория в органической химии . Ричардсон, Кэтлин Шуллер. (3-е изд.). Нью-Йорк: Харпер и Роу. ISBN 978-0060440848 . OCLC 14214254 .
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Фэйи, Роберт С.; Ли, До-Джэ. (апрель 1968 г.). «Полярные добавки к олефинам и ацетиленам. V. Бимолекулярные и термомолекулярные механизмы гидрохлорирования ацетиленов». Журнал Американского химического общества . 90 (8): 2124–2131. дои : 10.1021/ja01010a034 . ISSN 0002-7863 .
- ^ А., Кэрролл, Феликс (2010). Взгляды на структуру и механизм органической химии (2-е изд.). Хобокен, Нью-Джерси: Джон Уайли. ISBN 9780470276105 . OCLC 286483846 .
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Моотц, Дитрих; Диг, Аксель (июль 1992 г.). «2-Бутин и хлористый водород сокристаллизовались: геометрия твердого тела Cl-H.cntdot..cntdot..cntdot..pi. водородной связи с тройной связью углерод-углерод». Журнал Американского химического общества . 114 (14): 5887–5888. дои : 10.1021/ja00040a077 . ISSN 0002-7863 .
- ^ Ван, З.; Ту, Ю.; Фрон, М.; Чжан, Дж.; Ши, Ю. (1997). «Эффективный метод каталитического асимметричного эпоксидирования». Дж. Ам. хим. Соц. 119 (46): 11224–11235. дои : 10.1021/ja972272g .
- ^ Дэвис, ФА; Кумар, А.; Чен, Британская Колумбия (1991). «Химия оксазиридинов. 16. Короткий высокоэнантиоселективный синтез сегментов АВ-кольца γ-родомиционона и α-цитромицинона с использованием (+)-[(8,8-диметоксикамфорил)сульфонил]оксазиридина». Дж. Орг. хим. 56 (3): 1143–1145. дои : 10.1021/jo00003a042 .
- ^ Уэлин, Л.; Вирт, Т. (2001). «Новые хиральные электрофилы селена, связанные с полимером». Орг. Летт . 3 (18): 2931–2933. дои : 10.1021/ol0164435 . ПМИД 11529793 .
- ^ Перейти обратно: а б Парр, Р.Г.; Сентпалы, Л. В.; Лю, С. (1999). «Индекс электрофильности». Дж. Ам. хим. Соц. 121 (9): 1922–1924. дои : 10.1021/ja983494x .
- ^ Чаттарадж, ПК; Саркар, У.; Рой, ДР (2006). «Индекс электрофильности». хим. Откр. 106 (6): 2065–2091 гг. дои : 10.1021/cr040109f . ПМИД 16771443 .
- ^ Де Влешувер, Фрейя; Спейбрук, Вероника Ван; Варокье, Мишель; Герлингс, Пол; Де Профт, Фрэнк (2007). «Индекс электрофильности и нуклеофильности радикалов». Орг. Летт . 9 (14): 2721–2724. дои : 10.1021/ol071038k . ПМИД 17559221 .
- ^ Ола, Джордж А.; Жермен, Ален; Лин, Генри К.; Форсайт, Дэвид А. (1975). «Электрофильные реакции по одинарным связям. XVIII. Индикация протосольватированных де-факто замещающих агентов в реакциях алканов с ионами ацетилия и нитрония в сверхкислых средах». Дж. Ам. хим. Соц. 97 (10): 2928–2929. дои : 10.1021/ja00843a067 .
- ^ Солингапурам Сай, Киран Кумар; Гилберт, Томас М.; Клампп, Дуглас А. (2007). «Циклизации Кнорра и дистонические суперэлектрофилы». Дж. Орг. хим. 72 (25): 9761–9764. дои : 10.1021/jo7013092 . ПМИД 17999519 .
- ^ Лин Кинг, Джон В.; Эмрик, Джошуа Дж.; Келли, Марк Дж.С.; Херциг, Фолькер; Кинг, Гленн Ф.; Медзиградский, Каталин Ф.; Юлиус, Дэвид (5 сентября 2019 г.). «Проникающий в клетку токсин скорпиона обеспечивает специфическую модуляцию TRPA1 и боли» . Клетка . 178 (6): 1362–1374.e16. дои : 10.1016/j.cell.2019.07.014 . ISSN 1097-4172 . ПМК 6731142 . ПМИД 31447178 .
- ^ Чжао, Цзяньхуа; Лин Кинг, Джон В.; Полсен, Кэндис Э.; Ченг, Ифань; Юлиус, Дэвид (08 июля 2020 г.). «Вызванная раздражением активация и модуляция кальция рецептора TRPA1» . Природа . 585 (7823): 141–145. дои : 10.1038/s41586-020-2480-9 . ISSN 1476-4687 . ПМЦ 7483980 . ПМИД 32641835 .








