Реакция замещения
Реакция замещения (также известная как реакция одиночного замещения или реакция одиночного замещения) — это химическая реакция, во время которой одна функциональная группа в химическом соединении заменяется другой функциональной группой. [1] Реакции замещения имеют первостепенное значение в органической химии . Реакции замещения в органической химии классифицируются как электрофильные или нуклеофильные в зависимости от участвующего в реакции реагента, является ли промежуточное соединение , участвующее в реакции, карбокатионом , карбанионом или свободным радикалом , а также от того, является ли субстрат алифатическим реакционноспособное или ароматическим . Детальное понимание типа реакции помогает предсказать результат реакции. Это также полезно для оптимизации реакции с учетом таких переменных, как температура и выбор растворителя .
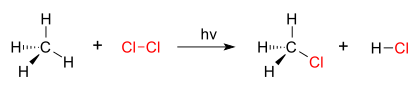
Хорошим примером реакции замещения является галогенирование . При облучении газообразного хлора (Cl 2 ) некоторые молекулы расщепляются на два радикала хлора (Cl•), свободные электроны которых сильно нуклеофильны . Один из них разрывает ковалентную связь C–H в CH 4 и захватывает атом водорода с образованием электронейтральной HCl. Другой радикал образует ковалентную связь с CH 3 • с образованием CH 3 Cl ( метилхлорид ).
| хлорирование метана хлором |
|---|
Нуклеофильное замещение
[ редактировать ]В органической (и неорганической) химии нуклеофильное замещение представляет собой фундаментальный класс реакций, в которых нуклеофил избирательно связывается с положительным или частично положительным зарядом атома или группы атомов или атакует его. При этом он заменяет более слабый нуклеофил, который затем становится уходящей группой ; оставшийся положительный или частично положительный атом становится электрофилом . обычно называют всю молекулярную структуру, частью которой являются электрофил и уходящая группа Субстратом . [1]
Наиболее общую форму реакции можно представить как
где R-LG указывает на подложку. Электронная пара ( : ) нуклеофила (Nuc:) атакует подложку ( R-LG ), образуя новую ковалентную связь Нук-R-LG . Прежнее состояние заряда восстанавливается при уходе уходящей группы (LG) с электронной парой. Основным продуктом в этом случае является Р-Нук . В таких реакциях нуклеофил обычно электрически нейтрален или отрицательно заряжен, тогда как субстрат обычно нейтральен или положительно заряжен.
Примером нуклеофильного замещения является гидролиз бромистого алкила . R-Br в основных условиях, где атакующим нуклеофилом является основание. ОЙ − и уходящая группа Бр − :
Реакции нуклеофильного замещения являются обычным явлением в органической химии, и их можно в общих чертах разделить на те, которые происходят по углероду насыщенного алифатического соединения или (реже) по ароматическому или другому ненасыщенному углеродному центру. [1]
Механизмы
[ редактировать ]Нуклеофильное замещение может протекать по двум различным механизмам: мономолекулярному нуклеофильному замещению ( SN 1 ) и бимолекулярному нуклеофильному замещению ( S N 2 ). Эти две реакции названы в соответствии с их законом скорости : S N 1 имеет закон скорости первого порядка, а S N 2 - второго порядка. [2]

Механизм S N 1 имеет две ступени. На первом этапе уходит уходящая группа, образуя карбокатион (C + ). На втором этапе нуклеофильный реагент (Nuc:) присоединяется к карбокатиону и образует ковалентную сигма-связь. Если субстрат имеет хиральный углерод, этот механизм может привести либо к инверсии стереохимии , либо к сохранению конфигурации. Обычно и то, и другое происходит без предпочтения. Результатом является рацемизация .
Стабильность карбокатиона (C + ) зависит от того, сколько других атомов углерода связано с ним. S N 1 обычно протекают на атомах, по крайней мере, с двумя связанными с ними атомами углерода. Это приводит к тому, что реакции [2] Более подробное объяснение этого можно найти на главной странице реакции SN1 .

Механизм S N 2 имеет всего одну ступень. Атака реагента и изгнание уходящей группы происходят одновременно. Этот механизм всегда приводит к инверсии конфигурации. Если субстрат, подвергающийся нуклеофильной атаке, является хиральным, реакция приведет к инверсии его стереохимии , называемой инверсией Вальдена .
Атака S N 2 может произойти, если задний путь атаки не стерически затруднен заместителями на субстрате. Следовательно, этот механизм обычно реализуется на беспрепятственном первичном углеродном центре. Если на подложке рядом с уходящей группой имеется стерическое скучивание, например, в третичном углеродном центре, замещение будет включать SN 1 , а не SN 2 . [2]

Другие типы нуклеофильного замещения включают нуклеофильное ацильное замещение и нуклеофильное ароматическое замещение . Ацильное замещение происходит, когда нуклеофил атакует углерод, который дважды связан с одним кислородом и одинарно связан с другим кислородом (может быть N, S или галогеном ) , называемый ацильной группой. Нуклеофил атакует углерод, вызывая разрыв двойной связи в одинарную. Затем двойник может реформироваться, выбрасывая при этом ушедшую группу.
Ароматическое замещение происходит в соединениях с системами двойных связей, соединенных в кольца. см. в разделе ароматические соединения Дополнительную информацию .
Электрофильное замещение
[ редактировать ]Электрофилы участвуют в реакциях электрофильного замещения , особенно в электрофильных ароматических замещениях .
В этом примере структура электронного резонанса бензольного кольца подвергается атаке электрофила E. + . Резонирующая связь разрывается, и образуется резонирующая карбокатионная структура. Наконец, протон выбрасывается и образуется новое ароматическое соединение.
 |
| 1: Свободный бензол + электрофил; 2а: Бензол атакует электрофил; 2б: Резонанс бензол-электрофильного интермедиата; 3: Замещенный продукт реакции |
|---|
Электрофильные реакции с другими ненасыщенными соединениями, кроме аренов, обычно приводят к электрофильному присоединению, а не к замещению.
Радикальная замена
[ редактировать ]В реакции радикального замещения участвуют радикалы . Примером может служить реакция Хунсдикера .
Металлоорганическое замещение
[ редактировать ]Реакции сочетания представляют собой класс реакций, катализируемых металлами, с участием металлоорганического соединения RM и органического галогенида R'X, которые вместе реагируют с образованием соединения типа RR' с образованием новой связи углерод-углерод . Примеры включают реакцию Хека , реакцию Ульмана и реакцию Вюрца-Фиттига . Существует множество вариаций. [3]
Замещенные соединения
[ редактировать ]Замещенные соединения — это соединения, в которых один или несколько атомов водорода заменены чем-то другим, например алкилом , гидроксилом или галогеном . Более подробную информацию можно найти на странице замещенных соединений .
Неорганическая и металлоорганическая химия
[ редактировать ]Хотя реакции замещения обычно обсуждаются в контексте органической химии, эта реакция является общей и применима к широкому кругу соединений. Лиганды в координационных комплексах подвержены замещению. Наблюдаются как ассоциативные, так и диссоциативные механизмы. [4] [5]
Ассоциативное замещение , например, обычно применяется к металлоорганическим и координационным комплексам , но напоминает механизм Sn2 в органической химии . Противоположный путь – диссоциативное замещение , аналогичный пути Sn1 .
Примеры ассоциативных механизмов обычно встречаются в химии плоских квадратных комплексов металлов 16e, например комплекса Васки и тетрахлорплатината . Закон ставки регулируется механизмом Эйгена-Уилкинса .

Диссоциативное замещение напоминает механизм S N 1 в органической химии. Этот путь можно хорошо описать цис- эффектом или лабилизацией лигандов CO в цис- положении. Комплексы, подвергающиеся диссоциативному замещению, часто являются координационно насыщенными и часто имеют октаэдрическую молекулярную геометрию . Энтропия активации для этих реакций характерна положительная, что свидетельствует о возрастании беспорядка реагирующей системы на скоростьопределяющей стадии. Диссоциативные пути характеризуются стадией , определяющей скорость , которая включает высвобождение лиганда из координационной сферы замещаемого металла. Концентрация замещающего нуклеофила не влияет на эту скорость, и можно обнаружить интермедиат с пониженным координационным числом. Реакцию можно описать с помощью k 1 , k -1 и k 2 , которые являются константами скорости соответствующих промежуточных стадий реакции:
Обычно этапом, определяющим скорость, является диссоциация L от комплекса, и [L'] не влияет на скорость реакции, что приводит к простому уравнению скорости:
Дальнейшее чтение
[ редактировать ]- Имянитов, Наум С. (1993). «Является ли эта реакция замещением, окислением-восстановлением или переносом?». Дж. Хим. Образование . 70 (1): 14–16. Бибкод : 1993JChEd..70...14I. дои : 10.1021/ed070p14.
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с Марч, Джерри (1985), Продвинутая органическая химия: реакции, механизмы и структура, 3-е издание , Нью-Йорк: Wiley, ISBN 9780471854722 , OCLC 642506595
- ^ Перейти обратно: а б с Брюс, Паула Юрканис (2011). Органическая химия (6-е изд.). 1900 Э. Лейк Авеню, Гленвью, Иллинойс, 60025: Pearson Education Inc., стр. 332–365. ISBN 978-0-321-66313-9 .
{{cite book}}: CS1 maint: местоположение ( ссылка ) - ^ Эльшенбройх, К.; Зальцер, А. (1992). Металлоорганические соединения: краткое введение (2-е изд.). Вайнхайм: Wiley-VCH. ISBN 3-527-28165-7 .
- ^ Басоло, Ф.; Пирсон Р.Г. «Механизмы неорганических реакций». Джон Уайли и сын: Нью-Йорк: 1967. ISBN 0-471-05545-X
- ^ Уилкинс, Р.Г. (1991). Кинетика и механизм реакций комплексов переходных металлов (2-е изд.). Вайнхайм: ВЧ. ISBN 1-56081-125-0 .


![{\displaystyle {\ce {L_ {\mathit {n}}ML<=>[-\mathrm {L},k_{1}][+\mathrm {L},k_{-1}]L_{\mathit {n}}M-\Box ->[+\mathrm {L} ',k_{2}]L_{\mathit {n}}ML'}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e0cfb8a46601d81d661e919a1b64b91ec3113586)
![{\displaystyle {\ce {Rate={{\mathit {k}}_{1}[L_ {\mathit {n}}ML]}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8adaf95dcf066302cf203f0dd7252129be849f03)