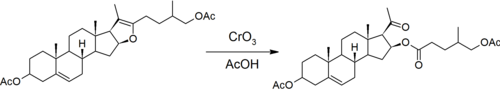Деградация маркера
— Деградация маркера это трехэтапный синтетический путь в химии стероидов , разработанный американским химиком Расселом Эрлом Маркером в 1938–1940 годах. Он используется для производства кортизона млекопитающих и половых гормонов ( прогестерона , эстрадиола и т. д.) из растительных стероидов, что сделало Мексику мировым центром производства стероидов сразу после Второй мировой войны . [1] Открытие деградации маркера впервые позволило производить значительные количества стероидных гормонов и сыграло фундаментальную роль в разработке противозачаточных таблеток и кортикостероидных противовоспалительных препаратов. В 1999 году Американское химическое общество и Мексиканское химическое общество назвали этот маршрут международным историческим химическим памятником. [1]
Первое крупномасштабное применение этого маршрута произошло в 1943 году, когда Рассел Эрл Маркер собрал 10 тонн ямса клубней , чтобы синтезировать 3 килограмма (6,6 фунта) прогестерона , что было самым большим разовым количеством прогестерона, которое было произведено к тому времени. . [1] Стоимость этой единственной партии составила 240 000 долларов США (примерно 3 миллиона долларов в 2009 году). [2] ) на момент его синтеза. [1]
Открытие разложения маркера привело к развитию тонкой химической промышленности в Мексике, которая, начав с нуля и менее чем за десять лет, поставляла более половины человеческих половых гормонов, продаваемых в Соединенных Штатах. Быстро развивающаяся промышленность привела к огромному расширению химического образования в Мексике.
Раннее развитие
[ редактировать ]Исследования Маркера в Государственном колледже Пенсильвании (ныне Университет штата Пенсильвания ) были направлены на поиск синтетических путей получения стероидных гормонов из «относительно недорогих исходных материалов». [3] Работая над серией растительных стероидов, называемых сапогенинами , он понял, что структура боковой цепи [примечание 1] Одно из соединений, сарсасапогенин , было неверно описано в литературе: вместо нереакционноспособной боковой цепи «двойного тетрагидрофурана » оно на самом деле имело гораздо более реакционноспособную боковую цепь « кетон » -спироацеталь . [3] Хотя кетон-спироацеталь был нереакционноспособным в основных или нейтральных условиях, он мог разлагаться в кислых условиях: действительно, Маркер описал его как «необычайно реакционноспособный». [3] Показывая истинную природу боковой цепи сарсасапогенина, Маркер открыл первый из этапов того, что впоследствии стало известно как деградация маркера.
Сарсасапогенин был слишком дорогим, чтобы быть коммерческим предшественником других стероидов, поэтому Маркер приступил к поиску более богатых источников сапогенинов, которые были бы более тесно связаны с прогестероном. Он идентифицировал одного кандидата в Trillium erectum («корень Бет» или «Wake-robin»), сапогенин, называемый диосгенин , который ранее был обнаружен в японском ямсе ( Dioscorea tokoro ). [1] [4] Маркер показал, что и сарсасапогенин, и диосгенин могут превращаться как в прогестерон, так и в прогестерон. [5] и другие стероидные гормоны. [6] [примечание 2] Количества диосгенина, которые можно было извлечь из T. erectum , все еще были неудовлетворительными, поэтому Маркер искал более богатые источники. В конце концов он наткнулся на другой вид Dioscorea , мексиканский ямс, известный в местном масштабе как cabeza de negro . [примечание 3] которого Сообщается, что клубни вырастают до 100 кг (220 фунтов) в весе. [1]
Маршрут от диосгенина
[ редактировать ]Как и в большинстве случаев химии стероидов, деградация маркера в значительной степени зависит от кинетического контроля , который разрушает боковую цепь сапогенина, оставляя при этом аналогичные функциональные группы в стероидном ядре (относительно) незатронутыми.
Первым шагом является реакция, которая привела Маркера к открытию того, что сапогенины имеют кетон-спиро-ацетальную структуру в боковой цепи. [7] Ацетали инертны в основных условиях, но могут гидролизоваться в кислых условиях. Маркер использует уксусный ангидрид для блокировки гидроксильной группы, образующейся при открытии шестичленного пиранового кольца. [8]
Затем пятичленное фурановое кольцо окислительно раскрывается хромовой кислотой . При этом образуется ацетильная боковая цепь прогестерона и этерифицированная гидроксильная группа в стероидном ядре.
Затем сложный эфир гидролизуют в сильноосновных условиях. Использование этанольного гидроксида натрия приводит к отщеплению воды с образованием двойной связи.
Результатом этой версии деградации маркера 1939 года является 16-дегидропрегненолон (3-гидроксипрегна-5,16-диен-20-он, 16-DP). [5] В 1940 году финальная стадия гидролиза была изменена на использование уксусной кислоты, в результате чего был получен более знакомый ацетат 16-дегидропрегненолона (16-ДПА). [9]
Продукты переработки
[ редактировать ]16-DP можно превратить в прогестерон в два этапа. Во-первых, двойная связь в кольце D гидрируется с последующим окислением Оппенауэром гидроксильной группы и одновременной миграцией оставшегося олефина из кольца B в кольцо A так, чтобы он находился в сопряжении с кетоновой карбонильной группой в положении 3. [5] трехэтапная процедура с участием Br 2 , CrO 3 и Zn/ HOAc . Альтернативно используется [1]
16-DP также может превращаться в тестостерон и последующие продукты – эстрон и эстрадиол . [1] [6]
Мексиканская стероидная индустрия
[ редактировать ]Ранние разработки Маркера были поддержаны Parke-Davis , ведущей американской фармацевтической компанией, которая теперь является частью Pfizer . [1] Однако Маркер понял, что с коммерческой точки зрения более целесообразно производить стероиды в Мексике, рядом с сырьем (мексиканская Dioscorea sp.; D. composita станет предпочтительным видом). [1] ), чем отправлять клубни обратно в США. Парк-Дэвис не верил, что с научной точки зрения возможно управлять предприятием по производству чистых химикатов в Мексике, и сотрудничество провалилось. [1] Вместо этого Маркер решил сам искать мексиканских партнеров и 1 декабря 1943 года оставил свой академический пост. [1] Одним из последствий этого разделения стало то, что деградация маркера так и не была запатентована . [1]
Маркер основал мексиканскую компанию Syntex [примечание 4] в начале 1944 года совместно с двумя мексиканскими инвесторами, Эмериком Сомло и Федерико Леманном. Говорят, что Маркер частично заплатил за свои 40% акций Syntex прогестероном. [1] тогда оценивался примерно в 80 долларов за грамм. [1] В течение года Syntex продавала прогестерон по цене 50 долларов за грамм. [1] Однако в мае 1945 года Маркер расстался со своими партнерами из-за спора о прибылях и основал новую компанию под названием Botanica-mex, которая позже была продана Gedeon Richter Ltd. и переименована в Hormonosynth (позже Diosynth). [1]
Трудности в производстве тонких химикатов в Мексике действительно были значительными: острая нехватка подготовленных химиков и отсутствие докторской программы по химии ни в одном мексиканском университете. Когда Маркер покинул Syntex, его коллеги не обнаружили никаких инструкций по производственному процессу и бутылок с реагентами, помеченных кодом. [1] Вместо Маркера они наняли Джорджа Розенкранца , венгерского химика-органика, получившего образование в ETH Zurich (Швейцарский федеральный технологический институт), который застрял на Кубе из-за вступления Соединенных Штатов во Вторую мировую войну. [1] Розенкранцу пришлось бы практически заново изобрести процесс производства прогестерона из диосгенина: он также основал Институт химии в Национальном автономном университете Мексики . [1] где одним из первых студентов-исследователей был Луис Э. Мирамонтес , позже ставший ключевым исследователем в Syntex.
Розенкранц также нанял для Syntex иностранных талантов, в том числе австрийского еврейского беженца (и натурализованного американца) Карла Джерасси и уругвайца Алехандро Заффарони . В 1951 году Джерасси, Мирамонтес и Розенкранц синтезировали в Syntex норэтистерон , первый перорально активный аналог прогестерона и жизненно важный ингредиент первых пероральных противозачаточных таблеток . [10] К этому времени Syntex и ее мексиканские конкуренты (в том числе Перси Лавон Джулиан , первый афроамериканский США химик, принятый в Национальную академию наук ) поставляли более половины человеческих половых гормонов, продаваемых в Соединенных Штатах. [примечание 5] а цена прогестерона упала до 2 долларов за грамм. [1] В том же 1951 году журнал Fortune опубликовал статью под заголовком: «Syntex совершает самый большой технологический бум, когда-либо существовавший к югу от границы»: к 1999 году, оглядываясь назад, Американское химическое общество сочло это преуменьшением , а не преуменьшением. хотя бы из-за поистине глобального влияния производства и исследований Syntex. [1] Влияние исследований Syntex можно увидеть в авторитетной монографии Стероиды « Луи и Мэри Физер » 1959 года : [11] На Syntex приходилось 30% всех цитируемых статей промышленных лабораторий. [1] В 1959 году Syntex превратилась в панамскую корпорацию и переместила свою штаб-квартиру в Пало-Альто, Калифорния , США. [12]
Примечания и ссылки
[ редактировать ]Примечания
[ редактировать ]- ^ Стероиды характеризуются четырьмя сросшимися кольцами атомов углерода (три шестичленных кольца и одно пятичленное кольцо). Многие стероиды также имеют «боковую цепь» из атомов углерода, обычно присоединенную к пятичленному кольцу.
- ^ Хотя в то время это еще не было известно, использование прогестерона в качестве предшественника других стероидных гормонов близко имитирует путь биосинтеза . Мужчины синтезируют прогестерон как предшественник тестостерона , а женщины синтезируют тестостерон как предшественник различных эстрогенов . Кортизон также синтезируется из прогестерона в организме человека, как и в промышленном процессе, разработанном после открытия деградации маркера.
- ^ Не путать с фруктом, известным как кабеса де негро или илама ( Annona purpurea ).
- ^ Сейчас часть Hoffmann-La Roche .
- ^ Доступность (относительно) дешевого прогестерона в (относительно) больших количествах создала рынок и побудила других производителей улучшить свои процессы производства стероидных гормонов: лучше всего это видно в случае кортизона , где продуктов Merck оригинальные 36 Двухступенчатый синтез из бычьей желчи был улучшен, чтобы оставаться конкурентоспособным по сравнению с кортизоном, полученным из мексиканского ямса.
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с т в v В «Рассел Маркер и мексиканская индустрия стероидных гормонов» . Американское химическое общество . Проверено 5 июня 2012 г.
- ^ «Калькулятор инфляции» . Архивировано из оригинала 18 июля 2011 г. Проверено 6 марта 2010 г.
- ^ Перейти обратно: а б с Маркер, Рассел Э .; Рорманн, Эвальд (1939), «Стерины. LIII. Структура боковой цепи сарсасапогенина», J. Am. хим. Соц. , 61 (4): 846–51, doi : 10.1021/ja01873a020 .
- ^ Цукамото; Уэно; Охта (1936), «Гликозиды Dioscorea tokoro I. Диоцин, диоскореасапуоксин и диосгенин», Журнал Фармацевтического общества Японии , 56 : 135 . Цукамото; Уэно; Охта (1937), «О конституции Диосгенина II», Якугаку Засши , 57 (11): 985, doi : 10.1248/yakushi1881.57.11_985 .
- ^ Перейти обратно: а б с Маркер, Рассел Э .; Рорманн, Эвальд (1939), «Стерины. LXXXI. Превращение сарсасапогенина в прегнандиол-3(α),20(α)», J. Am. хим. Соц. , 61 (12): 3592–93, doi : 10.1021/ja01267a513 . Маркер, Рассел Э .; Рорманн, Эвальд (1940), «Стерины. LXXVIII. Прегнандиолы из сарсасапогенина», J. Am. хим. Соц. , 62 (3): 518–20, doi : 10.1021/ja01860a017 . Маркер, Рассел Э .; Цукамото, Такео; Тернер, Д.Л. (1940), «Стерины. К. Диосгенин», J. Am. хим. Соц. , 62 (9): 2525–32, doi : 10.1021/ja01866a072 .
- ^ Перейти обратно: а б Маркер, Рассел Э. (1940), «Стерины. CV. Получение тестостерона и родственных соединений из сарсасапогенина и диосгенина», J. Am. хим. Соц. , 62 (9): 2543–47, doi : 10.1021/ja01866a077 .
- ^ Майерс, Расти Л.; Майерс, Ричард Л. (2007), 100 наиболее важных химических соединений: справочное руководство , Вестпорт, Коннектикут: Greenwood Press, стр. 205–8, ISBN. 978-0-313-33758-1 .
- ^ Дьюик, премьер-министр (2009), Натуральные лекарственные продукты: биосинтетический подход , Нью-Йорк: Wiley, стр. 281–83, ISBN. 978-0-470-74167-2 .
- ^ Маркер Р.Э., Крюгер Дж. (1940). «Стерины. CXII. Сапогенины. XLI. Получение триллина и его превращение в прогестерон». Дж. Ам. хим. Соц . 62 (12): 3349–3350. дои : 10.1021/ja01869a023 .
- ^ США 2744122 , Джерасси, Карл ; Мирамонтес, Луис и Розенкранц, Джордж , «Δ 4 -19-нор-17α-этиниландростен-17β-ол-3-он и процесс», опубликовано 10 мая 1956 г., передано Syntex .
- ^ Физер, Луи Ф .; Физер, Мэри П. (1959), Стероиды , Нью-Йорк: Ван Ностранд Рейнхольд, ISBN 0-278-91709-7 .
- ^ Джереффи, Гэри (1983). Фармацевтическая промышленность и зависимость в странах третьего мира (переиздание 2017 г.). Издательство Принстонского университета: Принстон. п. 110. ИСБН 9781400886227 . Проверено 11 января 2021 г.